慢性自发性荨麻疹(CSU)是一种以反复发作的瘙痒性风团和/或血管性
CSU 患者经标准治疗后症状仍未控制,临床应如何评估与优化治疗方案?如何结合患者报告结局实现更全面的疾病管理?

研究设计
CUPID-C是一项为期24周的多中心、随机、双盲、安慰剂对照的3期临床试验(NCT04180488),设计完全复制CUPID-A。研究在阿根廷、加拿大、中国、法国、德国、匈牙利、日本、西班牙和美国共9个国家开展。同时进行CUPID-A与CUPID-C的汇总分析(共289例患者)。
研究对象
纳入标准:6-80岁;CSU诊断>6个月;尽管使用H1-AH但仍有瘙痒和风团(连续6周以上);筛选期前服用稳定剂量H1-AH(最高推荐剂量的4倍,日本为2倍)至少3天;从未接受过奥马珠单抗;随机前7天内UAS7≥16且ISS7≥8。排除体重过低、有其他明确原因的
干预措施
患者按1:1随机分配至度普利尤单抗组或安慰剂组,持续24周。度普利尤单抗剂量基于体重:≥60kg成人/青少年:负荷剂量600mg,之后300mg每2周;<60kg的青少年及≤30kg儿童:负荷剂量400mg,之后200mg每2周;15-<30kg儿童:负荷剂量600mg,之后300mg每4周。患者继续接受背景H1-AH治疗(允许使用至4倍推荐剂量)。允许使用口服
疗效终点
-主要终点(美国FDA要求):第24周ISS7(瘙痒严重程度评分7天,0-21)较基线的变化。
-关键次要终点(美国FDA):第24周UAS7(荨麻疹活动评分7天,0-42)较基线的变化。
-欧洲EMA要求:UAS7为主要终点,ISS7为次要终点。
-其他次要终点:HSS7(风团严重程度)、UCT(荨麻疹控制测试)、DLQI、AAS7(血管性水肿活动评分)、达到UAS7≤6(良好控制)、UAS7=0(完全控制)及ISS7下降≥5分的患者比例等。
统计方法
连续终点采用协方差分析(ANCOVA),校正基线值、治疗组、基线是否有血管性水肿、地区及研究(汇总分析时)。合并使用补救药物或违规药物、因缺乏疗效停药者采用最差观察值结转(WOCF);其他原因停药采用多重插补。分类终点采用Cochran-Mantel-Haenszel检验。所有P值均为双侧,α=0.05。汇总分析P值为名义值。
患者基线特征
CUPID-C共随机151例受试者(平均年龄44.7岁;女性70.2%),其中6例青少年(12-<18岁)、3例儿童(6-<12岁)。两组基线特征均衡(表1)。
表1CUPID-C试验中安慰剂组和度普利尤单抗组的基线人口学和临床特征
关键基线数据:
-使用超推荐剂量H1-AH者占51.0%。
-基线UAS7≥28(重度疾病活动)者占59.6%。
-合并血管性水肿者22.5%。
-平均DLQI 12.2分(生活质量中重度损害)。
疗效结果
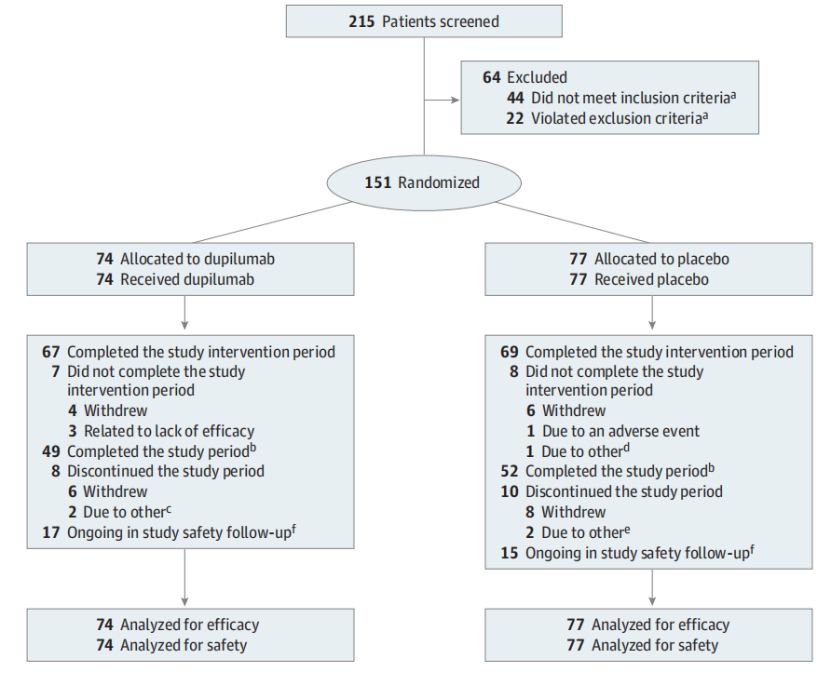
图1 CUPID-C患者处置流程
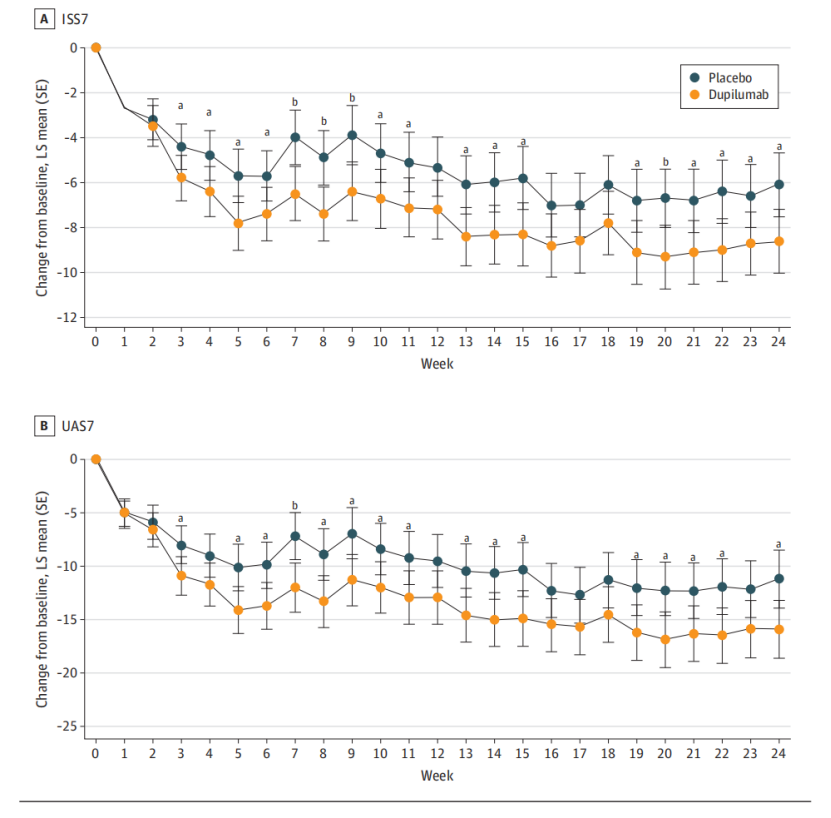
图2 度普利尤单抗组与安慰剂组在24周内ISS7和UAS7较基线的变化(LS均值变化,带误差线)
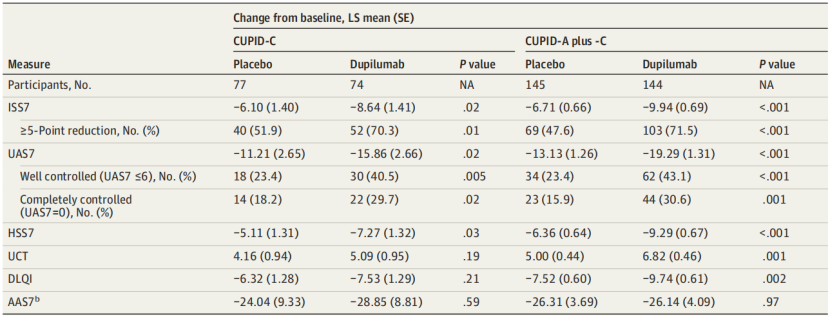
CUPID-C结果(第24周)
表2. 第24周时,按研究组别划分的度普利尤单抗治疗在CUPID-C及CUPID-A联合CUPID-C队列中对瘙痒和风团严重程度评分及荨麻疹活动度的改善情况
从治疗第3周起,度普利尤单抗组ISS7和UAS7改善已显著优于安慰剂组(图2)。
汇总分析(CUPID-A + CUPID-C,n=289)
在伴有血管性水肿的亚组中,度普利尤单抗同样有效(与总体一致)。无论基线血清总IgE水平(低于或高于40 IU/mL、60 IU/mL、100 IU/mL),度普利尤单抗均能改善瘙痒和荨麻疹活动度。
安全性结果
表3. CUPID-C 及 CUPID-A 联合 CUPID-C 合并队列中的安全性结局
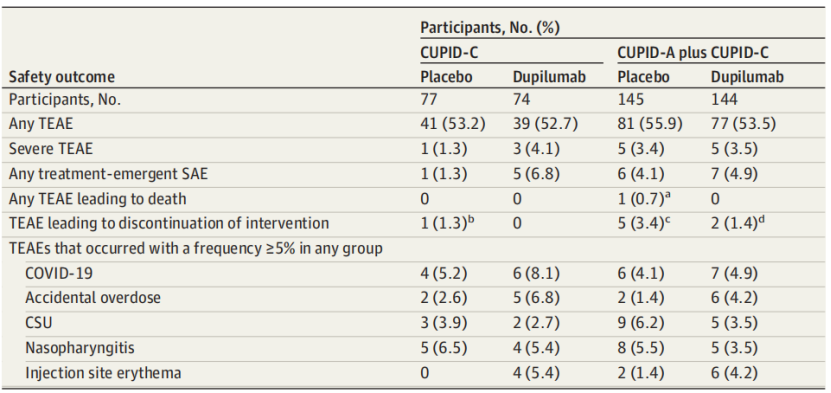
CUPID-C安全性
-任意治疗期间出现的不良事件(TEAE):度普利尤单抗组52.7%,安慰剂组53.2%。
-严重TEAE:度普利尤单抗组6.8%(5例),安慰剂组1.3%(1例)。
-导致停药的不良事件:度普利尤单抗组0%,安慰剂组1例(1.3%)。
-最常见TEAE(任一治疗组≥5%):COVID-19(8.1% vs 5.2%)、意外过量(6.8% vs 2.6%)、鼻
汇总分析(CUPID-A+CUPID-C)
-任意TEAE:度普利尤单抗组53.5%,安慰剂组55.9%。
-严重TEAE:度普利尤单抗组4.9%,安慰剂组4.1%。
-死亡:安慰剂组1例(
-导致停药:度普利尤单抗组2例(1.4%),安慰剂组5例(3.4%)。
-未见新的安全性信号。
CUPID-C成功验证了CUPID-A的结果:在H1-AH控制不佳且未使用过抗IgE的CSU患者中,度普利尤单抗显著降低瘙痒、风团及整体荨麻疹活动度,且起效迅速(第3周即显效)。汇总分析进一步提供了稳健的证据,疗效优于安慰剂,且独立于基线IgE水平。安全性特征与已知度普利尤单抗安全性一致,无新发安全信号。
本研究局限性:24周随访无法评估长期持久性;儿童及青少年患者数量有限;种族和民族多样性不足。尽管如此,该研究为H1-AH难治性且未使用过奥马珠单抗的CSU患者提供了新的有效治疗选择。
在CUPID-C 3期随机临床试验中,度普利尤单抗在H1-AH治疗仍有症状的未使用过抗IgE的CSU患者中显示出显著且具有临床意义的疗效,其结果与重复验证试验CUPID-A一致。CUPID-A和CUPID-C的汇总数据共同强化了度普利尤单抗在该人群中的临床获益和安全性。
参考文献
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。