


1
流感样症状是干扰素治疗初期最常见的不良反应,临床主要表现为
该症状的发生与干扰素刺激机体免疫系统,引发全身性炎症反应有关。尤其是当免疫系统试图清除病毒时,干扰素诱导机体产生的大量细胞因子,如肿瘤坏死因子、白细胞介素(IL)-1、IL-6等,作用于体温调节中枢引起发热。
对于轻度症状,建议患者注意休息并保证充足饮水;若出现高热、明显肌肉或关节酸痛等较重症状且难以耐受时,可予以非甾体抗炎药对症处理以减轻不适感。
总之,流感样症状是干扰素治疗过程中最常见的不良反应,其发生机制明确,通常持续时间短,症状轻微,多数患者可以耐受。

2外周血细胞减少
PEG-IFN-α-2b治疗过程中常出现外周血细胞减少,主要表现为中性粒细胞与血小板计数下降。临床观察表明,该不良反应的发生率为50%~70%,通常在治疗第2周开始出现,并随疗程延长呈现渐进性下降的特点。
中性粒细胞和血小板计数下降曾被视为严重不良反应,不仅会增加患者的感染和出血风险,也是影响患者的依从性导致无法完成疗程的主要原因之一。早期研究提示,其发生机制可能与干扰素直接作用于骨髓造血干细胞/祖细胞有关,通过抑制其增殖与分化,从而影响血细胞生成。我国首部《慢性乙型肝炎防治指南》曾建议,若患者在接受干扰素治疗过程中出现中性粒细胞计数<0.75×109/L和/或血小板计数<30×109/L,应立即停药。
但后期研究表明,干扰素能通过抑制
一项前瞻性队列研究显示,多数具有临床意义的感染事件与干扰素治疗相关的中性粒细胞减少之间无显著时间关联(P>0.001)。进一步的多因素回归分析表明,治疗期间中性粒细胞计数最低值与严重感染风险无独立相关性(校正后OR=1.00,95%CI:0.83~1.21,P=0.98)。
关于干扰素抗病毒治疗相关的血小板减少,有研究表明,治疗期间出现显著血小板减少(血小板计数<50×109/L)的比例为6.1%。值得关注的是,严重出血事件(定义为需要临床干预的出血,如
在罕见情况下,干扰素可能诱发TTP(血栓性
因此,治疗期间需定期监测患者的
综上所述,外周血细胞减少是干扰素治疗中的常见不良反应,曾一度被视为是严重不良反应。然而,进一步研究证实,其发生机制主要与抑制血细胞从骨髓向外周释放有关,因此通常不会引起严重感染,但仍要警惕TTP的可能。目前的治疗策略主要包括减少剂量及对症使用G-CSF或TPO-R激动剂。

3甲状腺功能异常
干扰素治疗诱发的甲状腺功能异常临床表现多样,可表现为甲状腺功能亢进(如
干扰素治疗可通过双重机制诱发甲状腺功能异常。其一为自身免疫性损伤,通过上调主要组织相容性复合体Ⅰ类分子表达和促进B细胞的活化,导致甲状腺过氧化物酶抗体(TPOAb)和
现有研究表明,干扰素α可激活JAK-STAT信号通路,其中IL-6/JAK2/STAT3轴作为免疫调节的核心环节,理论上可能参与甲状腺功能异常的发生过程。在遗传学层面,STAT3基因多态性与自身免疫性
一项纳入384例CHB患者的单中心回顾性研究显示,在接受PEG-IFN-α治疗的患者中,甲状腺功能异常组较功能正常组表现出更优的抗病毒疗效,具体表现为:其血清乙型肝炎病毒表面抗原(HBsAg)低载量(<250 IU/mL)发生率显著提高(29.8% vs
干扰素治疗诱发的甲状腺功能异常与多种危险因素密切相关,其中女性、治疗前高水平TSH、TPOAb阳性被证实为其重要的独立预测因。在临床实践中,此类甲状腺功能异常因其临床表现(如乏力、体重波动、心悸等)缺乏特异性,与CHB的全身症状及干扰素常见不良反应(如流感样症状、情绪障碍等)高度重叠,易导致诊断延迟或漏诊。更为重要的是,当患者进展为药物难治性甲状腺毒症(包括持续性Graves病或
因此,为尽早识别与管理干扰素相关的甲状腺功能异常,建议在治疗前评估患者的基线甲状腺功能及甲状腺自身抗体,并在治疗过程中密切监测相关指标,停药后继续随访至少1年。对于治疗前已存在甲状腺功能异常者,应在内分泌专科医师指导下将甲状腺功能得到有效控制后,再开始干扰素治疗。治疗过程中出现甲状腺功能亢进者可口服
概括而言,甲状腺功能异常是干扰素治疗中较为常见的不良反应,临床表现缺乏特异性。干扰素与甲状腺系统存在复杂的双向调控关系。最近的研究显示,治疗中TSH降低者治疗效果可能更好。在临床管理中,应根据甲状腺功能异常类型实施个体化治疗:甲状腺功能亢进患者需使用抗甲状腺药物,而甲状腺功能减退患者则应接受甲状腺激素替代治疗。

4神经精神症状
PEG-IFN-α-2b治疗过程中,部分患者可能出现一系列神经精神症状,主要表现为三类:情感障碍(如抑郁、焦虑、易激惹)、认知功能障碍(如注意力下降、记忆力减退)以及睡眠障碍(失眠或嗜睡),严重者可能出现幻觉、妄想等精神病性症状。大多数患者的症状轻微,并通常在停药后2~3个月内逐渐缓解。
干扰素通过多途径介导神经精神系统不良反应,其机制主要包括:调控下丘脑-垂体-肾上腺轴功能,干扰5-羟色胺及多巴胺等神经递质的合成与代谢,诱发神经炎症反应,或透过血脑屏障直接作用于神经元。
长期使用干扰素可能导致神经精神症状反复发作,对患者心理健康造成持续影响。其使抑郁症风险增加2~3倍,既往有抑郁病史者复发风险尤甚(aHR=22.2,95%CI:11.2~44.2)。中国台湾地区一项为期12年的大规模队列研究显示,干扰素α诱导性抑郁症缓解者的复发率(56.8/10万人年)显著高于无抑郁症对照组(4.1/10万人年,P<0.001)。
简而言之,干扰素治疗期间需密切监测神经精神症状,其发生机制多样。建议在治疗前筛查抑郁病史等危险因素,治疗期间定期评估精神状况,如出现中度以上抑郁症状[患者健康问卷-9(PHQ-9)≥10分]时,应及时转诊至精神科。对于曾出现干扰素相关神经精神症状的患者,再次使用干扰素复发风险高。因严重精神神经不良反应而停药者,不建议再次使用。

5其他不良反应
除前述主要不良反应外,干扰素治疗还可能引发食欲下降、体重减轻、脱发、皮疹、心律失常、亚临床肾功能改变、肝功能异常等不良反应,此类反应通常在停药后4~8周内自行缓解。根据一项横断面研究结果,在接受干扰素α治疗的CHB患者(n=100)中,尽管存在治疗应答不确定性、潜在不良反应及经济负担等问题,但其生活质量评分显著优于NA治疗组(n=100)及非抗病毒治疗组(n=87)(P<0.05)。这表明,尽管干扰素治疗可能引起多种不良反应,但并未对患者总体生活质量构成显著负面影响,可能与治疗带来的病毒学应答的改善及心理预期效应有关。

6结语和展望
PEG-IFN-α-2b治疗引发的诸多不良反应,涵盖血液、内分泌、神经精神及消化等系统,仍是临床应用中面临的重大挑战。近年来,随着对不良反应机制的深入认识,管理策略已从单纯处理逐步转向为基于风险分层的精准干预:在血液系统方面,采用G-CSF或TPO-R激动剂进行动态干预;针对甲状腺功能异常,基于JAK-STAT通路研究建立了早期分型干预方案;同时,通过PHQ-9构建了神经精神症状的预警与监测体系。
为最大程度实现治疗获益,建议对符合适应证的患者实施全程化管理:治疗前全面评估基线风险;治疗中动态监测血常规、甲状腺功能及心理状态,并建立以感染科为主导,内分泌科、精神科等多学科协作的诊疗模式,以实现不良反应的早期识别与精准干预(图1)。
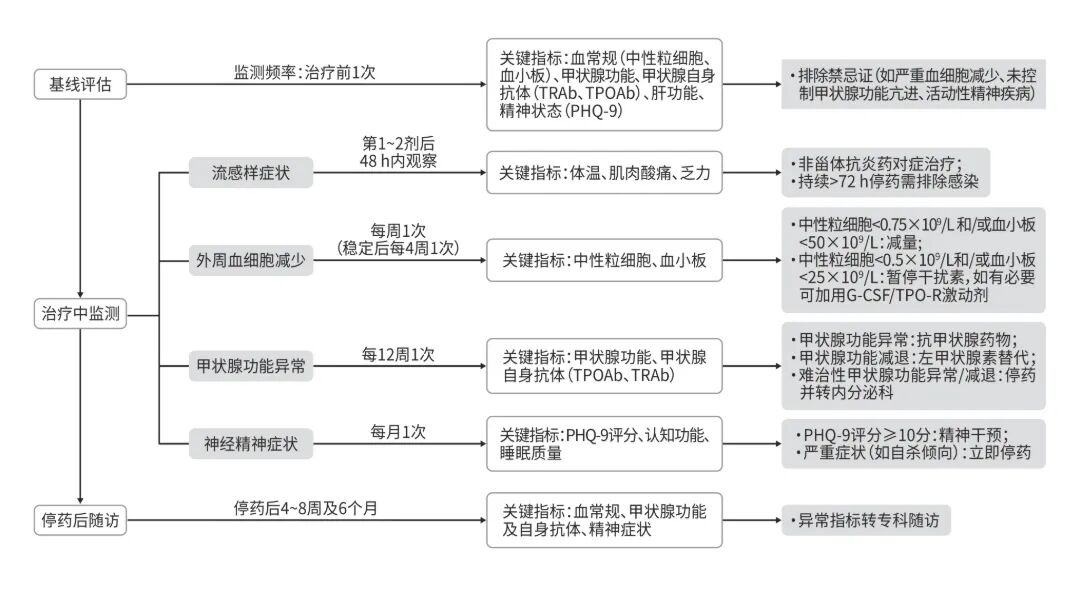
注: TPOAb,甲状腺过氧化物酶抗体;TRAb,促甲状腺激素受体抗体;PHQ-9,患者健康问卷-9。
图1 PEG-IFN-α-2b治疗CHB的不良反应监测与管理策略流程图
值得注意的是,甲状腺功能异常(特别是甲状腺功能亢进状态)与更优的病毒学应答之间存在显著关联,提示其可能不仅是药物不良反应,更反映了机体免疫系统激活的状态。这一发现对“不良反应必然负面”的传统观念提出了挑战,促使学界需重新审视不良反应与治疗效果之间的复杂关联。然而,现有支持证据多为回顾性研究,未来仍需开展样本量更大规模的前瞻性队列研究加以验证。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH260222

李欣怡, 叶卫江, 陈丹蕾, 等. 慢性乙型肝炎患者聚乙二醇干扰素α-2b治疗过程中不良反应的监测与管理[J]. 临床肝胆病杂志, 2026, 42(2): 414-419
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
