前言
然而,临床中约95%的晚期结直肠癌患者属于微卫星稳定(MSS)或错配修复完整(MMRp)型。这类肿瘤通常被认为是“冷肿瘤”,其特征是肿瘤浸润淋巴细胞少、新抗原负荷低。多项研究表明,传统的PD-1/PD-L1抑制剂单药或联合疗法在MSS CRC中的疗效极佳有限。因此,如何打破MSS结直肠癌的免疫耐药,识别该人群中可能获益的特殊分子亚群,并探索如双特异性抗体等新型免疫调节方案,已成为当前胃肠道肿瘤研究的重中之重。本报告详细介绍了一例伴有POLE突变及极高肿瘤突变负荷(TMB)的晚期MSS CRC患者,通过应用PD-1/ICOS双特异性抗体XmAb23104实现了超过2年的深度缓解。
患者基本情况
患者信息:患者为66岁男性,既往体健,无显著慢性病史。
既往病史及治疗史
2019年6月,患者因右侧结肠占位接受手术治疗。术后病理确诊为浸润性腺癌,根据AJCC分期标准评定为IIb期(pT4aN0),患者拒绝行术后辅助化疗。
2019年12月,患者在常规随访检查中发现局部复发及多发性腹膜转移。腹膜结节的病理活检证实了转移性结肠腺癌的诊断。患者于一线和二线分别接受FOLFOX(
由于腹膜及盆腔病灶压迫引起的难以忍受的疼痛,患者还接受了姑息性
入院检查与分子分型
2022年8月,患者因多线治疗失败后病情持续进展,为寻求临床试验机会入院。
入院影像学评估显示,患者盆腔及腹膜存在多处巨大的转移包块,病情危重。基因组分析显示,患者表现为MSS/pMMR,但肿瘤突变负荷(TMB)高达82 mut/Mb。这一数值远高于FDA定义的TMB-H阈值(10 mut/Mb),呈现出超突变特征。
进一步的基因组深度分析显示,患者携带POLE突变,并伴有BRCA1和BRCA2致病性突变,以及KRAS突变,PD-L1表达检测显示为阴性(CPS 0)。
表1 分子生物学分析结果
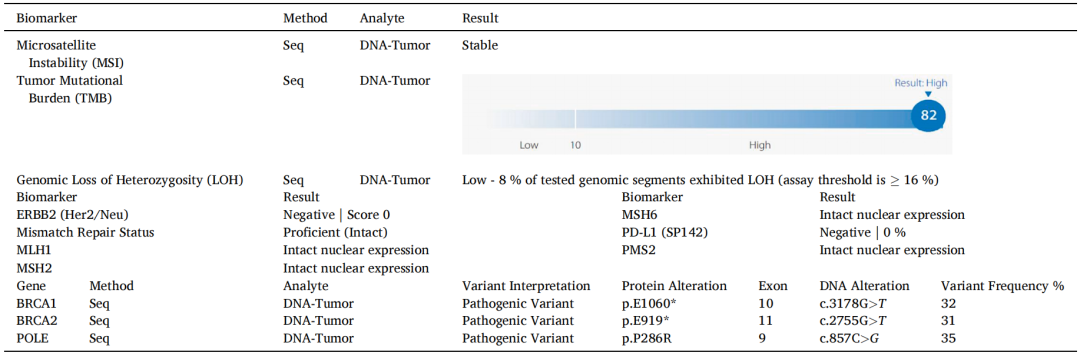
治疗方案与经过
基于上述特殊的分子背景,患者入组DUET-3临床研究(NCT03752398),治疗方案为:XmAb23104(10mg/kg,每3周一次,静脉滴注),在临床试验初期联合使用了伊匹木单抗。
患者于2022年9月正式开始治疗。在完成数个周期的治疗后,首个疗效评估周期的影像学检查即观察到了肿瘤的显著缩小。在完成21个周期的既定研究方案后,该试验终止,但鉴于患者获益显著,研究团队通过单患者扩大的调查性新药程序,确保了患者能够继续接受XmAb23104的单药维持治疗。
疗效评估与安全性
根据RECIST 1.1标准评价,该患者的最佳疗效评价为部分缓解(PR)。影像学数据显示,目标病灶的体积较基线水平缩小了31.7%。
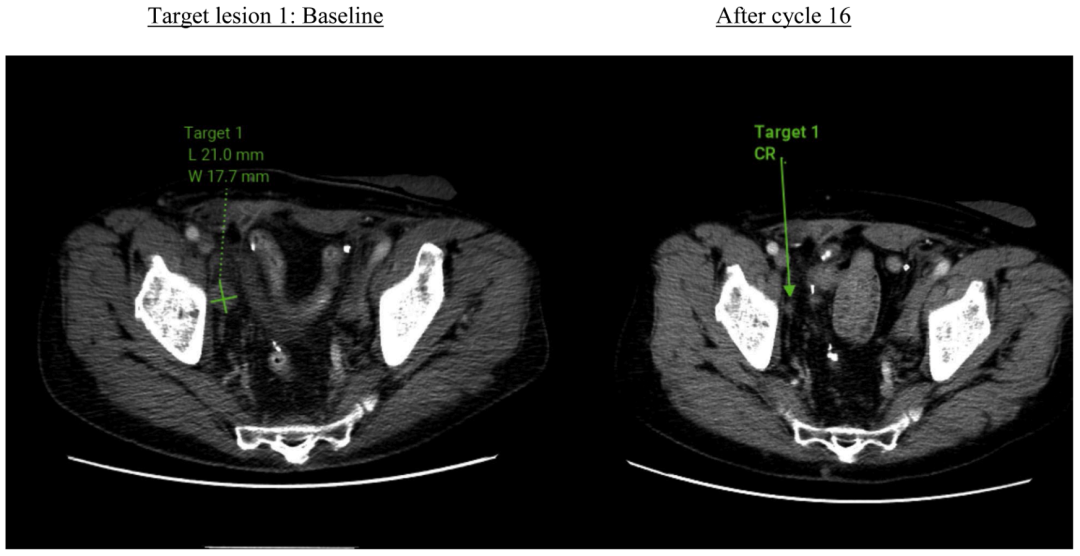
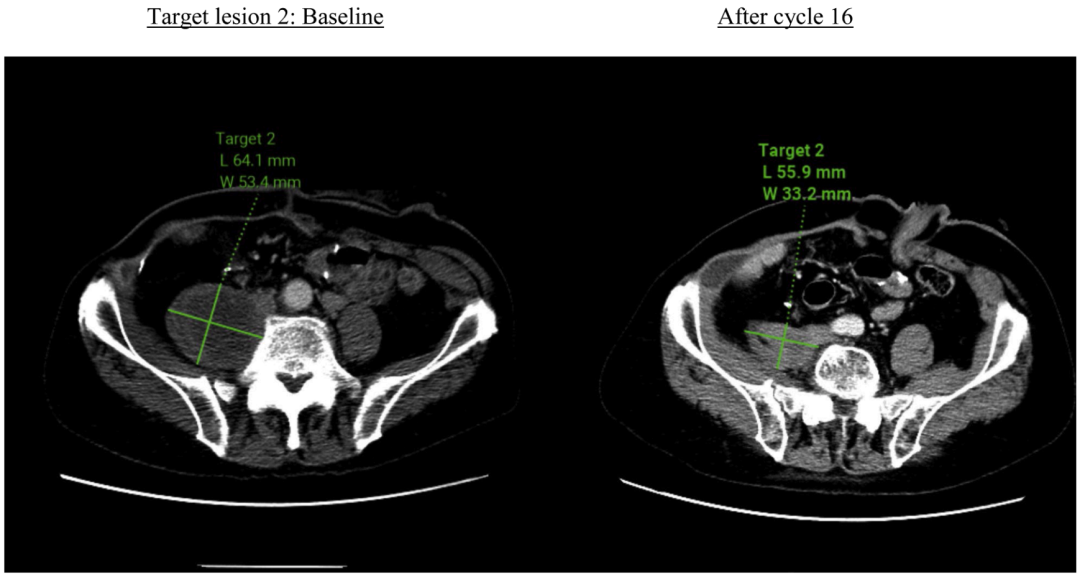
图1 靶病灶退缩情况
在治疗过程中,患者的肿瘤标志物癌胚抗原(CEA)呈现出明显的下降趋势,从入组时的8.2 ng/mL降至4.0 ng/mL,并长期维持在正常范围内。
此外,治疗显示出了令人振奋的疗效持久性。截至2025年9月的最后一次随访,患者的缓解状态已持续超过24个月,且最新一次CT扫描确认病情依然保持稳定。在长达三年的免疫治疗期间,患者表现出极佳的耐受性,未出现任何具有临床意义的免疫相关不良反应(irAEs),如常见的免疫性结肠炎、肺炎、肝炎或内分泌系统损害。患者的ECOG体能评分始终维持在1分,生活质量得到了极大改善。
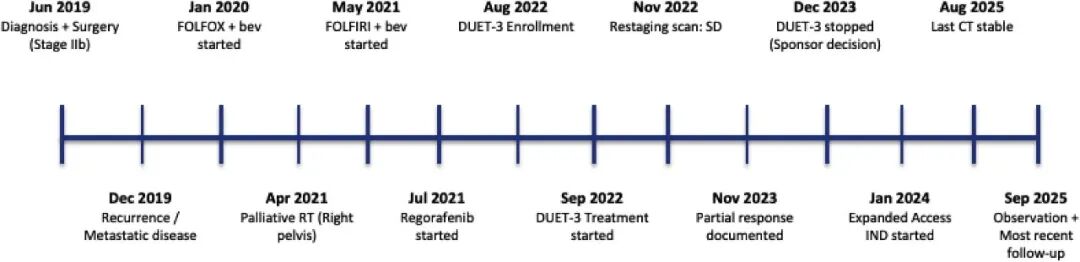
图3 患者治疗全过程
病例讨论
本案例中,一名对多线标准疗法均不敏感的晚期MSS结直肠癌患者,在应用PD-1/ICOS双特异性抗体后获得了长达24个月以上的深度缓解。这一非凡疗效背后的生物学机制值得从基因组学和免疫学两个层面进行深度剖析。
结直肠癌的免疫治疗敏感性长期以来被简单地等同于微卫星状态,然而,本病例证明了肿瘤内在的基因组不稳定性可以跨越微卫星状态,直接影响免疫原性。POLE基因负责DNA聚合酶ε的校对功能。当其外切酶结构域发生特定致病性突变时,DNA复制过程中的校对机制彻底失效,导致全基因组范围内突变激增。这种“超突变”状态虽然在微卫星层面表现为稳定,但其产生的非同义突变数量甚至远超典型的MSI-H患者。海量的新抗原能够显著增加肿瘤组织内的CD8+ T细胞浸润,将原本沉默的“冷肿瘤”在分子层面预加热,使其具备了响应免疫疗法的生理基础。
在免疫调节机制方面,XmAb23104的双重作用路径可能为缓解的持久性提供了保障。PD-1阻断作为一种“解除刹车”的策略,在处理具有高突变负荷的肿瘤时已有明确证据。但ICOS通路的引入提供了关键的协同效应。ICOS是一种在激活的T细胞上表达的诱导型共刺激分子。与PD-1的抑制作用相反,激动ICOS可以促进T细胞的生存、增殖以及促炎细胞因子的分泌。
在POLE突变背景下,肿瘤微环境已经存在大量由于新抗原识别而“预激活”的T细胞,双特异性抗体在阻断抑制信号的同时进一步增强共刺激信号,这种双向调节极大强化了免疫系统的抗肿瘤效能。这种协同增效在传统的单药或简单联合方案中难以实现。
此外,该患者同时携带的BRCA1/2突变亦不容忽视。尽管BRCA突变在结直肠癌中的精准临床价值仍处于探索阶段,但其引发的DNA同源重组修复(DDR)缺陷理论上会进一步加剧基因组的复杂性。DDR缺陷可能不仅增加了突变总量,还可能通过激活cGAS-STING等先天免疫信号通路,增强肿瘤微环境中的炎症状态。
最后,本案例也引发了对TMB作为生物标志物的反思。虽然FDA批准了TMB ≥10 mut/Mb作为免疫治疗的指标,但在MSS结直肠癌中,单纯的TMB水平往往无法转化为临床获益。本案例提示,突变的驱动源可能比单纯的突变拷贝数更为重要。通过对MSS人群进行深度的基因分型,识别出伴有DNA聚合酶突变或DDR修复缺陷的特殊亚群,能够显著提高免疫治疗的精准度和获益概率。
研究结论
本病例报道了一例伴有POLE突变和极高TMB的晚期MSS结直肠癌患者,通过PD-1/ICOS双特异性抗体XmAb23104治疗实现了超过两年的长效缓解。这一成果挑战了“MSS CRC对免疫治疗不敏感”的传统观念,强调了超越MSI状态进行精准分子分型的重要性。未来,针对由POLE/POLD1突变驱动或具有高新抗原负荷的特定MSS亚群,开展基于双特异性抗体的新型免疫疗法临床研究,有望为这部分预后极差的患者群体开辟全新的治疗路径。
参考文献:
1. .Jung S, Gates K, Collins H H, et al. Durable Response to Bispecific PD-1/ICOS Antibody and Ipilimumab in Advanced Microsatellite-Stable Colorectal Cancer: A Case Report[J]. Current Problems in Cancer: Case Reports, 2026: 100414.
撰写:Babel
排版:Babel
执行:Aurora
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)