近期,发表于European Heart Journal(IF:35.6)的一篇综述结合历史趋势和最新突破,对2040年冠状动脉血运重建技术进展进行前瞻性预测。文章梳理了冠脉疾病治疗格局的演变趋势,重点聚焦人工智能与多组学技术的应用价值,并描绘了心肌血运重建的未来图景:诊疗模式高度个体化,技术驱动型介入手段重塑

中心图
未来15年,哪些因素将影响心肌血运重建?其核心在于多组学领域的突破,即基因组学、脂质组学、蛋白质组学和代谢组学。
基因组学与无创影像学的融合催生了新兴学科——影像组学。定量影像生物标志物(如表征脂质坏死核心的低衰减斑块[LAP]、反映血管周围炎症的脂肪衰减指数[FAI])可转化为组织病理学概念,助力高危易感患者识别并提供客观决策依据。在AI时代,从无创影像中提取超越传统形态学的定量生物标志物日益可行。
英国生物银行制药蛋白质组学项目、美国"全民研究计划"、中国嘉道理生物银行、H3Africa计划等大型科研计划共同推动心血管健康向预测性与个性化医学转型。
影像组学将推动血运重建决策革新,在机械血运重建与新兴的"药物性血运重建"间实现精准选择。该体系推动诊疗范式从解剖学阈值向生物学风险分层转变,为精准药物预防方案(单克隆抗体、反义寡核苷酸[ASO]、小干扰RNA[siRNA]、基因靶向治疗)奠定基础。
未来 15 年,心肌血运重建策略的争议与抉择将围绕三大核心要素构成的复杂“三位一体”模型展开:

图1 心肌血运重建的“三角关系”
第一要素是心绞痛对预后的影响。ISCHEMIA与SCOT-HEART试验表明,心绞痛远期危害可能被低估。这可能导致未来减少激进的机械血运重建策略,降低对有创治疗的依赖。
第二要素是心肌冠脉灌注下降,可通过血流储备分数(FFR)、瞬时无波形比值(iFR)、造影衍生FFR(如定量血流比QFR)、FFR-CT、冠脉血流储备(CFR)检出。基于Lance Gould观点,这些生理学指标对不良预后的预测价值日益凸显,将推动更积极的药物/机械干预。
第三也是最具发展潜力的预后要素是高危斑块与易损病变。新版CAD-RADS 2.0共识推动了利用AI开展CCTA量化斑块分析的发展。
过去二十年间,多项试验通过有创与无创诊断工具探索斑块易损性概念,相关争论持续至今。一种前景广阔的策略是CCTA与正电子发射断层扫描(PET)联合应用。该技术可评估血流限制性/非限制性病变的代谢活性以优化预后判断。尽管操作复杂,但CCTA后行¹⁸F-
当前最先进的AI软件解决方案是冠状动脉斑块定量与血流动力学人工智能定量评估系统(AI-QCPHA)。根据EMERALD II研究,AI-QCPHA识别的18项特征可描述易损斑块的解剖学特性及血流限制性病变的血流动力学影响。通过分层聚类分析已明确可有效识别
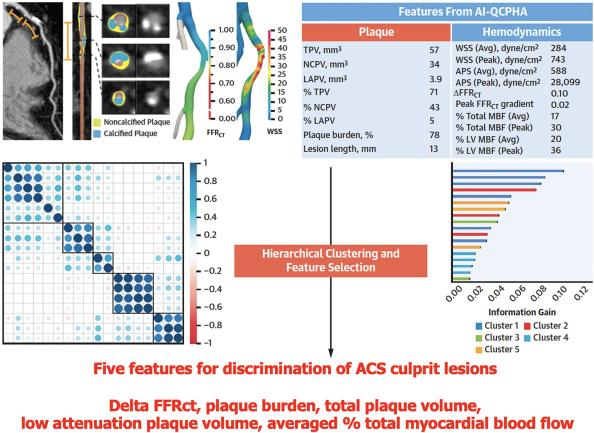
图2 AI-QCPHA
CCTA将发展成为全面的“一站式诊疗平台”,仅需单次影像检查即可完成精细综合评估(图3)。基于其提供的全面诊断信息,临床医生可直接进入导管室实施精密规划的经皮冠状动脉介入治疗(PCI),或无需传统有创
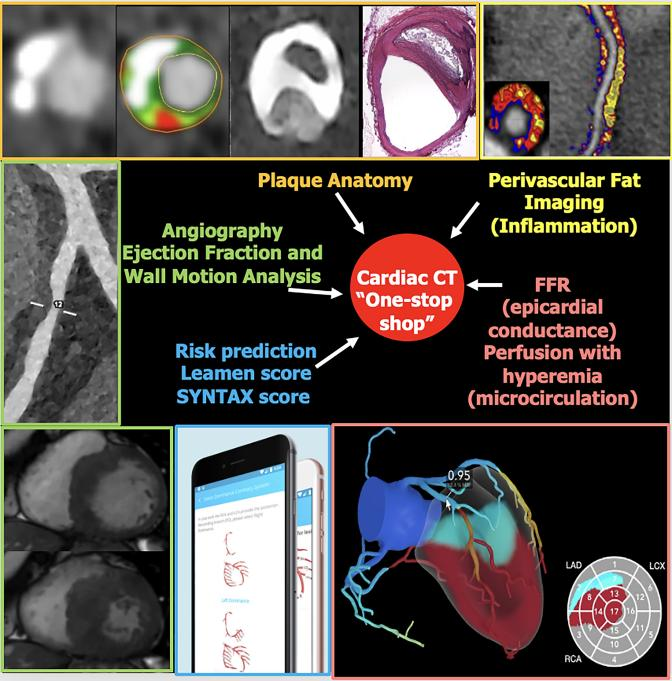
图3 CCTA作为“一站式评估”手段
CCTA衍生的关键参数——左心室心肌血流分布百分比(LV%MYO),可精准量化特定狭窄冠状动脉节段供血区域的缺血心肌范围(图4)。至2040年,CABG术前ICA检查将被淘汰。在新一代CCTA的独立引导下,心脏团队将常规制定CABG、PCI或药物治疗决策。CCTA作为"颠覆性"技术亦可能改变机械血运重建的准入路径。
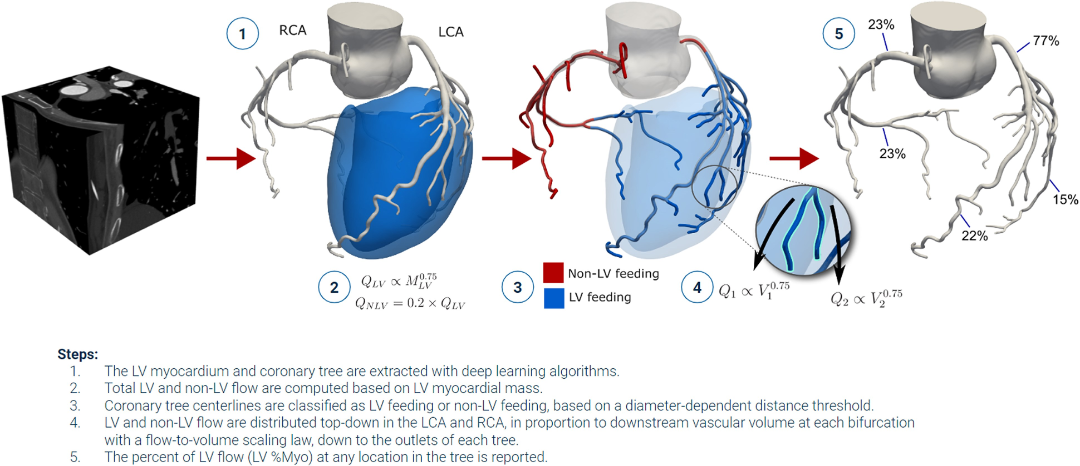
图4 LV%MYO计算方法学流程
近年来,光子计数探测器CT(PCD-CT)技术的出现标志着诊断范式的转变,加速了传统冠状动脉造影(CAG)的淘汰。光子计数技术实现了X射线光子向电信号的直接转换。该技术还能生成钆浓度分布图,可清晰区分梗死心肌与健康组织的差异。PCD-CT现已实现最高0.11mm的平面内分辨率,接近传统ICA空间分辨率(0.2mm)的一半。Vecsey Nagy等人的报告揭示,PCD-CT凭借超高分辨率使49%患者的冠脉疾病报告与数据系统(CAD-RADS)分型得以重新判定。
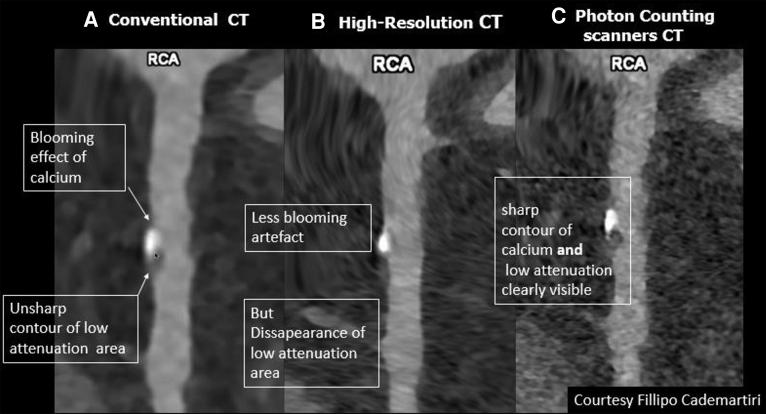
图5 同一患者常规CT、高分辨率CT与PCD-CT对比
核心问题在于:传统血管造影是否仍是评估狭窄病变的金标准?凭借更优的空间分辨率,PCD-CT有望成为新金标准。只有未来能验证此论断的正确性。
分层相位对比CT(HiP-CT)已实现20微米与2.6微米/体素分辨率,潜力可达2.26微米。该技术为理解传导血管与阻力血管的关系提供了新维度,揭示直径<400微米的动脉如何连接主要心外膜血管与心肌组织。
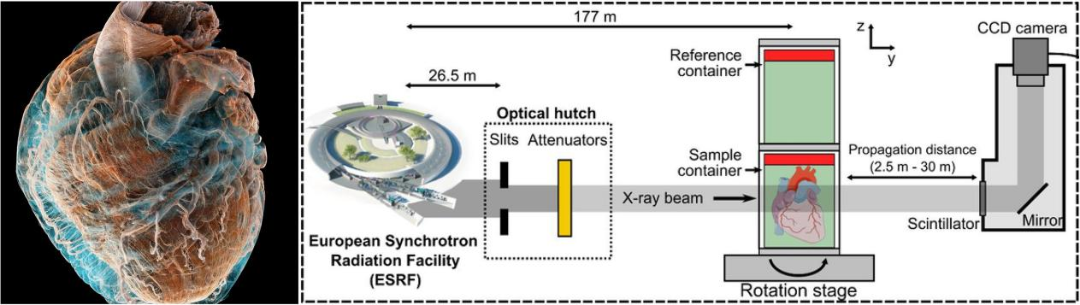
图6 左图:HiP-CT绘制成像(20微米);右图:格勒诺布尔同步辐射装置邻近实验场景
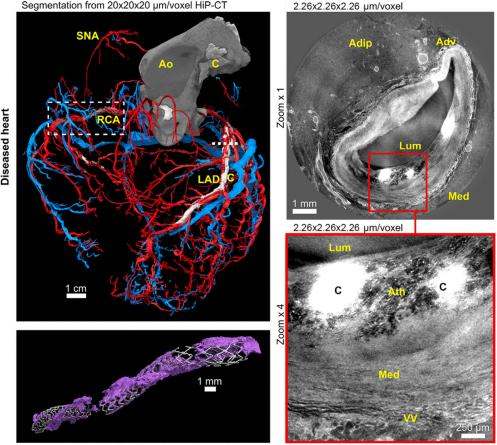
图7右冠脉起源横断面视图(2.26微米),清晰显示脂肪组织层、外膜、中膜及钙化结节与滋养血管
基于HiP-CT可提出假设:无论处于何种炎症状态,血管周围脂肪可能通过机械性牵拉与挤压影响这些微小前动脉及动脉血管的阻力,和/或作为生物活性物质的储存库,释放可诱发微血管网络
对于年轻患者的非钙化性、软性、局灶性脂质斑块,由新型强效抗
相比之下,老年患者将推动机械血运重建需求的增长,因其高发重度钙化斑块及对药物治疗无反应的限流性病变。高压球囊、切割球囊、刻痕球囊,以及定向旋切、旋磨旋切、轨道旋切、激光消蚀和伴或不伴球囊扩张的血管内碎石术,在处理此类复杂病例时仍将发挥关键作用。
过去十年间,全球PCI与CABG临床应用规模已显著下降,该趋势预计在未来15年持续。预计至2040年“无植入”将成主流。即便当下,血运重建技术体系正日趋多元化,融合多种技术策略。
"介入无残留"的愿景依然充满生命力,对生物可吸收技术的探索仍在继续(图8)。所有技术进步皆致力于在减薄支架梁厚度的同时增强其支撑强度。
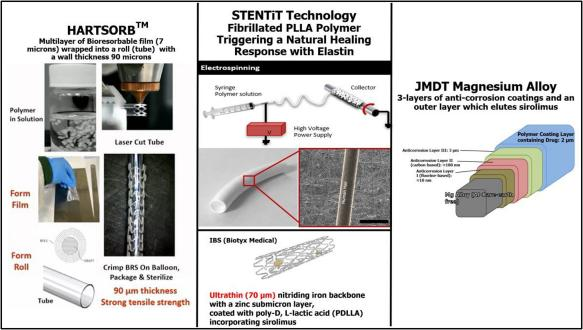
图8 新一代生物吸收支架示例
至2040年,新型材料与方法融入临床实践将改善PCI术后患者的远期预后。但若缺乏系统化培训推广,这些前沿技术将仅局限于科研、专家与产业讨论范畴,难以真正落地常规临床实践。
欧洲经皮心血管介入协会(EAPCI)与ESC心血管外科工作组临床共识声明:现有证据不支持通过PCI开通慢性完全闭塞(CTO)改善预后。迄今开展的RCT在样本量、患者选择偏倚及试验设计方面均存在局限。
心绞痛或
遗憾的是,过去二十年间介入心脏病学家尚未成功整合三类技术:通过成像技术实现闭塞路径可视化(如"Flying through"CT成像、前向光学相干断层扫描或光学相干反射测量);建立消融通道(如射频消融、激光导丝);沿闭塞血管路径导引器械(如磁导航)。介入心脏病学家能否在未来15年借助此三项技术协同应用获得更大突破,并使CTO治疗结局更具可预测性与普适性,仍是一个重要问题。
非ST段抬高型
透视引导PCI在未来二十年仍不可替代,但传统诊断性ICA作为诊断工具的价值将逐渐衰减,终被无创影像技术取代。
ST段抬高型心肌梗死(STEMI)治疗中,快速再灌注至关重要。一项极具前景的创新技术是剪切力激活的纳米治疗剂(SA-NTs)。这类智能纳米颗粒在正常血流中无害循环,而在血栓环境的病理性剪切应力作用下会裂解释放靶向组织型
纵观心梗治疗史(历经冠脉内溶栓、静脉溶栓、溶栓后PCI、直接PCI),若局部高效冠脉内溶栓成为现实,溶栓治疗将完成历史性闭环。
机械循环支持(MCS)在复杂高危PCI(HR-PCI)及
新近发布的DanGer Shock试验结果显示,微轴流泵显著降低6个月全因死亡率,但伴随出血、肢体缺血及肾脏替代治疗需求等并发症增加。亟需通过设备设计创新、安全性提升及精准患者筛选算法以明确MCS临床价值。
正如Holger Thiele在2024年Andreas Grüntzig讲座所言:提升CS救治效果与生存率的关键在于综合策略研究——涵盖预防干预、早期血运重建、特定患者左心室减负及阻断介导CS的炎症因子。
至2040年,由电纺微纤维或可降解超分子材料制备的冠脉旁路移植物将作为"现成耗材"备于手术室,彻底免除患者下肢取静脉之需。既往已在绵羊模型中验证此类移植物的可行性及通畅率。移植物基质可被多种细胞快速定植,激活缓慢的生物降解与生物修复进程。该临床前模型显示,移植物1年组织形态学检查可见内皮细胞存在。首例人体CABG已尝试开展,该技术更在
机器人辅助PCI(R-PCI)的核心优势在于显著降低术者辐射暴露。其屏蔽操作台设计既可改善人体工学,又能减少铅衣长期使用所致的骨科劳损。近期一项荟萃分析证实,R-PCI在手术时长、透视时间、造影剂用量、剂量面积乘积、院内MACE及1年全因死亡率方面,疗效与安全性均与传统PCI相当。
机器人心脏外科手术(主要用于全腔镜CABG)在特定中心已发展为常规手术的可行替代方案。机器人技术凭借更优操作灵活性、
尽管优势显著,机器人血管重建技术仍未得到广泛应用,其大规模推广受限于当前存在的技术局限。就R-PCI而言,主要瓶颈在于无法升级处理复杂PCI手术,且与血管内成像、功能学导丝及斑块修饰装置等先进介入工具不兼容。
尽管部分R-PCI成本效益分析显示其住院费用与传统PCI相当,但R-PCI系统初始成本高且需持续支付高额维护费与一次性耗材盒费用。值得注意的是,主流R-PCI系统之一(Corindus CorPath GRX)因市场接受度低迷已撤市并转向研发。但若广泛应用,此类技术终将实现更快速、可复现且精准的手术操作,从而改善患者预后。
至2040年,器械植入术后P2Y12抑制剂及其他抗凝剂的应用或将成为历史,有望彻底变革介入心脏病学与血管医学领域。这一潜在而大胆的范式转变,源于血管器械仿生CD31衍生肽涂层技术的创新研究。
CD31涂层可模拟健康内皮功能,通过"伪装作用"使植入物避开血液成分识别。该策略促进快速功能性内皮化,且不引发血栓炎症,有望广泛免除血管介入术后抗凝需求(图9)。
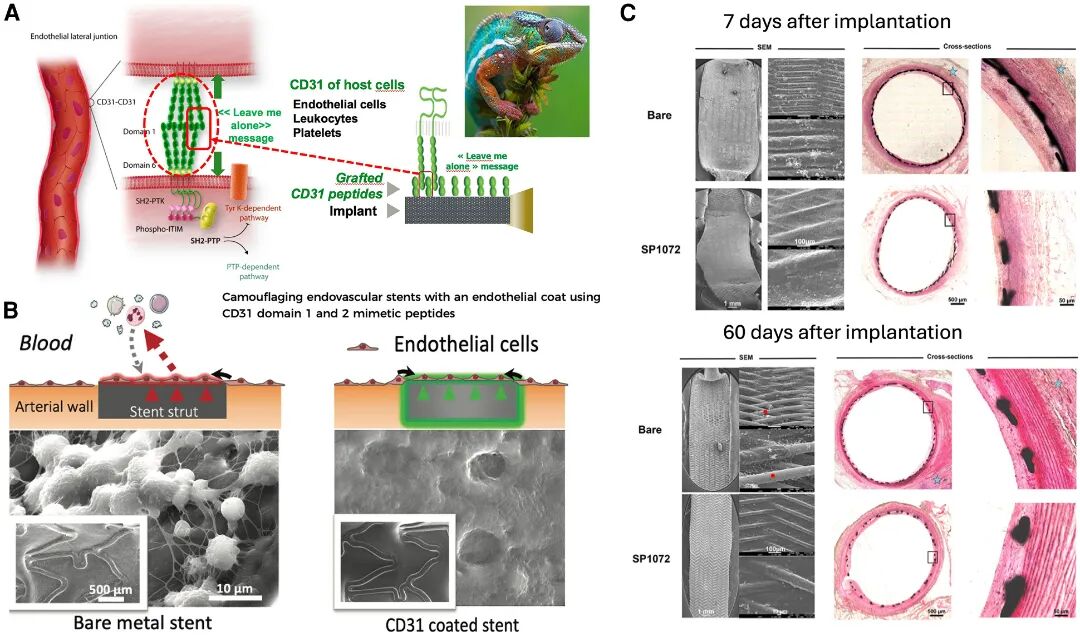
图9 CD31涂层技术
图A:血小板、白细胞与内皮细胞高表达CD31跨膜蛋白;图B:裸金属支架与CD31涂层支架对比;图C:兔模型CD31技术自膨支架7日及60日组织学表现
至2040年,介入导管室将显著提升安全性能,主要归功于光纤实时塑形(FORS)技术平台等突破。FORS技术通过实现导丝、导管等器械的实时无辐射三维可视化,即将彻底革新血管内手术。
FORS技术通常与商用透视系统联用,后者提供静态解剖路图(如
FORS技术目前应用范围限于主动脉及其分支血管与外周肢体血管,而冠状动脉等高度搏动结构则构成额外挑战。
FORS技术可与X射线系统交互并作为执行器运作,使X射线系统将射线束准直于FORS导丝尖端周围,实现极低剂量X线的血管局部评估。此外,此动态实时冠脉循环显像技术已用于无造影剂条件下判断
至2040年,影像技术演进将使模态界限趋于模糊:CMR将接近当前CT成像能力,即使对远端冠脉血管亦展现更优时间与空间分辨率;而新一代CT扫描仪将融合MRI技术特性,具备动态血流与组织成分分析功能。此外伴随AI进步,有创压力测量将日益减少。通过受多重流速影响的流线向量评估血流动力学,AI算法可构建无创压力-容积曲线,用以评估弹性、顺应性及机械功等参数。届时,30分钟MRI检查即可完成综合评估,包括负荷灌注、电影MRI心功能分析、延迟钆增强识别缺血区域梗死灶,以及心外膜大血管解剖成像。至2040年,MRI描绘冠脉解剖的可靠性或将媲美CCTA。
迄今影像整合的障碍在于:无法在手术室中、术者视野内,将影像信息与患者解剖结构进行实景同步定位(图18)。虚拟三维成像或可与机器人技术融合,构建眼-脑-手-机器人共生连接,同时保持术者与手术室真实三维空间的接触。这正是下一阶段的挑战所在。但可以预测,扩展现实(XR)以其多元能力未来将无处不在。
除经皮或外科术者的具体应用外,XR有望整合至心血管疾病诊疗全流程。但XR技术需克服购置与运维成本、医患参与研发不足、系统可靠性等多重障碍,方能在心血管医学领域充分发挥临床价值。
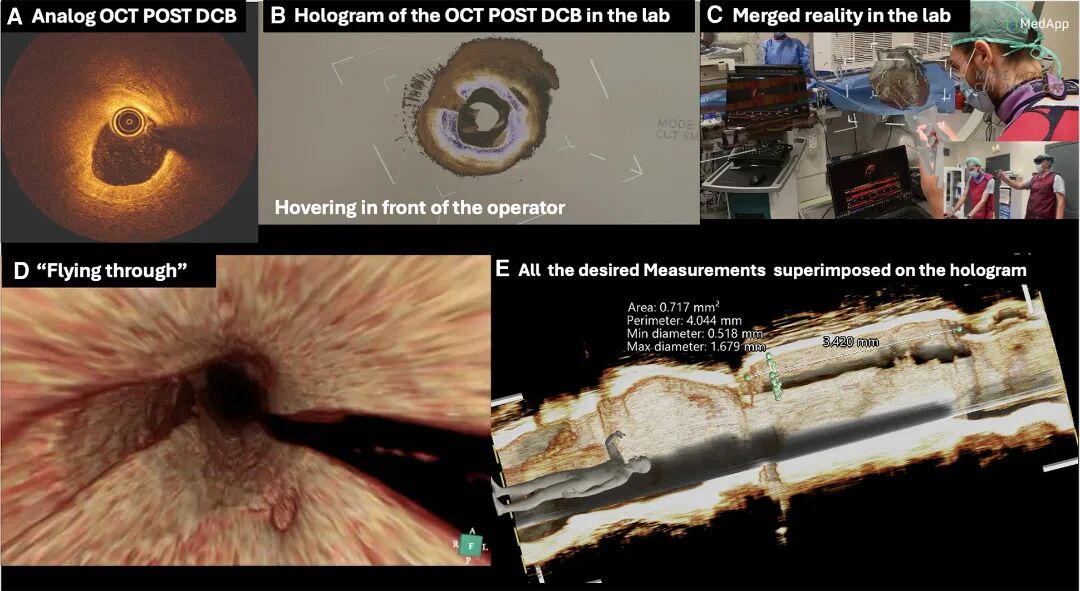
图10 OCT模拟信号(A),经转换为悬浮于术者前方的全息影像(B),与介入手术室实景融合(C),具备"腔内穿行"导航功能(D)并叠加定量参数于全息影像(E)
信源:Patrick W Serruys, Asahi Oshima, Gonçalo Ferraz-Costa, Scot Garg, Tsung-Ying Tsai, Faisal Sharif, Yoshinobu Onuma, Coronary revascularization: a long-term perspective, European Heart Journal, Volume 47, Issue 5, 1 February 2026, Pages 574–593, https://doi.org/10.1093/eurheartj/ehaf883
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)