Metadata Card
文献题目:Calsyntenin-3 suppresses inflammation via inhibition of TLR N-glycosylation and membrane localization
发表期刊:PNAS
发表时间:26.3.18
影响因子:9.6(中科院1区)
通讯作者/单位:
一句话总结:该研究通过全基因组CRISPR筛选发现CLSTN3能通过结合DDOST蛋白干扰OST复合物组装,抑制TLR受体的糖基化与膜转位,从而防止过度的炎症损伤。
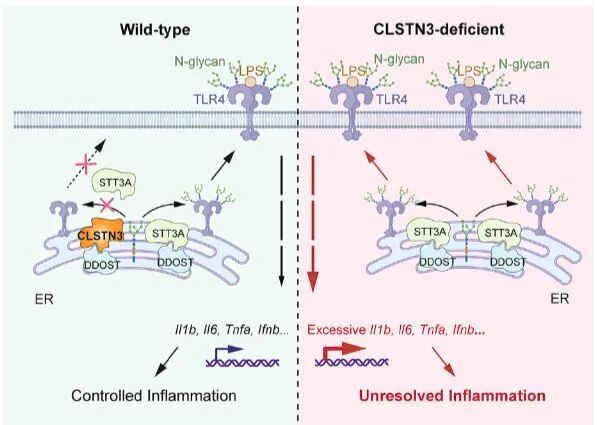
Graphical Abstract
Abstract
中文摘要:
英文摘要:
Excessive innate immune activation drives uncontrolled inflammation and multiple inflammatory diseases. Proper N-glycosylation of membrane-associated Toll-like receptor 4 (TLR4) is essential for its trafficking to the cell membrane and subsequent innate activation, yet the mechanisms regulating this process remain poorly understood. Through a genome-wide CRISPR screening, we identify calsyntenin-3 (CLSTN3) as a potent suppressor of TLR4-triggered inflammation in macrophages. Mechanistically, CLSTN3 binds to the oligosaccharyltransferase (OST) subunit DDOST, inhibiting its interaction with the catalytic subunit STT3A and impairing OST complex assembly, which reduces N-glycosylation and membrane translocation of TLR4. Furthermore, CLSTN3 also suppresses membrane translocation and activation of other TLRs, including TLR3, TLR7 and TLR9. In addition, CLSTN3 expression is reduced in multiple inflammatory diseases and correlates negatively with the cytokine expression in sepsis. Our findings reveal CLSTN3 as a potent suppressor of inflammation by controlling membrane-associated TLR translocation via glycosylation inhibition, presenting a target for intervening inflammatory diseases.
Background & Problem
背景:先天免疫受体(如TLR4)在感知病原体和启动宿主防御中至关重要。TLR4必须从内质网转位至细胞表面才能有效发挥作用。
痛点:尽管已知N-糖基化对受体贩运至关重要,但细胞如何精确调控这一过程以防止炎症过度激活仍不清楚。目前针对先天免疫信号通路的疗法难以实现对难治性炎症疾病的长期缓解,因此亟需寻找调控受体定位的新靶点。
Methodology
策略:研究者建立了含有NF-κB荧光报告系统的巨噬细胞系 (RAW264.7),利用全基因组CRISPR敲除库 (GeCKO) 筛选影响炎症消退的关键基因。
逻辑:筛选发现抑制因子(敲除后炎症增强)→ 聚焦膜相关分子 → 验证CLSTN3的功能 → 探究对TLR4转位的影响 → 通过蛋白质组学(IP/MS)寻找互作蛋白(DDOST)→ 阐明干扰OST复合物组装的机制 → 临床样本验证。
Key Results & Interpretation
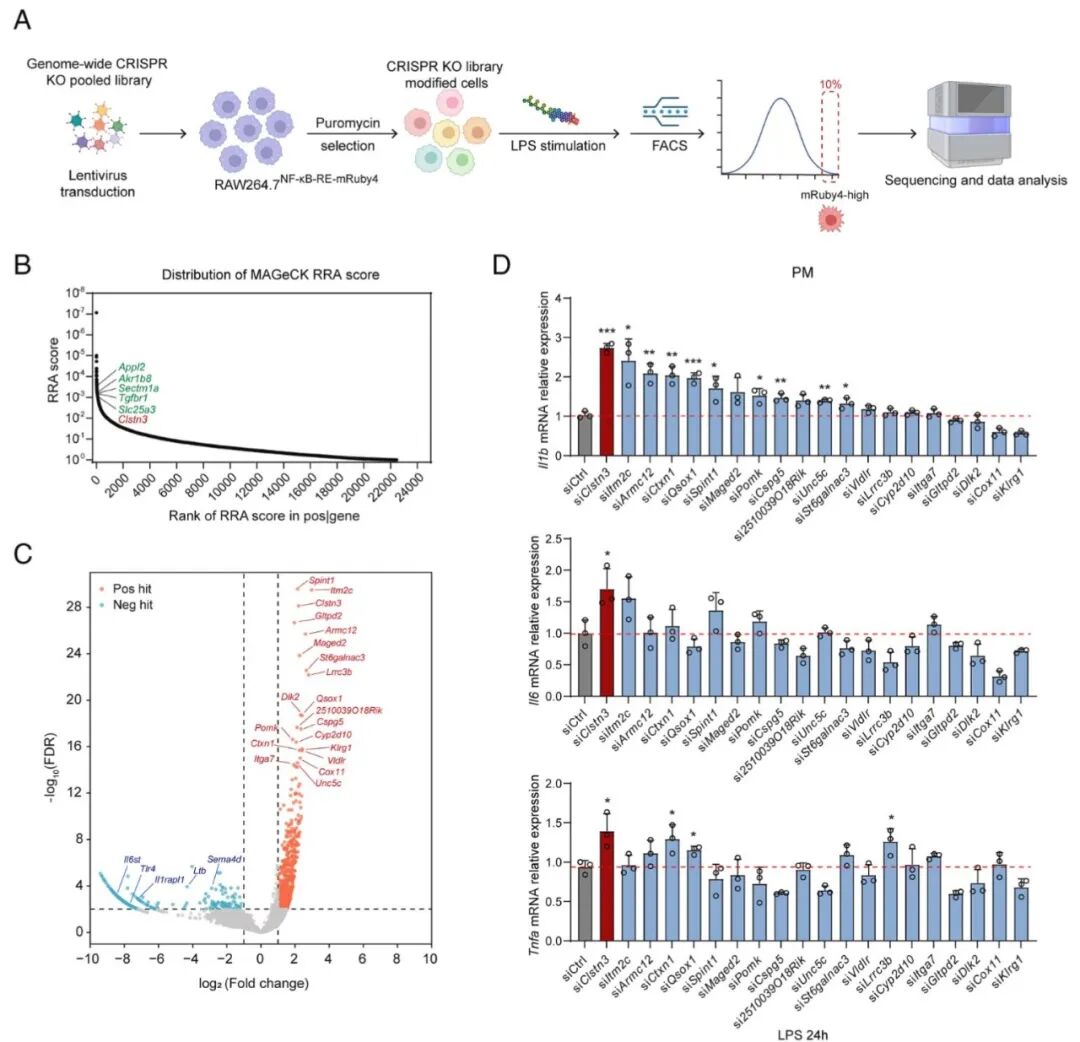
[1A]:展示了筛选流程:在带有 NF-κB 荧光报告系统的 RAW264.7 细胞中转导 GeCKO 慢病毒库,LPS 刺激 24 小时后通过 FACS 分选出 10% 荧光最强的细胞进行测序分析。
[1B]:MAGeCK RRA 评分结果显示,包括 Appl2、Sectm1a 在内的已知抑炎基因显著富集,证明了筛选系统的可靠性,同时发现了候选基因 Clstn3。
[1C]:通过火山图对膜相关基因进行深入分析,识别出多个正向(红点)和负向(蓝点)命中基因,其中 Clstn3 作为潜在的炎症抑制因子被锁定。
[1D]:在小鼠原代腹腔巨噬细胞 (PMs) 中利用 siRNA 敲低前 20 名候选基因,结果显示敲低 Clstn3 后,LPS 诱导的 Il1b、Il6 和 Tnfa 水平提升最为显著。
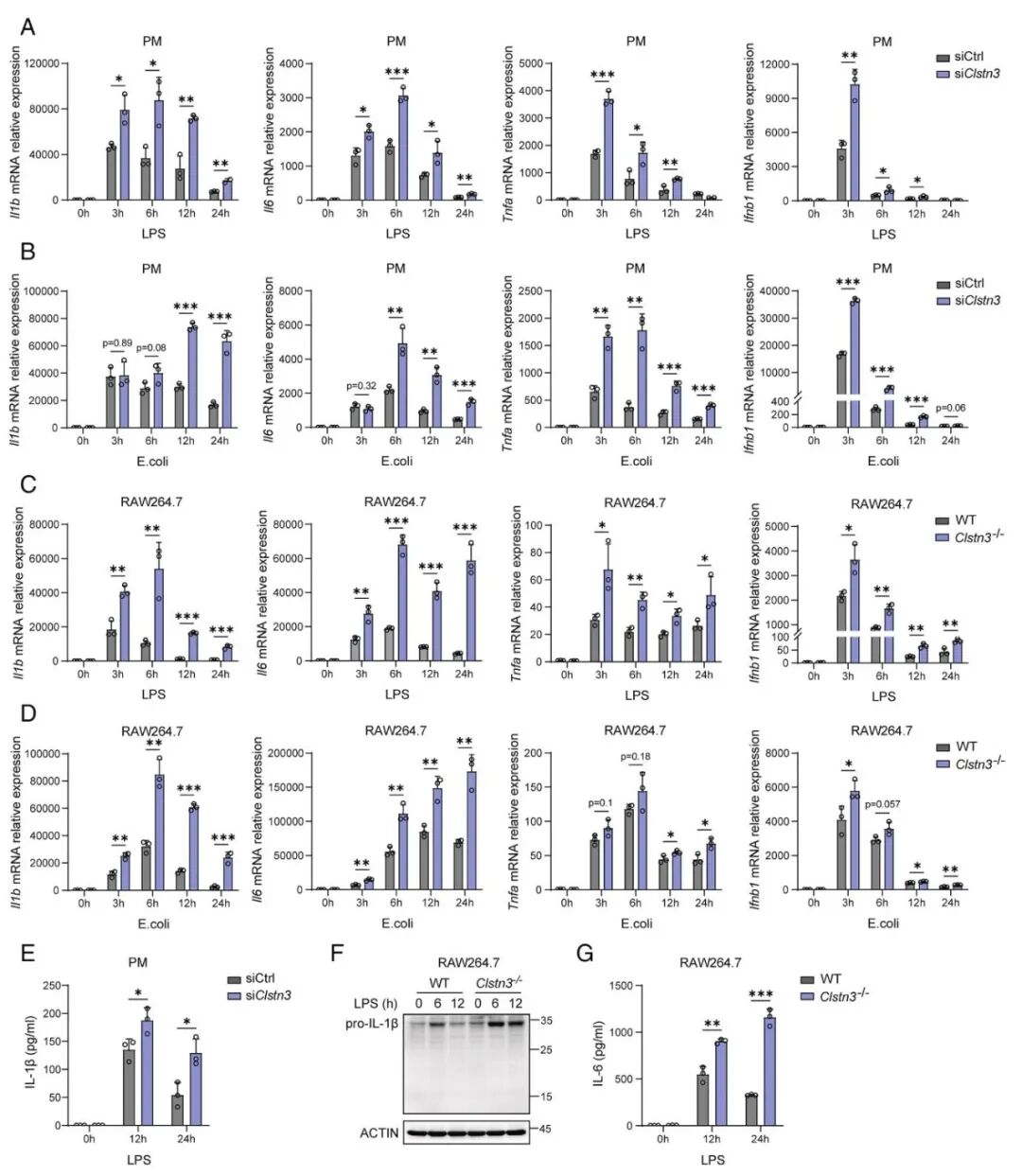
[2A-D]:时间梯度 RT-qPCR 表明,无论是在原代 PMs 还是 RAW264.7 细胞中,敲低或敲除 Clstn3 均显著上调了 LPS 或
[2E-G]:ELISA 和免疫印迹实验进一步证实,CLSTN3 缺失显著增加了上清液中成熟 IL-1β 和 IL-6 的蛋白水平。
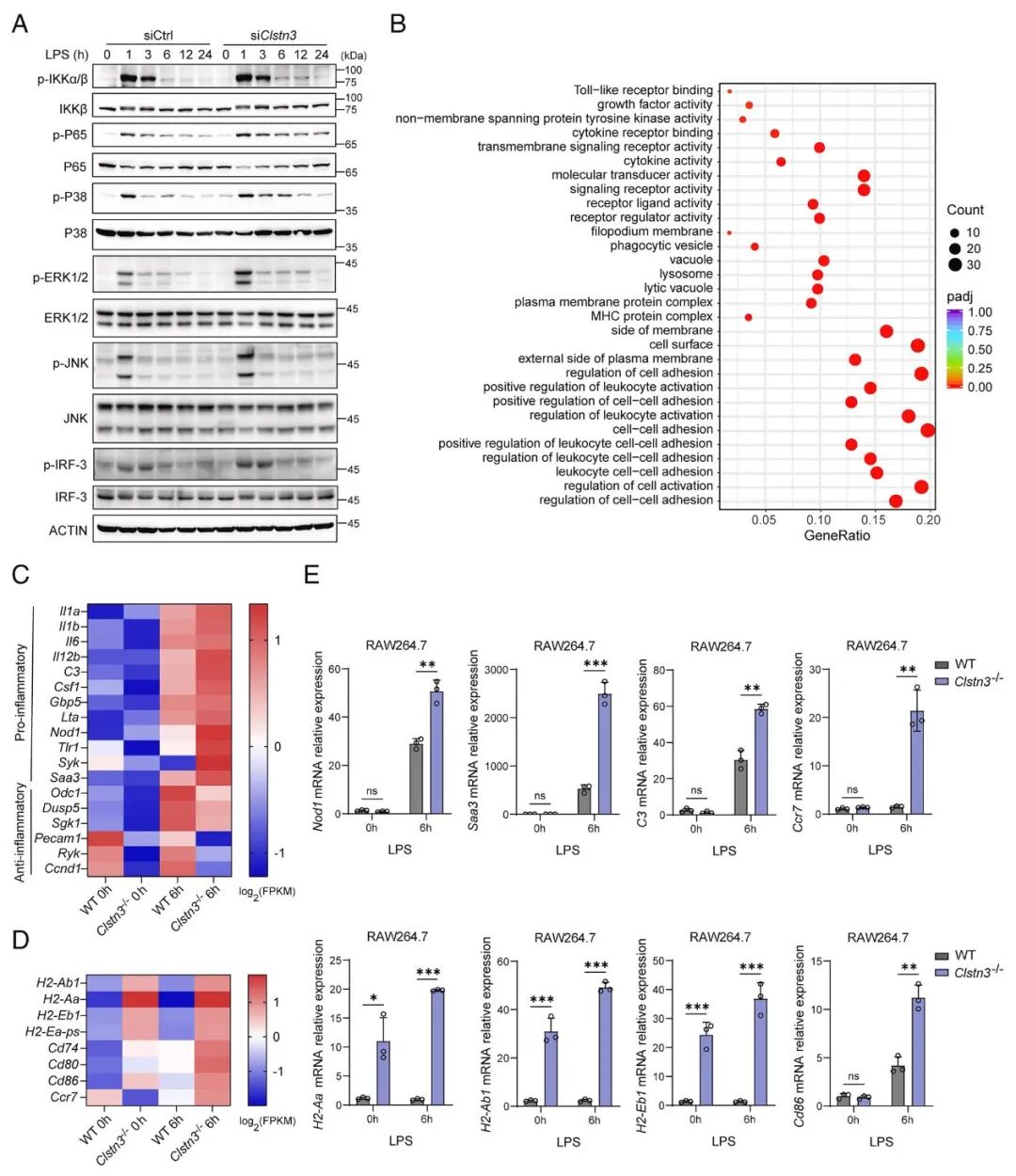
[3A]:信号通路分析显示,在 LPS 刺激下,CLSTN3 缺失细胞中 MAPK 家族(P38、ERK1/2、JNK)、NF-κB(IKKα/β、P65)以及 IRF-3 的磷酸化水平显著增强。
[3B-E]:RNA-seq 及 GO/KEGG 分析揭示 CLSTN3 缺陷细胞处于高度促炎状态,且多种细胞表面标记物(如 MHC II、Cd86、Ccr7)表达升高。
发现点3:CLSTN3 通过限制 TLR4 的细胞膜定位来调控炎症阈值
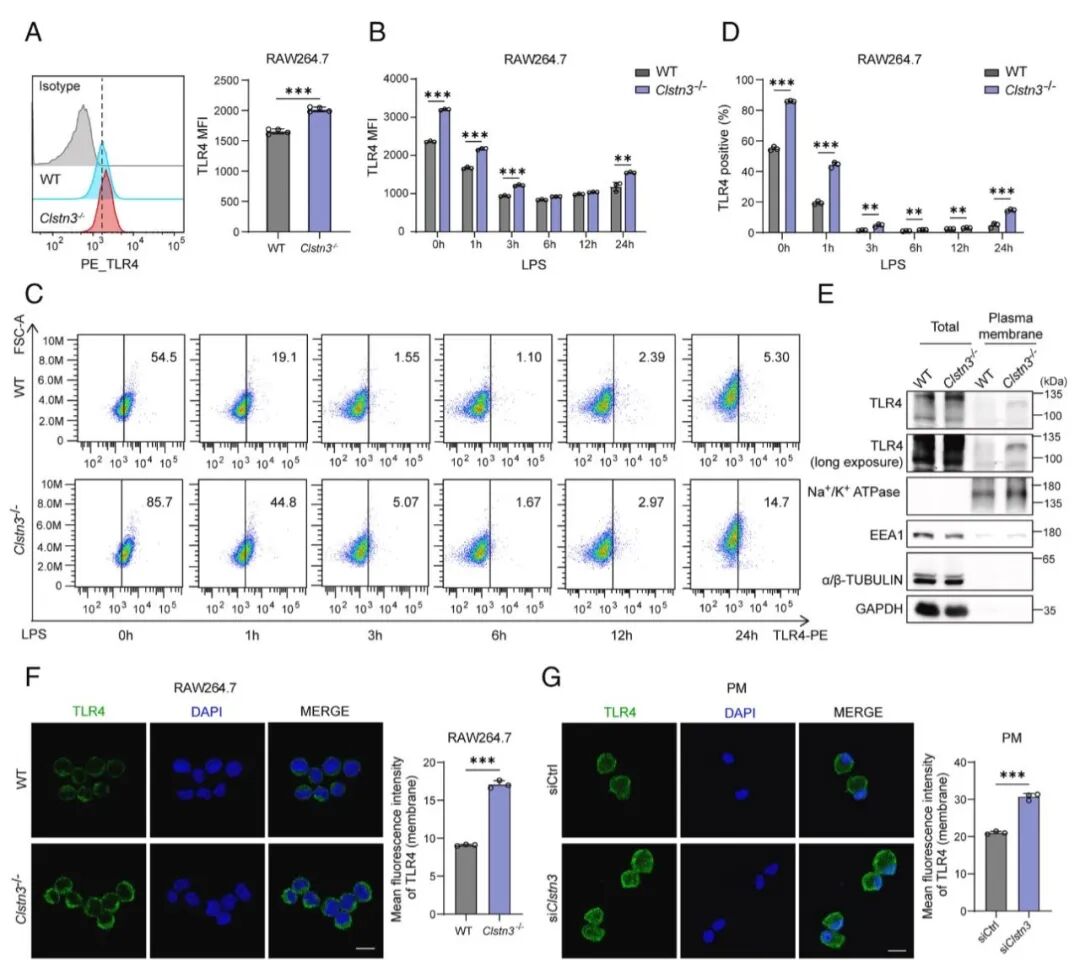
[4A-D]:流式细胞术分析表明,在稳态和 LPS 刺激过程中,CLSTN3 缺陷细胞表面的 TLR4 荧光强度 (MFI) 及阳性率均显著高于对照组。
[4E]:细胞膜蛋白组分提取后的免疫印迹实验确认,膜组分中的 TLR4 蛋白量在 CLSTN3 缺失后显著增多。
[4F-G]:免疫荧光共聚焦成像直观展示了在 RAW264.7 和原代 PMs 中,TLR4 在细胞膜上的分布密度因 CLSTN3 缺失而显著增加。
[后续排除实验]:补充数据表明,CLSTN3 不影响 TLR4 的 mRNA 转录、半衰期、核输出或蛋白降解途径(如溶酶体降解)。
发现点4:CLSTN3 通过抑制 N-糖基化阻断 TLR4 的膜转位
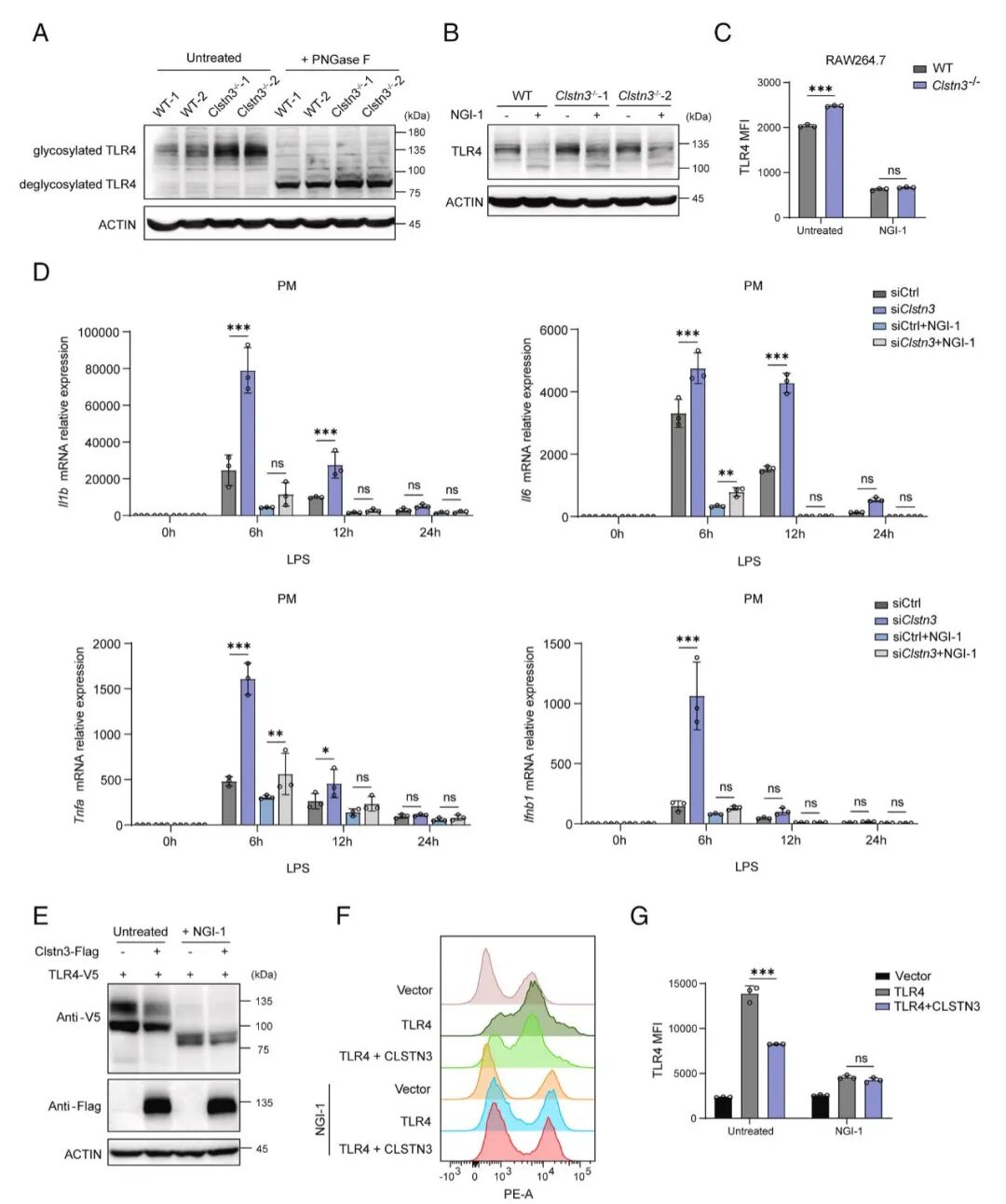
[5A]:免疫印迹显示,CLSTN3 缺失导致 TLR4 出现明显的“高度糖基化”(条带上移),而经 PNGase F糖苷酶处理后,该差异消失。
[5B-C]:使用 OST 抑制剂 NGI-1 处理后,CLSTN3 缺失导致的 TLR4 高度糖基化及其在细胞表面的高表达均被逆转。
[5D]:功能性回补实验显示,NGI-1 处理能够有效抵消因 CLSTN3 缺失而产生的过量促炎细胞因子。
[5E-G]:在 HEK293T 异源表达系统中,过表达 CLSTN3 可显著降低 TLR4 的糖基化水平和膜定位,且该效应可被 NGI-1 进一步模拟。
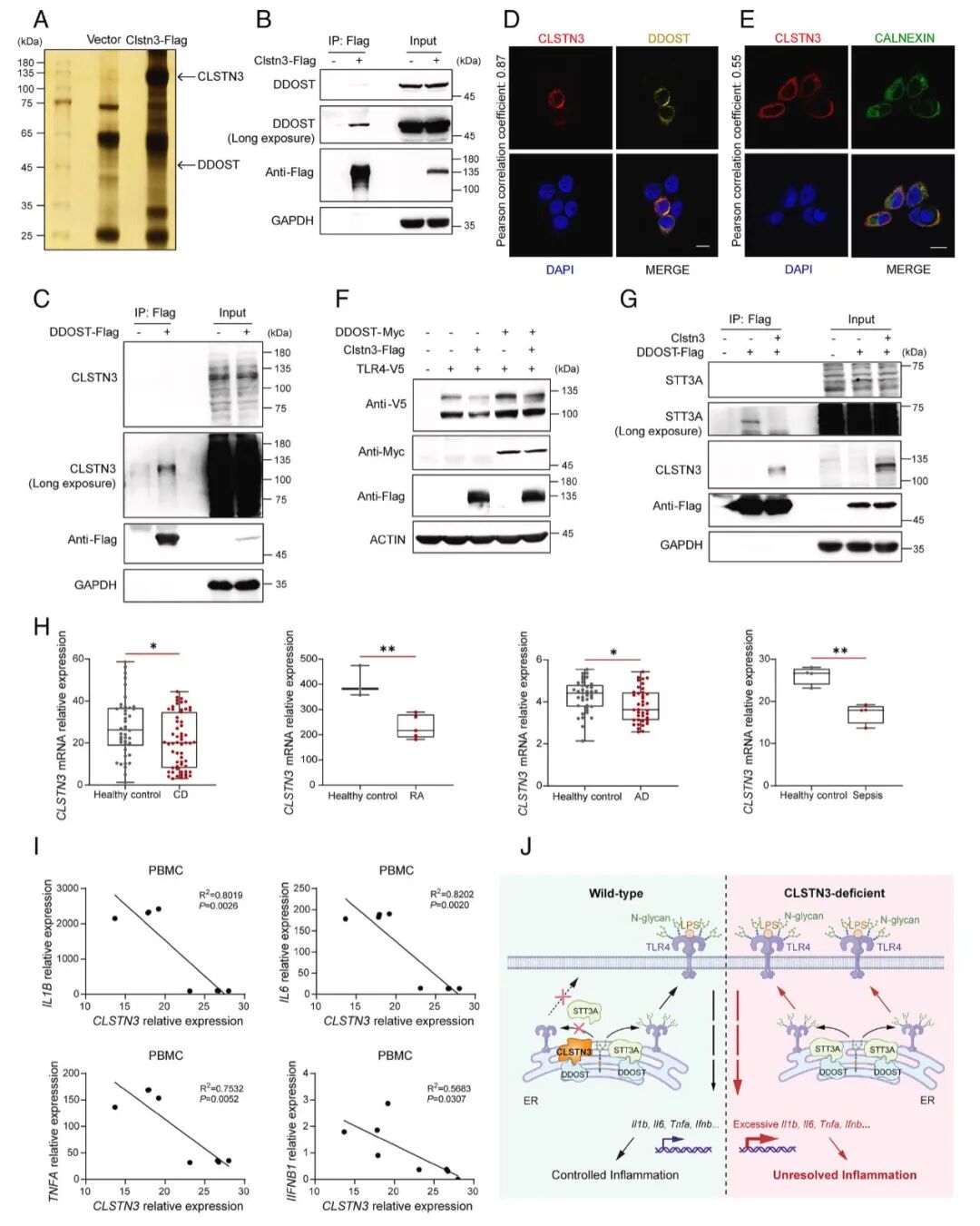
[6A-C]:质谱筛选及Co-IP验证发现,CLSTN3能够与OST复合物的关键非催化亚基DDOST发生内源性结合。
[6D-E]:免疫荧光共定位分析显示,CLSTN3与DDOST高度共定位,且主要定位于内质网 (ER)。
[6F]:竞争性实验证明,过表达CLSTN3会显著抑制DDOST介导的 TLR4 糖基化增强效应。
[6G]:CLSTN3的存在显著削弱了DDOST与催化亚基STT3A之间的相互作用,从而破坏了OST-A复合物的完整组装。
[H-I]:临床相关性分析显示,CLSTN3在 RA、CD、AD 和脓毒症患者中表达显著下降,且其表达水平与患者血清中 IL1B、IL6 等因子的水平呈显著负相关。
Innovation & Takeaway
✨ 创新点
1.首次揭示了传统认为在突触发育中起作用的CLSTN3在免疫系统中的重要功能。
2.从蛋白质转运的“源头”——内质网内的糖基化修饰入手,发现了调控TLR定位的内源性新靶点。
3.该机制不仅适用于TLR4,还涵盖了TLR3、7、9等多种膜相关受体。
✨ 科研启示
本研究提醒我们,许多神经系统蛋白可能在免疫系统中扮演着未被发掘的跨界角色。内质网内的翻译后修饰(如糖基化)是先天免疫反应的精细调节开关。
✨ 临床/应用价值
CLSTN3在多种炎症疾病中表达下降,预示着它可能成为脓毒症或自身免疫性疾病的诊断标志物。未来开发模拟CLSTN3功能的小分子或通过基因疗法回补CLSTN3,或许能成为治疗过度炎症反应的新策略。
局限性
OST复合物负责全细胞数千种蛋白的糖基化,CLSTN3如何实现对特定TLR受体的选择性调控而不同时干扰
潜在副作用风险,长期干扰OST组装可能引发大规模蛋白质稳态失衡或细胞毒性,而文中缺乏对此类代谢损伤的系统评估
对于CLSTN3抑制TLR7和TLR9的具体分子细节仍需进一步挖掘,CLSTN3是否与OST复合物的其他亚基存在相互作用,及其对OST-B复合物的影响也未得到完全阐明。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)