血管加压素(Vasopressin)作为一种非肾上腺素能血管加压药,在特定CS表型中可能具有重要治疗价值。药物策略须根据休克病因及表型个体化定制,因尚无普适性治疗方案。
近期,发表于ESC Heart Fail的一篇综述整合当前证据,重点阐述了血管加压素在CS复杂情境下的药理机制、临床应用及潜在不良结局。重点剖析血管加压素具治疗优势的临床场景,支持以病理生理学为导向的个体化治疗策略。
血管加压素,也称为
AVP通过结合G蛋白偶联受体(GPCRs),即V1a、V2和V3(旧称V1b)受体,发挥其多样的生物学效应,这些受体可激活不同的细胞内信号通路,并表现出特异性组织分布。
临床上可用的AVP制剂为水溶液,用于持续静脉输注,通常浓度为20单位/ml。给药前需用生理盐水或含
药代动力学方面,AVP的血浆半衰期约为10min。其部分在肝脏和肾脏中代谢,主要通过肾脏排泄。
AVP的强效血管收缩作用(主要通过V1a受体介导),可能导致显著的不良反应,尤其在高剂量或长期使用时。
缺血并发症是最受关注的不良反应。约8–10%的患者报告肢端缺血,10–20%可能出现肠系膜缺血。早期识别至关重要,应密切监测血清乳酸水平,仔细评估新发或加重的腹痛、腹胀及麻痹性
心肌缺血虽然相对少见,但可能因体循环后负荷增加而发生,尤其是在既往有CAD病史的患者中。
虽然AVP诱导V1a受体激活血小板理论上可能增加血栓风险,但不同休克状态的临床研究中,并未记录到患者血栓栓塞事件发生率增加。
在CS领域,支持AVP使用的证据仍然较少,且主要限于回顾性研究(表1)。
表1 AVP用于CS的研究证据
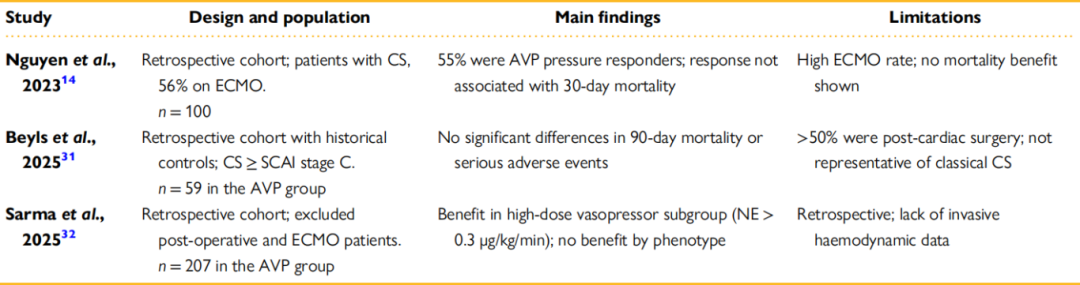
这些研究发现提示,在晚期CS(尤其需高剂量血管加压药,提示SVR降低及潜在混合性休克状态)患者中,AVP可能通过提高灌注压或减少儿茶酚胺用量带来一定获益。但现有证据仍非常有限。
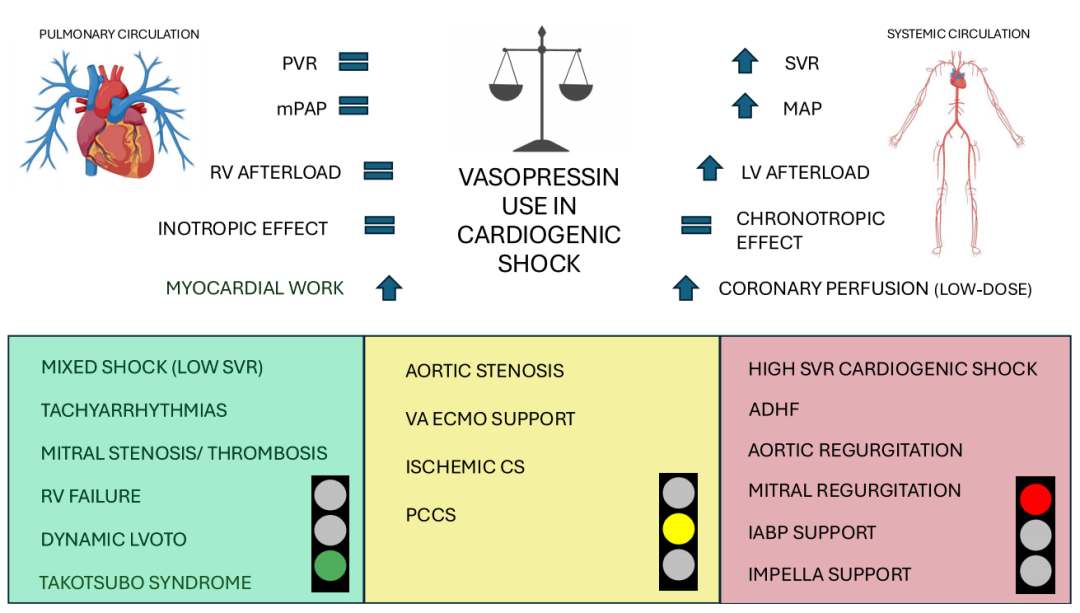
图1 CS中AVP的潜在血流动动力学效应及临床情景
绿色显示AVP可能有益的临床表型(左图)。红色显示AVP可能有害的情况(右图)。黄色显示使用须仔细评估(中间图)。ADHF,急性失代偿性

图2 基于休克学术研究联盟(SHARC)的AVP治疗CS流程
AMI,

此类CS由急性心肌梗死(AMI)引起,其原因可为急性缺血损伤引起的严重收缩功能障碍、梗死机械性并发症或与梗死相关
关键临床信息:AMI相关CS应优先考虑快速解除病因和早期机械循环支持(MCS),并使用左侧经皮心室辅助装置(pVAD)进行左室减负。当出现机械性并发症(如室间隔穿孔[VSR]或乳头肌断裂)时,禁用AVP。

对于急性失代偿性心力衰竭(ADHF)导致、SVR升高(通常SVRI > 2200 dyn·s·cm⁻⁵・m²)的CS,AVP通常不作为首选药物。此类情况应优先选择正性肌力药与血管扩张剂。
关键临床信息:低心输出量(CO)、高SVR患者须禁用AVP。
约25%的CS患者会进展为混合性休克(即初始心源性休克演变为分布性-炎症性休克),其院内死亡率显著更高。其血流动力学特征表现为:低CO、高充盈压、低SVR,即SVR较CO程度相对过低且不足以维持适当MAP。
关键临床信息:混合性CS需高剂量去甲肾上腺素(NE≥0.3 μg/kg/min)时,可考虑添加AVP(但证据有限)。
AVP在合并动力性左心室流出道梗阻(LVOTO)的CS患者中可能有特别治疗价值。
典型例子是主动脉瓣置换术后出现的所谓“自杀性左心室”。治疗通常包括BB与扩容以增加前负荷,但通过纯血管加压药(如AVP或
同样,肥厚型阻塞性
据报道,
关键临床信息:在动力性LVOTO引起的CS中,AVP或去氧肾上腺素应被视为首选的血管加压药。
关键临床信息:TTS合并LVOTO与CS时,可将AVP作为一线血管加压药与短效BB联用;必要时考虑采用左侧经皮心室辅助装置(p-VAD)行机械循环支持。

是由心肌顿抑、缺血-再灌注损伤及体外循环相关全身炎症反应共同驱动的低CO状态,常引发严重血管麻痹,加重泵功能衰竭。术前
关键临床信息:PCCS中若以血管麻痹为主或合并右心室功能障碍时考虑使用AVP,同时评估早期MCS;单纯左心泵衰竭禁用AVP。

相反,AVP在心搏骤停后综合征管理中可能有重要价值。此时AVP有助于恢复血流动力学稳定,尤其当儿茶酚胺类药物因心律失常复发风险受限时。AVP对室性/室上性快速性心律失常所致血流动力学不稳定患者也可能有益。当快速性心律失常以右心衰竭为主时,AVP对肺血管阻力的中性效应使其更具优势。
关键临床信息:心脏骤停期间禁用AVP;心搏骤停后综合征可考虑AVP;持续存在或反复发作的快速性心律失常所致血流动力学不稳定可考虑AVP。
在严重瓣膜病变所致CS中,AVP可在特定情况下使用。当降低后负荷有益时(如急性重度二尖瓣[MR]或主动脉瓣反流[AR]),通常不宜使用AVP。
重度
关键临床信息:急性重度MR或AR所致CS禁用AVP;重度MS、左心室流入道梗阻或重度AS可考虑AVP。
心包填塞是一种血流动力学急症,心包内压升高损害舒张期充盈并快速抑制CO。确定性治疗为紧急心包引流。心包穿刺术准备期间,可通过补液与血管升压药进行短期稳定;去甲肾上腺素或为首选,因其通过α受体介导的静脉收缩增强静脉回流,同时提升MAP。
关键临床信息:虽有药理学依据,但AVP用于PE相关休克缺乏临床证据;去甲肾上腺素为一线血管加压药。
MCS常用于病情加重或难治性CS病例。
主动脉内球囊反搏(IABP)主要通过降低左心室后负荷提供心脏支持,其升高
静脉-动脉体外膜肺氧合(VA-ECMO)常需血管加压药维持足够MAP。ECMO多用于晚期CS或难治性心脏骤停,此类场景常伴全身炎症反应。在难治性心脏骤停动物模型中(复苏30分钟后启动VA-ECMO),与去甲肾上腺素相比,AVP给药与更快乳酸清除、减少液体需求及降低低
关键临床信息:IABP或左心室Impella支持患者应避免使用AVP;伴血管麻痹的VA-ECMO患者可考虑使用AVP。
未来应优先开展前瞻性、实用性、结合生物标志物与表型分层的研究。
入组目标应包括:低心脏指数伴不适当SVR低的混合性休克、以血管麻痹为突出表现的PCCS、重度AS伴低血压、以及右心衰竭所致休克。需通过循环生物标志物(肾上腺髓质素、血管生成素-2、和肽素)联合有创血流动力学或
关键终点应涵盖:无器官支持存活天数、急性肾损伤与肾脏替代治疗需求、具临床意义的快速性心律失常、ICU住院时长及30天死亡率。对接受MCS患者进行预设亚组分析至关重要。

采用病理生理学导向的思路,对于判断AVP在哪些CS中可能获益或可能存在潜在危害至关重要。尽管现有证据有限且多源自回顾性研究,但在以下情况中AVP或具重要价值:伴SVR降低的混合性/晚期CS、快速性心律失常、右心衰、TTS、重度AS、二尖瓣流入道梗阻及动力性流出道梗阻。
信源:Simone Filomia, Marco Giuseppe Del Buono, Gianluigi Saponara, Alessia d’Aiello, Daniela Pedicino, Francesco Moroni, Antonio Abbate, Tommaso Sanna, Vasopressin in cardiogenic shock: pathophysiology, clinical evidence, and therapeutic perspectives, ESC Heart Failure, Volume 13, Issue 1, February 2026, xvag053, https://doi.org/10.1093/eschf/xvag053
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)