第21届欧洲
要点一览

中重度活动性溃疡性结肠炎患者,接受古塞奇尤单抗静脉注射诱导治疗早期可观察到症状改善:QUASAR研究的事后分析
摘要编号:OP10
UC症状(如排便频率增加、直肠出血和腹痛)严重影响患者的生活质量。STRIDE-II达标治疗框架将症状缓解作为UC管理的短期治疗目标。早期症状改善具有临床意义,因为它会影响患者满意度、治疗依从性和长期结局。本研究评估了接受古塞奇尤单抗诱导治疗的中重度活动性UC临床试验参与者(pts)的早期症状改善和缓解情况。
在为期12周的3期、随机、双盲QUASAR诱导研究中,中重度活动性UC患者在第0、4、8周接受静脉注射古塞奇尤单抗200mg或安慰剂治疗。这项事后分析评估了治疗前14天内,梅奥排便频率(SFS)和直肠出血(RBS)子评分(基于每日患者报告结局[PRO-2]数据)相对于基线的变化,以及达到症状应答(症状性梅奥评分[SFS和RBS之和]较基线下降≥30%且≥1分)和症状缓解(SFS为0或1分;RBS为0分)的患者比例(观察数据集)。
采用重复测量混合效应模型估算古塞奇尤单抗组与安慰剂组在SFS和RBS较基线变化的最小二乘(LS)均值差。古塞奇尤单抗400mg皮下注射诱导治疗(第0,4,8周)第2周的数据来自3期、安慰剂对照ASTRO研究(NCT05528510)。
QUASAR全分析集包括701例参与者。到第6天,接受古塞奇尤单抗治疗的患者在SFS(LS均值差:-0.122 [95%CI:-0.240,-0.005];p=0.041)和RBS(-0.124 [-0.239,-0.009];p=0.034)方面较安慰剂组有更大的改善(图1)。到第14天,与安慰剂组相比,古塞奇尤单抗治疗组SFS和RBS的LS均值差分别为-0.180(95%CI:-0.306,-0.055;p=0.005)和-0.280(95%CI:-0.406,-0.155;p<0.001)。
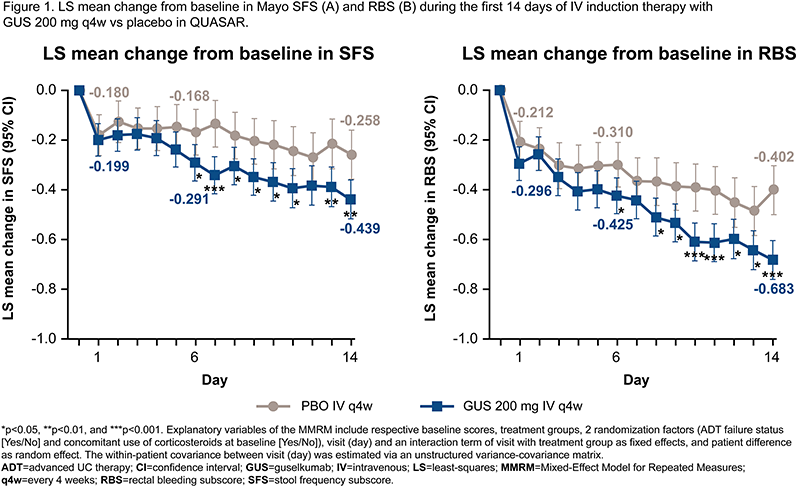
在第6天和第14天,古塞奇尤单抗组分别有29.5%(114/387)和41.7%(160/384)的患者达到症状应答,而安慰剂组分别为22.0%(54/245)和26.4%(64/242)(两项p<0.05);古塞奇尤单抗组分别有7.8%(31 p="">0.05)(图2)。在皮下注射诱导治疗(ASTRO研究)中,第2周时,皮下注射古塞奇尤单抗组有35.8%的患者达到症状应答,安慰剂组为25.9%;两组分别有12.2%和7.9%的患者达到症状缓解。
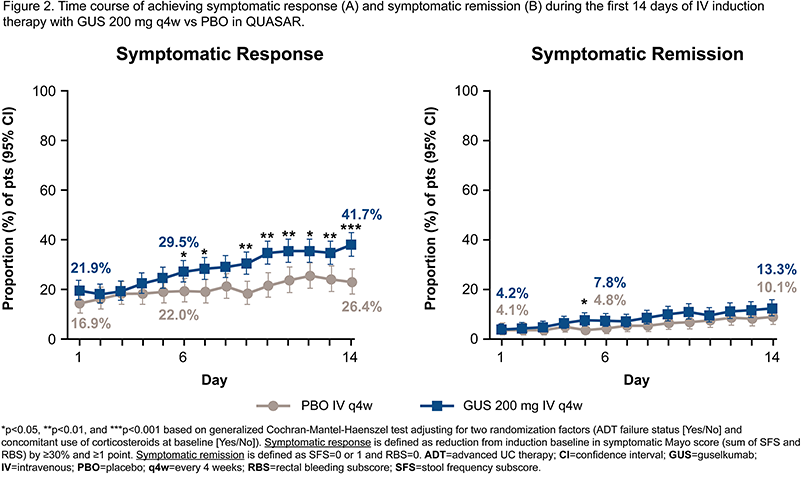
接受古塞奇尤单抗治疗的患者,在静脉诱导治疗后第6天即出现SFS和RBS的快速改善——二者均为反映UC活动性的重要临床指标。这些发现强调了早期症状控制的临床价值,并与STRIDE-II短期治疗目标相一致。
古塞奇尤单抗治疗溃疡性结肠炎的疗效和安全性:QUASAR长期扩展研究第140周结果
摘要编号:DOP104
QUASAR是一项评估古塞奇尤单抗用于中重度活动性UC患者的2b/3期研究。本次,研究者报告了正在进行的QUASAR长期扩展研究(LTE)第140周的疗效和安全性结果。
古塞奇尤单抗静脉注射诱导治疗应答者被随机分配接受皮下注射维持治疗:古塞奇尤单抗100mg q8w(GUS100),古塞奇尤单抗200mg q4w(GUS200),或安慰剂(PBO)。参与者在第8-32周期间可调整剂量至200mg。完成第44周随访的参与者可进入长期扩展研究,继续其当时的治疗方案。研究揭盲后,安慰剂组参与者停药。研究者评估了随机分配至古塞奇尤单抗组且未接受剂量调整即进入LTE长期扩展研究患者的疗效。数据分析方法为:1)“观察数据集”(AO);2)无应答者填补(NRI)法,后者考虑治疗失败或数据缺失的参与者。在所有接受LTE治疗的参与者中评估安全性。
总体而言,随机分配至古塞奇尤单抗组的参与者中有87.0%进入了长期扩展研究,其中88.8%完成了至第140周的治疗。在第140周,在古塞奇尤单抗100mg组和古塞奇尤单抗200mg组的参与者中,分别有80.1%和81.5%达到临床缓解;在第0周达到临床缓解的参与者中,分别有86.5%和87.5%在第140周维持了临床缓解(图;AO)。
在第140周时处于临床缓解的210例参与者中,205例(97.6%)在第140周前已停用皮质类固醇≥8周。在古塞奇尤单抗100mg组和古塞奇尤单抗200mg组的参与者中,分别有92.1%和92.3%达到症状缓解,84.6%和84.0%达到内镜改善,55.9%和51.2%达到内镜缓解,77.1%和80.3%达到组织-内镜黏膜改善(图;AO)。NRI结果在数值上低于AO结果。无论是否有生物制剂和/或Janus激酶(JAK)抑制剂治疗史,疗效均保持一致(图)。
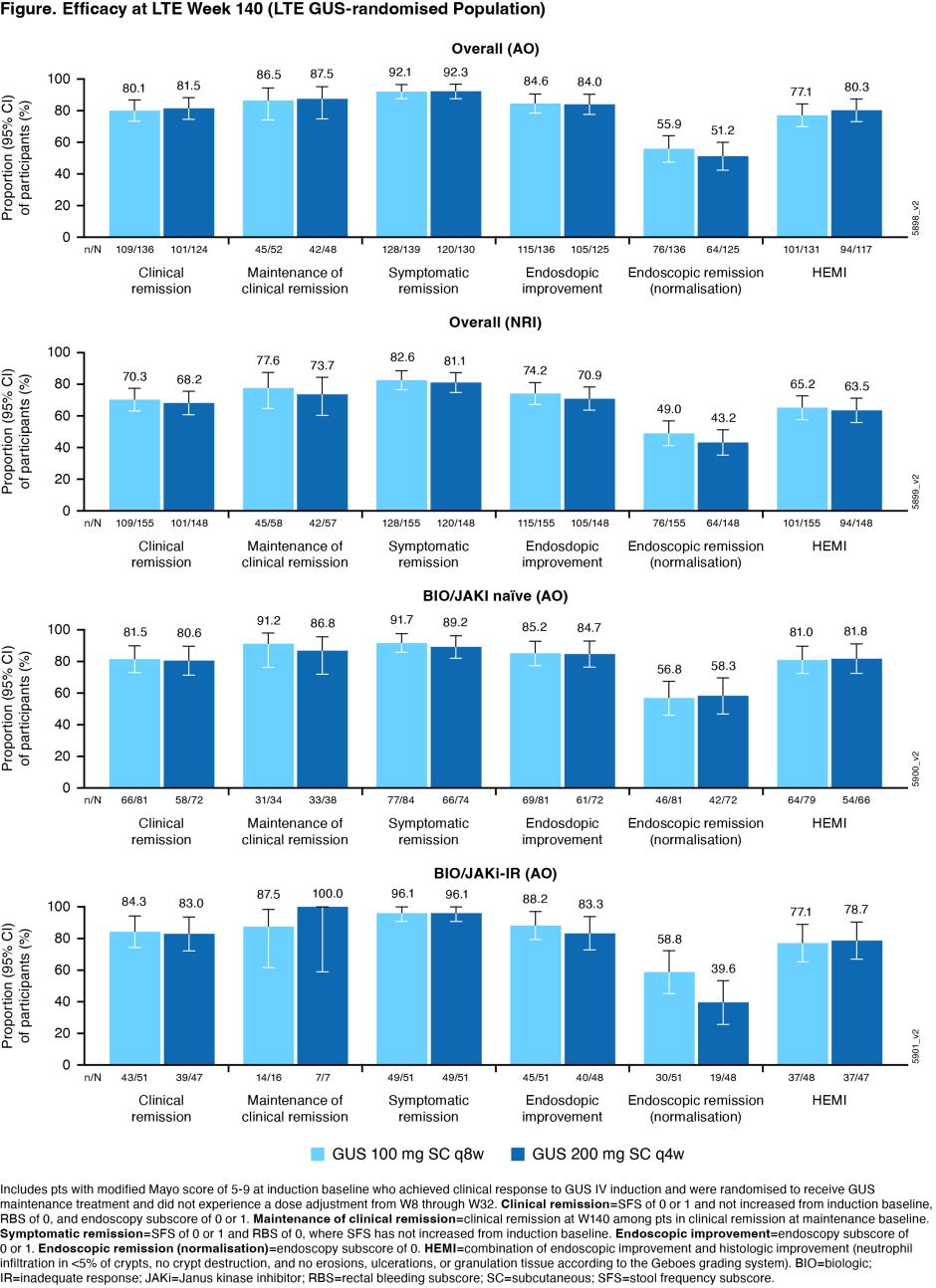
古塞奇尤单抗两个剂量组中出现≥1次不良事件(AE)的参与者人数/每100患者年相似(GUS100,45.0;GUS200,48.1),在数值上高于安慰剂组(67.1)(表)。古塞奇尤单抗组报告了1例死亡(
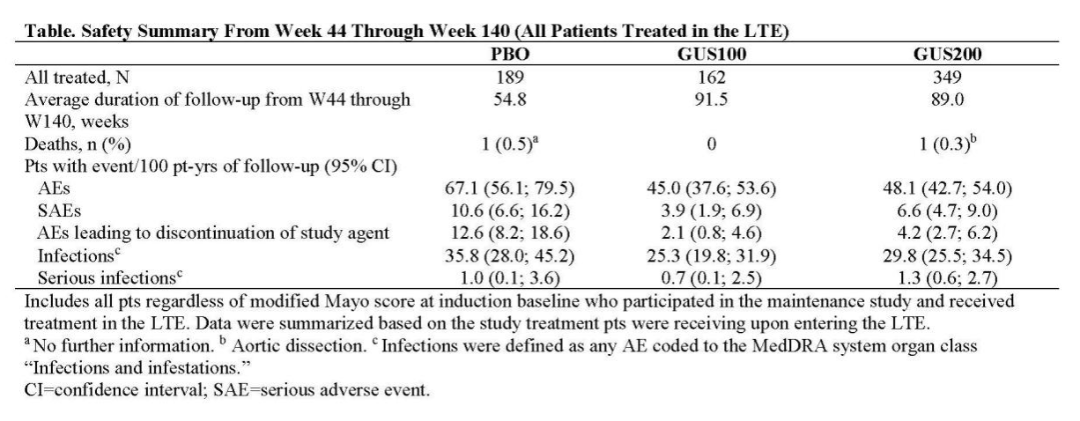
在UC患者中,两种古塞奇尤单抗维持剂量方案均在至第140周的随访中显示出持续的临床、内镜和组织学疗效。无论患者既往是否接受过生物制剂和/或JAK抑制剂治疗,古塞奇尤单抗的疗效均持续维持。尽管NRI结果在数值上低于AO结果,但由于维持期和长期扩展期的高保留率,总体趋势是一致的。未观察到新的安全性问题。
皮下注射古塞奇尤单抗治疗中重度活动性溃疡性结肠炎的疗效(根据诱导第12周的临床应答状态分层):3期ASTRO研究第48周的结果
摘要编号:DOP105
ASTRO研究是一项3期、随机、双盲、治疗贯穿设计(treatthrough)的研究,评估了皮下注射古塞奇尤单抗诱导和维持治疗中重度活动性UC的疗效。本次探索性分析的目的是:评估古塞奇尤单抗皮下注射诱导治疗患者在第12周(W12)时达到或未达到临床应答者在第48周(W48)的临床和内镜结局。
符合入组标准的患者,既往记录显示对常规或先进的UC治疗应答不足或不耐受。ASTRO采用治疗贯穿设计,参与者被随机(1:1:1)分配至三组:①古塞奇尤单抗400mg皮下注射,q4w(共3次)诱导→古塞奇尤单抗100mg皮下注射,q8w维持(组1;N=139);②古塞奇尤单抗400mg皮下注射,q4w(共3次)诱导→古塞奇尤单抗200mg皮下注射,q4w维持(组2;N=140);或安慰剂皮下注射(组3;N=139);无论其在诱导第12周的临床应答情况(仅限组1和组2)如何,均持续接受原定治疗方案治疗至第48周。
临床应答定义为:改良梅奥评分较基线下降≥30%且≥2分,同时直肠出血子评分较基线下降≥1分或达到直肠出血子评分0分或1分。本研究按古塞奇尤单抗剂量方案,分别报告了诱导治疗应答者与无应答者在第48周的临床缓解、临床应答、内镜应答及内镜缓解(定义见表)情况。
本分析共纳入267例接受古塞奇尤单抗治疗的患者,其中67.4%(180/267)在第12周达到诱导治疗临床应答。在第48周,在古塞奇尤单抗诱导治疗临床应答者中,临床缓解率为51.6%-60.7%,临床应答率为74.7%-82.0%,内镜改善率为59.3%-66.3%,内镜缓解率为35.2%-41.6%(表)。在第48周,在古塞奇尤单抗诱导治疗无应答者中,临床缓解率为25.0%-25.6%,临床应答率为48.8%-56.8%,内镜改善率为32.6%-40.9%,内镜缓解率为7.0%-25.0%(表)。

接受古塞奇尤单抗皮下注射诱导治疗后达到临床应答的患者,在第48周时的临床和内镜结局优于诱导后未达到临床应答的患者。然而,在诱导治疗后未达到临床应答但继续接受古塞奇尤单抗皮下注射维持治疗的患者中,仍有一部分在第48周时达到了临床和内镜终点,这表明对于部分患者,第12周之后继续使用古塞奇尤单抗治疗仍可获益。
静脉和皮下注射古塞奇尤单抗诱导治疗在不同体重四分位和BMI亚组溃疡性结肠炎患者中的疗效相似:3期QUASAR和ASTRO研究第12周结果
摘要编号:DOP103
古塞奇尤单抗(GUS)是一种双重作用的IL-23p19亚基抑制剂,可强效中和IL-23并结合CD64受体(细胞上产生IL-23的受体)。3期QUASAR和ASTRO研究已证实,在中重度活动性UC患者中,静脉注射(IV)和皮下注射(SC)古塞奇尤单抗诱导治疗的疗效和安全性相似。肥胖可能影响皮下注射药物的药代动力学和药效学参数。这项事后分析的目的是探讨与静脉注射诱导相比,UC患者的体重和
参与者患有中重度活动性UC(改良梅奥评分5-9分,基线梅奥直肠出血子评分≥1分,且梅奥内镜子评分≥2分),并且对口服皮质类固醇、AZA/6-MP/MTX、生物制剂、Janus激酶抑制剂和/或1-磷酸鞘
在第12周,评估不同基线体重四分位和标准BMI亚组(即,低体重[<18 kg/m2]、健康体重[≥18,<25 kg/m2]、超重[≥25,<30 kg/m2]和肥胖[≥30 kg/m2])中,临床应答和临床缓解情况。临床应答定义为改良梅奥评分较基线下降≥30%且≥2分,直肠出血子评分较基线下降≥1分,或直肠出血子评分为0分或1分;临床缓解定义为排便频率子评分为0分或1分且较基线无增加,直肠出血子评分为0分,内镜子评分为0分或1分且内镜下未见黏膜脆性增加。分别针对QUASAR研究与ASTRO研究计算体重四分位及BMI亚组。
QUASAR和ASTRO的纳入标准相似,随机化研究人群的基线人口统计学和疾病特征也相似。在所有基线体重四分位(图1)和所有基线BMI(图2)亚组中,与安慰剂相比,接受古塞奇尤单抗静脉注射或皮下注射诱导治疗的参与者,在第12周达到临床应答和临床缓解的比例相似,治疗效应也相似。
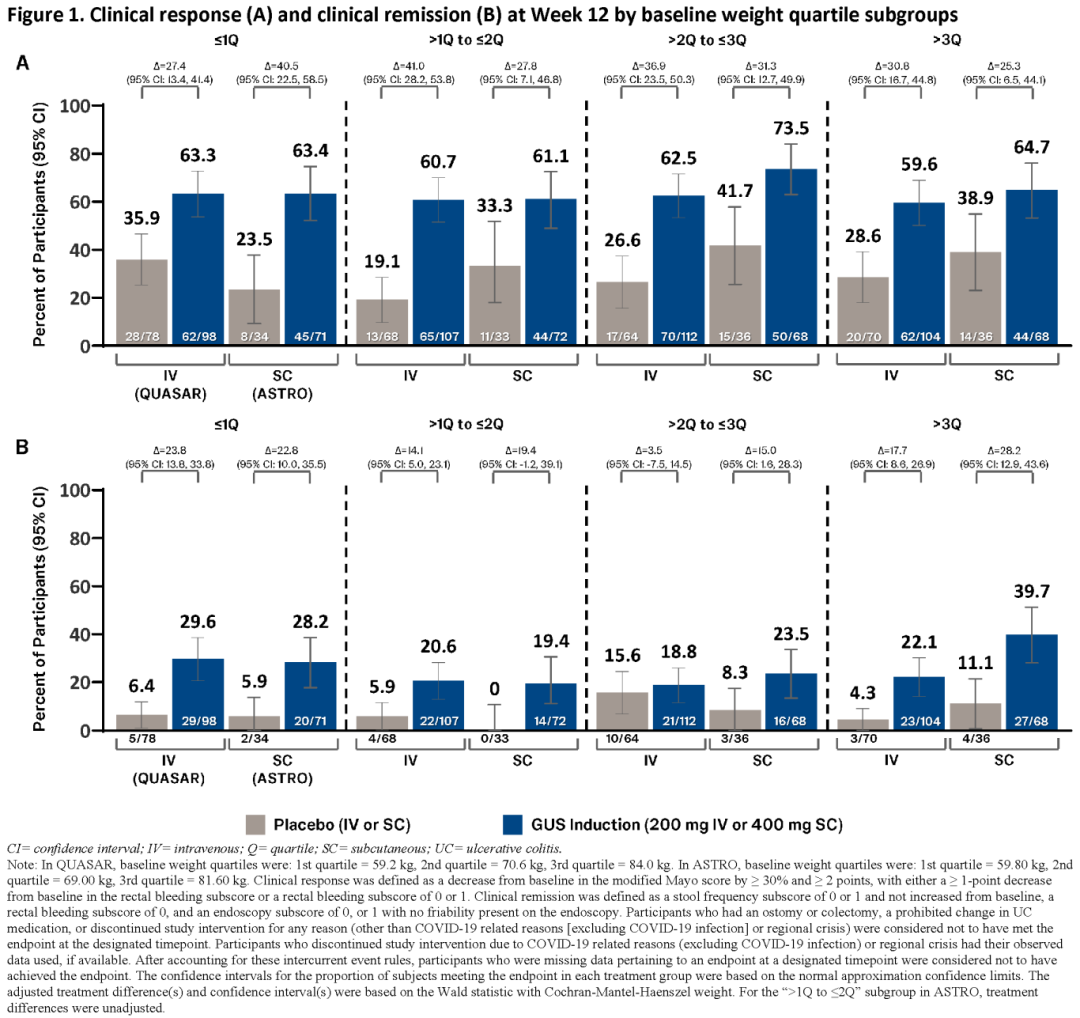
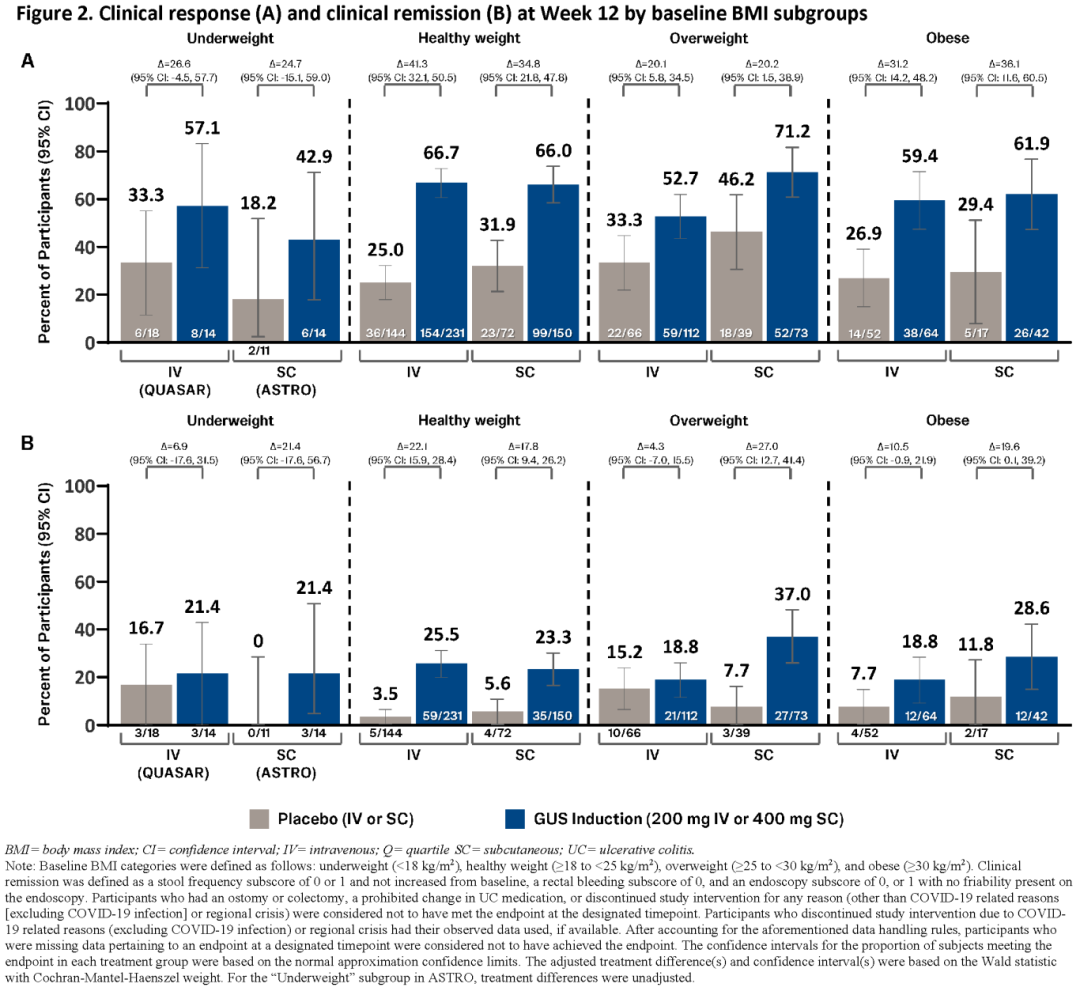
与安慰剂相比,无论参与者的基线体重或BMI如何,古塞奇尤单抗静脉注射和皮下注射诱导治疗对中重度活动性UC患者有效性相似。肥胖似乎并未降低古塞奇尤单抗皮下注射诱导治疗的疗效。
中重度活动性克罗恩病患者的肠外表现:3期GALAXI 2&3研究结果
摘要编号:DOP001
在IBD患者中,肠外表现(EIMs,包括关节、皮肤和眼部表现)很常见。3期GALAXI 2&3研究评估了古塞奇尤单抗治疗中重度活动性CD的疗效,本次分析呈现了GALAXI 2/3研究合并分析数据中截至第48周(Wk48)报告的肠外表现。
患者被随机分配至以下治疗组:古塞奇尤单抗200mg,第0/4/8周静脉注射,然后古塞奇尤单抗100mg皮下注射,q8w(N=286)或200mg皮下注射,q4w(N=296),或安慰剂(PBO,N=148)。本研究中也包括了乌司奴单抗(UST),但当前分析未包含UST。皮质类固醇(CS)在第12周前维持基线剂量,第12周起开始强制减量。肠外表现包括关节炎/关节痛、结节性红斑/坏疽性脓皮病以及虹膜炎/葡萄膜炎,是克罗恩病活动指数(CDAI)评分的组成部分,每次随访进行记录这些表现,在第12周和第48周时记录原有肠外表现的缓解情况和新发EIM。
总体而言,古塞奇尤单抗治疗组有34.5%(201/582)、安慰剂组有42.6%(63/148)的患者在基线时存在肠外表现(表)。在基线时存在肠外表现的患者中,古塞奇尤单抗组和安慰剂组分别有89.1%和90.5%报告了关节炎/关节痛,结节性红斑/坏疽性脓皮病分别见于18.4%和25.4%的患者;虹膜炎/葡萄膜炎的发生率较低,分别为5.5%和3.2%,由于样本量较小未进行评估。总体而言,基线时有肠外表现的患者中,古塞奇尤单抗组和安慰剂组分别有14.4%(29/201)和17.5%(11/63)基线时正在接受泼尼松治疗。
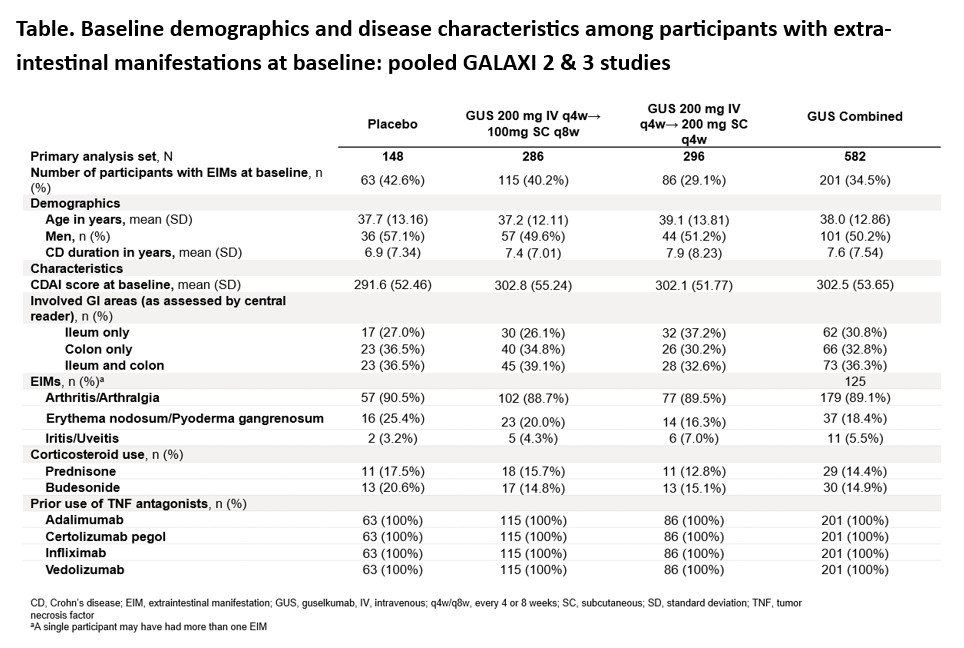
图1A显示了在基线和第12周时有肠外表现患者的百分比。古塞奇尤单抗组(59.2%)在诱导治疗后(第12周)整体肠外表现缓解率显著高于安慰剂组(42.9%):关节炎/关节痛(55.3% vs 33.3%),结节性红斑/坏疽性脓皮病(75.7% vs 56.3%)。
总体而言,第12周新发肠外表现的发生率较低,分别为2.6%和8.1%。从基线到第12周,古塞奇尤单抗组(两个剂量合并)的加权EIM CDAI组分评分较安慰剂组改善更大(LS均值[SE]:-5.4 [0.43] vs -0.70 [0.83])。
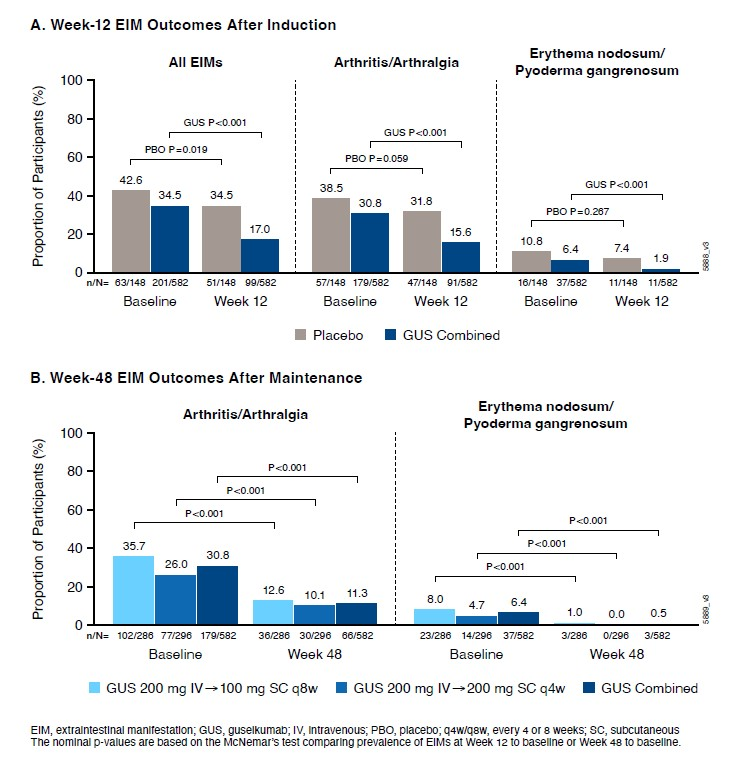
在第48周,两个古塞奇尤单抗组中伴关节炎/关节痛或结节性红斑/坏疽性脓皮病的患者比例均较基线下降(图1B)。第48周时,两组加权EIM CDAI组分评分相较基线的LS均值变化[SE]相似:古塞奇尤单抗100mg皮下注射,q8w组(-5.5 [0.57]),古塞奇尤单抗200mg皮下注射,q4w组(-6.1 [0.57])。
与安慰剂相比,接受古塞奇尤单抗治疗的患者在第12周肠外表现缓解率更高,且改善持续到第48周;第12周时新发肠外表现的发生率也更低。这些结果提示,古塞奇尤单抗可能改善CD患者的肠外表现,并可能具有预防作用。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)