
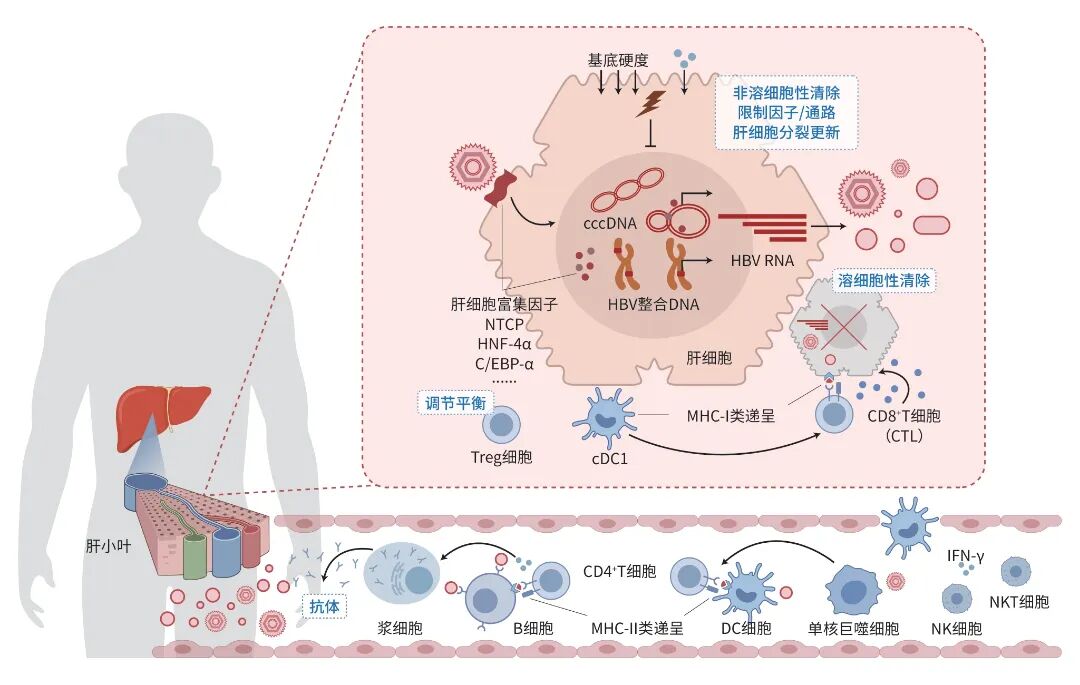
注: HBV是一种嗜肝DNA病毒,感染肝细胞后形成cccDNA和整合DNA,转录产生多种HBV RNA以合成病毒抗原和子代病毒,过程中多种肝细胞富集因子对感染复制的建立与维持具有重要作用。宿主通过溶细胞性、非溶细胞性、限制性因子/通路、肝细胞分裂更新及抗病毒抗体等多种机制控制和清除HBV,期间各类免疫细胞、细胞因子及细胞外基底硬度变化等协同作用。cccDNA,共价闭合环状DNA;HBV,乙型肝炎病毒;NTCP,钠离子-牛磺
图1 HBV感染与控制清除机制示意图

1HBV感染复制概述
HBV是一种独特的嗜肝DNA病毒,其基因组约为3.2 kb的部分松弛环状DNA(rcDNA),通过逆转录复制完成生命周期。HBV感染肝细胞始于依赖

2调控HBV感染复制的宿主因子
HBV的复制高度依赖宿主特异性因子及肝细胞稳态环境。多种肝细胞富集转录因子,包括肝细胞核因子4α、CCAAT增强子结合蛋白α、过氧化物酶体增殖物激活受体α、视黄醇X受体和特异性蛋白1等,可直接结合cccDNA上不同启动子及调控元件,协同激活病毒转录,并与HBV嗜肝性密切相关。HBV编码的非结构蛋白乙型肝炎病毒X蛋白(HBx)在复制过程中发挥关键作用,可通过与宿主染色质修饰复合物相互作用,促进cccDNA乙酰化及转录活化。最近一项研究提示,HBx还可通过上调热
综上所述,HBV感染复制依赖宿主在受体识别、转录调控、代谢稳态及微环境信号等多层面的支持。深入解析这些宿主因子及其作用网络和机制,不仅有助于理解HBV的嗜肝性和持续感染基础,也可为开发靶向关键环节的新型抗病毒策略提供理论依据。
HBV通常被认为是一种“隐匿型”病毒,其感染过程并不引发强烈的天然免疫识别或干扰素级联反应。因此,肝细胞中对HBV具有抑制作用的限制性因子多依赖于固有表达和维持。在干扰素刺激基因中,存在许多具有较强抗HBV功能的分子,其通过多方面机制,在HBV感染复制的不同阶段发挥抑制作用。代表性因子包括载脂蛋白B mRNA编辑酶催化亚基3A/B,可通过胞嘧啶脱氨作用损伤或破坏cccDNA;干扰素刺激基因20具有3′-5′外切核酸酶活性,可降解HBV RNA;三结构域蛋白22通过泛素化干扰乙型肝炎病毒核心蛋白(HBc)组装;锌指抗病毒蛋白识别富CpG序列的HBV RNA并促进其降解;SAM结构域和HD结构域蛋白1通过降低胞内脱氧核苷三磷酸浓度限制逆转录过程。表观遗传调控分子如SET结构域分叉组蛋白赖氨酸甲基转移酶1、蛋白质精氨酸甲基转移酶5和去乙酰化酶3可介导cccDNA组蛋白去乙酰化或甲基化修饰,维持其低转录活性。染色体结构维持蛋白5/6复合物可直接结合cccDNA并阻断其转录,实现“功能性清除”;而HBx通过招募DDB1-CUL4 E3连接酶可促使该复合物降解,从而“解锁”cccDNA活性。近年研究表明,MX2作为一种鸟苷三磷酸酶,可干扰HBV RNA稳定性并抑制cccDNA形成,对病毒复制具有直接限制效应;肌节同源盒基因1作为转录调控因子,可结合HBV增强子Ⅱ/核心启动子区,抑制HBx表达与病毒转录,显著降低HBV复制活性。
上述多元化的作用机制体现了HBV限制性网络的多样性与层级性,其可在不依赖外源干扰素的情况下,于肝细胞内维持基础活性;在应激、炎症或代谢信号增强时,部分因子的表达可进一步上调,抗病毒效应随之放大。通过表观遗传调控及复制包装阻断等途径,这些因子共同维持宿主的内源性抗病毒稳态,从而在缺乏强烈免疫炎症反应的背景下抑制HBV复制。深入理解其作用机制及动态调控,有助于揭示病毒与宿主之间的平衡机制,并可为打破HBV转录复制状态提供潜在靶向策略。

3“非溶”与“溶”细胞性HBV清除
在HBV感染过程中,动物模型研究提示,病毒可实现近乎100%的肝细胞感染。因此,单纯依靠溶细胞性清除病毒,理论上会造成不可逆的
非溶细胞性HBV清除主要依赖宿主细胞间的细胞因子协同网络与细胞内抗病毒通路。其中,CD8+ T细胞与自然杀伤(NK)细胞分泌的干扰素γ是非溶细胞性清除的关键因子,而肝细胞及树突状细胞产生的内源性及外源性导入的干扰素α/β可通过Janus激酶/信号转导与转录激活因子通路启动一系列干扰素刺激基因的表达,诱导多种抗病毒限制性分子(如载脂蛋白B mRNA编辑酶催化亚基3A、干扰素刺激基因20、三结构域蛋白22等)表达,从而引发cccDNA降解或抑制病毒转录。白细胞介素6等炎性细胞因子可通过信号转导与转录激活因子3抑制肝细胞内肝细胞核因子4α的活性,从而降低cccDNA的转录活性。除细胞因子外,肝脏力学信号是一种全新的自然控制清除HBV机制:肝脏的物理硬度具有很大的生理性变化范围(1~7 kPa),在HBV急性和慢性感染清除进程中可观察到一过性肝脏物理硬度升高,而肝细胞基底硬度升高能通过机械力感知通路激活Yes相关蛋白,进而诱导一系列具抗病毒功能因子的表达并降低肝细胞核因子4α水平,从而显著抑制HBV转录、抗原表达及促进cccDNA清除。此外,在肝细胞发生有丝分裂时,原有病毒cccDNA分子因缺乏黏附宿主染色体的机制,可被大量稀释丢失;而肝细胞的死亡更新也会促进宿主自然清除HBV。
综上所述,各类非溶细胞性清除机制,通过细胞因子、细胞内抗病毒基因、代谢和微环境调控网络等动态协同,可在不杀伤宿主肝细胞的条件下抑制乃至清除HBV,这对控制病毒感染、维持免疫稳态和影响感染结局及治疗应答等均具有重要影响。
溶细胞性清除是宿主消除HBV最直接的方式,主要依赖CTL的作用,并有NK和自然杀伤T细胞(NKT)等协同参与。当内含活化cccDNA或整合HBV DNA的肝细胞在主要组织相容性复合体Ⅰ类(MHC-Ⅰ)分子上呈递病毒抗原时,CTL可识别并诱导其凋亡,通过穿孔素-颗粒酶、死亡因子/死亡因子配体及肿瘤坏死因子相关凋亡诱导配体/死亡受体5等途径直接裂解杀伤靶细胞。NK/NKT则可识别MHC-Ⅰ缺失或应激信号介导的非特异性杀伤,并通过分泌干扰素γ和白细胞介素12促进CTL活化。这些细胞协同作用,在急性感染阶段可实现病毒复制的迅速清除。小鼠模型研究表明,肝内1型经典树突状细胞在此过程中通过“cross-dressing”机制呈递HBV来源的MHC-Ⅰ类抗原,有效激活并扩增HBV特异性CTL群体,形成高效的局部抗病毒效应簇。共刺激受体如OX40和4-1BB的信号可显著恢复慢性乙型肝炎中功能衰减的CD8+ T细胞效能,增强杀伤活性并改善病毒控制,提示共刺激途径可能成为重塑慢性乙型肝炎HBV特异性免疫的潜在靶标。
溶细胞性免疫虽能有效清除病毒感染细胞,但过强反应常导致肝细胞坏死与炎症放大。CD4+辅助性T细胞分泌白细胞介素2等支持CTL扩增与记忆维持,而肝脏局部免疫环境则在效应强度与组织保护间发挥关键调控作用。近期研究提出“肝脏免疫调速器”模型,即肝内树突状细胞、肝窦内皮细胞及肝巨噬细胞通过代谢和共刺激信号调节CTL阈值,实现病毒控制与组织耐受的动态平衡。通过单细胞与空间转录组进一步发现,在部分慢性乙型肝炎患者中,效应T细胞虽呈功能衰减但仍维持抗病毒转录特征,与病毒低水平控制相对应。
综上所述,溶细胞性清除代表宿主强效的抗病毒模式,但如何兼顾清除效应与组织保护,是HBV免疫干预的重要挑战。肝脏免疫微环境及共刺激信号共同决定了这一反应的幅度与结局,为未来基于精准免疫治疗实现乙型肝炎治愈提供了新的视角。

4HBV感染体液免疫应答及抗体介导的清除
体液免疫应答在HBV感染的自然控制与清除中发挥重要的辅助与维持作用,其核心在于B细胞介导的中和抗体产生与抗原特异性记忆形成。HBV感染后,抗原经树突状细胞、巨噬细胞及肝窦内皮细胞摄取、加工后,通过MHC-Ⅱ分子呈递给CD4+辅助性T细胞,从而驱动各类HBV特异性B细胞活化与分化。以滤泡辅助T细胞为主分泌的白细胞介素21在其中发挥关键调节作用,可促进B细胞分化与高亲和力抗体生成,还能促进CD8+ T细胞的抗病毒效应。活化的B细胞在T细胞驱动下于生发中心经历克隆扩增、体细胞突变和亲和力成熟,最终分化为浆细胞,产生抗HBV表面抗原抗体(抗-HBs)、抗HBV前S1/S2抗体(抗-preS1/S2) 及抗HBV核心抗体(抗-HBc)等。其中,抗-HBs可阻断HBV颗粒进入肝细胞并促进病毒颗粒及HBsAg清除;抗-HBc则主要反映既往或持续感染,与细胞免疫活性密切相关;抗-preS1抗体可直接阻断乙型肝炎表面抗原大蛋白与钠离子-牛磺胆酸共转运蛋白的结合,其功能角色日益受到关注。在自限性乙型肝炎个体中,抗-HBs与抗-preS1抗体通常在病毒DNA下降同期或稍后出现,提示体液免疫应答在感染清除和持续巩固中发挥重要作用。除直接中和作用外,抗体通过多种Fc受体依赖机制介导病毒清除。例如,已感染肝细胞表面的HBsAg或HBcAg可被特异抗体识别后,触发补体依赖性细胞毒作用或抗体依赖的细胞介导细胞毒作用,由NK细胞、巨噬细胞等效应细胞执行杀伤。抗体还可促进免疫复合物被肝内巨噬细胞吞噬、增强抗原呈递并强化后续T细胞应答。
然而,在慢性乙型肝炎患者中,B细胞功能常处于受损或异常激活状态。外周及肝内可检测到大量CD21⁻/CD27⁻“耗竭型”B细胞,其对HBsAg刺激反应低下,表现为抗体产生不足及记忆维持缺陷。须指出的是,宿主对不同HBV抗原的免疫强度存在差异:HBc特异性T细胞与抗体应答通常更为强健,而HBs特异性免疫因长期高抗原暴露而常呈现功能耗竭或免疫耐受,HBsAg本身则可干扰抗病毒免疫及促进形成免疫异质性微环境。相反,在功能性治愈或自然控制者中,抗-HBs浆细胞及记忆B细胞比例显著高于慢性乙型肝炎患者,提示恢复B细胞应答是病毒清除中的重要环节。针对共刺激受体的调节可有效改善HBV特异B细胞反应,例如,OX40配体-OX40受体与诱导性共刺激分子配体-诱导性共刺激分子轴信号被证实有助于增强滤泡辅助T细胞功能,从而促进B细胞分化与抗体亲和力成熟。此外,抗原特异性B细胞在肝脏局部也可通过抗原呈递功能促进T细胞再激活,形成细胞免疫与体液免疫的正反馈环路。
体液免疫在HBV感染控制中的作用不仅体现在中和与清除环节,还通过维持长期免疫记忆与协同细胞免疫实现持续控制。慢性乙型肝炎中B细胞耗竭与抗体功能障碍是病毒持续存在的重要机制,而恢复B细胞活性、强化滤泡辅助T细胞-B细胞相互作用以促进功能性抗体产生,是未来深入研究的重要方向。

5展望:HBV自然清除的障碍与靶向干预策略
尽管大多数急性乙型肝炎患者可自然自愈,以及部分慢性乙型肝炎患者可最终实现HBsAg血清学转换,但大量研究表明,cccDNA与整合DNA仍可在肝细胞中长期残留,并具有转录潜能。这些病毒基因组的持续存留构成乙型肝炎“难彻底治愈”的核心病毒学基础,即使HBsAg转阴后仍存在再激活风险;与此同时,病毒利用多重机制逃逸和拮抗宿主免疫:HBsAg和HBeAg的持续高表达可诱导特异性T、B细胞功能耗竭。肝脏具有特殊的免疫稳态环境,肝窦内皮细胞和肝巨噬细胞可分泌白细胞介素10、转化生长因子β等因子抑制抗原呈递和T细胞活化,调节性T细胞、髓系抑制细胞及耗竭型NK细胞进一步削弱HBV特异性免疫效应。上述因素再叠加肝细胞代谢与力学环境变化(如氧化还原状态失衡、基底硬度持续性升高),共同推动抗HBV免疫应答损伤状态的形成。综上,HBV清除的障碍并非单一因素所致,而是病毒基因组持久性、特殊天然免疫环境、病毒特异性免疫功能损伤和耗竭以及肝脏微环境调控等的综合作用。
基于对HBV感染慢性化和难治愈机制的认知,乙型肝炎干预已从“单一抗病毒”转向“病毒抑制与免疫重建并重”的综合方向。随着小核酸药物和抗病毒抗体等新型治疗手段能够显著降低HBsAg载量,其能否进一步促进宿主抗病毒免疫应答的恢复,已成为当前重要的科学问题。与此同时,基于免疫检查点(程序性死亡受体1)等阻断、共刺激受体调控和T细胞受体工程化T细胞疗法等诸多疗法正被探索。干扰素仍是当前实现功能性治愈的主力药物,其与小干扰RNA或代谢调节剂联合应用及其自身生物学特性的优化,有望提升治疗效果。乙型肝炎治疗性疫苗和免疫增强剂等免疫重塑策略,为长期免疫记忆的恢复提供了新方向。然而,如何在重建有效免疫的同时避免过度炎症和肝损伤,仍是亟待解决的关键挑战。通过整合病毒学、免疫学、系统生物学与人工智能大数据等多学科视角和手段,进一步揭示自然清除与清除障碍恢复机制,将为提升功能性治愈水平奠定新的理论与技术基础。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH260102

叶建宇, 王冰, 顾乐言, 等. 乙型肝炎病毒感染的自然控制和清除[J]. 临床肝胆病杂志, 2026, 42(1): 7-13
来源:临床肝胆病杂志
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
