

1资料与方法
招募2023年4月—2024年5月昆明医科大学第二附属医院收治的符合《慢性乙型肝炎防治指南(2022年版)》诊断标准的HBV感染者为研究对象。排除标准:(1)恶性肿瘤及自身免疫疾病患者;(2)孕期妇女。
收集患者性别、年龄、BMI、母婴史、
HBV RNA 检测采用上海仁度生物科技HBV核酸测定试剂盒(RNA 捕获探针法)及全自动核酸检测分析系统(AutoSAT),结果小于定量下限100拷贝/mL判定为阴性。高敏HBV DNA检测采用豪洛捷HBV核酸检测试剂盒及配套全自动核酸检测系统(PANTHER System),结果小于检测下限10 IU/mL判定为阴性。HBsAg定量检测采用sysmex化学发光试剂盒及HISCL-5000全自动免疫分析仪,方法为双抗体夹心化学发光法定量检测。肝功能相关指标均采用BECKMAN COULTER原装试剂盒配套仪器BECKMAN15 COULTERAU 5821检测。

2结果
本研究共纳入134例HBV感染者,根据HBeAg状态将患者分为HBeAg阳性组(n=45)及HBeAg阴性组(n=89)。两组间年龄、HBV DNA阳性率及定量值、血清HBV RNA阳性率及定量值、HBsAg、抗-HBe、ALT比较,差异均有统计学意义(P值均<0.05),其余指标差异无统计学意义(P值均>0.05)(表1)。
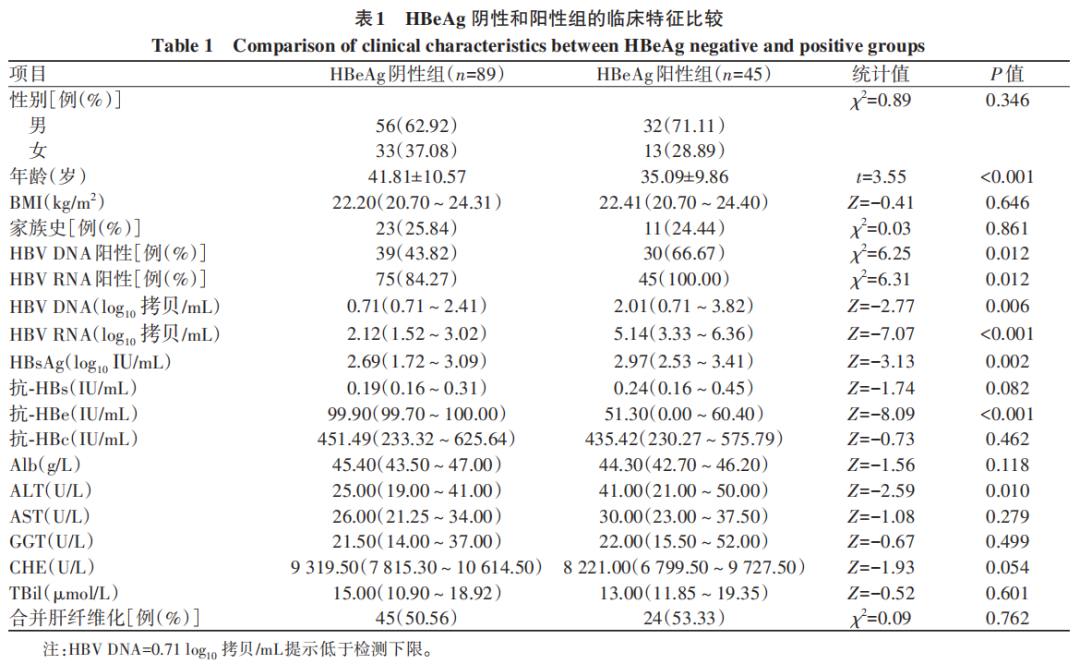
在HBeAg阴性组(n=89)的研究队列中,血清HBV RNA阴性组(n=14)与阳性组(n=75)HBV DNA、HBsAg和GGT水平比较,差异均有统计学意义(P值均<0.05)(表2)。
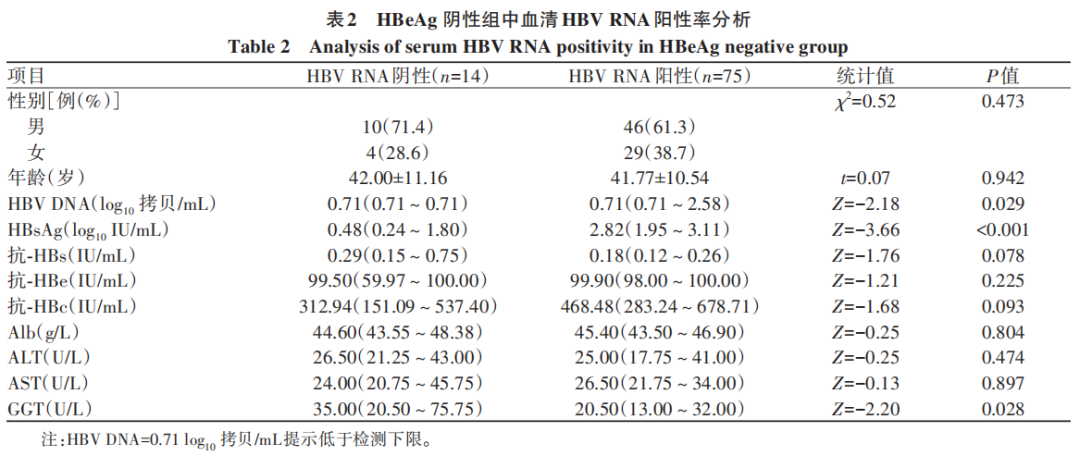
HBeAg阳性及阴性组使用抗病毒药物时长≥1个月的患者分别有28例和62例,28例HBeAg阳性患者HBV RNA阳性率达到了100%;62例HBeAg阴性患者血清HBV RNA阳性率和定量水平在不同治疗时长组间比较,差异均有统计学意义(P值均<0.05)(表3)。
89例HBeAg阴性组患者中经治疗62例,未治疗27例,HBV RNA水平分别为2.07(1.52~2.82)log10 拷贝/mL、2.69(1.80~3.55) log10拷贝/mL,经治组与未治疗组比较,差异有统计学意义(Z=2.034,P=0.042);45例HBeAg阳性组患者中经治疗28例,未治疗17例,HBV RNA水平分别为4.56(3.25~5.90) log10拷贝/mL、5.71(4.63~7.62) log10 拷贝/mL,经治组与未治疗组比较,差异无统计学意义(Z=1.721,P=0.087)。
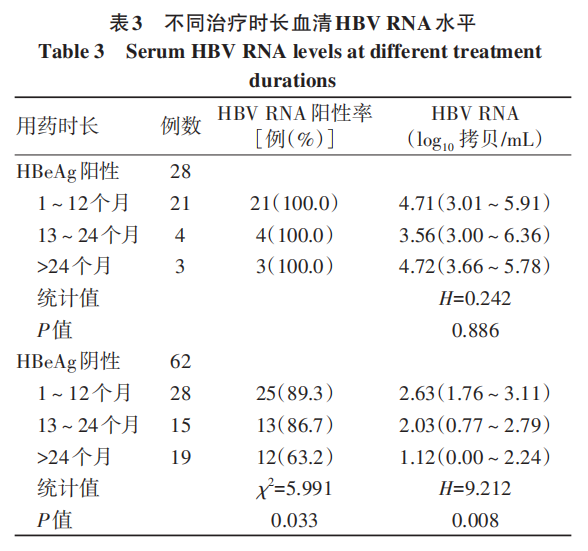
HBeAg阴性组患者的血清HBV RNA仅与HBV DNA和HBsAg存在正相关(P值均<0.05),与ALT及AST无显著关联(P值均>0.05)(图1);HBeAg阳性组患者的血清HBV RNA水平与HBV DNA、HBsAg及HBeAg均呈现显著正相关性(P值均<0.05),但与AST和ALT均无显著关联(P值均>0.05)(图2)。
图1 HBeAg阴性组血清HBV RNA与其他指标相关性
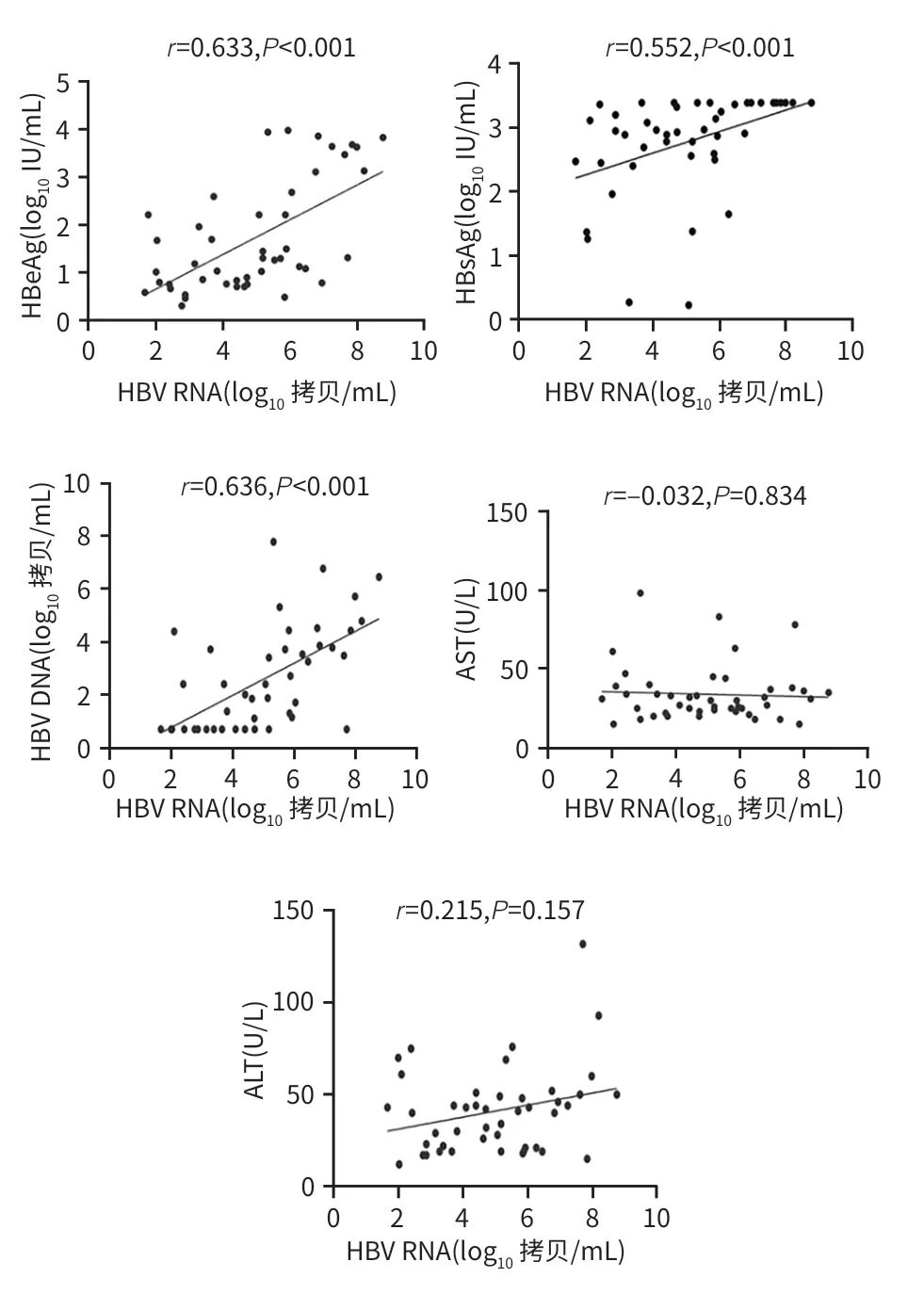
图2 HBeAg阳性组血清HBV RNA与其他指标相关性

3讨论
HBV感染威胁全球人类生命与健康,国内外指南确定的治疗目标是通过最大限度地持续抑制HBV复制,以阻止疾病进展为肝硬化、肝衰竭和肝细胞癌。cccDNA是HBV持续存在的分子基础,作为稳定的微型染色体存在于细胞核中。cccDNA的根除被认为是HBV清除的金标准,全面监测cccDNA的转录活性,对于评估抗病毒治疗的效果和疾病进展风险具有重要意义,但肝内cccDNA检测需要行肝活检,属于有创性操作,难以用于临床动态监测。血清HBV RNA是一种新型血清学标志物,以病毒颗粒的形式在CHB患者的血液中循环,主要来源于肝内cccDNA的直接转录,包含pgRNA及其剪切变异体,pgRNA是HBV复制的关键,它被包裹在病毒衣壳内,并通过逆转录生成病毒基因组。现已有多项研究证明血清HBV RNA可视为肝内cccDNA的非侵入性替代工具。根据慢性HBV感染的自然史,从免疫清除阶段进入非活动性携带阶段的标志是HBeAg转阴。对于HBeAg阳性的CHB患者而言,实现HBeAg血清学转换且HBV DNA检测不到被视为一个较为理想的治疗终点。这表明患者对CHB感染已达到部分免疫控制状态,从而有助于改善长期的临床预后。
本研究显示,在HBeAg阳性组内血清HBV RNA、HBV DNA阳性率及定量值水平均高于HBeAg阴性组,这与既往研究结论一致,提示在HBeAg阳性患者中,cccDNA的活跃程度和病毒复制水平显著高于阴性患者。HBeAg阳性组内ALT定量中位数高于HBeAg阴性组,表明HBeAg阳性患者的肝脏炎症活动度更高,肝脏病变活动更为严重。相关研究证实在40%低病毒载量且HBeAg阴性的患者中,肝活检仍显示存在不同程度的损伤,这一发现进一步支持了HBeAg状态与肝脏炎症活动度之间的关联性。有研究证明血清HBV RNA阳性是CHB患者抗病毒治疗过程中HBeAg阳性及肝硬化的危险因素,但在本研究中,对患者行肝脏瞬时弹性成像及肝脏脂肪衰减程度检查评估肝纤维化情况,发现两组之间并无显著差异(P=0.762)。本研究未进行肝纤维化四项血清学指标及肝穿刺活检等检查,仅凭肝脏瞬时弹性成像判断肝纤维化程度,存在证据单一问题,研究结果可能存在偏倚,下一步研究需结合多维度数据与动态监测来进一步验证血清HBV RNA水平与肝纤维化之间的关系。
NUC在抑制HBV DNA复制方面具有良好效果,并具有长期应用的安全性,是目前最主要的抗病毒药物。IFN在CHB治疗中具有显著的抗病毒和免疫调节作用,可以有效提高HBsAg清除率,其联合NUC治疗在实现功能性治愈、增强免疫调节作用以及降低病毒反弹风险方面较单用NUC类药物有较大优势。Wang等在HBeAg阳性CHB患者使用Peg-IFN治疗期间,发现血清HBV RNA与肝内cccDNA的相关性比其他HBV标志物更强,进一步表明了血清HBV RNA可能是反映cccDNA水平的理想无创替代标志物。如何选择抗病毒治疗方案需要同时考虑宿主和病毒因素,尽管目前难以达到乙型肝炎治愈的目的,但持续的抗病毒治疗可有效延缓疾病进展。
本研究HBeAg阴性组中,未接受抗病毒治疗的慢性HBV感染者的血清HBV RNA中位水平高于经治者,表明抗病毒治疗能够有效抑制HBV在体内的复制和转录活动,这对于减轻肝脏炎症以及降低疾病进展风险等方面具有重要意义,凸显了抗病毒治疗在慢性HBV感染管理中的关键作用。并且,在HBeAg阳性患者中,血清HBV RNA检测结果均为阳性,定量水平普遍较高。HBeAg阴性患者中,血清HBV RNA的定量水平和阳性检出率在不同治疗时间均存在显著性差异,并随着抗病毒治疗时间的延长逐渐下降。
本研究结果显示,在HBeAg阳性组中,血清HBV RNA 水平与HBV DNA、HBeAg、HBsAg水平呈显著正相关,在HBeAg阴性组中,上述相关性减弱,这一发现与其他学者研究结果相似。Song等发现,在未经抗病毒治疗的慢性HBV感染者中,血清HBV RNA水平与血清HBV DNA、HBsAg定量均呈正相关,且在HBeAg阳性CHB患者中更为明显;而在启用NUC抗病毒治疗后,患者血清HBV RNA与HBV DNA、HBsAg之间的相关性逐渐减弱甚至消失。HBeAg阳性和HBeAg阴性患者HBsAg来源的不同可部分解释这一现象,Wooddell等在慢性HBV感染的黑猩猩中证明,在HBeAg阴性阶段,HBV整合的频率增加,导致>90%的信使RNA来源于整合的HBV序列,而只有10%来自cccDNA,这也进一步削弱NUC治疗患者中HBsAg在HBeAg阴性患者中预测cccDNA水平和转录活性方面的价值。同时,本研究发现,即使在HBeAg、HBV DNA双阴性患者中,仍可检出血清HBV RNA,该结果与Mak等的研究相同。后者显示,所有患者均达到了无法检测到HBV DNA的状态,仍有73%的患者可检测到HBV RNA。这些证据支持HBV RNA可作为接受NUC治疗的病毒抑制患者中反映cccDNA活性的更好替代标志物。
血清HBV RNA水平可作为肝内HBV cccDNA的替代性标志物,在疗效评估、疾病进展预测、停药时机选择及预后分析等方面均展示出较高的价值。然而,目前血清HBV RNA尚无国际校准品和统一的检测方法,可能会影响血清HBV RNA检测结果的准确性和可比性。除此之外,还需开展大规模、前瞻性、系统性研究,深入挖掘血清HBV RNA与现有传统标志物、检测方法和预测模型的互补性,验证其在CHB诊疗中的实际应用价值,并优化相关检测方法和预测模型,为CHB患者的治疗提供更加精确、个性化的指导。
积极抗病毒治疗可有效抑制体内病毒转录活性。血清HBV RNA作为反映肝内cccDNA转录活性的指标之一,比HBV DNA灵敏度更高。在HBeAg阳性患者中,无论HBV DNA状态如何,血清HBV RNA均为阳性,无需额外行该检测,以避免医疗资源的浪费。HBeAg阴性且高敏HBV DNA低于检测下限时可完善血清HBV RNA检测,以便更全面监测病毒转录情况。
本研究的不足:首先,纳入的样本量相对有限,且未按照免疫状态进行详细分组,结果可能存在偏倚,未来将进一步扩大样本量并进行详细分组以比较血清HBV RNA的差异;其次,本研究为横断面研究,下一步研究将进行随访以进一步观察血清HBV RNA的动态变化及HBeAg血清学转换情况;此外,本研究为单中心研究,今后有必要开展多中心研究,进一步验证血清HBV RNA在抗病毒治疗过程中的作用。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH251012

尹红静, 李丽梅, 程霞, 等 . 血清HBV RNA对慢性乙型肝炎患者抗病毒治疗效果的评估价值[J]. 临床肝胆病杂志, 2025, 41(10): 2030-2036
来源:临床肝胆病杂志
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
