
Fecal Detection of Calprotectin Subunits Links Inflammatory Bowel Disease Activity With Chronicity of Intestinal Inflammation
Gastroenterology
PMID: 41295942 [IF=25.9]
来源:IBD Daily
炎症性肠病 (IBD) 全球发病率持续上升,其肠道慢性炎症机制尚不明确。粪便钙卫蛋白 (CP) 是临床常用的IBD生物标志物,由S100A8和S100A9形成的异源四聚体构成,浓度 > 150 μg/g提示疾病活动。然而,CP在肠道中的生物学功能存在争议。临床中部分IBD患者有活动症状但粪便CP浓度 ≤ 150 μg/g,现有CP检测方法存在诊断缺口。已有研究表明,S100A8和S100A9的不同蛋白构型 (如二聚体与四聚体) 可能发挥截然不同的作用,同源二聚体具有促炎特性,而异源四聚体 (CP) 则不然。但IBD患者肠道中这些蛋白构型的存在情况及其功能尚不清楚。本研究旨在解析IBD患者粪便中S100A8/S100A9的蛋白构型及其生物学功能,探索其与疾病活动度和炎症慢性化的关联,并阐明其对肠道上皮和T细胞的炎症调控作用。
研究共纳入多个独立IBD队列。首先利用德国IBDome队列 (包含360份IBD组织样本与54份对照) 通过批量RNA测序 (Bulk RNA-seq) 分析肠道黏膜S100A8/S100A9表达与临床、内镜及组织学疾病活动度的相关性 (组间比较采用Wilcoxon检验)。
研究构建人结肠上皮类器官单层,经S100A8/S100A9二聚体刺激后进行单细胞RNA测序,分析上皮细胞亚群的细胞因子反应和信号通路活性。从健康人外周血分离CD4+和CD8+ T细胞,体外给予同源二聚体或CP刺激,通过流式细胞术检测活化标志物 (CD25、CD69)、效应分子 (Granzyme B) 及细胞因子 (IL-17A),并通过批量RNA测序和免疫印迹检测NF-κB、STAT3等信号通路。组间比较采用ANOVA或Kruskal‑Wallis检验。此外,利用Rag1−/−小鼠 (缺乏适应性免疫) 验证S100A8/A9二聚体的促炎作用是否依赖于T细胞。
➤活动期IBD患者粪便中存在S100A8/S100A9二聚体,且其黏膜表达与疾病活动度密切相关
通过对IBD患者肠道黏膜进行转录组分析,研究发现炎症肠黏膜中S100A8和S100A9的表达水平显著高于非炎症肠黏膜组织及健康对照 (图1A);两者的黏膜表达量与CD和UC患者的组织学疾病活动度均呈显著正相关 (图1B、1C),且S100A8和S100A9在IBD患者黏膜中表达高度协同 (图1D)。随后,以人重组蛋白为参照,尺寸排阻色谱明确S100A8与S100A9等比例混合主要形成CP异源四聚体,同时存在少量二聚体 (图1E),而S100A8或S100A9单独则形成同源二聚体 (图1F),为粪便样本的构型判定提供了标准。实验流程如图1G所示。进一步对活动期CD和UC患者 (粪便CP > 500 μg/g) 的粪便进行尺寸排阻色谱分离,在分子量对应于二聚体的色谱组分中 (图1H、1I),通过LC-MS/MS清晰检测到S100A8和S100A9 (图1J),且二聚体浓度与同一来源样本中的CP相当 (图1K)。结肠镜灌洗液样本同样证实了二聚体的存在 (图1L、1M、1N、1O)。而健康对照的粪便中未见二聚体信号 (图1J)。综上,活动期IBD患者粪便和肠腔中除CP四聚体外还存在大量S100A8/S100A9二聚体,且其黏膜表达水平与疾病严重程度紧密相关,为后续探索二聚体的生物学功能与临床价值奠定了关键基础。
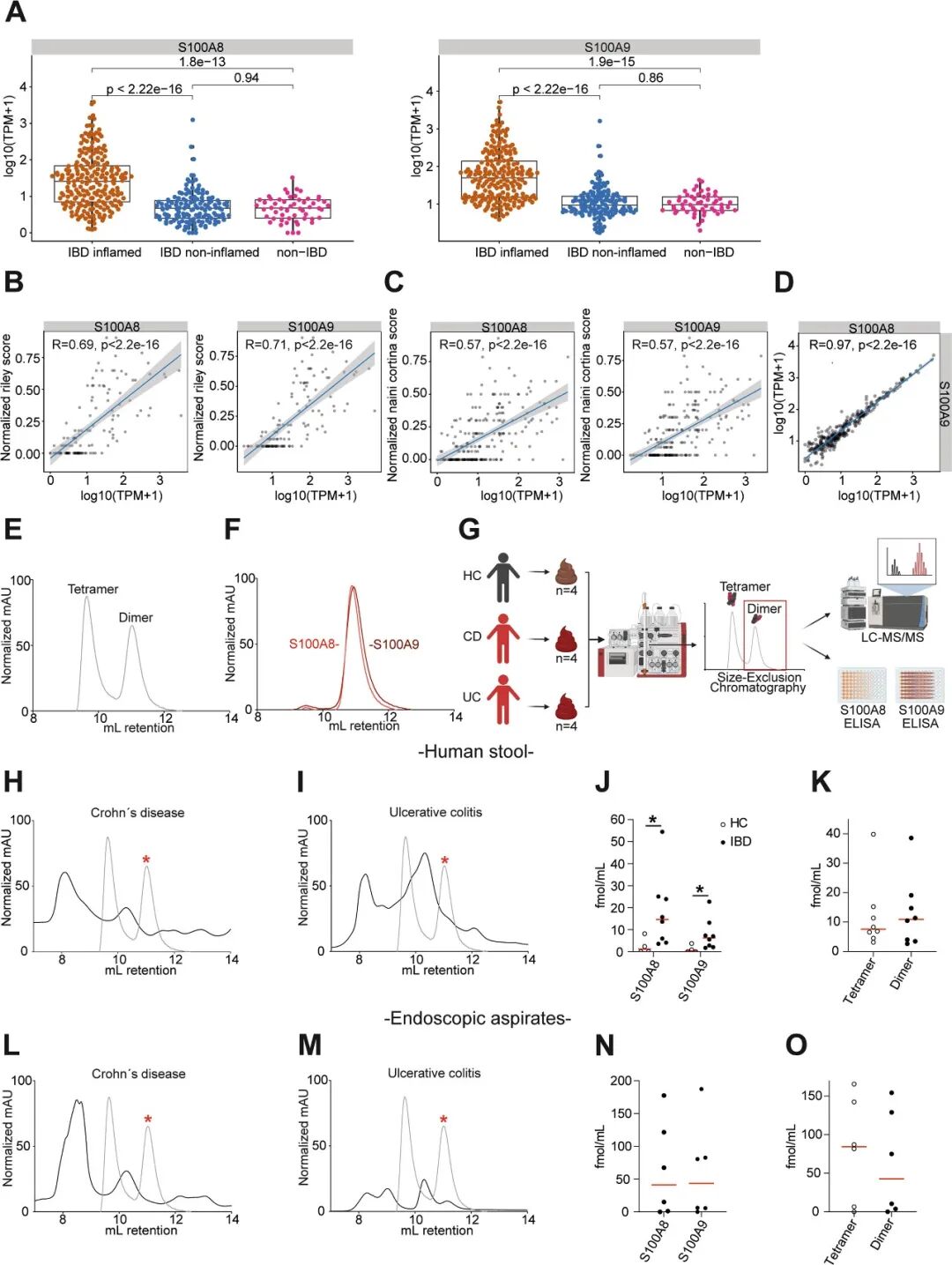
图1. IBD患者粪便中S100A8和S100A9二聚体的检测。
➤S100A9二聚体检出与低CP水平IBD患者的临床和内镜疾病活动度相关,现有临床CP检测存在诊断缺口
四种临床常规粪便CP检测试剂盒均能识别重组S100A8/S100A9异源四聚体,但无法检测S100A8或S100A9同源二聚体 (图2A);相比之下,研究专用的ELISA可特异性检测S100A8或S100A9二聚体,且不识别CP (图2B、2C),证实现有临床检测存在诊断缺口。研究流程如图2D所示。随后,对来自奥地利和荷兰两个独立IBD队列共539例患者进行检测,发现粪便S100A8二聚体检出率为46%,S100A9为15%,且两者的检出率与粪便CP浓度是否超过150 μg/g无明确关联 (图2E、2F);健康对照中几乎无S100A9检出,仅少数有微量S100A8。进一步对粪便CP ≤ 150 μg/g的356例IBD患者进行分析,逻辑回归分析显示,S100A9二聚体的检出与临床疾病活动度显著相关 (未校正OR=2.14,P=0.022),校正年龄、性别及疾病类型后关联仍稳健 (OR=2.27,P=0.015),而S100A8检出无此关联 (图2G)。最后在德国队列的84例IBD患者中验证,低CP浓度 (≤ 150 μg/mL) 患者的结肠灌洗液中,S100A9浓度与临床、内镜疾病活动性均呈正相关 (图2H、2I)。临床CP检测无法识别具有潜在诊断价值的S100A8/A9二聚体,粪便S100A9二聚体检出可作为低CP浓度IBD患者判断临床和内镜活动度的补充标志物。
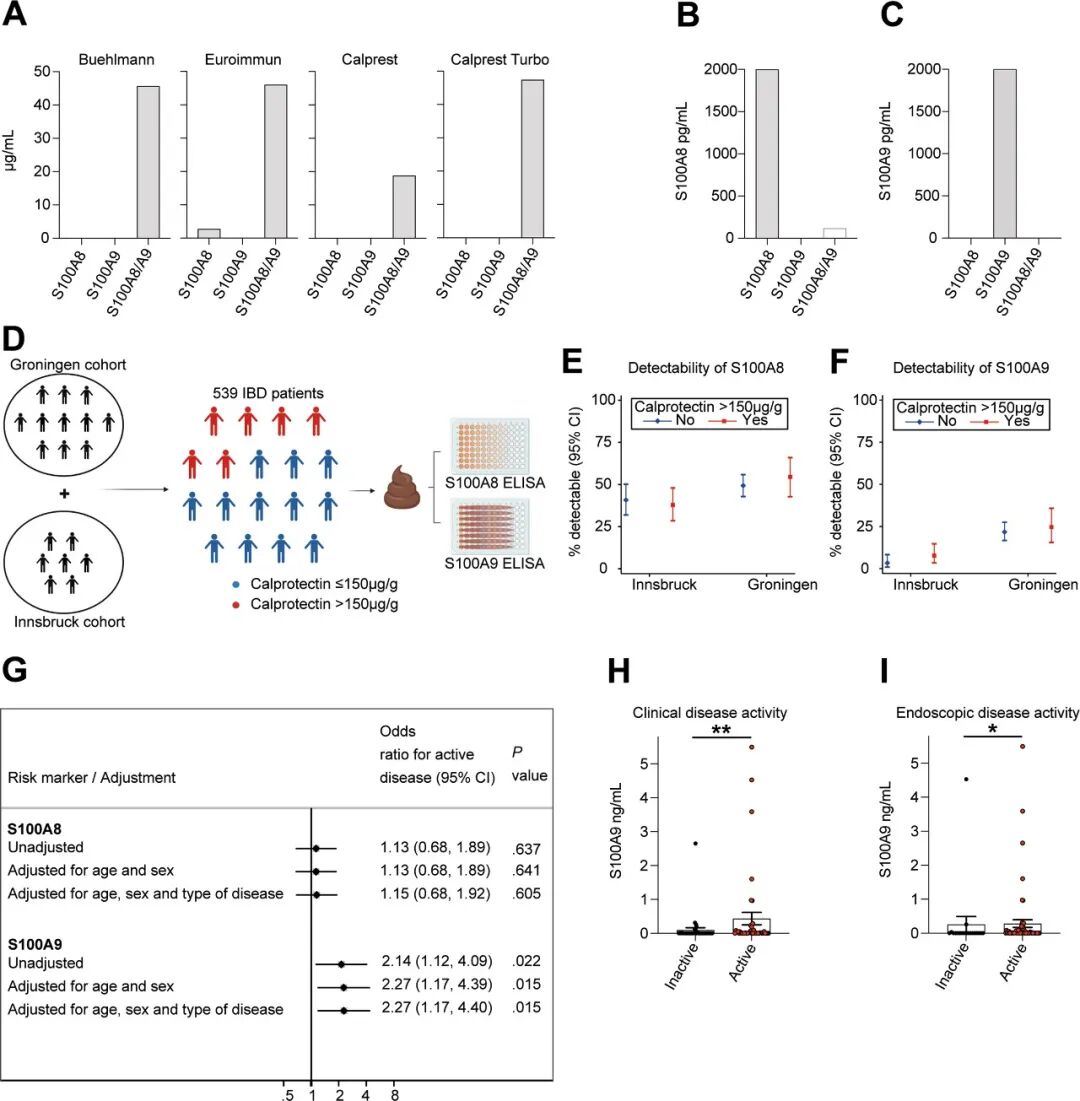
图2. S100A8和S100A9的定量及其与IBD疾病活动度的关系。
➤人S100A8/S100A9同源二聚体可加重小鼠肠道炎症,敲除S100a9可缓解小鼠肠道炎症
研究通过多种小鼠肠炎模型系统评估了S100A8/A9二聚体的体内促炎功能 (图3A)。首先在DSS诱导的急性结肠炎野生型小鼠中连续4天灌胃人重组S100A8或S100A9同源二聚体,结果发现小鼠体重显著下降 (图3B)、结肠组织学损伤评分明显升高 (图3C、3D),同时结肠黏膜中CD4+和CD8+ T细胞的浸润数量显著增加 (图3E、3F);而灌胃CP异源四聚体的小鼠则未出现上述效应,表明二聚体的促炎作用具有构型特异性。在S100a9敲除小鼠中同样观察到,人S100A8或S100A9二聚体仍可加重DSS结肠炎,排除了人鼠蛋白嵌合效应的干扰。在Il10−/−慢性自发性结肠炎模型中,连续7天灌胃S100A8或S100A9二聚体同样显著加重了结肠炎的组织学损伤 (图3G、3H)。此外,在西方饮食诱导的CD样肠炎模型 (Gpx4+/−IEC和Xbp1−/−IEC小鼠) 中,灌胃S100A8或S100A9二聚体也进一步恶化了肠黏膜炎症。反之,在DSS结肠炎模型中,S100a9−/−小鼠的体重下降程度减轻、结肠组织学评分显著低于野生型及杂合子对照 (图3I-K)。在西方饮食诱导的CD样肠炎模型中,S100a9−/−与Gpx4+/−IEC双突变小鼠的肠炎评分较单突变对照明显降低 (图3L);在Xbp1−/−IEC自发性肠炎模型中,S100a9−/−与Xbp1−/−IEC双突变小鼠的肠炎评分同样显著改善 (图3M)。研究证实,S100A8和S100A9同源二聚体是肠道炎症的驱动因子,而S100a9是介导肠炎发生发展的关键基因。
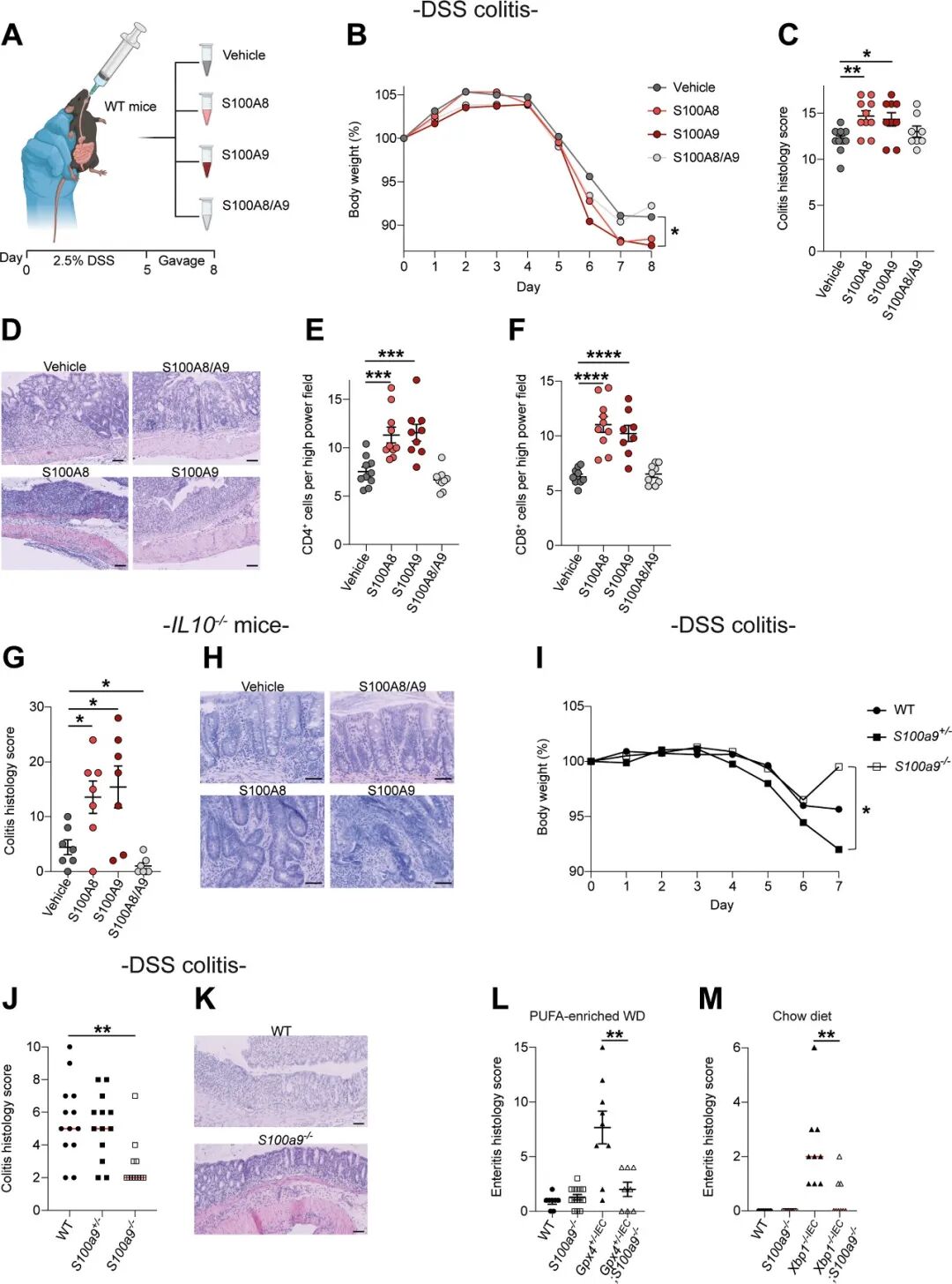
图3. 人S100A8和S100A9同源二聚体促进小鼠肠道炎症。
➤人S100A8/A9同源二聚体可诱导人结肠上皮炎症反应并激活特异性促炎信号通路
研究首先通过免疫共沉淀结合LC-MS/MS构建了IBD患者粪便中S100A8/A9的蛋白互作网络 (图4A),不仅证实S100A8与S100A9之间存在相互作用 (图4B、4C),还发现二者与多种肠上皮相关蛋白 (如Galectin-4、MMP15) 存在互作,提示二聚体可能直接靶向并调控肠上皮细胞功能。随后,利用人结肠上皮类器官进行单细胞RNA测序 (图4D),发现经S100A8或S100A9同源二聚体刺激后,多种结肠上皮细胞亚型 (特别是杯状细胞和结肠细胞) 中炎症相关细胞因子的表达被广泛诱导,例如杯状细胞中趋化因子配体CCL20显著上调 (图4E)。进一步通路活性分析发现,S100A8二聚体主要激活结肠上皮细胞中的TNF和NF-κB信号通路,而S100A9二聚体则诱导缺氧信号通路活化 (图4F)。研究从蛋白互作网络和单细胞转录组层面首次揭示了人S100A8/A9同源二聚体可直接作用于人结肠上皮,通过激活不同的促炎信号通路广泛诱导上皮细胞炎症因子表达,从而促进肠道炎症发生发展。
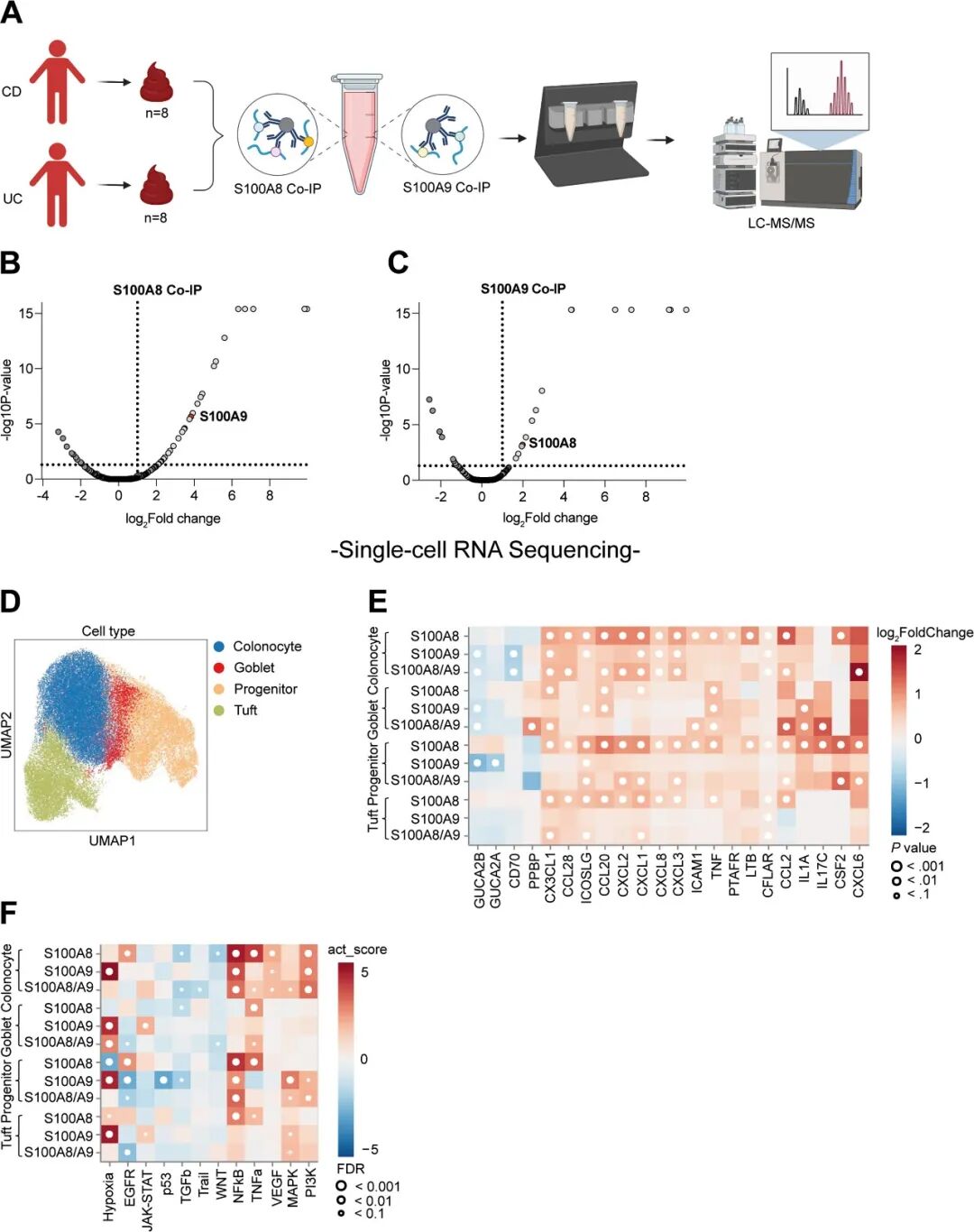
图4. 人S100A8和S100A9同源二聚体诱导上皮细胞因子反应。
➤人S100A8/A9同源二聚体可增强人CD4+和CD8+ T细胞的活化,激活NF-κB及JAK/STAT信号通路并诱导促炎细胞因子分泌
为明确二聚体对适应性免疫的直接影响,研究从健康人外周血分离CD4+和CD8+ T细胞进行体外刺激实验 (图5A)。流式细胞术检测显示,S100A8或S100A9同源二聚体可显著促进CD4+T、CD8+ T细胞的活化,表现为活化标志物CD25、CD69的表达显著上调,同时效应记忆T细胞 (CD45RO+) 比例增加 (图5B-G),而CP无上述效应,表明二聚体的促活化作用具有构型特异性。此外,S100A9二聚体可增加CD8+ T细胞中颗粒酶B的表达 (图5H),且S100A8和S100A9二聚体均能诱导CD3+ T细胞分泌IL-17A,但不影响IFN-γ或TNF-α的产生 (图5I)。通过对CD8+ T细胞的转录组和蛋白水平验证,研究发现S100A8/A9二聚体可激活NF-κB和JAK/STAT信号通路 (图5J-L),这两个通路是T细胞活化和炎症反应的核心通路。最后,通过抗原反应性T细胞富集实验,检测到针对S100A9二聚体的抗原特异性记忆CD4+ T细胞。综上,人S100A8和S100A9同源二聚体可直接增强人CD4+和CD8+ T细胞的活化与促炎功能,且S100A9本身可作为T细胞识别的抗原靶点。
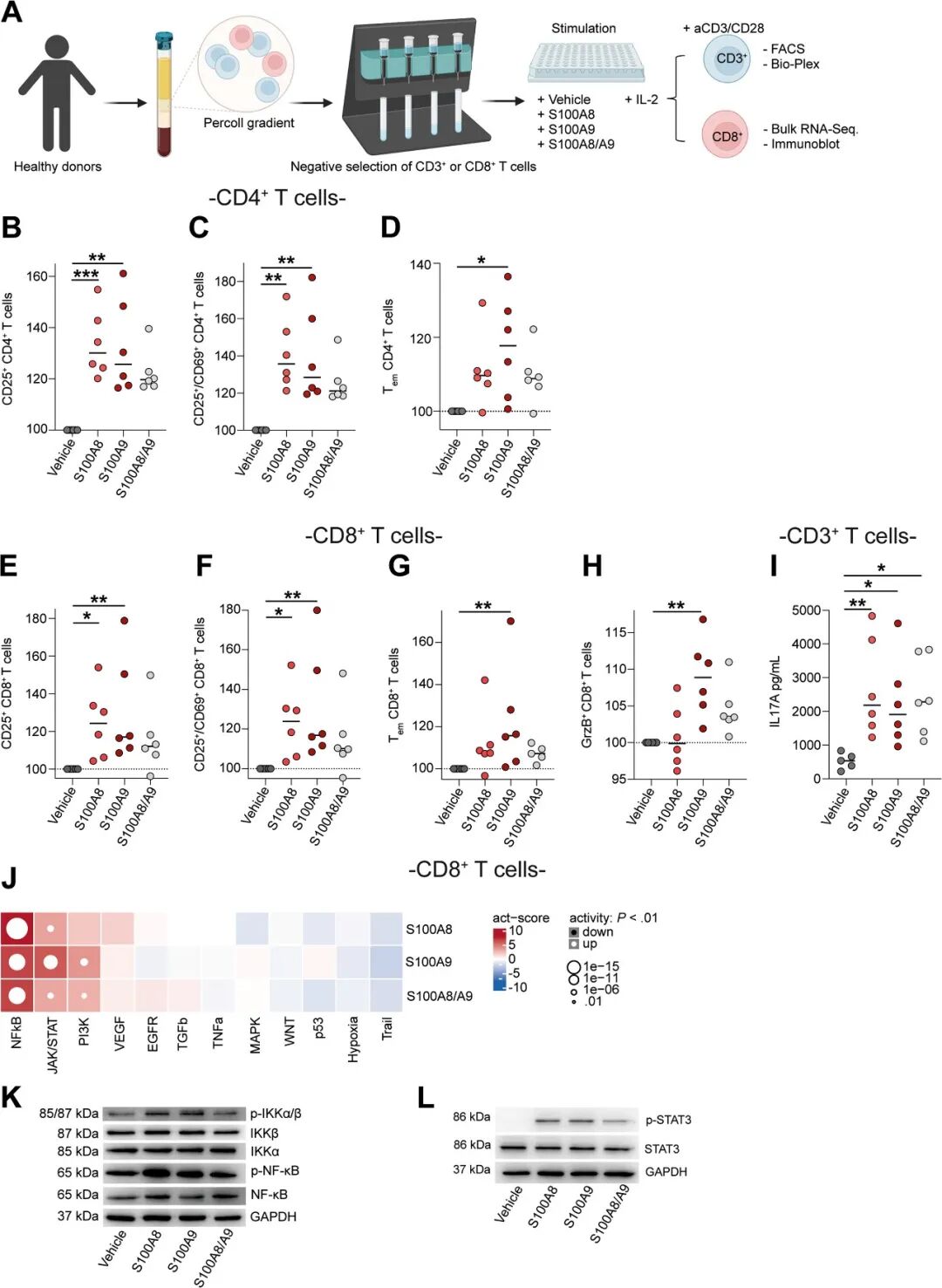
图5. 人S100A8和S100A9同源二聚体增强T细胞活化。
➤S100A8/A9同源二聚体的促结肠炎作用依赖于适应性免疫,药物抑制S100A9可有效缓解小鼠急性和慢性结肠炎
为明确S100A8/A9二聚体促炎作用的免疫依赖性及靶向治疗潜力,研究首先利用缺乏适应性免疫的Rag1−/−小鼠构建DSS结肠炎模型,并灌胃人重组S100A8或S100A9同源二聚体。结果发现,与溶剂对照组相比,二聚体处理组小鼠的体重下降曲线 (图6A)、结肠组织学损伤评分 (图6B) 及组织切片 (图6C) 均无显著差异,证明二聚体的致结肠炎作用依赖于适应性免疫。随后,使用S100A9特异性小分子抑制剂Paquinimod进行药理学干预。在DSS诱导的急性结肠炎野生型小鼠中,连续7天口服Paquinimod可显著降低结肠组织学评分、减轻黏膜炎症损伤 (图6D、6E)。在Il10−/−慢性自发性结肠炎模型中,连续14天给予Paquinimod同样显著改善结肠组织学炎症 (图6F、6G)。研究从遗传和药理学两个层面系统阐明,S100A8/A9同源二聚体依赖适应性免疫细胞 (特别是T细胞) 驱动肠道炎症,而靶向抑制S100A9可同时缓解急性和慢性实验性结肠炎,为IBD的免疫靶向治疗提供了强有力的临床前依据。
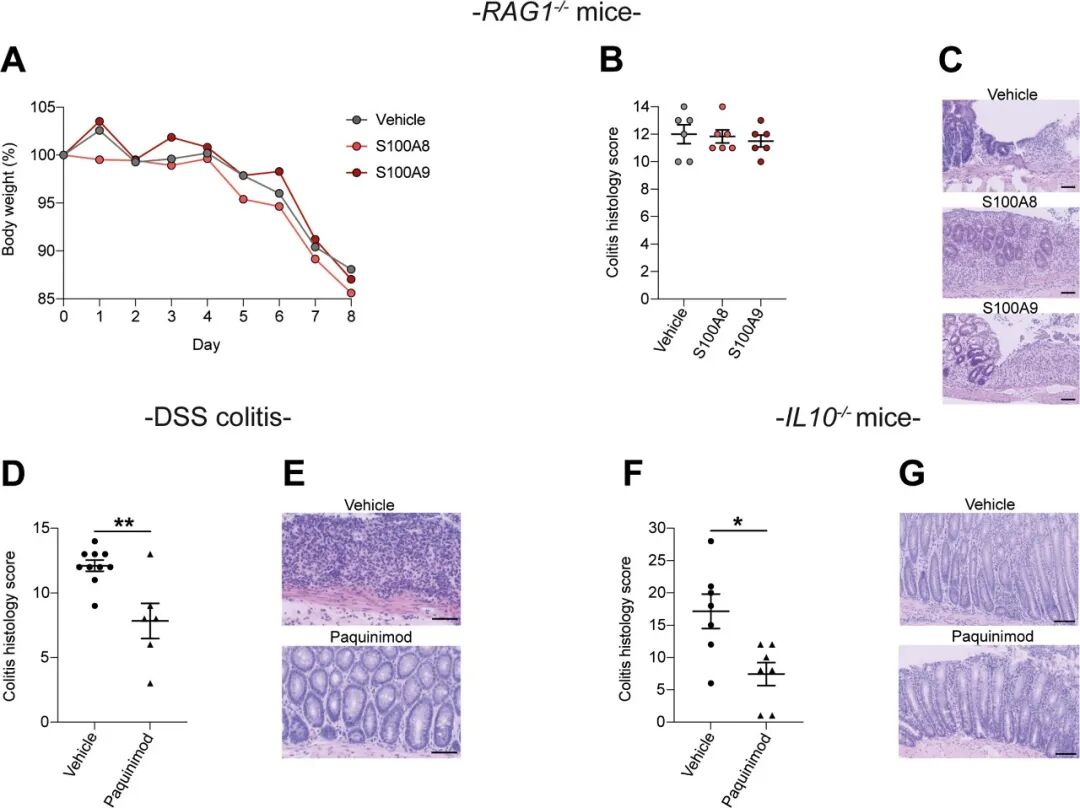
图6. 人S100A8和S100A9同源二聚体的致结肠炎作用需要适应性免疫。
粪便中S100A8与S100A9二聚体不仅可能是肠道炎症的新型生物标志物,也是IBD的潜在抗炎治疗靶点。未来仍需开展以大样本、内镜终点为指标的大型对照试验,以确立靶向S100A8/S100A9在IBD诊断或治疗中的临床价值。