
痴呆综合征的核心病理特征为神经退行性变伴脑细胞死亡。目前,神经退行性变已被纳入阿尔茨海默病研究框架,且与多种痴呆综合征的病情进展、疾病分期密切相关。血液生物标志物具备易获取、可规模化、微创的优势,为神经退行性变研究提供了新方法。神经丝轻链(NfL)、总Tau、胶质纤维酸性蛋白(GFAP)、泛素羧基末端水解酶L1(UCH-L1)均为新兴的神经退行性病变血液标志物。
近期发表于《Neurology》的一项美国REGARDS双种族前瞻性队列研究证实:血浆GFAP、NfL水平升高,可显著增加全因死亡、痴呆特异性死亡及心血管特异性死亡风险,且该关联存在显著种族差异,为老年人群死亡风险分层与早期预警提供了关键外周血指标。
研究从REGARDS队列中随机抽取受试者亚组,按年龄(45~54岁20%、55~64岁20%、65~74岁25%、75~84岁25%、≥85岁10%)、种族(黑人50%、白人50%)、性别(男性50%、女性50%)分层,以最大化年龄与种族差异的统计效能。研究终点死亡事件包括:全因死亡、痴呆特异性死亡、心血管特异性死亡及其他原因死亡。
最终纳入917名受试者,基线平均年龄67.4岁(SD=12.1),女性占49.4%,黑人占48.6%;平均随访11.1年(SD=5.7),51.0%受试者死亡,其中9.2%(86/935)为痴呆特异性死亡。
GFAP完全校正模型中,三分位最高组较最低组的原因特异性风险比(HR)为2.20(95%CI 1.46-3.29);以连续变量分析,每升高1个标准差,校正后全因死亡风险增加88%(HR=1.88,95%CI 1.43~2.46)。NfL与UCH-L1呈现相似趋势:NfL三分位最高组较最低组HR=2.87(95%CI 1.82~4.54),每升高1个标准差,校正后全因死亡风险增加89%(HR=1.89,95%CI 1.54~2.32);UCH-L1三分位最高组较最低组HR=1.40(95%CI 1.09~1.79),每升高 1 个标准差,校正后全因死亡风险增加22%(HR=1.22,95%CI 1.08~1.37)。
此外,GFAP、NfL的三分位与连续变量水平,均与种族存在交互作用,进而影响全因死亡风险关联强度。黑人受试者中,GFAP、NfL三分位组间比较及每1标准差增量的HR值均低于白人受试者,提示种族可修饰生物标志物与全因死亡的关联强度。
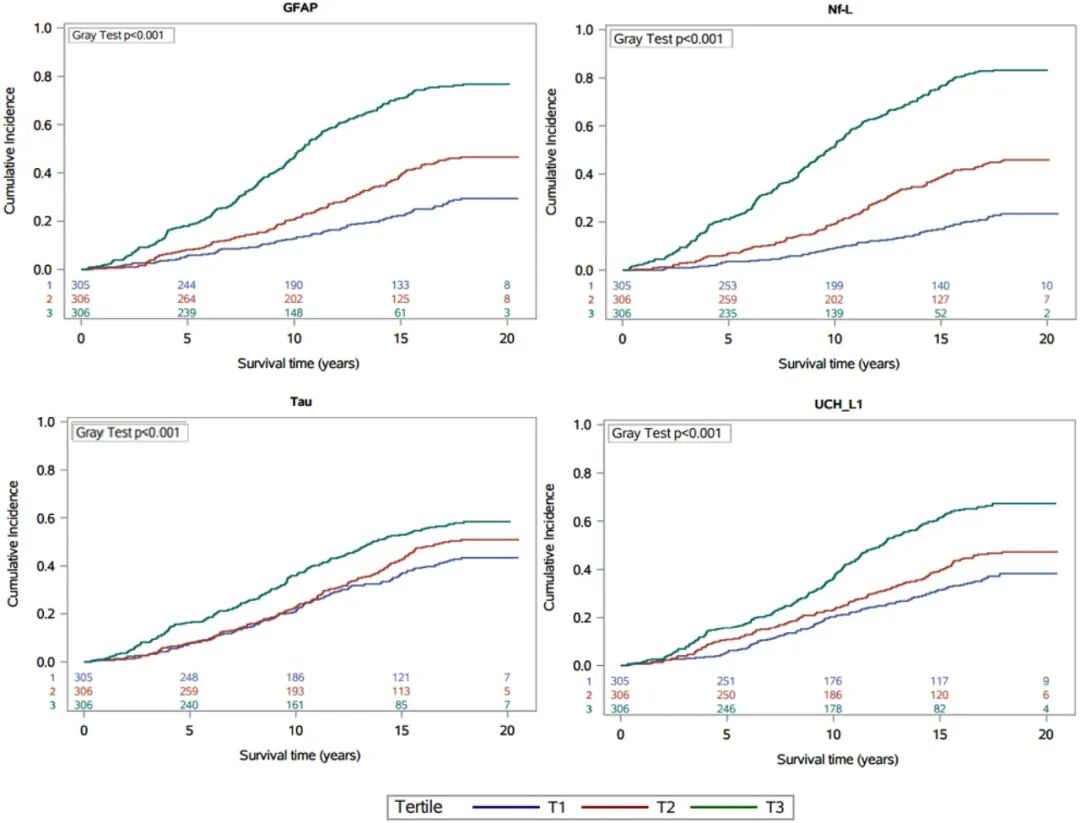
图1 不同生物标志物下全因死亡时间的累积发生率曲线
完全校正模型中,GFAP与痴呆特异性死亡的关联最强:每升高1个标准差,校正后痴呆特异性死亡风险升至5.66倍(HR=5.66,95%CI 2.91~11.00)。NfL每升高1个标准差,校正后痴呆特异性死亡风险升至2.72倍(HR=2.72,95%CI 1.57~4.71)。总Tau以连续变量分析时,与痴呆特异性死亡无显著关联(每1标准差增量HR=1.22,95%CI 0.84~1.76)。
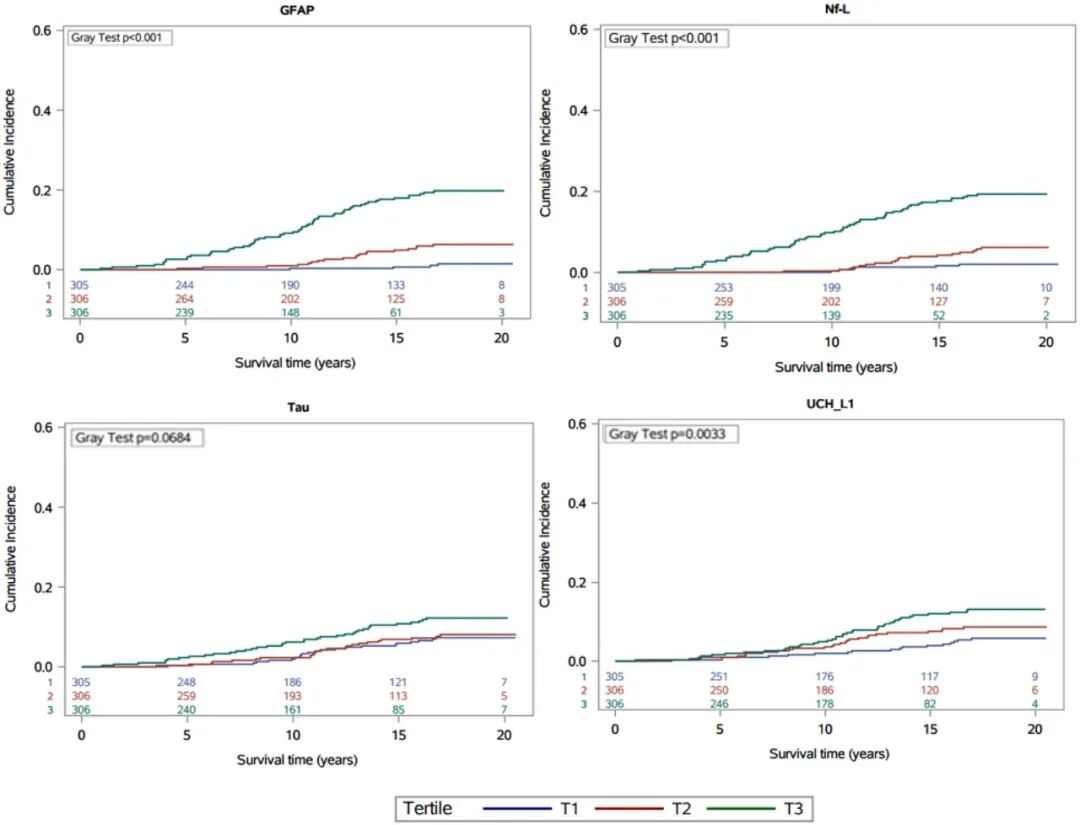
图2不同生物标志物下痴呆症特定死亡率的时间累积发生率图
心血管特异性死亡方面,NfL的关联强度最高:完全校正模型中,NfL每升高1个标准差,校正后心血管特异性死亡风险升至2.27倍(HR=2.27,95%CI 1.72~2.98)。GFAP每升高1个标准差,校正后心血管特异性死亡风险升至2.13倍(HR=2.13,95%CI 1.25~3.62);UCH-L1与该终点呈轻度相关,总Tau无显著关联。
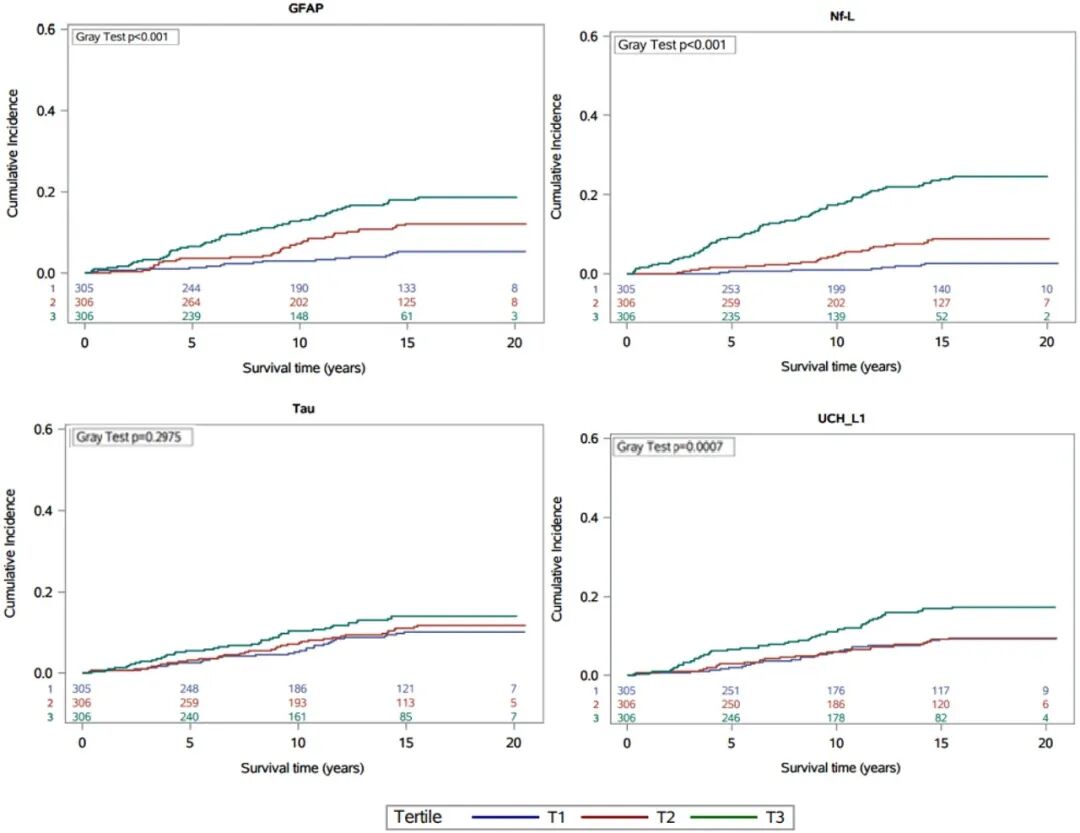
图3各生物标志物对应的心血管特异性死亡率的时间累积发生率曲线
这项人群双种族队列研究证实:校正竞争风险后,基线血浆GFAP、NfL水平升高,与随访9.5年的全因死亡、痴呆特异性死亡、心血管特异性死亡风险升高均相关,且该关联主要由白人受试者驱动。UCH-L1与全因死亡、其他原因死亡相关;总Tau仅三分位最高组与痴呆特异性死亡相关,连续变量分析无关联。总体而言,研究提示上述标志物对痴呆特异性死亡的预测特异性有限,仅GFAP、NfL与该终点的关联更显著。
结果与既往非痴呆人群的队列研究一致,即循环NfL水平与全因死亡风险相关。研究结果与先前在无痴呆人群中进行的人群研究一致,即循环NfL与全因死亡率相关。REGARDS研究队列的平均年龄(67岁)较心血管健康研究(CHS)队列(77岁)年轻,且黑人参与者比例更高(49%vs13%),这可能有助于提高研究结果的适用性。与CHS研究结果相似,研究发现血浆NfL与痴呆特异性死亡率相关。
GFAP是脑星形胶质细胞损伤的特异性标志物,健康人群中表达水平极低,阿尔茨海默病患者脑组织中GFAP水平显著升高。研究发现,完全校正后GFAP水平升高与全因死亡相关,该关联强度高于芝加哥健康与老龄化项目(CHAP,1327名老年受试者)的结果。研究还发现GFAP与痴呆特异性死亡率存在更强的关联,这高于CHS研究中观察到的结果。
总Tau与死亡风险的关联,在神经退行性疾病、
参考文献:Sawyer RP, Blair J, Judd SE, et al. Circulating Biomarkers of Neurodegeneration and All-Cause and Dementia-Specific Mortality. Neurology. 2026;106(7):e214752. doi:10.1212/WNL.0000000000214752