前言
尽管PD-1/PD-L1抑制剂单药已成为驱动基因阴性、PD-L1阳性晚期
研究简介
PD-1和PD-L1抑制剂已被证实可与抗血管生成药物在NSCLC中产生协同作用。本研究旨在对比贝莫苏拜单抗联合安罗替尼与帕博利珠单抗,在既往未接受过治疗、驱动基因阴性且PD-L1阳性的晚期NSCLC患者中的疗效。
这项设盲、随机、对照的III期CAMPASS试验在中国79家中心开展。入组患者为18-75岁、IIIB-IV期鳞状或非鳞状NSCLC患者,既往未接受过针对晚期、复发或转移性疾病的系统性治疗,PD-L1肿瘤比例评分≥1%,预期生存期≥3个月,至少存在1个可测量病灶,且东部肿瘤协作组(ECOG)体能状态评分为0或1。患者按2:1比例随机分配,分别接受静脉输注贝莫苏拜单抗(第1天1200 mg)联合口服安罗替尼(第1-14天每日12 mg)或静脉输注帕博利珠单抗(第1天200 mg)联合安慰剂,每3
随机化由中心完成,并根据肿瘤组织学类型、PD-L1肿瘤比例评分及脑转移情况进行分层。研究者知晓治疗分配情况,患者及统计师对分组设盲。主要终点为无进展生存期(PFS),由盲态独立评审委员会(IRC)依据实体瘤疗效评价标准1.1版,在意向治疗人群(所有随机分配患者)中评估。安全性在所有接受至少1剂研究药物的随机分配患者中评估。本文报告的的结果来自针对PFS的预定最终分析。本研究已停止招募,仍在进行中,已在ClinicalTrials.gov注册(注册号NCT04964479)。
2021年8月6日至2022年12月14日期间,共531例患者被随机分配(354例至贝莫苏拜单抗联合安罗替尼组,177例至帕博利珠单抗联合安慰剂组)。其中449例(85%)为男性,82例(15%)为女性,493例(93%)为汉族。贝莫苏拜单抗联合安罗替尼组有2例患者、帕博利珠单抗联合安慰剂组有1例患者未接受治疗,因此被排除在安全性分析人群之外。
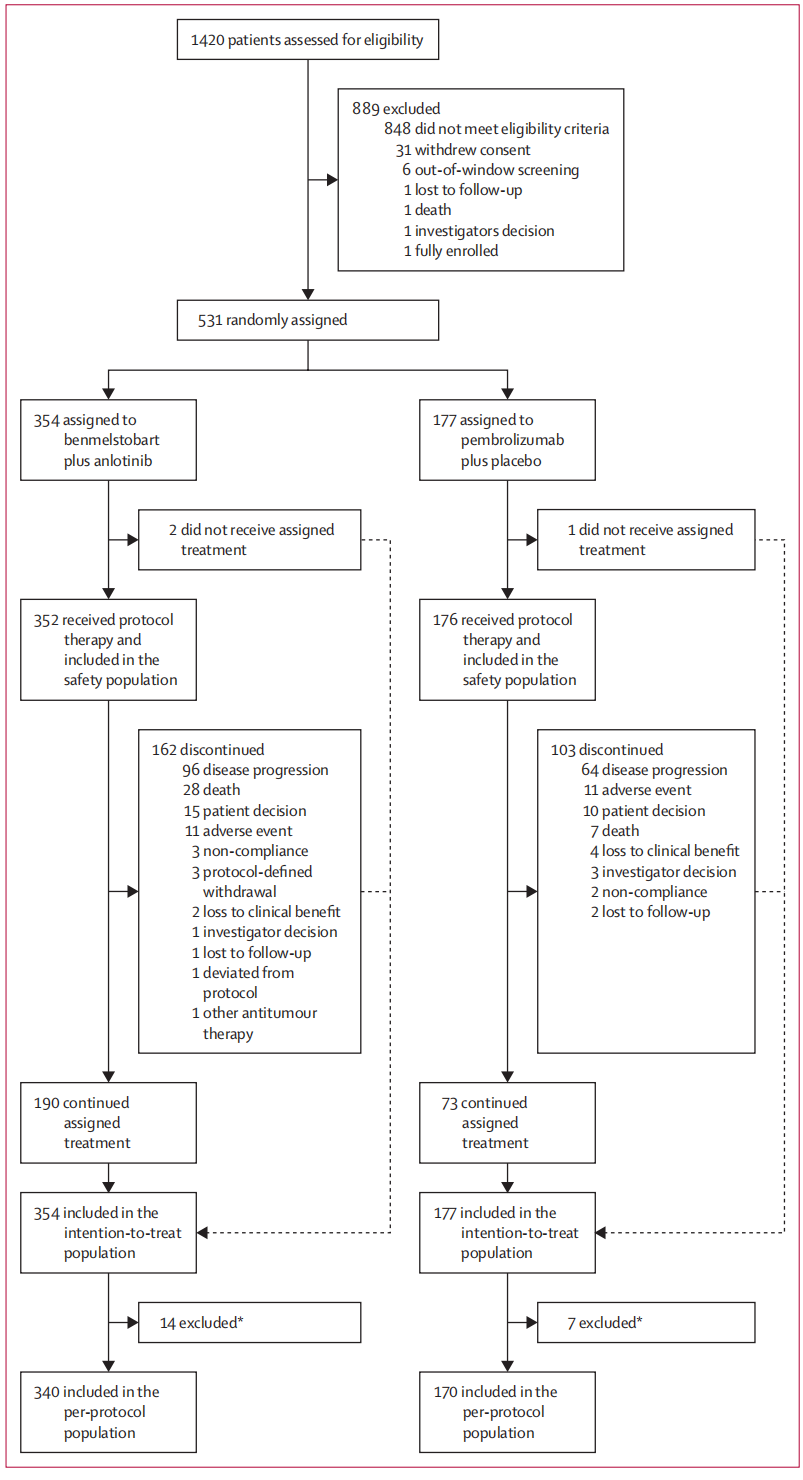
图1. 试验概况(上下滑动查看)
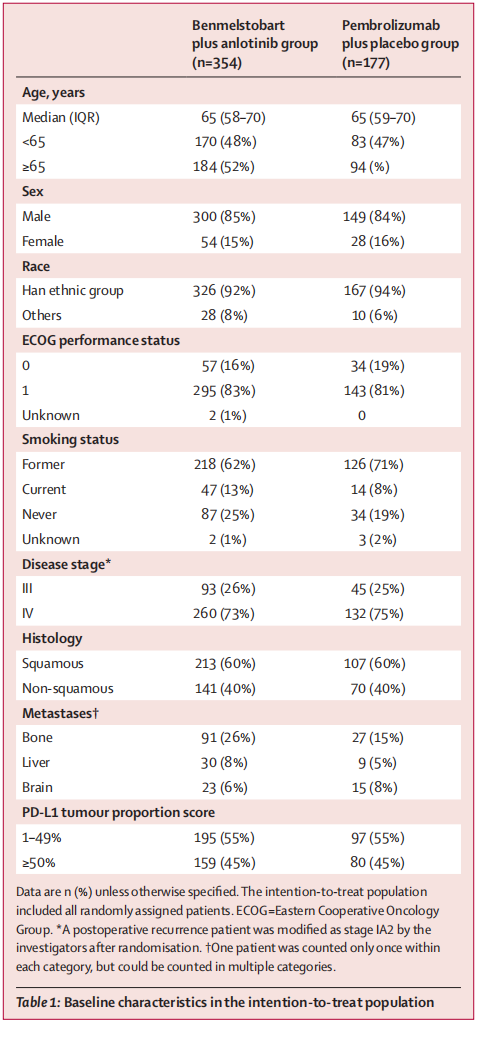
表1. 意向治疗人群的基线特征(上下滑动查看)
贝莫苏拜单抗联合安罗替尼组的中位随访时间为11.4个月(95% CI:9.4个月-13.1个月),帕博利珠单抗联合安慰剂组为10.6个月(95% CI:9.0个月-13.0个月),两组中位PFS分别为11.0个月(95% CI:9.2个月-12.6个月)和7.1个月(95% CI:5.8个月-9.5个月)(风险比[HR]=0.70,95% CI:0.54-0.90;log-rank检验P=0.0057)。
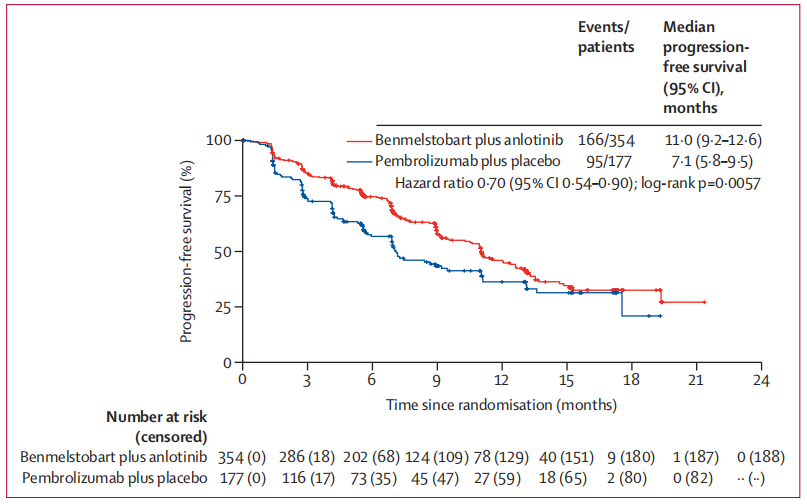
图2. 意向治疗人群的PFS
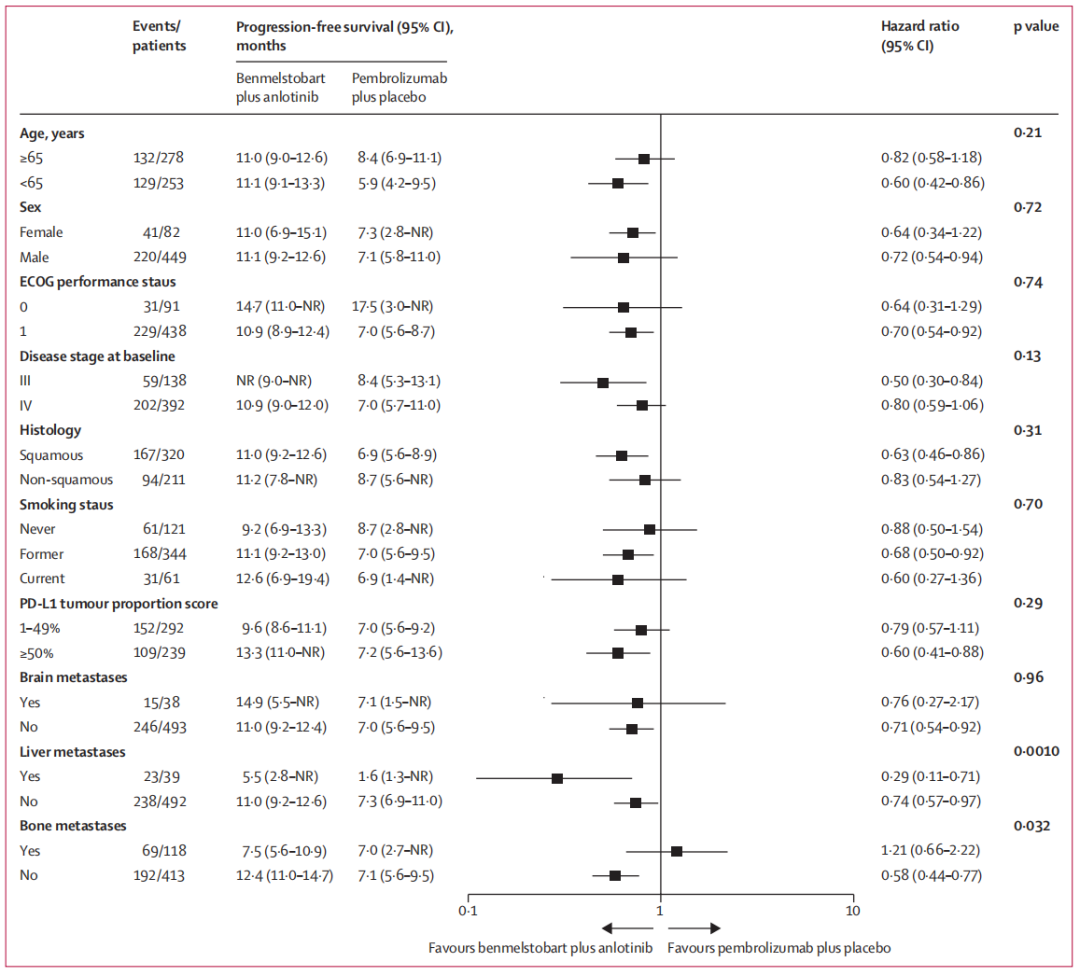
图3. 意向治疗人群PFS的亚组分析
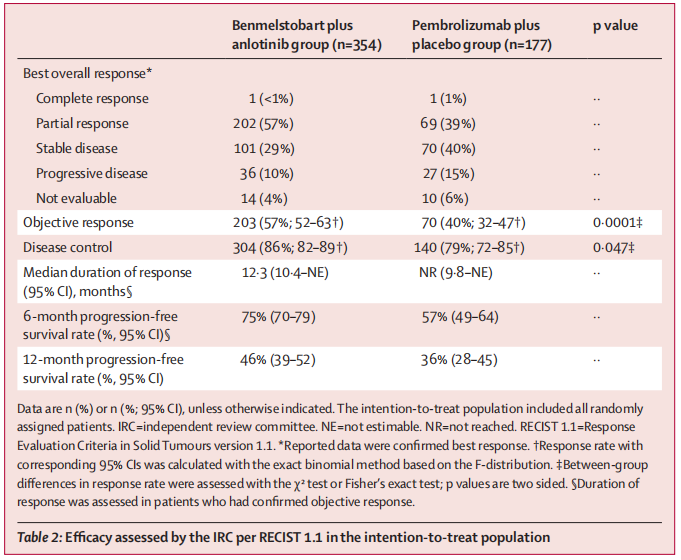
经IRC评估,贝莫苏拜单抗联合安罗替尼组354例患者中,203例(57%,95% CI:52%-63%)获得确认客观缓解。帕博利珠单抗联合安慰剂组177例患者中,70例(40%,95% CI:32%-47%)获得确认客观缓解(P=0.0001)。两组各有1例患者达到完全缓解。贝莫苏拜单抗联合安罗替尼组疾病控制率为86%(304例,95% CI:82%-89%),帕博利珠单抗联合安慰剂组为79%(140例,95% CI:72%-85%)(P=0.047)。贝莫苏拜单抗联合安罗替尼组确认的中位缓解持续时间(DoR)为12.3个月(95% CI:10.4个月-未达到),帕博利珠单抗联合安慰剂组中位DoR尚未达到(95% CI:9个月-未达到)。
表2. IRC根据RECIST 1.1在意向治疗人群中评估的疗效
安全性分析显示,贝莫苏拜单抗联合安罗替尼组352例患者中,206例(59%)发生≥3级治疗相关不良事件(TRAEs),帕博利珠单抗联合安慰剂组176例患者中,51例(29%)发生TRAEs,其中最常见的是
贝莫苏拜单抗联合安罗替尼组有89例(25%)患者发生严重TRAEs,帕博利珠单抗联合安慰剂组有37例(21%),其中最常见的是
贝莫苏拜单抗联合安罗替尼组发生5例(1%)治疗相关死亡(2例死于咯血,免疫介导性肺部疾病、疾病进展、感染性
贝莫苏拜单抗联合安罗替尼较帕博利珠单抗联合安慰剂可延长PFS,且未出现新的安全性信号,提示贝莫苏拜单抗联合安罗替尼可作为驱动基因阴性、PD-L1阳性晚期NSCLC的一线治疗选择。更长时间的随访正在进行中,以评估其对总生存期的影响。
参考文献:Zhong H, Wang J, Yang R, et al. Benmelstobart plus anlotinib versus pembrolizumab as first-line treatment for PD-L1-positive, advanced non-small-cell lung cancer (CAMPASS): a blinded, randomised, controlled, phase 3 trial. Lancet Oncol. 2026 Mar 10:S1470-2045(26)00049-5.
撰写:Faline & Kenken
审校:Faline
排版:Kenken
执行:Faline
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)