对小脑
5岁女童,出生数月后出现肌张力低下和眼球运动异常。原发性凝视和眼球扫视运动及平稳跟踪运动不稳,继而发展成小脑共济失调,
5岁时因第二次精神状态发生轻微降低再次住院。她存在昏睡,长时间癫痫发作,全身肌张力障碍加重,不明原因的发烧。脑脊液检查无明显异常。肌酸激酶增加到4939 U/L(正常参考范围75-230),然后在48小时内恢复正常。脑电图显示右颞叶和全身周期性放电,叠加背景节律弥漫性减慢。重新启动
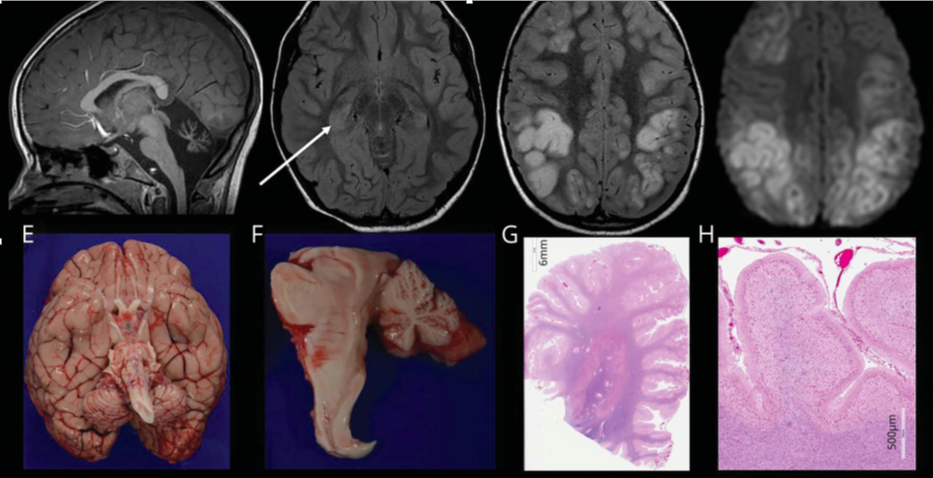
图 严重的CACNA1A基因相关疾病的神经影像学和组织病理学特征 (A–D) 5岁时入院第2天(A,B)和第10天(C,D)的脑MRI。(A) 矢状位T1图像提示小脑蚓部萎缩;(B)轴位FLAIR图像提示右侧海马信号增强、体积增大(箭头);(C)轴位FLAIR序列提示皮质高信号;(D)轴位DWI序列提示皮质多处弥散受限,以额顶部为主(未显示相应的表观扩散系数图)。(E-H)神经病理学结果。(E)大脑大体图像显示小脑和脑干偏小;(F)脑干和小脑的中矢状切面突出了蚓部和小脑半球偏小;(G)整个小脑半球提示脑叶萎缩;(H)在高倍镜下显示小脑叶已经完全丧失浦肯野细胞和外部颗粒细胞层并伴有胶质增生。
尽管完全控制了癫痫发作,但是该患者仍是脑病患者,需要继续大量的通气支持。她从入院第5天到第9天接受脉冲类固醇(甲基强的松龙每疗程30mg/kg)。在第8天,右瞳孔扩张。复查脑显像提示弥漫性水肿和双侧椎管突出,伴随光谱分析上的N-乙酰天冬氨酸低峰和可能出现的乳酸峰。
患者在入院的第8-10天,除了持续输注高渗盐水外,还接受了多疗程的
死亡后进行脑活检和神经病理学检查(图E-H)。小脑蚓部和半球萎缩,脑干内无其他病灶。浦肯野细胞完全丧失。右侧枕叶可见累及大脑皮质的出血性病变。
与CACNA1A基因相关的偏瘫性
本病例是CACNA1A基因相关疾病导致的致命性迟发性脑水肿。这种表型可能代表最严重的疾病谱末端。CACNA1A基因相关疾病的脑水肿机制被假设包括通过神经元电压门控钙通道的功能障碍而产生的细胞毒性反应和异常的神经递质释放。
在最近的急性发作中,患者的临床特征包括发烧和癫痫发作。结合海马体信号改变和脑水肿的影像学表现,推断是由于炎症/免疫介导促使研究人员进行脉冲类固醇和静脉注射免疫球蛋白的研究。在病因不明的急性难治性脑水肿病例中应考虑严重的CACNA1A相关疾病。
除颅内高压治疗(如高渗盐水、甘露醇)外,皮质类固醇治疗在一些CACNA1A基因相关疾病急性发作相关的脑水肿病例中也能获益。在发作性共济失调Ⅱ型中,
该患者最初在死亡前几年出现张力减退和显著的小脑征象,MRI上有孤立小脑蚓部萎缩的证据。已知CACNA1A基因相关疾病与孤立性小脑萎缩有关,即使在没有发作性临床表现的情况下,在对儿童期共济失调进行鉴别诊断时,也应考虑到这一脑部影像学表现。临床医生根据CACNA1A基因相关疾病的早期诊断应考虑进行预防性药物治疗试验。尽管没有证据表明药物治疗会改变临床结局,但鉴于表型亚型患者急性发作的严重性,进行预防性药物治疗试验是合理的。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)