前言
BCSC具有独特的表型可塑性,可在上皮间质转化(EMT)和间质上皮转化(MET)状态间动态转换,且受Notch、PI3K/AKT/mTOR、Hedgehog(Hh)和Wnt/β-catenin等关键信号通路调控。此外,BCSC与TME中的癌症相关成纤维细胞(CAF)、免疫细胞、细胞因子及缺氧微环境的相互作用,进一步强化其干细胞特性、转移能力和治疗耐药性,成为乳腺癌恶性进展的核心调控网络。
► 1.BCSC核心标志物及功能特性
BCSC的生物学行为依赖特异性标志物的调控,已鉴定的核心标志物通过靶向关键信号通路,共同维持其自我更新、致瘤性、转移能力和耐药性,且具有显著的亚型特异性。例如经典BCSC标志物CD44,通过胞内域切割激活干细胞相关基因,且可被骨形态发生蛋白2(BMP2)上调,增强BCSC的转移潜能,与肿瘤侵袭前沿富集及肺转移密切相关;CD133与乳腺癌脑转移相关,在ER+/HER2-亚型中,高表达CD133的肿瘤细胞DNA修复能力较弱,但免疫活性更强,新辅助化疗应答更佳,而低表达则与高增殖以及较差的预后相关。
此外,ALDH、转录因子相关标志物、CD29(ITGB1)以及GD2通过调控不同信号通路,促进肿瘤的增殖、耐药以及转移。这些标志物通过特异性信号通路调控其生物学行为,且与乳腺癌亚型、临床表型密切关联,为精准识别和靶向BCSC提供了分子基础。
► 2.BCSC驱动肿瘤复发与转移的机制
BCSC是乳腺癌复发和转移的核心驱动力,其独特的生物学特性和多层面调控机制共同促进肿瘤恶性进展。
在肿瘤复发调控中,常规治疗难以清除处于静止期的BCSC,这些存活的BCSC以循环肿瘤细胞(CTC)形式进入血液循环,播散至远处器官并形成播散性肿瘤细胞(DTC),经长期休眠后重新激活,最终引发肿瘤复发。
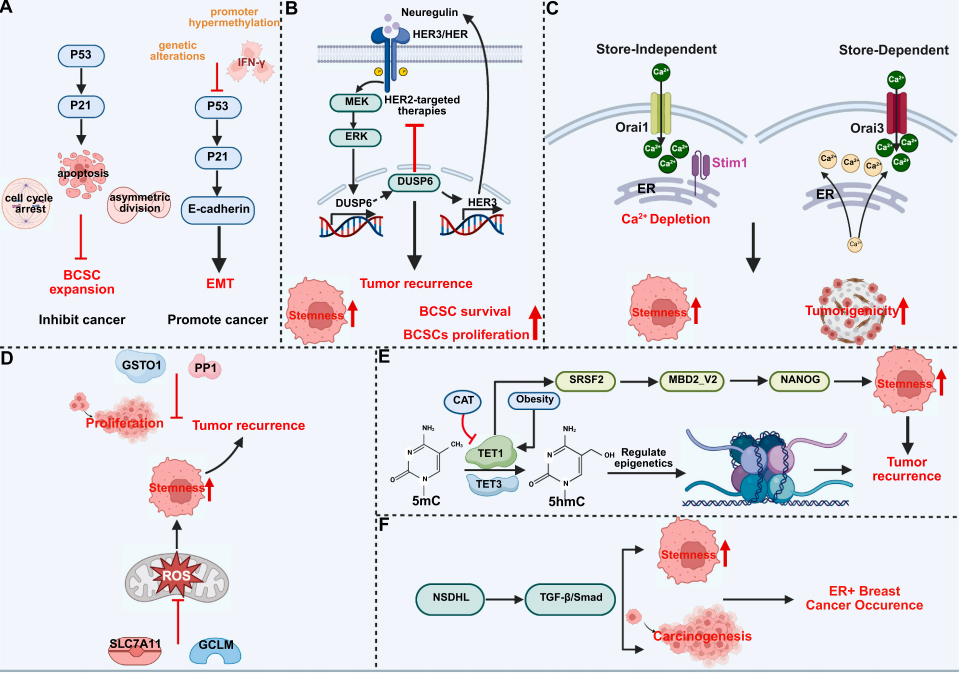
图1:BCSC介导的肿瘤复发分子机制1
在肿瘤转移调控中,EMT是核心机制,通过破坏上皮细胞极性与细胞间黏附,增强BCSC的间质迁移能力,为其脱离原发肿瘤、侵入循环系统奠定基础。并且多条信号通路通过诱导EMT增强BCSC的转移潜能,其中HER2/STAT3、CXCL12/CXCR4通路的激活是关键调控环节。此外,不同BCSC亚型在转移过程中呈现明确的功能分工:间质样BCSC主要负责原发肿瘤的播散,而上皮样BCSC则在远处器官中启动转移灶的定植与生长。
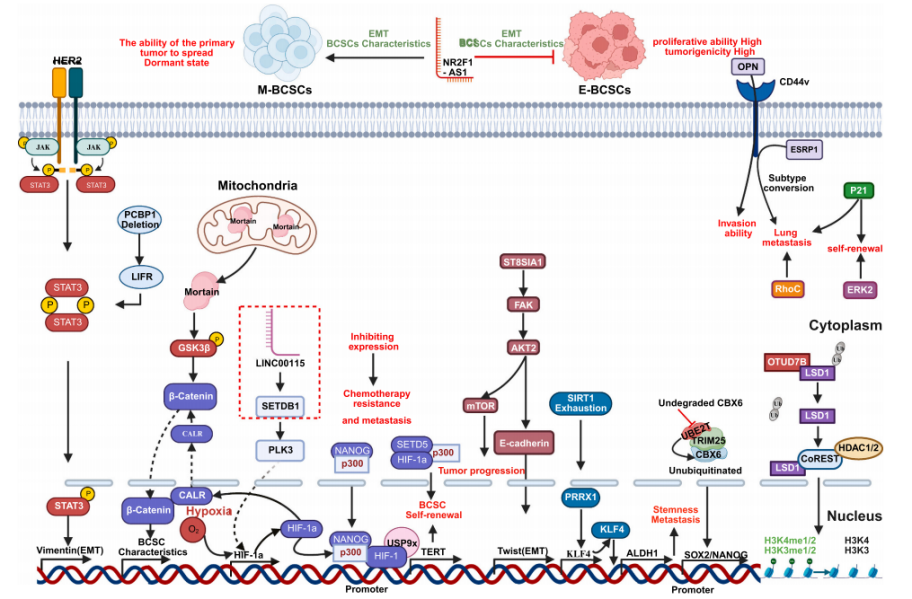
图2:通过BCSC驱动肿瘤转移的关键分子通路1
► 3. BCSC与肿瘤微环境的串扰机制
TME作为复杂的动态系统,通过细胞成分、细胞因子及缺氧、pH值与BCSC形成紧密串扰,使BCSC维持干细胞特性和恶性表型。例如缺氧微环境作为TME的核心特征,通过HIF-1α上调多能性因子(OCT4、NANOG),激活Notch通路促进EMT,增强BCSC的增殖和转移能力;而CAF通过分泌神经生长因子、miR-221、Hh配体等分子,激活PI3K/AKT、Notch通路,促进BCSC扩增和内分泌耐药。
此外,TME中IL-6、IL-8、CXCL1等细胞因子介导的信号传递,免疫细胞相互作用等多组分的协同作用,形成多层次调控网络,持续强化BCSC的恶性表型。
► 4. BCSC的耐药机制
BCSC通过多种机制协同构成耐药网络,是化疗失败与肿瘤复发的核心原因。其耐药机制主要包括:
过表达ABC转运体(尤其ABCG2)主动外排化疗药物,减少细胞内药物积累;
JAK/STAT3通路、RAC1剪接变体RAC1B等信号通路维持干细胞特性,增强耐药性;
EMT及miR-200家族下调通过激活STAT3信号强化干细胞样表型;
自噬在代谢和治疗应激下支持细胞存活,且对ALDH+、CD29高表达/CD61+等不同亚型的调控依赖不同通路,适度自噬可维持BCSC休眠与耐药。
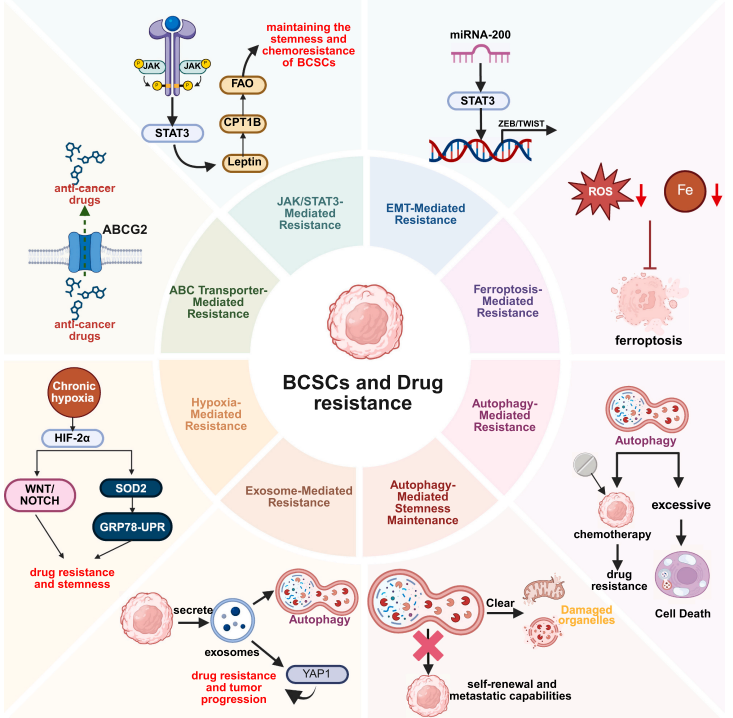
图3:BCSC耐药的主要机制1
► 5.靶向BCSC的治疗策略
靶向BCSC的治疗策略聚焦标志物、关键信号通路及TME三大核心方向。针对BCSC标志物,紫檀芪、ATRA/DEAB、miR-760等可分别靶向CD44、ALDH、NANOG,或通过山奈酚联合
针对关键信号通路,mTOR、Hh、Notch、Wnt通路抑制剂可抑制BCSC增殖、耐药及侵袭,纳米颗粒递送系统能提升Notch抑制剂的靶向特异性。
针对TME,通过
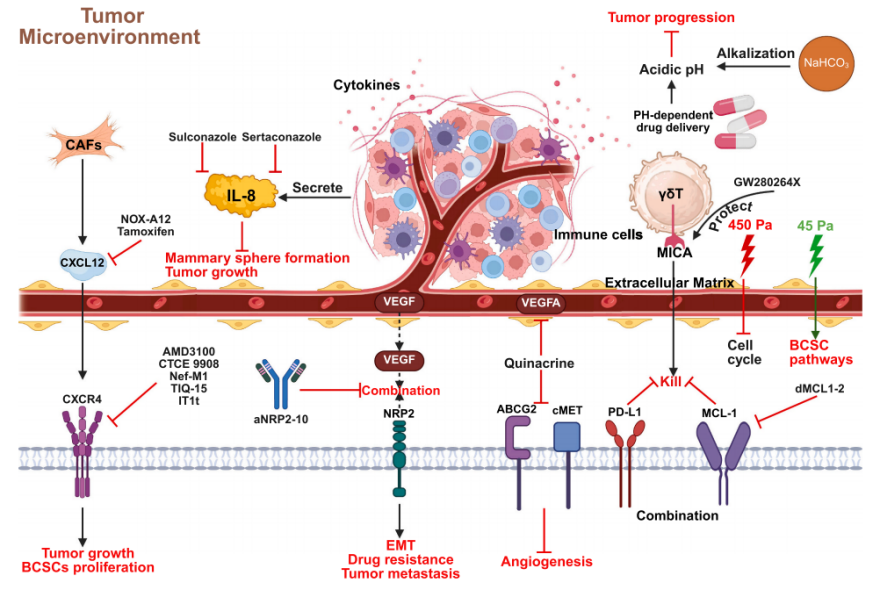
图4:肿瘤微环境与BCSC行为的临床相关性1
总结
BCSC作为乳腺癌恶性进展的核心驱动因素,通过自身特异性标志物、关键信号通路与肿瘤微环境的复杂串扰,调控自我更新、转移和耐药等关键生物学行为,是导致肿瘤复发和治疗失败的根本原因。当前针对BCSC的靶向策略已取得预临床进展,但临床转化仍面临挑战,主要归因于BCSC的高异质性、表型可塑性及TME的动态复杂性。未来研究需重点关注BCSC表型转换的调控机制,通过深入解析BCSC的调控网络,有望开发出更精准、有效的治疗方案,降低乳腺癌的复发率和死亡率,改善患者临床结局。
参考文献:
1.Zhang H, Sun Y, Liu R, et al. The role of tumor microenvironment and signaling pathways in regulating breast cancer stem cells: Implications for therapy resistance and tumor recurrence. Drug Resist Updat. 2026;84:101315.
编辑:Sineike
审校:KIKI
排版:Seren
执行:Ocean
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)