Metadata Card
文献题目:ANGPTL2 inhibits macrophage pyroptosis and alleviates rheumatoid arthritis progression by regulating mitophagy via IGFBP5
发表期刊:cell death & disease
发表时间:26.3.12 Online
影响因子:9.6(中科院1区)
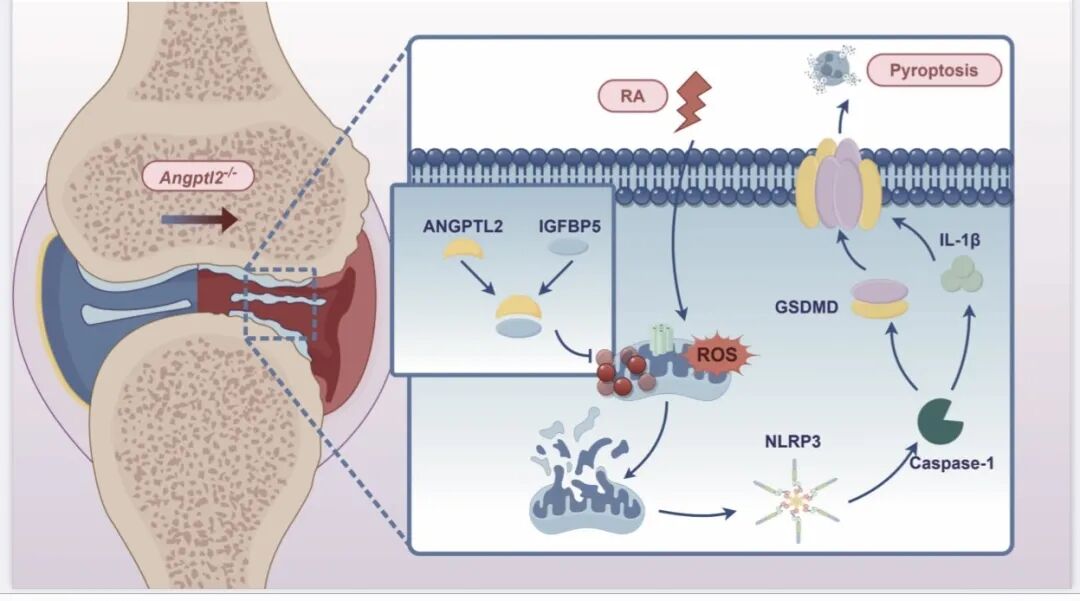
一句话总结:本研究首次证明ANGPTL2通过与IGFBP5互作增强线粒体自噬,进而抑制巨噬细胞NLRP3炎性体激活及焦亡,缓解RA病情。
Graphical Abstract
Abstract
英文摘要
Dysregulated macrophage pyroptosis and impaired mitophagy have emerged as critical drivers of rheumatoid arthritis (RA) progression, yet their upstream regulatory mechanisms remain unclear. Previous studies have demonstrated that ANGPTL2 deficiency aggravates alveolar bone loss in periodontitis, a condition that shares mechanistic similarities with RA in terms of bone destruction. Given the established link between periodontitis and RA, these findings suggest that ANGPTL2 may also play a protective role in RA-related joint pathology. In this study, we demonstrate that ANGPTL2 deficiency worsens joint inflammation, bone erosion, and macrophage pyroptosis in mice with collagen-induced arthritis (CIA). Mechanistically, ANGPTL2 loss impairs mitophagy and promotes mitochondrial dysfunction by inhibiting IGFBP5, leading to sustained NLRP3 inflammasome activation. Intra-articular administration of AAV-Angptl2 restores mitophagy, suppresses pyroptosis, and alleviates RA pathology. These findings identify ANGPTL2 as a key regulator of macrophage mitophagy and suggest its therapeutic potential in RA.
中文摘要
失调的巨噬细胞焦亡和受损的线粒体自噬已成为类风湿
Background & Problem
背景:类风湿关节炎(RA)是一种以慢性滑膜炎和进行性骨破坏为特征的自身免疫病,其中巨噬细胞介导的炎症反应起关键作用。 NLRP3炎性体介导的细胞焦亡(Pyroptosis)是导致关节损伤的重要环节。
痛点:尽管目前的DMARDs和生物制剂改善了疾病控制,但仍有许多患者面临炎症驱动的不可逆骨破坏。调节NLRP3激活的upstream 机制尚不完全清楚,尤其是线粒体质量控制(线粒体自噬)如何在该过程中发挥抑制作用,亟需深入研究。
Methodology
策略:研究者结合了体内CIA小鼠模型(WT vs Angptl2−/−)和体外巨噬细胞(RAW264.7和BMDMs)刺激模型。
逻辑:
1.体内验证:通过敲除小鼠观察ANGPTL2对RA病理的影响。
2.体外机制:利用RNA-seq筛选受ANGPTL2调控的下游通路,聚焦线粒体自噬。
3.互作探究:证明ANGPTL2与IGFBP5的直接物理结合及其功能依赖性。
4.治疗试验:采用AAV介导的基因治疗验证临床转化潜力。
Key Results & Interpretation
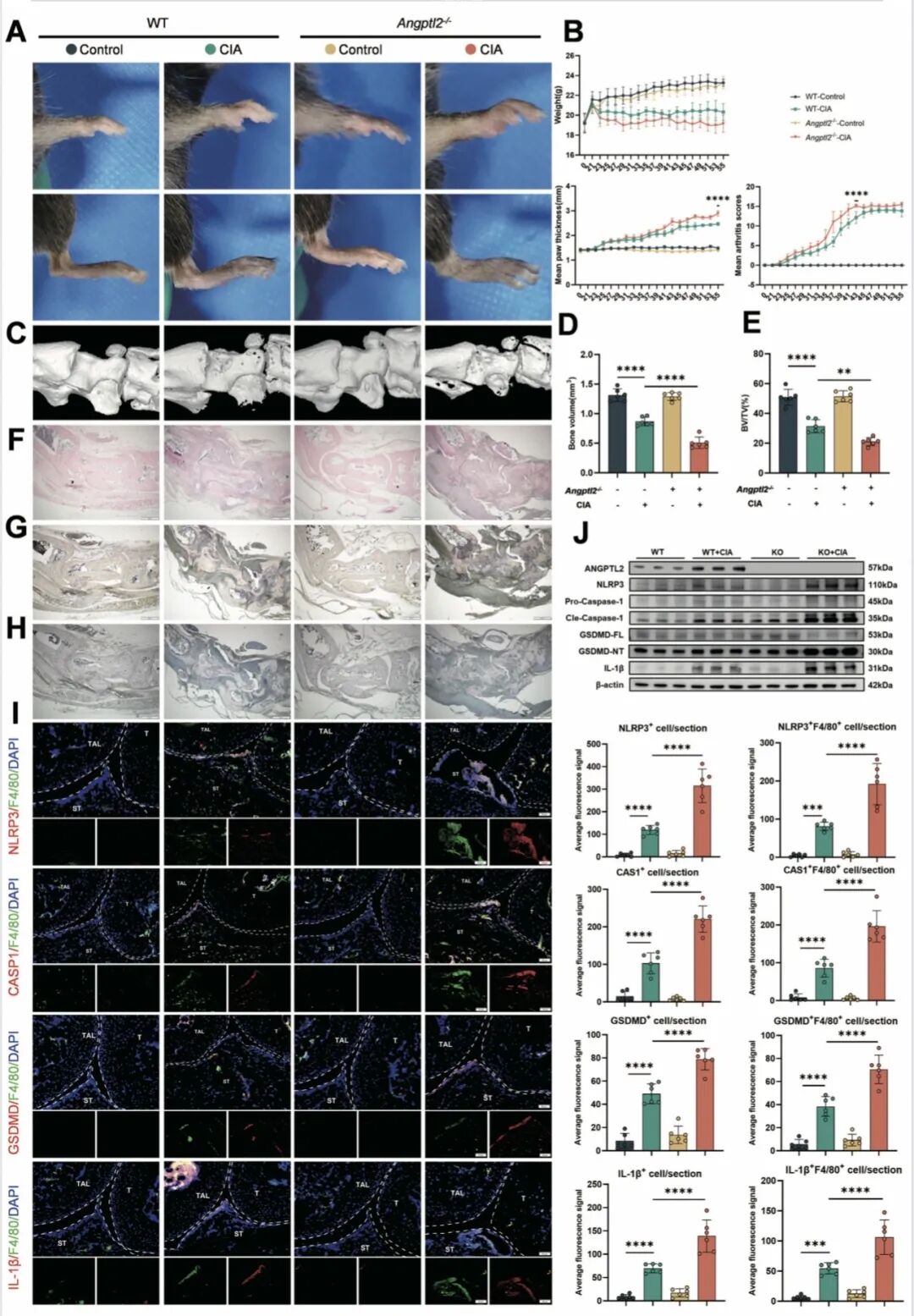
[A-B]:小鼠爪部形态及监测体重、临床评分发现,Angptl2−/−小鼠在CIA诱导后足肿胀更严重、评分更高且体重下降明显,证明了ANGPTL2的抗炎保护作用。
[C-E]:Micro-CT 重建及定量分析显示,敲除组距骨骨量和骨体积分数(BV/TV)显著降低,证实了其严重的骨破坏表型。
[F-H]:组织学染色显示敲除组滑膜增生与炎性浸润剧烈,TRAP染色揭示破骨细胞活性增强,而ALP染色提示成骨活动受抑,揭示了骨代谢失衡。
[I-J]:双重免疫荧光与 Western Blot 检测证实,Angptl2−/−小鼠关节巨噬细胞中 NLRP3、GSDMD、Caspase-1 和 IL-1β 表达显著升高,证明其焦亡水平大幅增加。
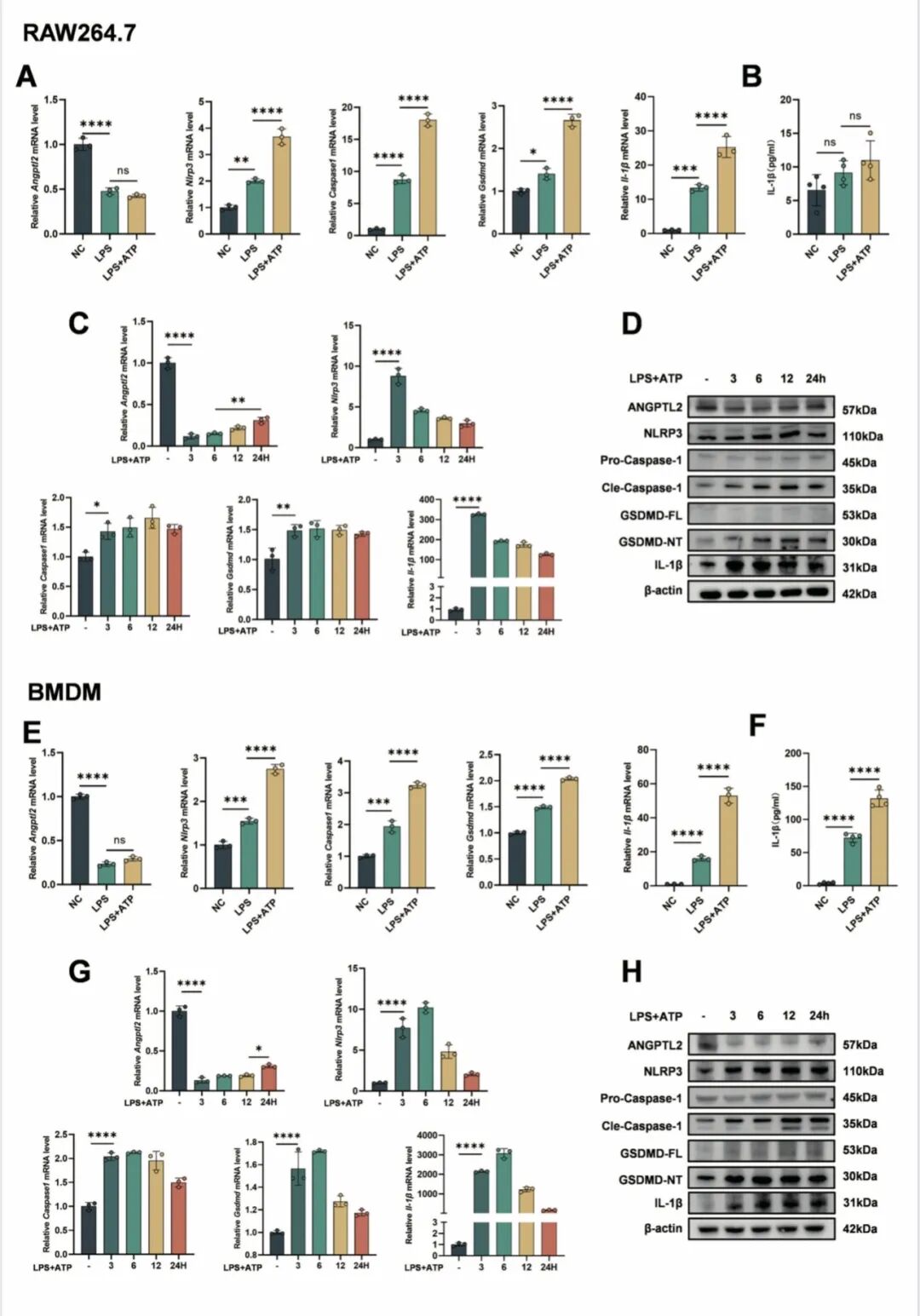
[Fig 2A-H]:在 RAW264.7 和 BMDM 中,LPS 或 LPS+ATP 刺激导致 Angptl2 表达急剧下降,且时间梯度实验显示其表达量与焦亡标记物的诱导呈明显的负相关趋势。
【raw264.7不表达asc,理论上无法诱导焦亡,一般研究会避开这个细胞系】
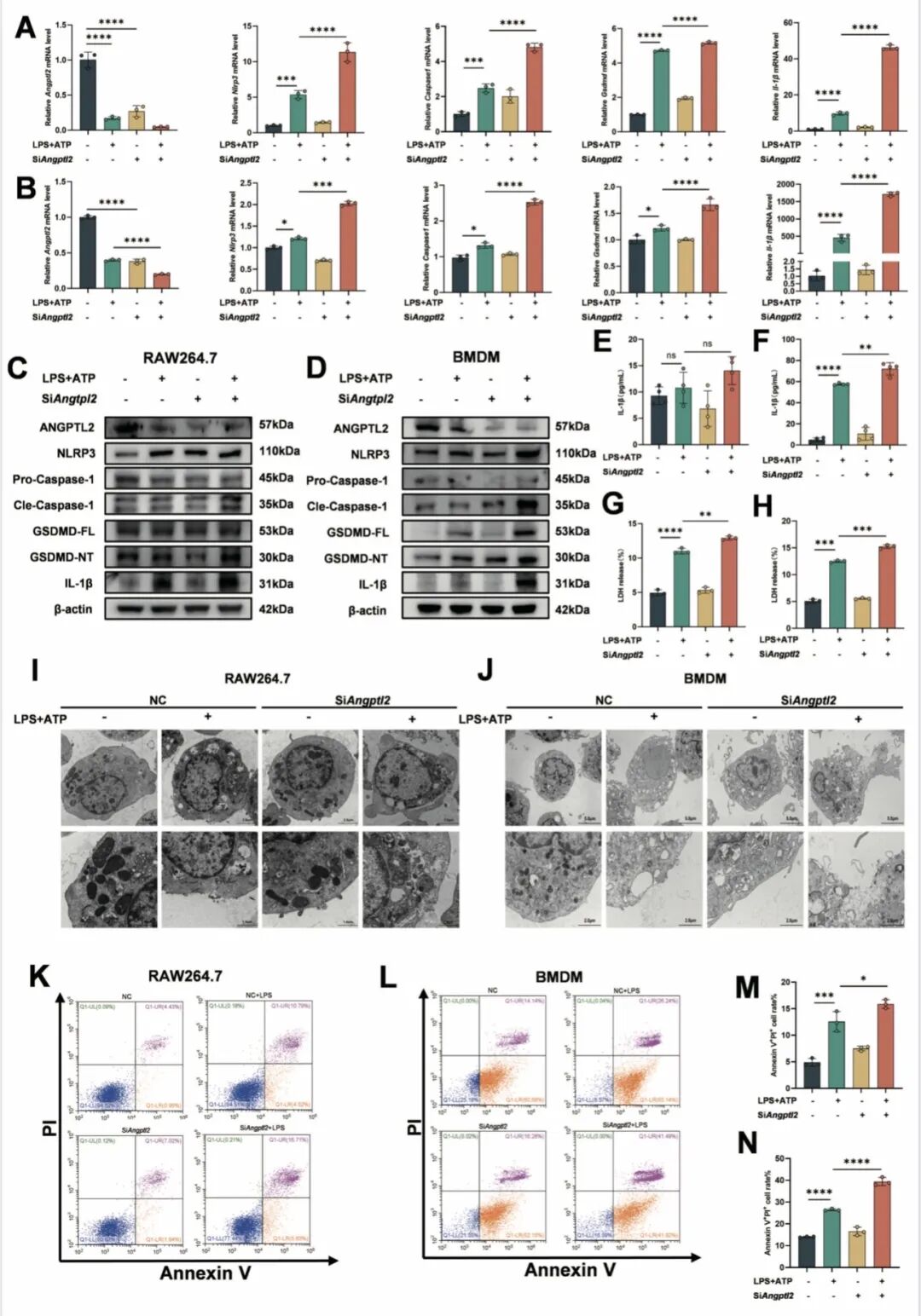
[Fig 3A-D]:通过 siRNA 敲低 Angptl2 后,刺激组细胞内 NLRP3、GSDMD 及 IL−1β 蛋白水平显著激增,从功能缺失角度证实了其对焦亡的抑制作用。
[Fig 3E-H]:LDH 释放实验与 ELISA 检测结果一致,表明 ANGPTL2 缺失会导致细胞膜通透性增加及炎性因子大量释放。
[Fig 3I-N]:透射电镜(TEM)观察到典型的焦亡形态(质膜破裂、细胞器肿胀),流式细胞术进一步确证了 Annexin V+/PI+ 细胞比例升高。
发现点3:转录组分析锁定线粒体自噬异常:ANGPTL2 缺失导致线粒体稳态失衡
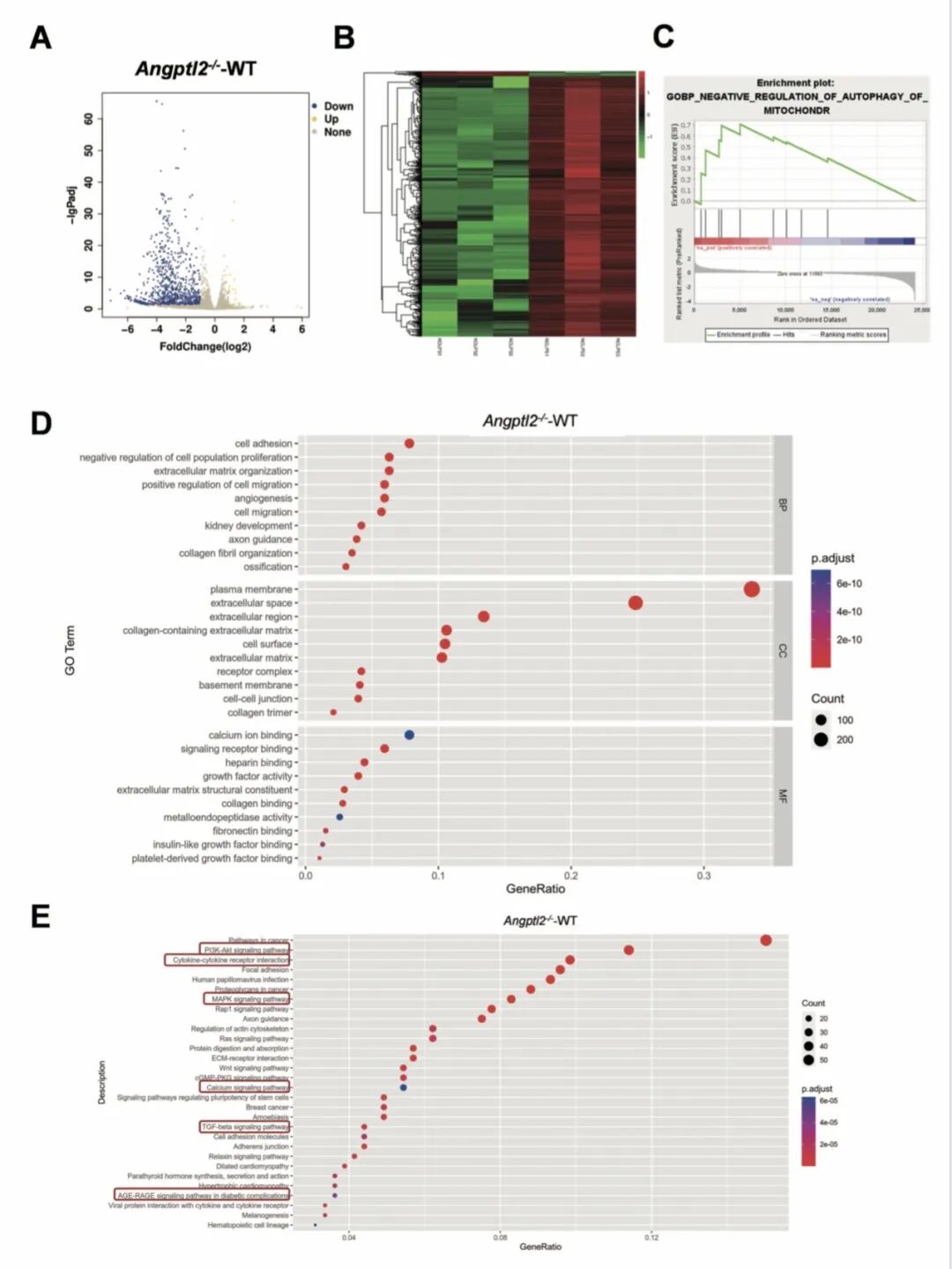
[Fig 4A-E]:测序结果分析锁定线粒体自噬。GSEA 富集分析显示“线粒体自噬负调控”基因集在敲除组显著升高,KEGG 通路分析则指向了广泛的炎症反应和代谢失调。
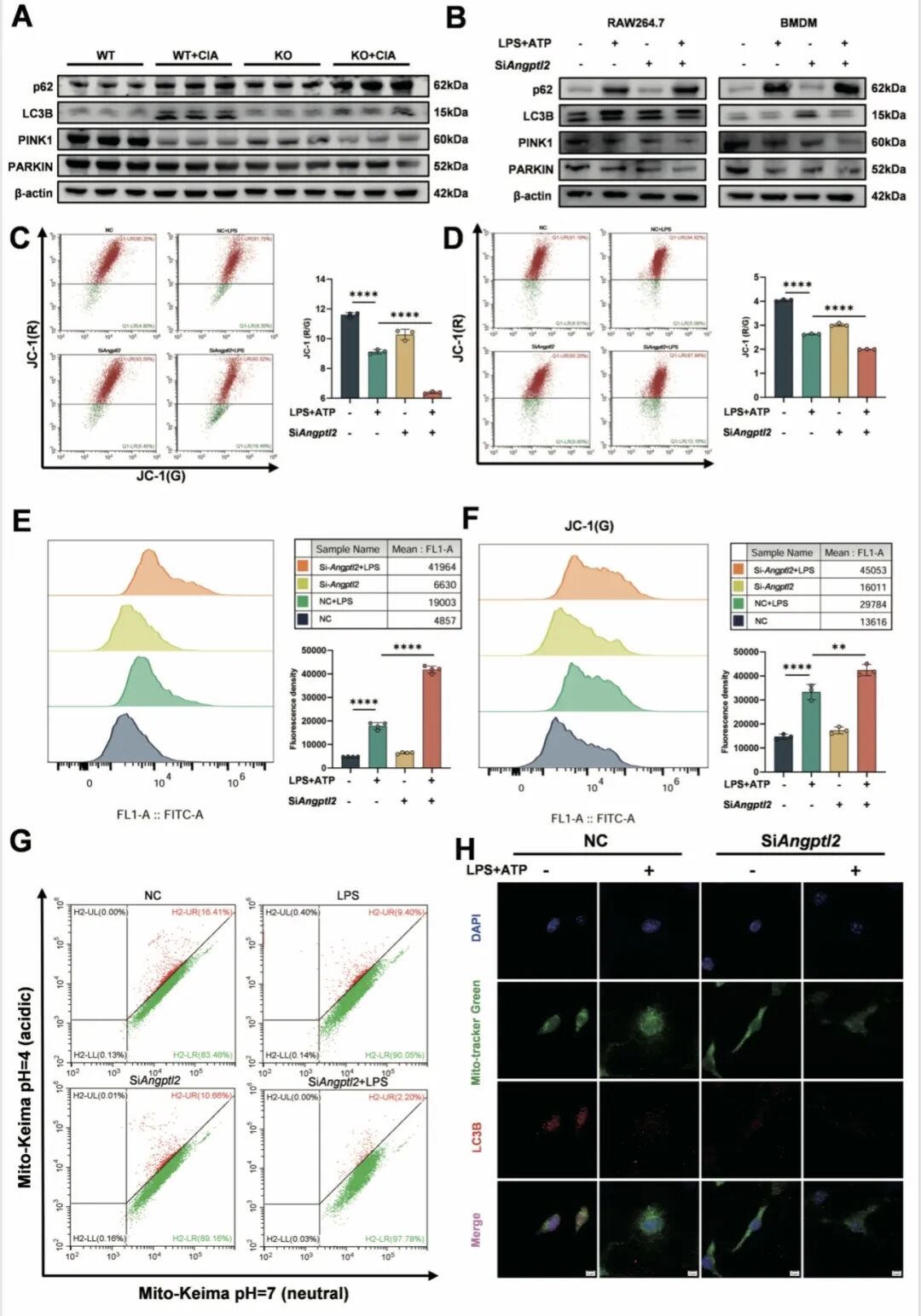
[Fig 5A-B]:WB 检测证实,ANGPTL2 缺失显著抑制了 PINK1、PARKIN 及 LC3B-II 的水平,伴随 p62 堆积,标志着线粒体自噬流的中断。
[Fig 5C-F]:JC-1 染色显示线粒体膜电位崩溃,流式检测发现细胞内 ROS 水平剧增,揭示了严重的线粒体功能障碍。
【Increased intracellular ROS accumulation was detected in both RAW264.7 cells andBMDMs lacking ANGPTL2 under LPS + ATP stimulation (Figure 5E, F). 原文说是LPS+ATP刺激,图EFG都只标注了LPS】
[Fig 5G-H]:通过 Mito-Keima 报告系统及共聚焦显微镜观察,ANGPTL2 缺失细胞中线粒体自噬小体的形成和招募显著减少。
【这里还有个疑问,H图的方法学描述为先固定、破膜,染LC3B后再去染MitoTracker,Triton都把脂质层破坏的差不多了,膜电位也没了,染料是附着在哪里?这里要染线粒体是不是用抗体,比如TOM20更合适一点】
补充知识点:mt-Keima系统如何指示线粒体自噬
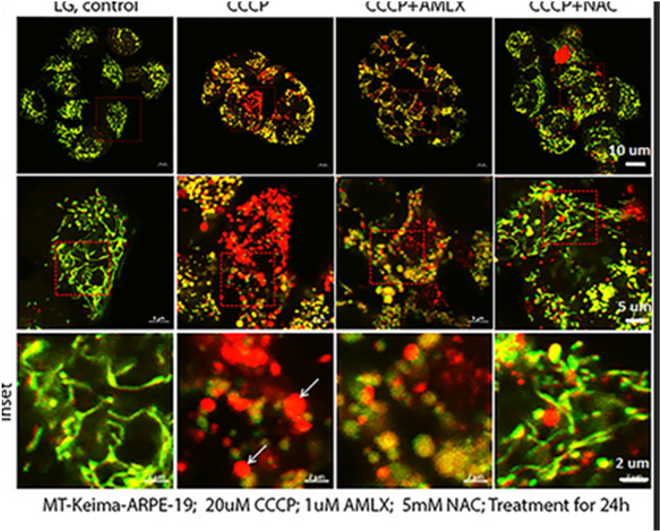
【Keima 是一种源自珊瑚的荧光蛋白。在mt-Keima系统中,这种蛋白被添加了线粒体靶向信号(MTS),使其特异性地定位在线粒体基质中。
它的独特之处在于其激发光谱会随 pH 值的变化而发生显著偏移:
1、正常线粒体中(中性 pH ≈ 8.0):Keima 主要被 440 nm(青蓝色光)激发。
2、溶酶体中(酸性 pH ≈ 4.5):当线粒体被包裹进自噬溶酶体后,Keima 的化学性质发生变化,它转而主要被 550-580 nm(绿/黄色光)激发。
图像中出现的红色颗粒点即代表正在发生的线粒体自噬事件。红色信号占总信号的比例越高,说明线粒体自噬水平越强,作者本文直接用流式读取信号】
发现点4:挽救实验与机制解析:ANGPTL2 通过与 IGFBP5 互作重启线粒体自噬并减少焦亡
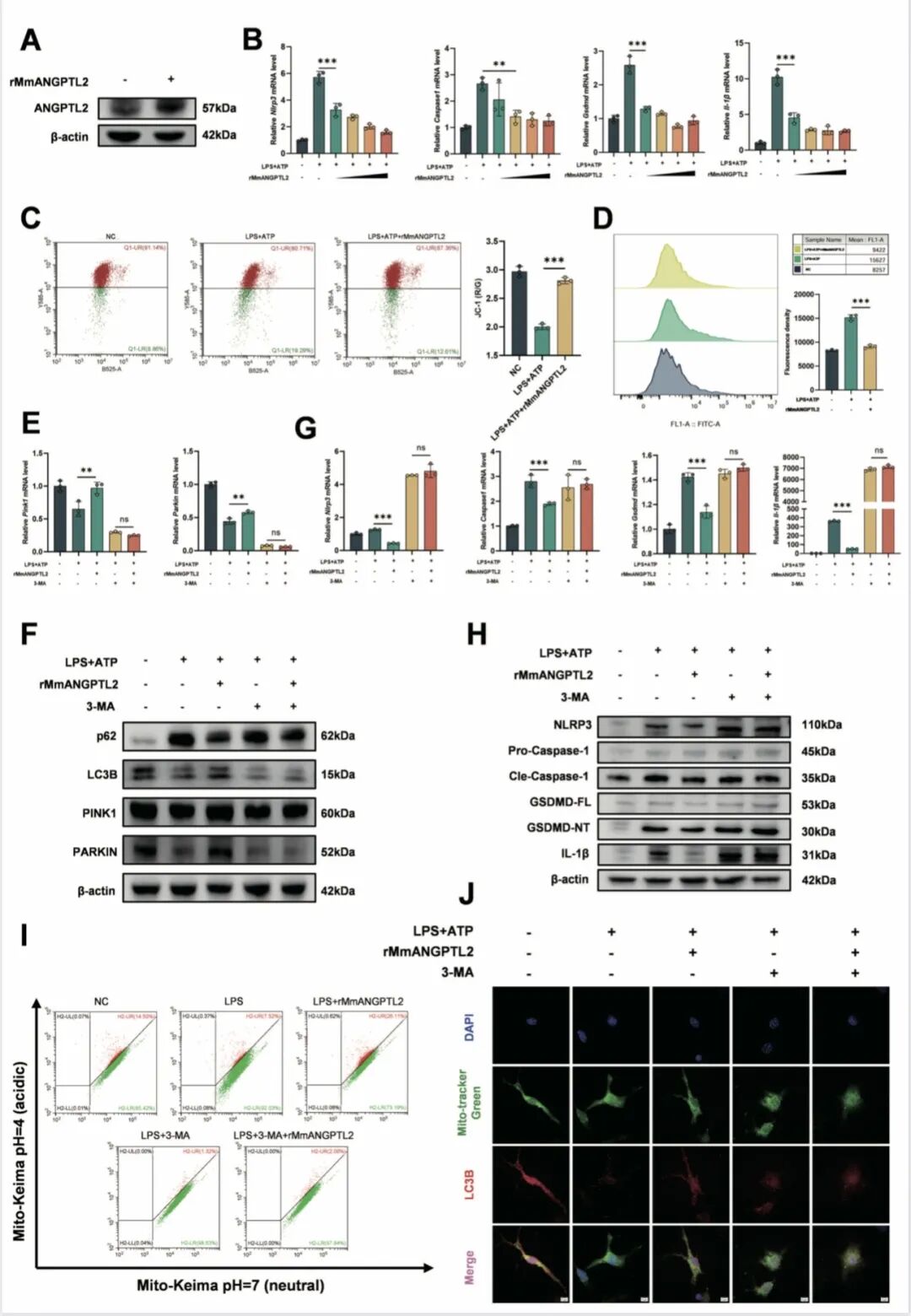
[Fig 6A-H]:添加重组 ANGPTL2 蛋白,能剂量依赖性地恢复线粒体自噬并抑制焦亡,但若使用自噬抑制剂 3-MA,这种保护效应将被完全抵消,证明了自噬依赖性。【这里用3-MA这种广谱的自噬抑制剂吗?图E:线粒体自噬和pink1 parkin的mRNA水平没有必然联系】
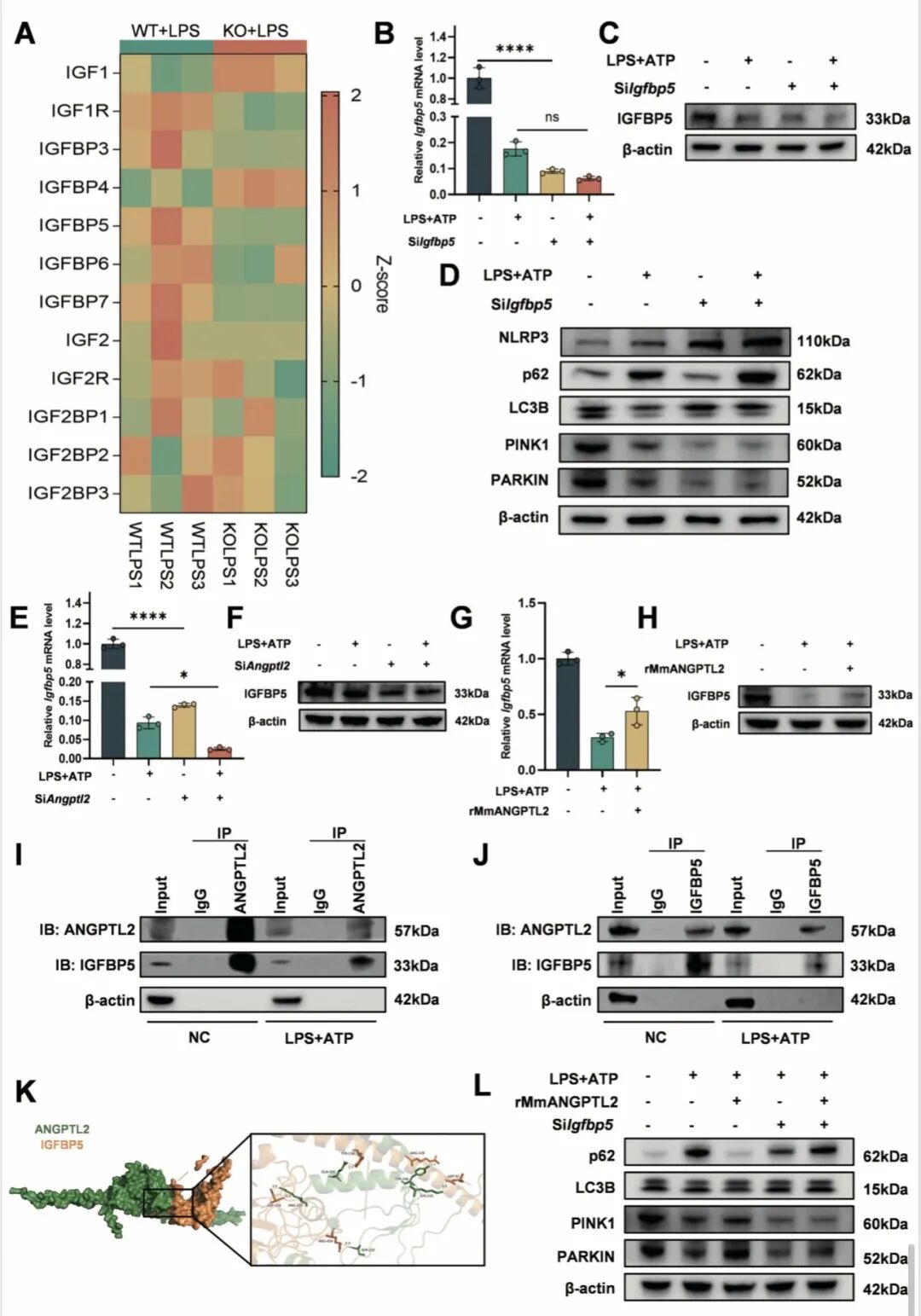
[Fig 7A-H]:转录组分析筛选出 IGFBP5 为下游执行分子。实验证明 ANGPTL2 正向调控 IGFBP5 的表达,而敲低 IGFBP5 会模拟 ANGPTL2 缺失的促炎表型。
[Fig 7I-K]:Co-IP 实验证实了胞内 ANGPTL2 与 IGFBP5 的物理结合,蛋白对接模型揭示了两者的互作界面。
[Fig 7L]:挽救实验确证,若 IGFBP5 被敲低,ANGPTL2 蛋白则无法恢复线粒体自噬流,证明了该轴线的完整性。
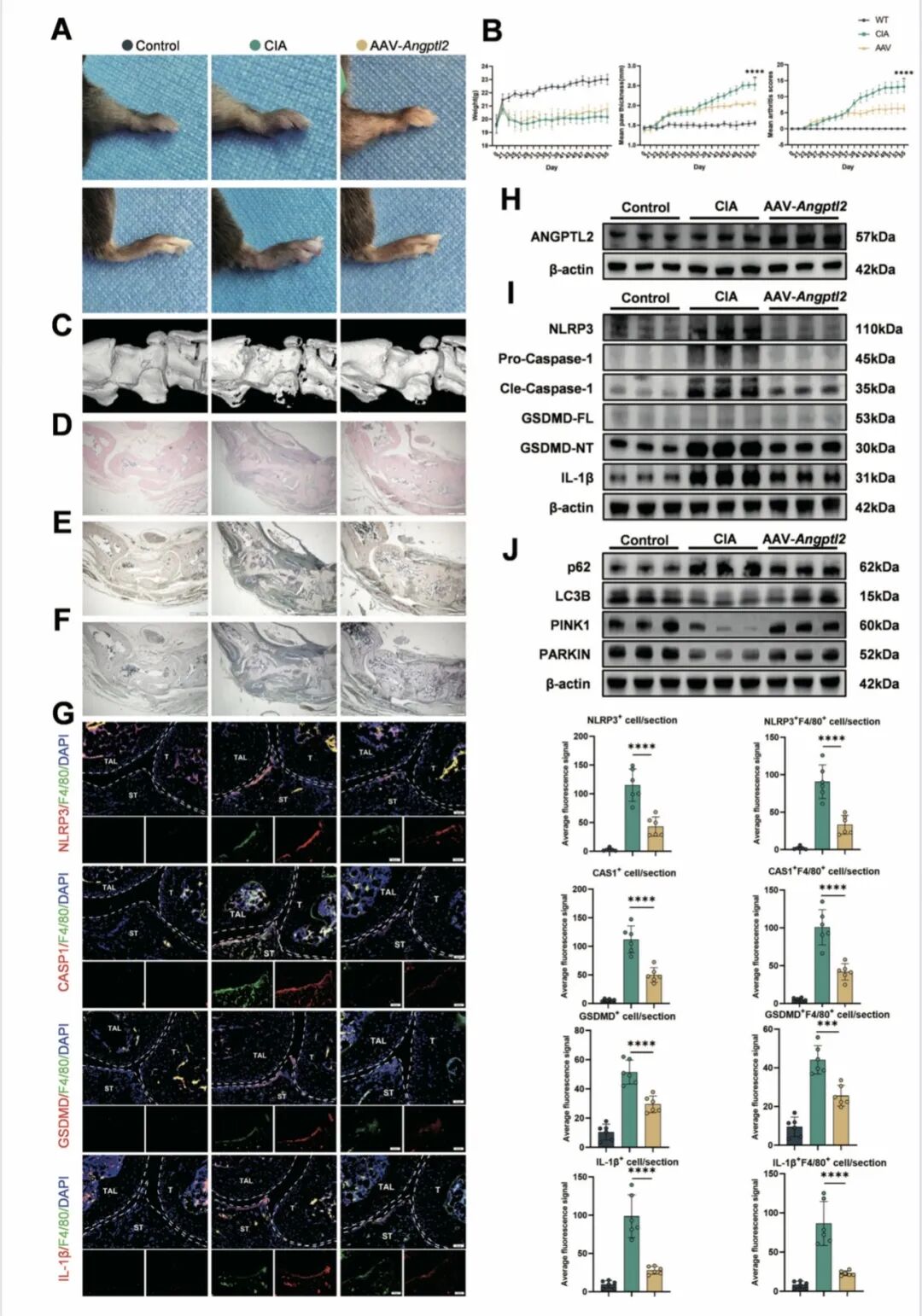
[8A-C]:关节腔注射 AAV-Angptl2 治疗后,小鼠肿胀消退,Micro-CT 重建显示其骨骼结构完整性得到良好保存。
[8D-F]:组织切片显示治疗组滑膜炎症显著抑制,破骨细胞介导的骨吸收减少,而 ALP 标记的成骨活动增强。
[8G-J]:原位荧光和组织 WB 确认治疗后关节内巨噬细胞焦亡蛋白显著减少,PINK1/PARKIN 线粒体自噬通路被成功重启。
Innovation & Takeaway
✨ 创新点
1. 首次确立了ANGPTL2-IGFBP5-线粒体自噬轴在RA中的调节作用。
2. 发现了ANGPTL2虽作为分泌蛋白,但其胞内功能(维持线粒体质量控制)对抑制焦亡至关重要。
✨ 科研启示
该研究将免疫代谢(线粒体功能)与经典的炎症死亡通路结合,提示我们在研究分泌蛋白时,应更多关注其内吞后的非经典胞内效应。
✨ 临床/应用价值
ANGPTL2-IGFBP5轴的发现为RA提供了一个新的“代谢免疫检查点”。 局部AAV介导的ANGPTL2补充有望成为一种减少全身免疫抑制副作用的新型靶向疗法。
医脉通是专业的在线医生平台,“感知世界医学
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)