文献来源:中华炎性肠病杂志,2026年第10卷第1期
作者:杜佳惠1
作者单位:1中山大学附属第六医院普通外科(结直肠外科);2广东省结直肠盆底疾病研究重点实验室;3 广州市黄埔区中六生物医学创新研究院;4广东省消化系统疾病临床医学研究中心
通信作者:陈钰锋
引用本文:杜佳惠,陈钰锋. 超加工食品在

【摘要】炎症性肠病(IBD)目前发病机制尚未完全明确,西方饮食可能是其重要影响因素之一。超加工食品(UPF)广泛存在于西方饮食中,近年来被发现可损伤肠道黏膜屏障、诱导
【关键词】超加工食品;炎症性肠病;肠道菌群;免疫反应;黏膜屏障
炎症性肠病(inflammatory bowel disease,IBD)是一类慢性肠道炎症性疾病,主要包括
一、UPF的定义及其分类
1.UPF的定义:许多食品在加工过程需使用食品添加剂(如乳化剂、甜味剂、着色剂等)或采用特定的烹饪方法进行处理。为更好地帮助消费者了解食品的加工水平及其对健康的潜在影响,巴西营养学家Monteiro等 [ 4 ]最早提出Nova食品分类( 表1 ),将食品分为4大类,包括UPF在内。UPF是指主要由仅用于工业用途的多种成分配制,并经过一系列复杂工业加工过程而形成的食品,通常含有很少或不含天然食物成分。

2.UPF的分类:目前对UPF无统一的亚分类标准,在研究中多根据传统食物类别进行分类 [ 5 ],见表2 。

二、UPF与IBD的关系
以往研究多关注单一UPF亚类或添加剂对IBD的影响,如针对含糖饮料的研究表明,与从不饮用者相比,每日饮用含糖饮料>1份者CD发病风险显著升高 [ 6 ];乳化剂的研究也表明减少乳化剂摄入可以改善IBD症状,减少疾病复发 [ 7 ]。随着Nova分类的提出和应用,越来越多的研究开始关注UPF对IBD的影响。
1.UPF对IBD发病的影响:近年来有多项大型队列研究关注UPF对IBD发病风险的影响,虽然这些研究在UPF定义和观测指标上有所不同,但多数研究参照Nova分类,且观测指标采用UPF摄入量占总能量摄入的百分比 [ 8 , 9 , 10 , 11 , 12 ]。其中,最早的研究是基于法国NutriNet-Santé队列,主要观测指标为膳食中的UPF重量百分比,其结果并未发现饮食模式及UPF比例与IBD发病风险相关,这可能与其随访时间短(仅2.3年)导致新发病例较少(105 832例参与者中仅有75例发病)有关 [ 8 ]。然而,随后一项前瞻性队列研究纳入了全球21个不同收入国家共116 087例35~70岁成年人,长达9.7年的随访结果表明,与每天摄入UPF<1份者相比,每天摄入UPF≥5份者IBD发病风险增加82%,每天摄入1~4份者风险也增加67%,进一步分析发现UPF摄入显著增加CD的发病风险,而不增加UC的风险,但该研究与其他研究不同的是,其UPF定义为内含食品添加剂、人造成分或其他化学成分的各种包装和配制的食品与饮料,且主要观测指标为每日UPF份数 [ 9 ]。UPF影响CD和UC发病的这种差异也在随后的研究得到证实,基于美国人群的研究和基于英国生物库的研究均观察到类似结果 [ 10 , 11 ]。与此不同,另一项研究纳入了欧洲8个国家共413 590例参与者,结果并未发现UPF摄入会增加IBD发病风险,但发现高摄入未加工或最低限度加工食品(特别是水果和蔬菜)与CD发病下降有关,但在UC中未观察到这一现象,值得注意的是,该研究中IBD病例主要依赖患者自我报告,其病例数较少,可能存在漏报情况 [ 12 ]。后续的荟萃分析也提示UPF高摄入可显著提升CD而非UC的发病风险 [ 13 , 14 ]。因此,UPF高摄入可增加CD的发病风险,但其对UC发病风险的影响还有待进一步证实。
2.UPF对IBD疾病活动的影响:除了影响发病,UPF高摄入也被发现与IBD的疾病活动和炎症水平密切相关。近期有研究表明,在UC患者中UPF高摄入组的疾病活动频率和炎症发作频率显著高于UPF低摄入组,但在CD患者中未观察到显著差异,在CD中无显著差异可能是由于研究中用于评估炎症的
三、UPF影响IBD的机制
UPF种类繁多且成分复杂,目前关于UPF影响IBD的机制研究主要集中于其食物成分、食品添加剂和烹饪过程产生的中间成分。研究发现其可能损伤肠道屏障功能,包括黏膜屏障、菌群屏障和免疫屏障,从而介导IBD的发病和进展 [ 3 ]。
1.UPF可损伤肠道黏膜屏障:肠道黏膜屏障主要由肠上皮细胞及其紧密连接构成的机械屏障及杯状细胞分泌黏蛋白mucin-2(MUC2)形成的黏液层(化学屏障)组成,可抵御有害物质和病原体入侵 [ 17 ]。黏液层由内层(细菌较少)和外层(共生菌富集)组成,各种原因引起的机械屏障损伤和黏液层异常,可促使有害物质和病原体入侵,诱发肠道炎症 [ 2 ]。
高脂饮食在CD小鼠模型中可诱导肠上皮细胞的脂质过氧化,产生炎症细胞因子,促进肠道炎症 [ 18 ]。高盐饮食也被发现在动物模型中可显著降低紧密连接蛋白occludin的表达,使肠上皮通透性增加,同时可激活上皮细胞的坏死性凋亡通路,进一步加重肠道炎症 [ 19 , 20 ]。高糖饮食除了可直接影响肠上皮细胞间的紧密连接,诱发氧化应激,还可促使嗜黏蛋白的细菌富集,加速黏液分解和黏液屏障的破坏,损伤肠道屏障功能 [ 21 , 22 ]。
在食品添加剂中,乳化剂卡拉胶可调控紧密连接蛋白zonula occluden-1(ZO-1)的重新分布,并改变细胞骨架纤维肌动蛋白的结构,导致肠上皮通透性增加,影响肠上皮的屏障功能 [ 23 ]。具有着色作用的膳食微粒二氧化钛纳米颗粒也被发现在小鼠模型中可诱导活性氧的生成,增加肠上皮的通透性 [ 24 ]。另一种具有防腐作用的膳食微粒银纳米颗粒在大鼠模型中不仅可促使绒毛顶端细胞脱落,还可诱导回肠杯状细胞增多和异常黏液(唾液酸化黏蛋白)分泌增加 [ 25 ]。增稠剂麦芽糊精在小鼠实验中也可引发杯状细胞的内质网应激感应蛋白上调和黏蛋白MUC2表达下降,导致黏液层变薄,加重肠道炎症 [ 26 ]。
2.UPF可损伤肠道菌群屏障:肠道菌群可通过阻止病原体定植,并产生短链脂肪酸等抗炎代谢物来发挥防御作用,同时可调控上皮细胞增殖和分化,维持正常肠道生理功能。IBD患者常见的菌群失调表现为菌群多样性减少、有益菌的减少和有害菌的过度生长 [ 27 ]。
关于UPF对菌群的直接影响的研究较少。一项西班牙人群的研究发现高摄入UPF在女性可促使肠杆菌( Enterobacteriales)等诱发肠道炎症和IBD的有害菌富集以及黑
更多的研究关注UPF不同组分的影响。研究表明,高脂饮食会降低肠道菌群多样性,并通过促进胆汁酸分泌改变肠道菌群,使拟杆菌( Bacteroides)等耐胆汁的厌氧菌丰度增加,促进肠道炎症 [ 31 ]。高盐饮食在小鼠模型中也可降低乳酸杆菌( Lactobacillus)的丰度,并减少保护性短链脂肪酸的产生,促进葡聚糖硫酸钠(dextran sulfate sodium,DSS)诱导的结肠炎 [ 32 ]。高糖饮食则被发现可导致普雷沃菌( Prevotella)、黏附性侵袭性
同时,乳化剂、甜味剂等多种食品添加剂也被发现可改变肠道菌群并影响其产生短链脂肪酸的能力 [ 33 ]。乳化剂聚
3.UPF可损伤肠道免疫屏障:肠道具有免疫屏障功能,当肠道的共生菌及病原体易位可激活toll样受体(toll-like receptors,TLR)等模式识别受体,启动异常免疫信号通路,同时,固有层免疫细胞异常增殖与活化,分泌促炎细胞因子,加之免疫调节细胞功能缺陷导致抑制性细胞因子分泌不足,共同引发肠道免疫异常激活,促进IBD的发生和进展 [ 37 ]。
高脂饮食可导致大鼠组织中白细胞介素10(interleukin-10,IL-10)表达下降和下游的Janus激酶(JAK)-信号转导及转录激活因子3(STAT3)通路活性降低,损伤IL-10的免疫调节功能 [ 38 ]。高盐饮食在小鼠模型中可刺激树突状细胞产生IL-1β,诱导T细胞产生IL-17A和干扰素γ(interferon γ,IFNγ)等促炎因子 [ 39 ];同时抑制Foxp3 +调节性T细胞,进一步激活促炎的辅助性T细胞17(T helper cell 17,Th17) [ 40 , 41 ]。高糖饮食则可诱导CD4 +T细胞线粒体中活性氧水平上升,通过激活转化生长因子β(transforming growth factor-β,TGF-β)信号通路促进Th17细胞分化,促进炎症;同时还可通过TLR2通路,促进巨噬细胞向M1型极化,分泌炎症因子,加重肠道炎症 [ 42 , 43 ]。
乳化剂卡拉胶在体外实验也被发现能激活核因子κB(nuclear factor-κB,NF-κB)通路,诱导IL-8等促炎因子的产生,并通过TLR4受体介导炎症反应 [ 44 ]。甜味剂三氯蔗糖在小鼠模型中可激活TLR4/NF-κB信号通路,使
此外,UPF在加工过程(如高温烹饪)产生的糖化终产物(advanced glycation end product,AGE)被发现可激活TLR、NF-κB等炎症通路,介导炎症因子的分泌和免疫细胞的募集,促进肠道炎症 [ 47 , 48 ]。UPF影响IBD的机制可见 图1 [ 49 ]。
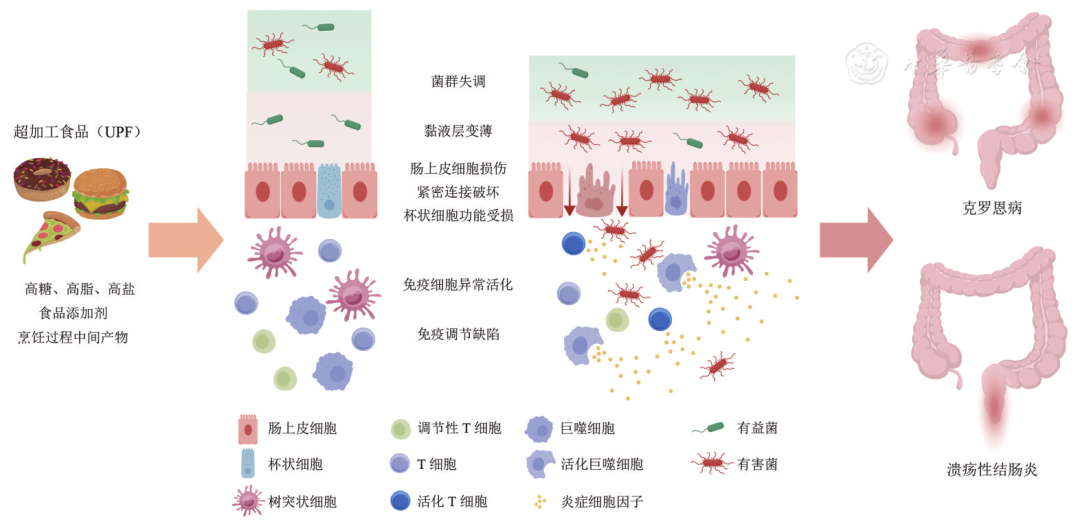
图1 超加工食品影响炎症性肠病的机制图(通过BioGDP.com绘制 [ 49 ])
四、针对UPF的IBD饮食管理
目前研究表明多种饮食模式在改善IBD病情方面具有潜在益处,包括CD排除饮食(Crohn′s disease exclusion diet,CDED)、特殊碳水化合物饮食(specific carbohydrate diet,SCD)、低发漫饮食(low-FODMAP diet)以及地中海饮食(Mediterranean diet,MD),这些饮食模式均在不同程度上限制或避免了UPF的摄入 [ 3 , 50 ]。鉴于UPF对IBD的影响,在IBD患者的饮食中,建议选择优质蛋白质,并限制或避免高糖、高盐、高脂食物以及含有大量食品添加剂的加工食品,如无明显禁忌(急性期或合并狭窄、肠瘘),建议多摄入蔬菜、水果、全谷物等天然食物 [ 51 ]。
综上所述,UPF可通过损伤肠道黏膜屏障、诱导菌群紊乱、引发免疫异常等机制,促进IBD的发病和进展,IBD患者应限制或避免UPF的摄入。后续的研究应继续关注干预UPF摄入对IBD患者的作用,以期为IBD患者的饮食指导提供更多依据。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)