编者按
3月18日,强生宣布Icotrokinra获美国食品药品监督管理局(FDA)正式批准上市,用于治疗12岁及以上青少年和成人的中重度斑块状
图源:FDA官网

疾病负担沉重,临床需求迫切
数据显示,中国银屑病患者约数百万,其中中重度患者约占总数的25% 。目前,中重度斑块状银屑病的主要治疗方案以外用药物、光疗、传统免疫抑制剂及生物制剂注射为主。然而,传统药物长期使用存在副作用明显、疗效不佳等问题;而生物制剂虽疗效显著,但注射给药的方式给部分患者带来不便和心理负担,导致依从性受限。临床亟需安全、有效且便捷的口服精准靶向治疗方案 。
关键III期ICONIC研究:疗效与安全性双突破,研究结果展现优越性
此次批准基于关键性III期临床试验ICONIC-LEAD、ICONIC-ADVANCE 1 & 2 及 ICONIC-TOTAL 研究的积极结果。其中,ICONIC-LEAD研究是一项为期52周的随机、双盲、安慰剂对照多中心临床试验,共纳入684例中重度斑块状银屑病患者,评估了Icotrokinra(每日一次200mg)对比安慰剂的疗效和安全性 。
研究结果显示,治疗第16周,该药在短期疗效、长期缓解、特殊部位
表1 截至第16周的共同主要终点与关键次要终点
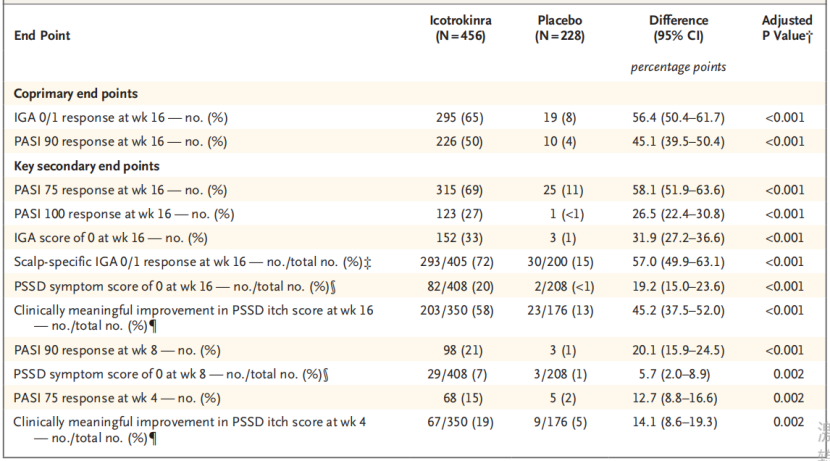
ICONIC-LEAD研究显示,第16周时,Icotrokinra组65%的患者实现IGA 0/1分(皮损完全清除或几乎清除) ,而安慰剂组仅为8%(p<0.001);实现PASI 90(病情改善≥90%)的患者比例达50% ,安慰剂组仅为4%(p<0.001) 。
ICONIC-ADVANCE 1和2研究显示,在第16周,Icotrokinra在疗效上优于现有口服TYK2抑制剂
长期疗效稳定,解决临床复发痛点
至治疗第52周,Icotrokinra的疗效持续稳定。在第24周重新随机分配到Icotrokinra组的成年患者中,高达84%的患者维持了PASI 90应答,而重新随机分配到安慰剂组的患者中,该比例仅为21%(p<0.001),证实了该药能有效降低疾病复发风险 。
攻克难治部位,解决临床治疗难点
针对临床上极为棘手的头皮、生殖器部位皮损,ICONIC-TOTAL研究显示,Icotrokinra同样展现出卓越疗效:
-头皮银屑病:治疗组66% 的患者实现头皮特异性IGA评分0/1,安慰剂组仅11% 。
-生殖器银屑病:治疗组77% 的患者达到生殖器医生总体评估(sPGA-G)评分0/1,安慰剂组仅21% 。
-手足银屑病:治疗组42% 的患者达到手足医生总体评估评分0/1,安慰剂组为26% 。
该药为口服剂型,每日一次,无需注射,服用便捷。作为全球首创的口服IL-23R拮抗剂,它成功将强大的生物制剂疗效与口服给药的便利性结合,从根本上解决了部分患者对注射的恐惧和不便,大幅提升患者用药体验和治疗依从性 。
安全性良好,耐受性优异

机制精准靶向:全球首创口服IL-23R拮抗剂

未来展望:中国上市在即,拓展治疗版图
信源:
1. 强生官方新闻稿及相关公开资料
2. FDA官网公开信息
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。