在自身免疫性疾病领域,
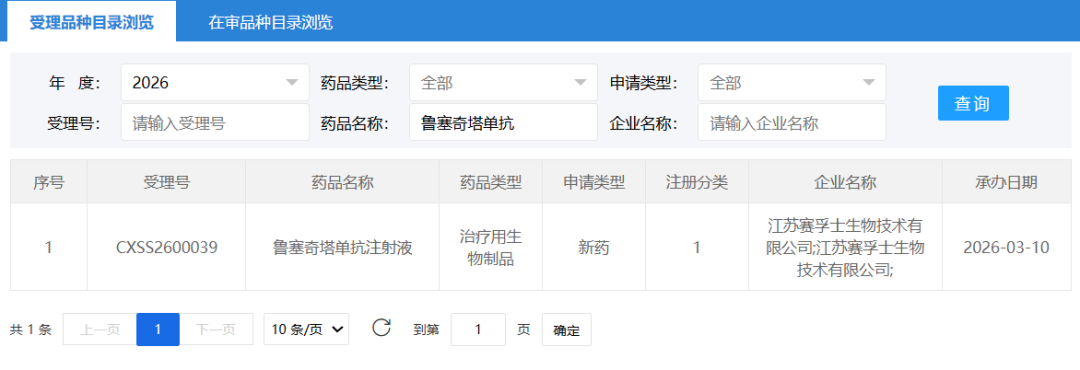
这一局面即将迎来重要突破。2026年3月10日,荃信生物宣布,其自主研发的靶向IL-17A的高亲和力单克隆抗体——鲁塞奇塔单抗的新药上市申请(NDA)已正式获国家药品监督管理局药品审评中心(CDE)受理,用于治疗成人活动性强直性脊柱炎1。这意味着国内AS患者离拥有全新的治疗选择又近了一步。
AS是一种主要侵犯骶髂关节和脊柱的慢性进行性炎症性疾病,严重时可导致脊柱强直和关节畸形,极大影响患者生活质量。目前,临床治疗重点在于控制炎症、延缓病程,但现有方案对部分患者疗效有限或存在禁忌。
IL-17A是AS发病机制的关键因子,近年来,IL-17A抑制剂在AS治疗中的地位逐渐提升。鲁塞奇塔单抗正是一款靶向IL-17A的高亲和力单克隆抗体,通过特异性阻断IL-17A与受体的结合,抑制炎症信号通路,从源头干预疾病进展。
此次NDA受理,标志着该产品向正式获批上市迈出关键一步。作为临床急需品种,其审评进程备受关注,有望为国内庞大的AS患者群体带来一款安全、有效且可及的创新药物。
鲁塞奇塔单抗的此次上市申报,主要基于一项多中心、随机、双盲、安慰剂对照的III期临床试验。该研究的积极成果已于2025年10月在全球风湿免疫领域顶级学术会议——美国风湿病学会年会(ACR)上以口头报告形式发布,获得国际学界的广泛关注与高度评价。
研究结果显示2,对于对非甾体抗炎药反应不足或存在禁忌的活动性AS患者,鲁塞奇塔单抗在为期52周的治疗过程中持续显著改善疾病活动度及临床症状,同时展现出良好的安全性与耐受性。此外,在既往接受过肿瘤坏死因子(TNF)抑制剂治疗的患者亚组中,鲁塞奇塔单抗同样表现出明确的临床获益。
1.主要终点达成,疗效显著
治疗16周时,鲁塞奇塔单抗组的ASAS40应答率高达40.4%,显著优于安慰剂组的18.9%(P<0.0001)。这意味着近半数患者在疼痛、功能等多维度实现了临床意义上的显著改善。
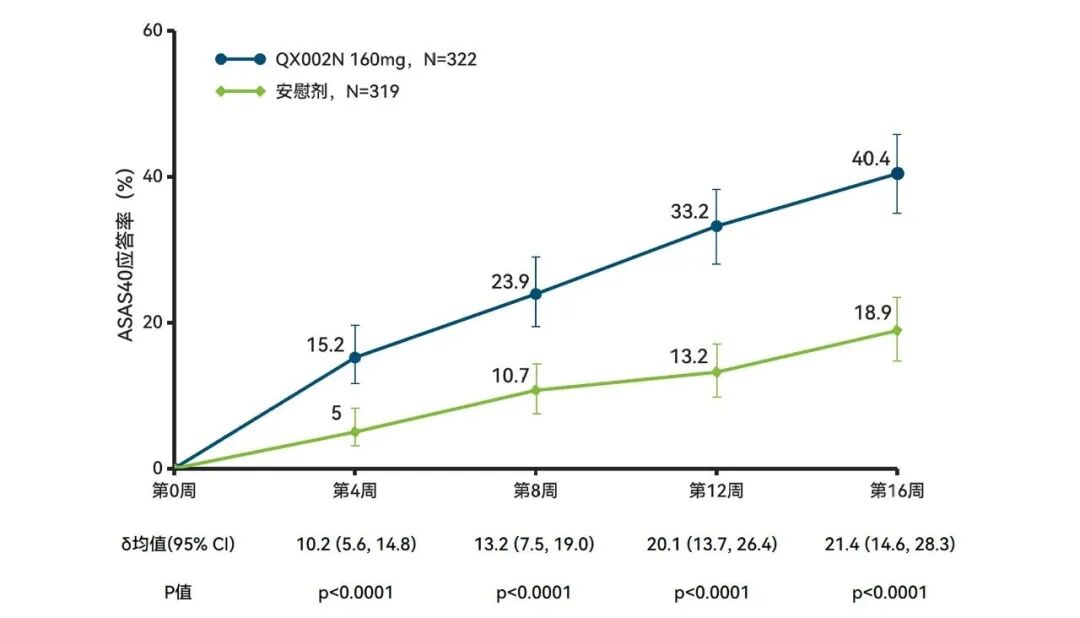
治疗16周期间,ASAS40应答率
2.客观影像学证据,直击病灶
研究不仅关注临床症状,更通过
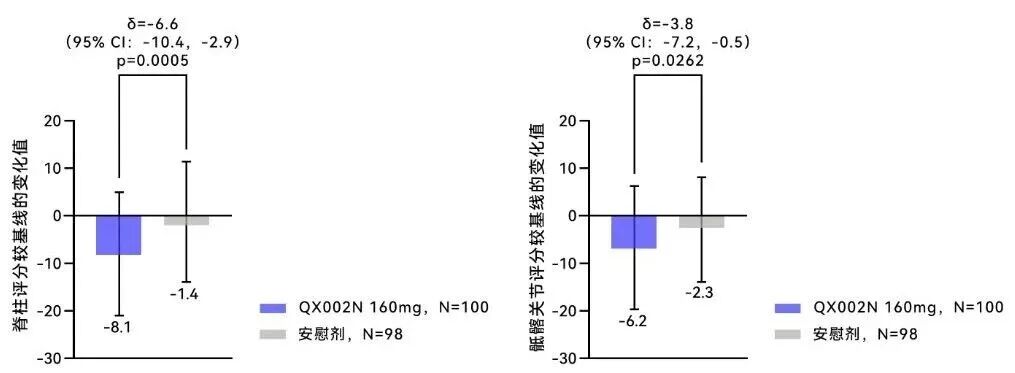
第16周时,SPARCC评分较基线的平均变化
3.广泛人群获益,安全耐受
研究显示,鲁塞奇塔单抗组整体安全性与耐受性良好,为长期用药提供了保障。
鲁塞奇塔单抗基于全国多中心、大样本量的III期研究数据表示,该药物在控制炎症、缓解症状及影像学改善方面展现出稳健的疗效表现。随着其上市申请获受理,这款国产IL-17A抑制剂有望在不久的将来进入临床,帮助更多AS患者在疾病早期实现有效干预,延缓结构性损伤进展,真正改变患者的疾病轨迹。
信源
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)