IgA肾病是全球范围内最常见的原发性肾小球肾炎,也是导致
Povetacicept是一种BAFF/APRIL双靶点抑制剂,通过抑制B细胞及
RAINIER(NCT06564142)是一项全球性的Ⅲ期随机、双盲、安慰剂对照试验,评估Povetacicept 80mg每四周一次皮下注射联合标准治疗对比安慰剂联合标准治疗在IgA肾病成人患者中的疗效和安全性。试验共随机入组605例患者,其中主要队列随机557例,探索性队列随机48例。两个队列的入组标准相同,但主要队列的估算肾小球滤过率(eGFR)要求为≥30 mL/min/1.73m²,探索性队列的eGFR要求为20至<30 mL/min/1.73m²。
本次中期分析人群为主要队列中的199例,主要终点是第36周时24小时尿蛋白/肌酐比值(UPCR)较基线的百分比变化,两个次要第36周时血清Gd-IgA1较基线的百分比变化以及(基线有
接受Povetacicept治疗的IgA肾病患者,其24小时UPCR较基线降低52.0%,与安慰剂相比,UPCR降低达49.8%(P<0.0001),具有统计学显著性和临床意义(表1,图1)。
Povetacicept治疗使血清Gd-IgA1较基线降低77.4%,与安慰剂(较基线增加9.1%)相比,实现了79.3%的降低(P<0.0001),具有统计学显著性和临床意义;
在基线有血尿的IgA肾病患者中(安慰剂组N=36,Povetacicept组N=67),Povetacicept治疗组有85.1%的患者实现了血尿消退,与安慰剂(23.4%)相比,实现了61.7%改善(P<0.0001),具有统计学显著性和临床意义(表1)。
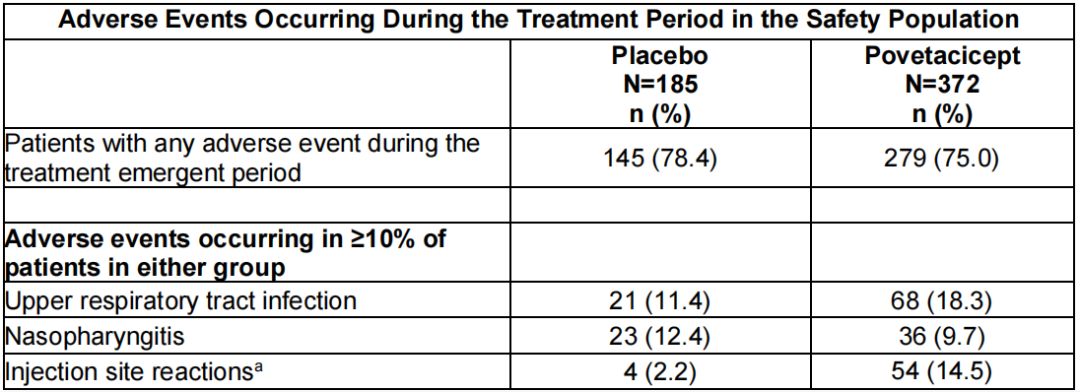
Povetacicept总体安全且耐受性良好,严重不良事件发生率在安慰剂组为4.3%(185例患者中发生8例),在Povetacicept组为3.0%(372例患者中发生11例)。感染相关严重不良事件的发生率在安慰剂组和 Povetacicept 组均为0.5%(表2)。
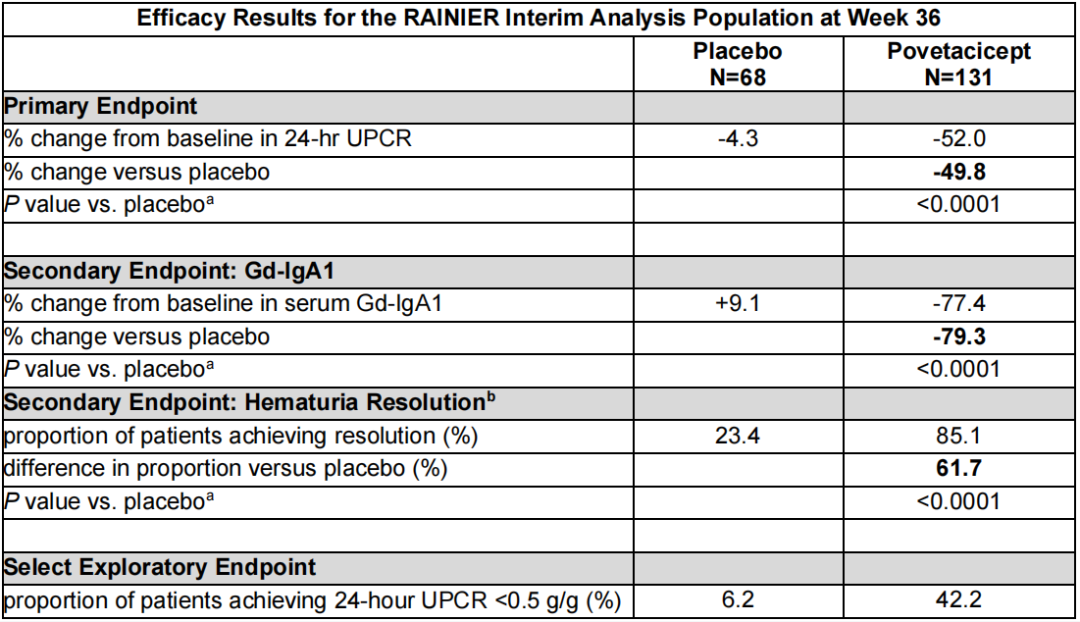
a:双侧P值。
b:针对基线存在血尿的患者(安慰剂组 N=36,povetacicept 组 N=67)的血尿消退情况
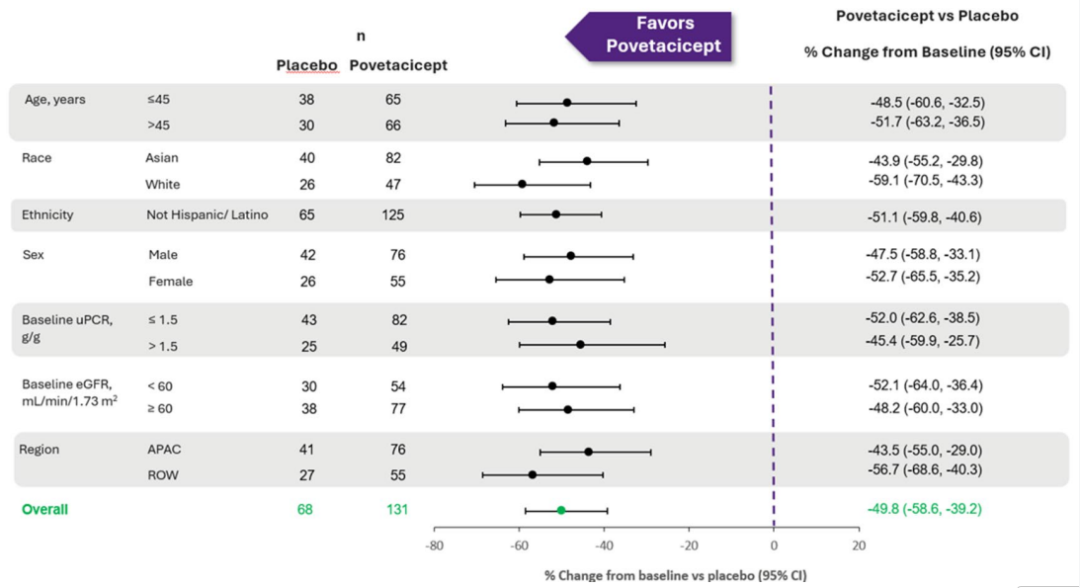
图1 第36周时24小时UPCR较基线变化的百分比预设亚组分析
表2 安全性人群在治疗期间出现的不良事件
目前,美国食品药品监督管理局(FDA)已授予Povetacicept用于治疗IgA肾病的生物制品许可申请(BLA)滚动审评资格。展望未来,该药物有望以皮下自动注射器的给药形式上市,届时患者可实现居家自行给药,每四周注射一次即可,切实为广大IgA肾病患者带来新的治疗福音。
参考文献
1.https://news.vrtx.com/news-releases/news-release-details/vertex-announces-positive-week-36-interim-analysis-results
_gl=1*14i5y4w*_ga*MzY1MjcxNTg3LjE3NzMxMTg5MDU.*_ga_60HPP96Z4B*czE3NzMxMjE0ODMkbzIkZzEkdDE3NzMxMjE0OTckajQ2JGwwJGgw*_ga_VRYNL0F5DE*czE3NzMxMjE0ODMkbzIkZzEkdDE3NzMxMjE0ODUkajU4JGwwJGgw
2.Kim J, Kamal F, Lafayette R. Current trial landscape of IgA nephropathy therapy. Med. 2026 Jan 9;7(1):100940. doi: 10.1016/j.medj.2025.100940.
医脉通是专业的在线医生平台,“感知世界医学