引言
胆管癌(CCA)是一种高度异质性的恶性肿瘤,根据解剖位置分为
胆管癌的解剖学亚型:差异大于共性1
Anatomic subsets of cholangiocarcinoma: More different than alike
由于病例罕见,临床研究常将iCCA、pCCA、dCCA三者合并为胆道癌(BTC)以完成入组,但这掩盖了亚型间的关键差异。这篇综述概述了CCA不同解剖学亚型在胚胎起源、致癌机制、免疫特征以及临床管理上的根本差异。
表1 iCCA和pCCA/eCCA的核心差异
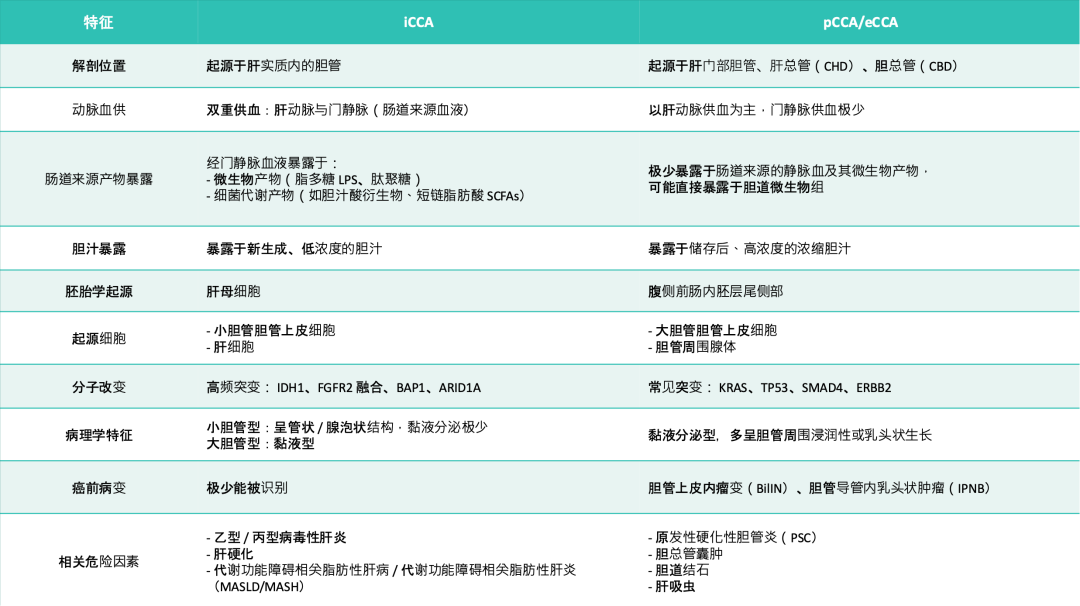
生物学与胚胎学差异:iCCA起源于肝内的肝母细胞或小胆管细胞;而pCCA/dCCA(即eCCA)起源于前肠内胚尾侧的原始内胚层,由大胆管及导管周围腺体(PBGs)中的胆管干细胞/祖细胞分化而来。
动脉血液供应差异:iCCA位于肝实质内,接受肝动脉和门静脉的双重供血,因此直接暴露于门静脉循环携带的肠道微生物产物(如LPS、短链脂肪酸)及代谢物。相比之下,pCCA/dCCA的供血主要来自肝动脉系统(如胆囊动脉、胰十二指肠后上动脉等),几乎无门静脉供血,主要暴露于储存浓缩的胆汁。
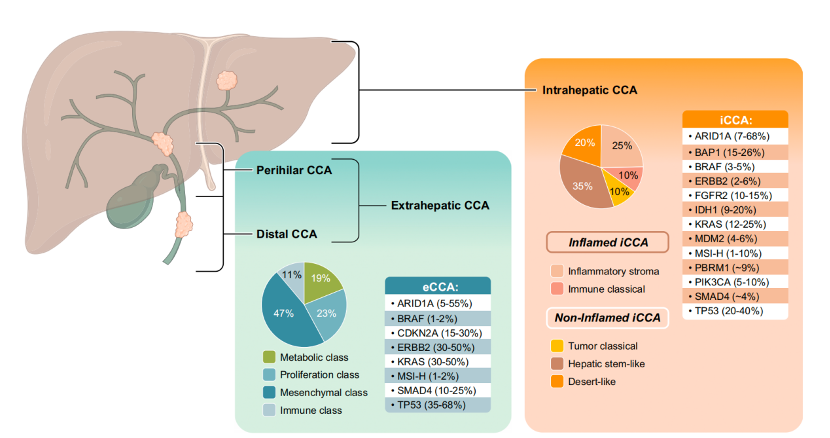
图1 iCCA和eCCA的遗传异质性
遗传学异质性: iCCA表现出特定的基因组图谱,常见IDH1/2突变(10%–20%)和FGFR2融合(10%–15%),以及 BAP1、ARID1A和PBRM1的失活突变 。相比之下,eCCA的分子特征以经典致癌基因和抑癌基因突变为主,包括KRAS(30%–60%)、TP53(30%–35%)和 CDKN2A 缺失(10%-15%)。
徐琦 教授
浙江省肿瘤医院
本篇综述为我们理清了一个核心临床问题:iCCA和pCCA/dCCA在生物学和遗传学范围内是截然不同的两种疾病,而非一个疾病的不同部位。小胆管型的iCCA与慢性肝病更相关,多暴露于新生成、未浓缩的胆汁;大胆管型CCA与慢性胆道炎症与胆道结构异常更相关,暴露于储存浓缩的胆汁环境;从分子图谱角度,iCCA常见可靶向的IDH1突变和FGFR2融合。eCCA的分子特征以经典致癌基因和抑癌基因突变为主。这决定了系统治疗时,iCCA有更多的靶向治疗的选择,例如IDH1抑制剂
打破“冷”肿瘤困局——胆管癌免疫治疗的精准分层与微环境重塑策略2
Stratifying cholangiocarcinoma: tumor microenvironment, molecular drivers, and novel immunotherapeutic approaches.
尽管免疫检查点抑制剂(ICB)联合化疗已成为晚期胆管癌的一线标准,但单药ICB疗效有限(总体应答率5~10%),TME的屏障是关键因素。本文重点分析了间质细胞类型丰度、解剖学位置、驱动突变、病因(肝吸虫、HBV、PSC)以及三级淋巴结构(TLS)的存在对免疫微环境的影响,并探讨了基于这些特征的患者分层策略。
间质细胞对TME的影响:肿瘤相关巨噬细胞(TAMs)和中性粒细胞不仅在CCA中高度浸润,更通过分泌TGF-β1、募集Tregs及释放中性粒细胞胞外诱捕网(NETs)构建了坚固的免疫抑制屏障。癌症相关成纤维细胞(CAFs)促进结缔组织增生,并与髓源性抑制细胞(MDSC)协同塑造免疫抑制性微环境。
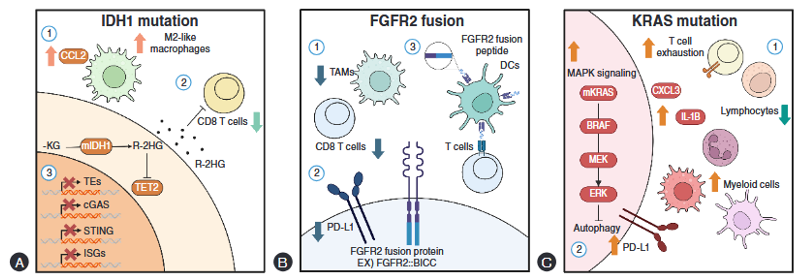
图2 分子驱动变异对TME的影响
分子驱动变异对TME的影响:在CCA中,IDH1突变与更“冷”的TME、免疫浸润减少相关。
1) IDH1突变促进巨噬细胞募集因子CCL2的过表达,增加了M2样巨噬细胞向肿瘤的浸润。
2) R-2HG直接抑制T细胞功能,导致细胞因子减少和效应功能减弱。
3) R-2HG抑制TET2去甲基化,进而导致I型和II型干扰素应答下调。
值得注意的是,小鼠模型中,IDH1抑制剂艾伏尼布可增加CD8+ T细胞浸润/活化,同时伴随PD-1与CTLA-4上调。艾伏尼布+抗CTLA-4在模型中显示出协同降低肿瘤负荷的作用。
FGFR2融合突变同样与免疫细胞浸润减少相关。尽管FGFR2融合蛋白产生的新抗原可被TILs识别,但T细胞被排斥在肿瘤之外。相反,KRAS突变肿瘤具有高度炎症特征,通过ERK信号通路稳定PD-L1表达,KRAS抑制剂与抗PD-1联用在临床前模型中显示出潜力。
三级淋巴结构:TLS的存在通常与较好的预后相关,但其位置至关重要。肿瘤内TLS提示免疫细胞有效浸润,与良好预后相关;而肿瘤周围TLS则可能提示免疫排斥。此外,成熟的滤泡样TLS(包含生发中心)比单纯的淋巴聚集体更能预测良好的生存期和免疫治疗响应。
徐琦 教授
浙江省肿瘤医院
克服CCA的免疫抑制障碍需要深入理解肿瘤间异质性。本综述将驱动基因与免疫微环境联系起来,对临床用药极具启发。为什么IDH1突变的胆管癌对PD-1单药治疗不敏感?答案就在于R-2HG——它既驱动肿瘤发生,又系统性压制了抗肿瘤免疫。这提示我们,免疫治疗不应是“一刀切”。对于IDH1突变的患者,未来或许可以考虑IDH抑制剂联合化疗±CTLA-4抑制剂的组合,而非盲目等待PD-1的疗效。对于TLS缺乏或高TAM浸润的“冷肿瘤”,则需探索重塑TME的联合策略(如CD40激动剂或抗CSF-1R)。
IDH突变胆管癌:靶向治疗一线探索新证据3
Results from the safety lead-in for a phaseⅠb/2 study of ivosidenib plus durvalumab and gemcitabine/cisplatin as first-line therapy in patients with locally advanced, unresectable or metastatic cholangiocarcinoma with an IDH1 mutation
2026 ASCO GI公布了艾伏尼布(IVO)+
截至2025年7月10日共纳入7例患者,治疗持续时间为1~4个月。其中1例部分缓解,4例疾病稳定,疾病控制率达100%。在安全性方面,6例患者(86%)报告≧3级AE。研究中仅观察到1例

图3 安全性特征
徐琦 教授
浙江省肿瘤医院
尽管度伐利尤单抗联合GemCis方案已确立为一线标准治疗,然而,对于携带IDH1突变的特定亚群,如何进一步提升疗效仍是临床痛点。从前述文献可知,IDH1突变通过其代谢产物R-2HG重塑肿瘤免疫微环境,且临床前研究证实,IDH1抑制剂艾伏尼布可有效逆转上述免疫抑制状态,不仅能显著增加肿瘤内CD8+ T细胞的浸润与活化,还可同步上调PD-1与CTLA-4的表达,与免疫检查点抑制剂联用展现出显著的协同抗肿瘤效应,这为IDH1抑制剂联合免疫化疗的一线治疗策略提供了坚实的理论基础。
本研究的初步数据证实,在标准免疫化疗基础上联合艾伏尼布进行一线治疗,初步显现出抗肿瘤活性,且并未产生非预期的叠加毒性。基于安全导入期优异的疾病控制表现与可耐受的安全性,该四药方案已进入扩展阶段,以期为IDH1突变CCA患者探索新的一线治疗标准。
FGFR2选择性抑制剂Lirafugratinib的临床耐药机制揭示4
Mechanisms of Clinical Resistance to Selective FGFR2 Inhibition by Lirafugratinib
近年来,FGFR2已成为iCCA等多种实体瘤的重要治疗靶点。Lirafugratinib作为一种高选择性、不可逆的FGFR2抑制剂,在II期研究中对FGFR抑制剂初治的FGFR2融合/重排iCCA患者的客观缓解率(ORR)达88%5。近日发表于《Annals of Oncology》的一项研究,进一步探索了Lirafugratinib在FGFR2改变(融合/重排/突变)实体瘤中的临床耐药机制。研究的主要终点是描绘Lirafugratinib获得性耐药的基因图谱,并对比其与泛FGFR抑制剂(如
研究共纳入28例接受Lirafugratinib治疗并出现疾病进展的FGFR2变异晚期实体瘤患者,包括FGFR抑制剂初治组(n=16)和FGFR抑制剂经治组(n=12)。肿瘤类型以肝内胆管癌为主(22例),其余包括胃
FGFR抑制剂初治患者的耐药机制分析:在FGFR抑制剂初治组中,中位治疗时长为4.6个月,若仅纳入FGFR2融合或已知应答突变患者,中位治疗时长为6.4个月。在16例初治患者中,12例(75%)患者在接受Lirafugratinib治疗并出现疾病进展后检测到获得性耐药相关的基因变异。与泛FGFR抑制剂耐药患者相比,初治患者出现M538I(7例)和L618F(6例)FGFR2激酶结构域突变的频率显著增加(p<0.001),而泛FGFR抑制剂常见的V565F和N550K突变频率则显著降低;初治患者出现RTK-MAPK旁路激活(包括KRAS、NRAS、BRAF突变等)更频繁(p=0.009)。此外,还观察到1例FGFR3融合,提示其为FGFR2选择性抑制下的潜在特异性逃逸机制。9例患者携带超过一种耐药变异。在同时携带FGFR2突变和RTK-MAPK变异的患者中,FGFR2突变的VAF通常更高,提示其是主要的耐药驱动因素。
FGFR抑制剂经治患者的耐药机制分析:Lirafugratinib在既往FGFR抑制剂耐药人群中仍观察到临床疗效,中位治疗时长为3.7个月。在12例既往接受过泛FGFR抑制剂治疗的患者中,ctDNA动态分析显示:与初治患者相比,经治患者中M538I/L618F的频率降低,而N550K/K642R更常见(p<0.0001),表明既往治疗史对后续治疗的选择有深远影响。
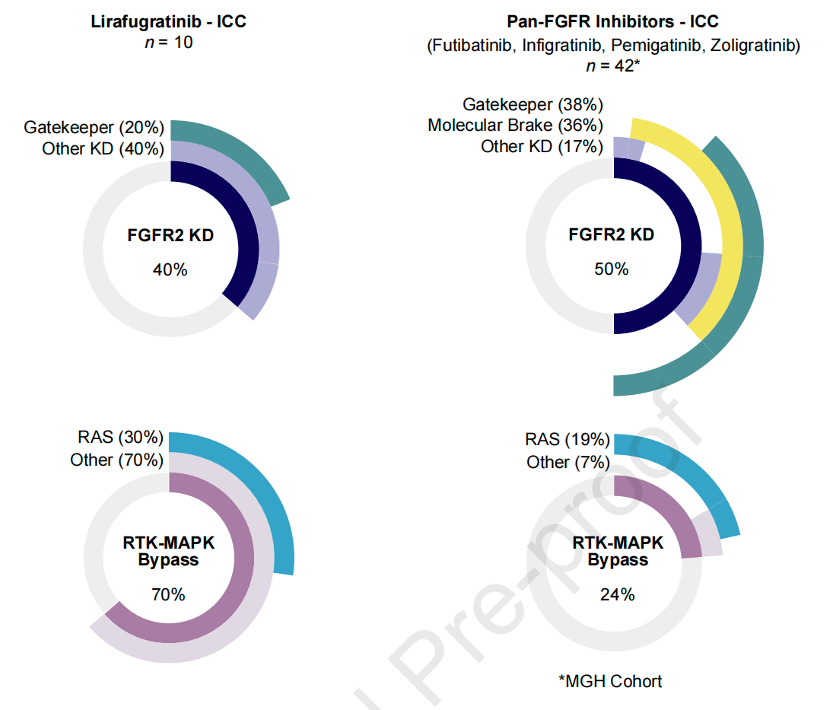
临床前模型进一步探索:在携带FGFR2融合的ICC13-7细胞系中诱导表达临床观察到的突变,观察到M538I、L618F、K660M突变导致Lirafugratinib的IC50值分别上升59.3倍、23.9倍和19.6倍,而V565F突变仍保持敏感。在携带M538I/M539L双突变的ICC27 PDX模型中,Lirafugratinib治疗无效,而福巴替尼则能有效抑制肿瘤生长。分子动力学模拟进一步揭示,M538I突变通过破坏Lirafugratinib与Phe646的疏水相互作用,导致药物结合不稳定,从而介导耐药。
徐琦 教授
浙江省肿瘤医院
胆管癌中FGFR2融合/重排已获批药物多为泛FGFR抑制剂,但临床长期获益受获得性耐药限制:常见FGFR2激酶结构域二级突变(N550、V565等)+各类旁路。Lirafugratinib作为首创的高选择性FGFR2抑制剂,展现出与泛FGFR抑制剂截然不同的耐药机制图谱。它能有效克服包括守门位点V565F/L和分子刹车位点N550H在内的多种泛FGFR抑制剂耐药突变,支持其在泛FGFR抑制剂治疗失败后的序贯使用潜力。然而,M538I、L618F等特定激酶域突变及RTK-MAPK旁路激活的频繁出现构成了新的挑战。研究结果强调了单药FGFR抑制的局限性,并提示未来需探索基于ctDNA指导的序贯治疗或如联合针对RTK-MAPK节点的抑制剂等的联合治疗策略,以应对耐药异质性。
总结
综合本期四篇文献,我们可以看到CCA的治疗正在向精准化和全程化迈进。纵观当前CCA的研究进展,明确CCA亚型之间的本质差异是迈向精准治疗的关键一步。基于NGS检测的靶向治疗可为患者争取宝贵生存时间。此外,针对IDH1突变和FGFR2融合等靶点的新型药物正在不断涌现,部分已在后线治疗中展现出明确疗效,并逐步向一线推进。与此同时,耐药机制的深入解析也为后续联合治疗策略的设计提供了重要依据。未来,随着多模态分子分层的深入、联合治疗策略的优化及新型靶向药物的涌现,CCA的精准治疗将迎来更广阔的发展空间,造福更多患者。
徐琦 教授
浙江省肿瘤医院
浙江省肿瘤医院 肝胆胰胃内科副主任
主任医师 副教授 硕士生导师
中国抗癌协会肿瘤肝脏病学专业委员会委员
中国抗癌协会胃部肿瘤整合康复专业委员会委员
杭州临床肿瘤研究会胃癌研究分会副主委
杭州临床肿瘤研究会胰腺癌研究分会副主委
浙江省数理医学学会胃癌专业委员会常委
浙江省抗癌协会肿瘤转移专业委员会常委
杭州临床肿瘤研究会县域肿瘤研究分会常委
浙江省中医药文化交流协会中西医结合肿瘤专业委员会常委
浙江省抗癌协会胃癌专业委员会青年委员
浙江省数理医学学会盆腔肿瘤多学科诊疗专业委员会委员
浙江省医学会肿瘤营养与治疗学分会青委会委员
浙江省抗癌协会抗癌药物专业委员会临床肿瘤药学学组成员
浙江省医学会第四届医学鉴定专家库成员
浙江省肿瘤医院伦理委员会委员
参与国际及国内多中心临床研究百余项
曾多次在胃癌、结直肠癌MDT比赛中获奖
免责声明:
本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批号:M-TIBSO-CN-202603-00020
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)