激素受体阳性/人表皮生长因子受体 2 阴性(HR+/HER2-)是
PI3K/AKT/mTOR通路
PAM通路是目前乳腺癌领域研究较为深入的通路,超过70%的乳腺癌会出现导致该信号通路异常激活的变异。PAM通路的异常激活会导致细胞过度增殖、抵抗凋亡,促进肿瘤的发生和进展,此外,还会影响肿瘤对内分泌治疗、PARP抑制剂、化疗和靶向治疗的耐药,导致癌症进展和更差的预后。因此,阻断该通路为逆转耐药提供了新的治疗思路。
PAM通路中的关键节点和调节因子包括PI3K、AKT、mTOR、TSC1/2和PTEN,在HR+/HER2-乳腺癌中,导致PAM通路异常的最常见原因为PIK3CA激活突变、AKT1激活突变和/或PTEN失活。
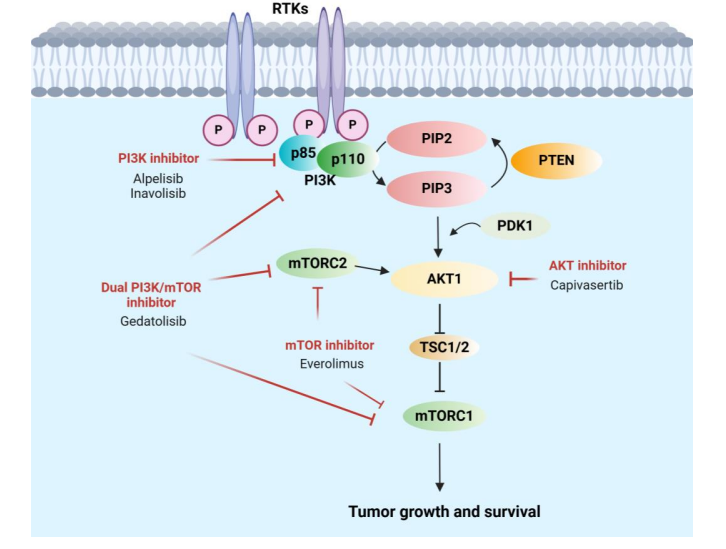
图1:PI3K通路及美国FDA批准或获快速通道资格认定的PI3K抑制剂[1]
PI3Ks
PI3Ks主要参与调节信号传导、膜运输和代谢通路。PI3K可分为三类,其中Ⅰ类PI3K是由催化亚基和调节亚基组成的异源二聚体:
催化亚基分为p110α、β、δ、γ四种,分别由PIK3CA、PIK3CB、PIK3CD和PIK3CG编码;
调节亚基可分为p85α、p85β和p85γ,分别由PIK3R1、PIK3R2和PIK3R3编码。
其中,PIK3CA突变是PAM通路中最常见的遗传改变,可见于所有乳腺癌亚型,其他基因突变虽然频率较低,但也可能是与耐药相关的生物标志物。PIK3CA的突变主要发生在两个热点区域:螺旋结构域和激酶结构域。这些突变作为PI3K活性的功能获得性突变,可能导致AKT/mTOR下游信号异常激活,从而促进肿瘤发生发展。
AKT和PTEN
AKT是PI3K通路的另一个关键组成部分,分别由AKT1、AKT2和AKT3编码。在肿瘤细胞中,AKT1能够参与肿瘤细胞的增殖和生长,促进肿瘤发生并抑制凋亡,而AKT2则通过调节细胞骨架动力学,使肿瘤细胞更易于侵袭和转移。
PTEN是一种抑癌基因,能够编码具有双重特异性的脂质和蛋白磷酸酶,可下调PI3K/AKT信号传导;还可以通过对PIP3的去磷酸化负向调节PI3K/AKT通路,抑制生长和生存信号。此外,在乳腺癌中,PTEN功能丧失会导致PI3K信号激活。
mTOR
mTOR是PI3K/AKT信号通路下游的一种
其他PI3K通路相关基因
除上述核心节点外,PI3K通路中还有其他基因发挥关键调控作用,例如抑癌基因TSC1和TSC2,它们可形成TSC1/2复合物,负向调节mTORC1信号传导;PDK1会在PI3K通路激活后,参与对AKT1的激活;而RET的激活可诱导PI3K/AKT通路的激活,是乳腺癌治疗的潜在靶点。
通路间的相互作用
PI3K通路各节点不仅具有单独的作用,也会与其他通路产生相互作用,在癌细胞信号传导中形成一个复杂的网络。因此在研发精准治疗方案时,也需要考虑不同通路之间的协同效应。
其中的典型代表是PI3K和ER通路在乳腺癌中的相互作用。ER+乳腺癌是一种
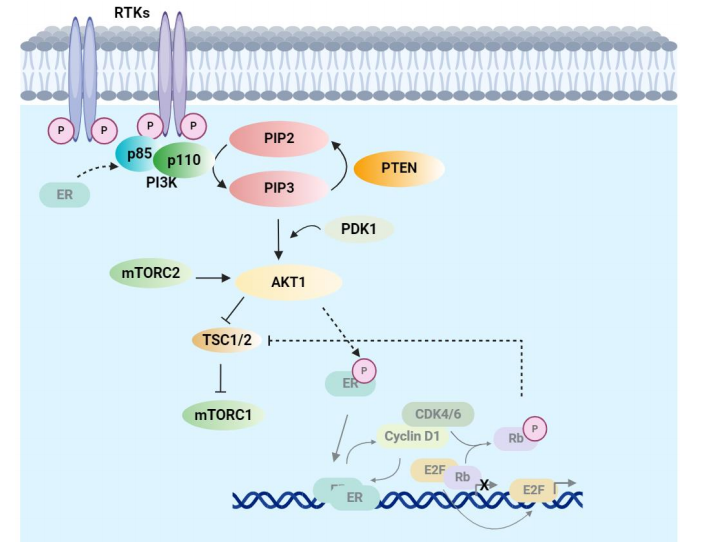
图2:HR+/HER2-乳腺癌中PI3K通路、细胞周期与ER通路的串扰[1]
建立HR+/HER2-乳腺癌特异性基因谱
由于PI3K/AKT/mTOR通路异常与治疗耐药密切相关,进入精准检测时代以后,对于标准治疗后出现疾病进展的转移性HR+/HER2 -乳腺癌患者,通常会进行基因检测,明确通路相关基因变异状态以指导下一步治疗。对于晚期或转移性HR+/HER2-乳腺癌,二线治疗方案的选择高度依赖于患者肿瘤或ctDNA中可检测到的基因组生物标志物信息。
因此,对于需要制定二线治疗方案的HR+/HER2-乳腺癌患者,NGS乳腺癌Panel具有重要的临床价值,可以检测肿瘤中是否在关键的乳腺癌相关基因(包括ESR1、PIK3CA、AKT1、PTEN,以及PI3K通路或其他协同通路中的其他基因)。在极少数情况下,还可能需要进行RNA测序以检测RET融合、NTRK融合等。如果需要评估微卫星不稳定性(MSI)和肿瘤突变负荷(TMB),可以选择包含MSI和TMB的NGS Panel。
结论
本综述盘点了PI3K/AKT/mTOR/PTEN通路中各节点及其基因异常形式,阐明了其在HR+/HER2-乳腺癌发生发展、治疗耐药中的关键作用,为该亚型乳腺癌精准治疗手段的开发提供了理论与临床参考。目前,已经有一些靶向PI3K通路中不同节点的药物获得FDA批准,或在临床试验中显示出有希望的结果。未来,随着PAM通路调控机制的深入解析、临床医师与分子病理学专家的深度协作,以及NGS、PCR等基因检测技术的普及与标准化推进,HR+/HER2-乳腺癌的精准治疗将逐步走向成熟并广泛落地,有望让更多患者从个体化诊疗中获益。
审批编号:CN-179605
有效期至:2027-03-09
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)