跨界解析“真菌-宿主-细菌-代谢产物”轴:揭示共生真菌经C型凝集素受体通路加重结肠炎的机制
Colonic Engyodontium fungus triggers neutrophil antimicrobial activity to suppress Lactobacillusjohnsonii-derived glutamic acid-maintained Tregs
Journal of Clinical Investigation
PMID: 41770903 [IF=13.6]
主要通讯作者
唐策,
来源:IBD Daily
目前,尽管通过内转录间隔区 (ITS) 测序检测到了丰富的真菌信号,但由于许多真菌来源于饮食/水、缺乏耐温性或需要严苛的培养条件,全球范围内从人类粪便中识别出的真菌仅约200种,从小鼠肠道中分离出活体共生真菌更是极具挑战。这直接导致了测序信号可能仅反映死菌或瞬时真菌DNA,限制了我们对活体共生真菌在肠道免疫稳态中功能逻辑的认知。
在免疫识别方面,模式识别受体如C型凝集素受体 (CLRs) 在感应真菌成分中发挥核心作用。例如,Dectin-1已被证明能限制致病性念珠菌的入侵,而Dectin-2 (基因: 人CLEC6A/小鼠Clec4n) 主要识别α-甘露糖,并激活SYK-CARD9信号通路以诱导Th17等免疫应答。然而,肠道共生真菌是否通过Dectin-2等受体主动调节肠道的免疫微生态平衡、以及是否会影响肠道的黏膜炎症,目前仍缺乏系统性的证据。
本研究围绕“真菌如何重塑肠道免疫环境”这一核心,利用自主研发的真菌纯化技术,揭示了侧齿霉菌 (Engyodontium) 通过Dectin-2-钙卫蛋白轴精准打击益生菌及其保护性代谢产物的致病模型,为IBD的精准干预提供了全新靶点。
研究整合了临床队列分析、多组学测序及多种转基因小鼠模型。在微生物层面,利用Dectin-2-Fc融合蛋白建立真菌纯化体系,首次分离并鉴定出肠道关键共生侧齿霉属真菌Engyodontium sp.。在机制层面,通过单细胞RNA测序、骨髓移植嵌合实验及中性粒细胞体外模型,解析了真菌诱导钙卫蛋白分泌的信号通路。在免疫代谢层面,结合非靶向与靶向代谢组学,筛选出调控调节性T细胞 (Treg) 稳态的关键代谢物L-
1. 肠道共生侧齿霉菌的鉴定及其对粘膜免疫与微生物群的调控
研究团队利用自主构建的Dectin-1/2-Fc融合蛋白作为分子探针,从鼠源及人源粪便中捕获并纯化了优势真菌组分。ITS测序与形态学鉴定确认,侧齿霉菌 (Engyodontium sp.) 是Dectin-2在肠道中的主要识别对象,其定植于肠腔及上皮表面。在稳态小鼠模型中,侧齿霉菌的定植显著增加了结肠固有层 (cLP) 中性粒细胞的比例,同时降低了调节性T细胞 (Treg) 的比例,并伴随显著的
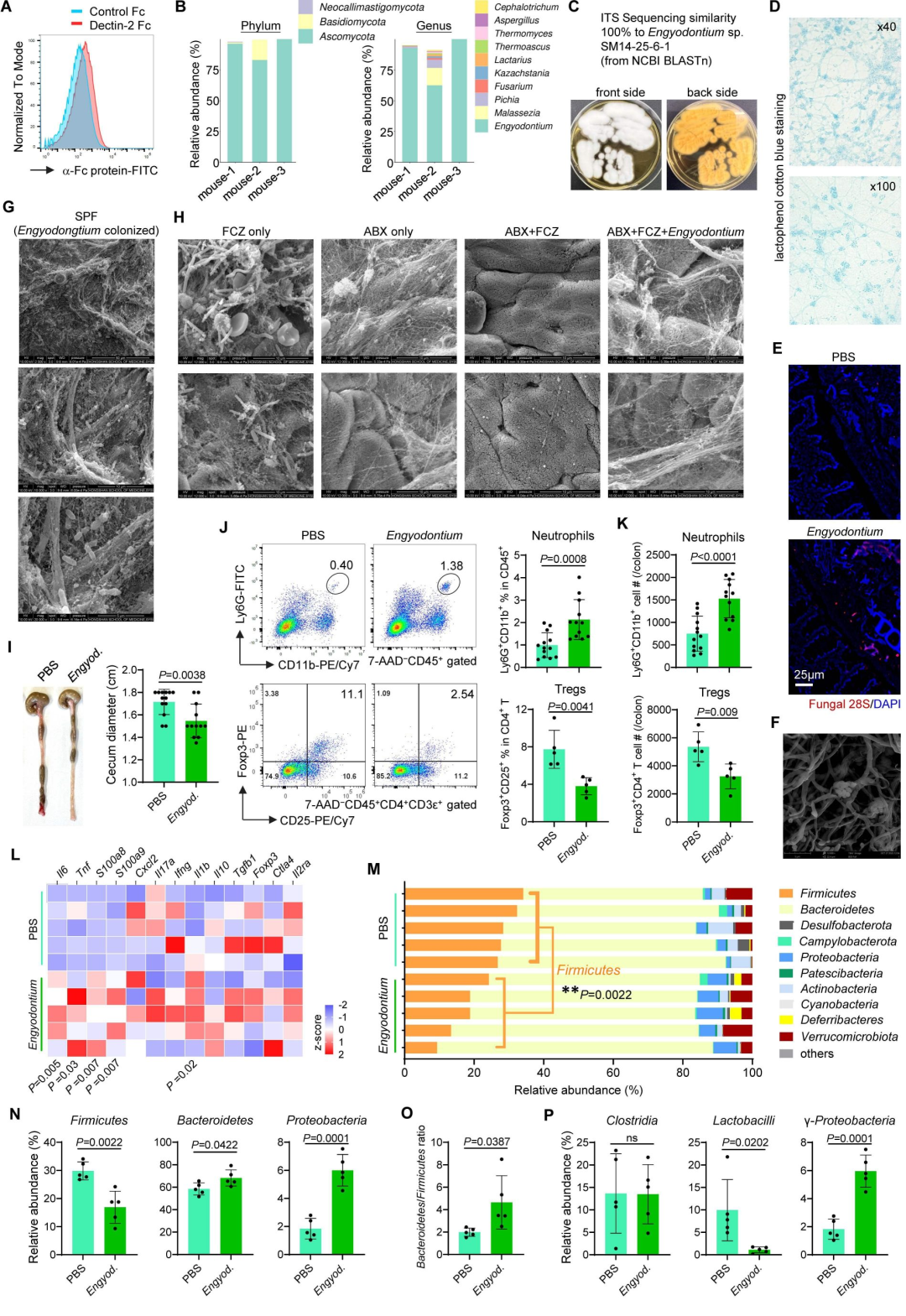
图1. 肠道共生侧齿霉菌在稳态下对粘膜免疫谱及共生微生物群的调节作用。
2. 侧齿霉菌诱导上皮趋化因子分泌并介导中性粒细胞招募
实验发现,侧齿霉菌Engyodontium在肠炎模型中表现出显著的致病性,显著加剧了DSS诱导的结肠炎症状。机制上,该真菌通过TLR2-TRAF6信号通路直接诱导结肠上皮细胞高表达趋化因子CXCL1/2,从而招募大量中性粒细胞浸润。通过CXCR1/2阻断或TRAF6抑制,可显著缓解侧齿霉菌介导的中性粒细胞积累及肠炎恶化,证实了该过程由上皮信号启动并由中性粒细胞驱动 (图2)。
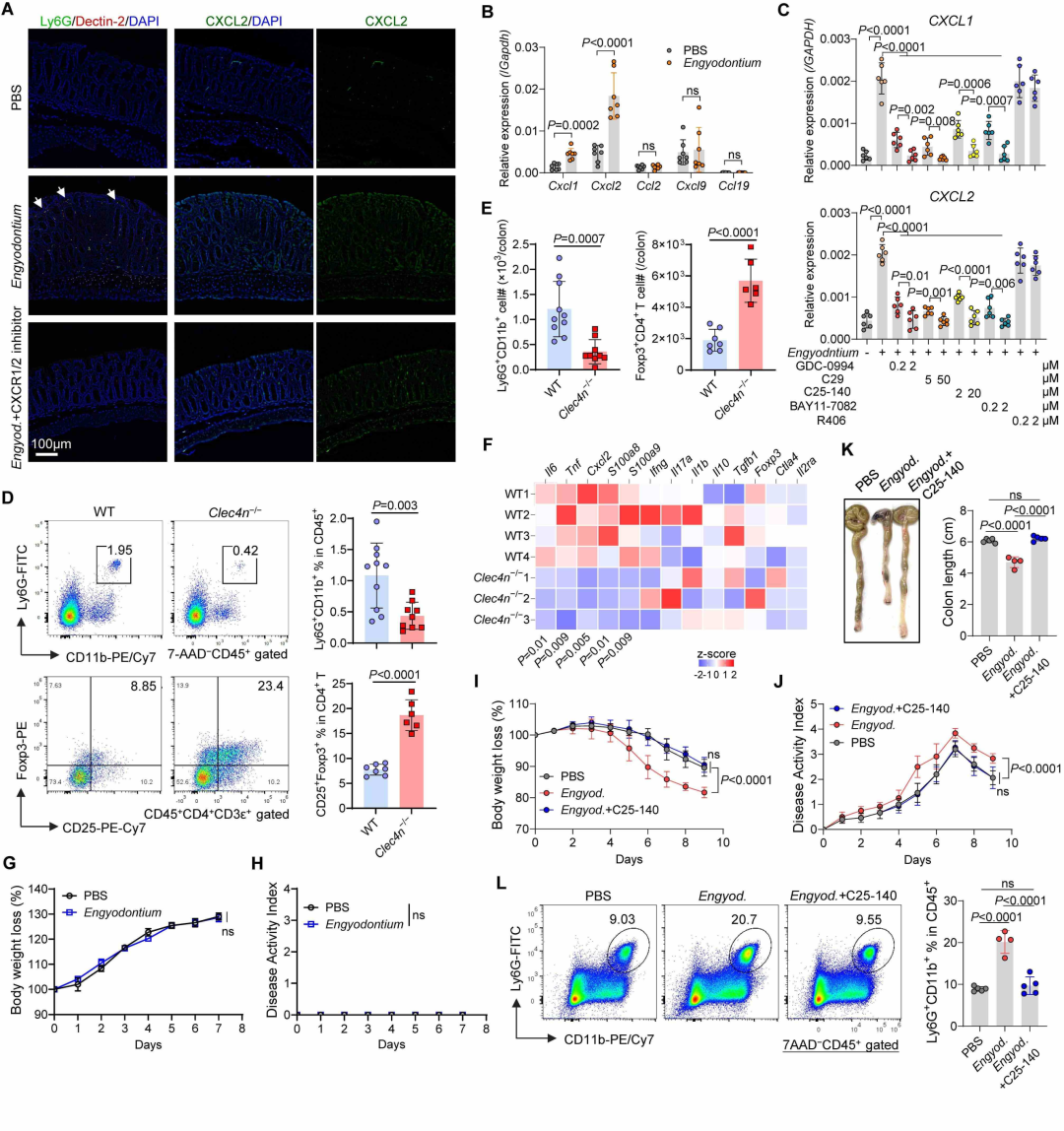
图2. 侧齿霉菌诱导肠上皮趋化因子产生并介导中性粒细胞招募以加重结肠炎。
3. Engyodontium经由Dectin-2-CARD9信号通路驱动炎症
为了验证受体特异性,研究者在Dectin-2缺失 (Clec4n−/−) 及CARD9缺失 (Card9−/−) 小鼠中进行验证。结果显示,这两种基因缺失小鼠均能抵抗侧齿霉菌引起的肠炎加重。侧齿霉菌仅在野生型小鼠中诱导中性粒细胞扩张及Treg抑制,而在Clec4n−/−或Card9−/−小鼠中,这种免疫失衡得到显著逆转。与之相对,Dectin-1在该真菌诱导的炎症放大中作用有限 (图3)。
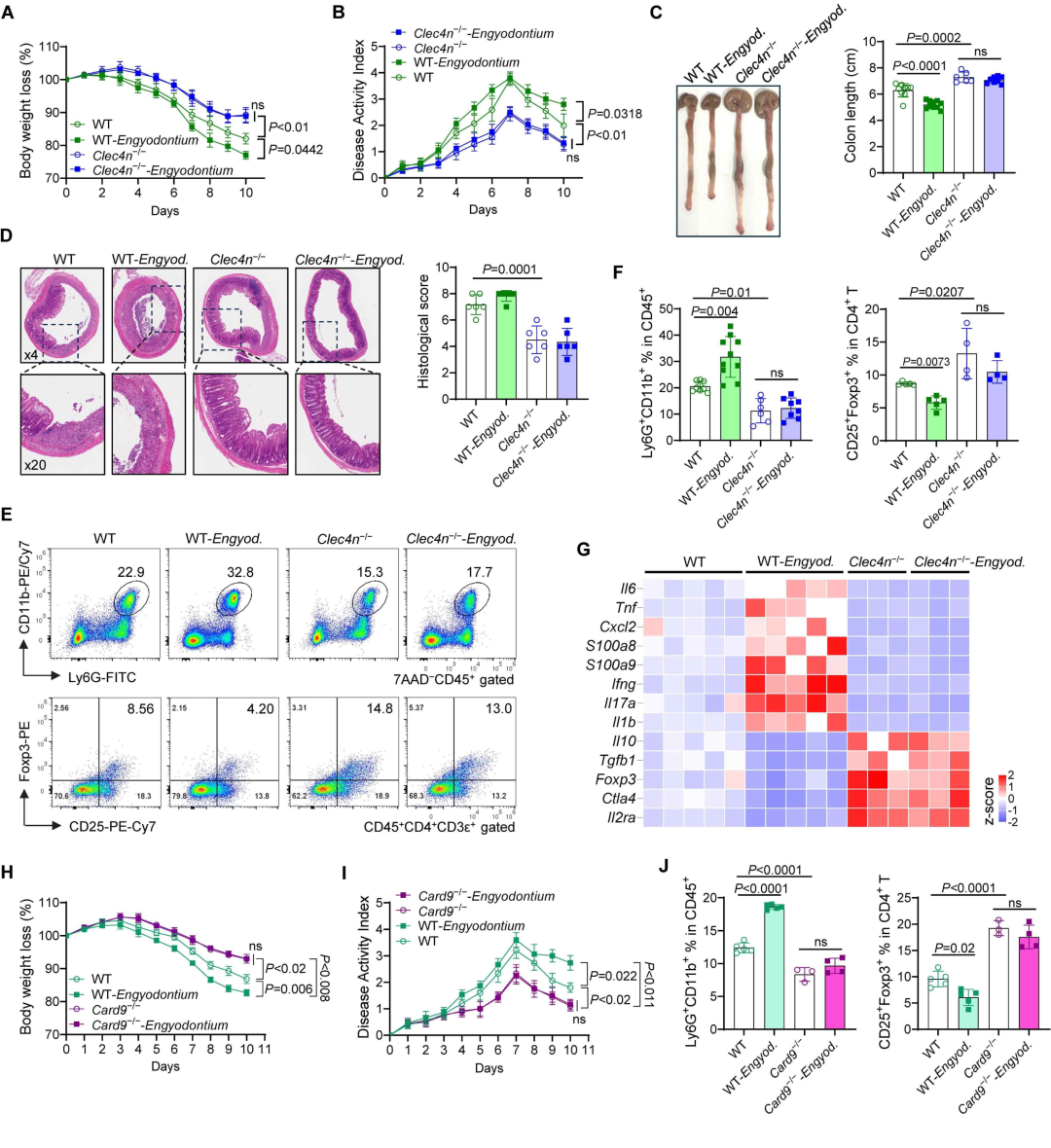
图3. 侧齿霉菌经Dectin-2-CARD9信号通路驱动中性粒细胞激活并促进肠炎进展。
4. 侧齿霉菌介导的肠炎恶化依赖于肠道细菌群落重构
通过共饲养 (Co-housing) 和
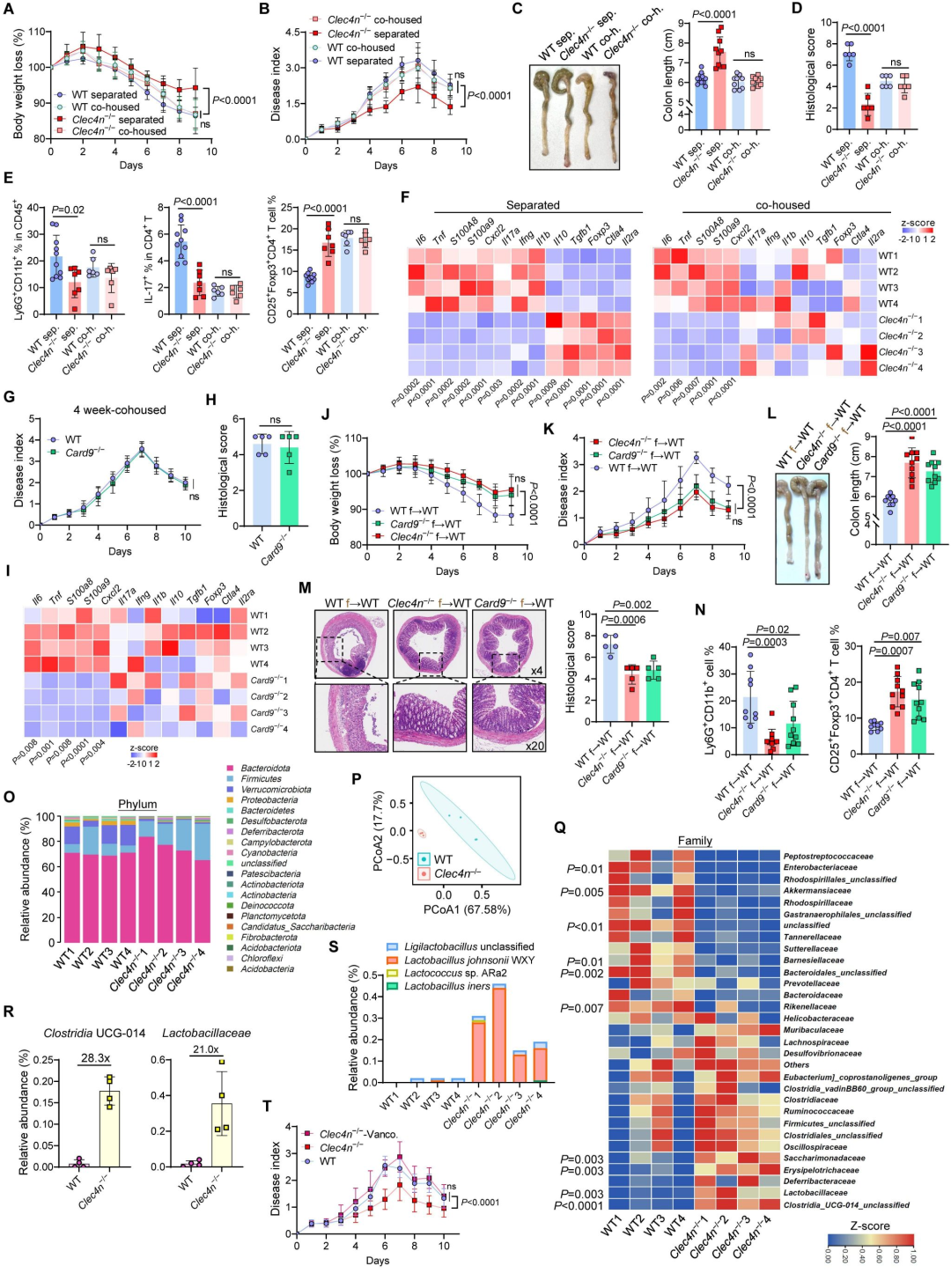
图4. 侧齿霉菌介导的肠炎加重及其对保护性Treg细胞的抑制依赖于肠道菌群的重构。
5. 钙卫蛋白介导对约氏乳杆菌的抑制及此菌的代谢保护作用
研究者发现,侧齿霉菌激发的Dectin-2-CARD9信号诱导中性粒细胞产生大量的抗菌肽——钙卫蛋白 (S100A8/A9)。钙卫蛋白通过其抗菌活性,特异性地抑制约氏乳杆菌WXY株在肠道内的定植。非靶向代谢组学分析显示,约氏乳杆菌定植显著富集了
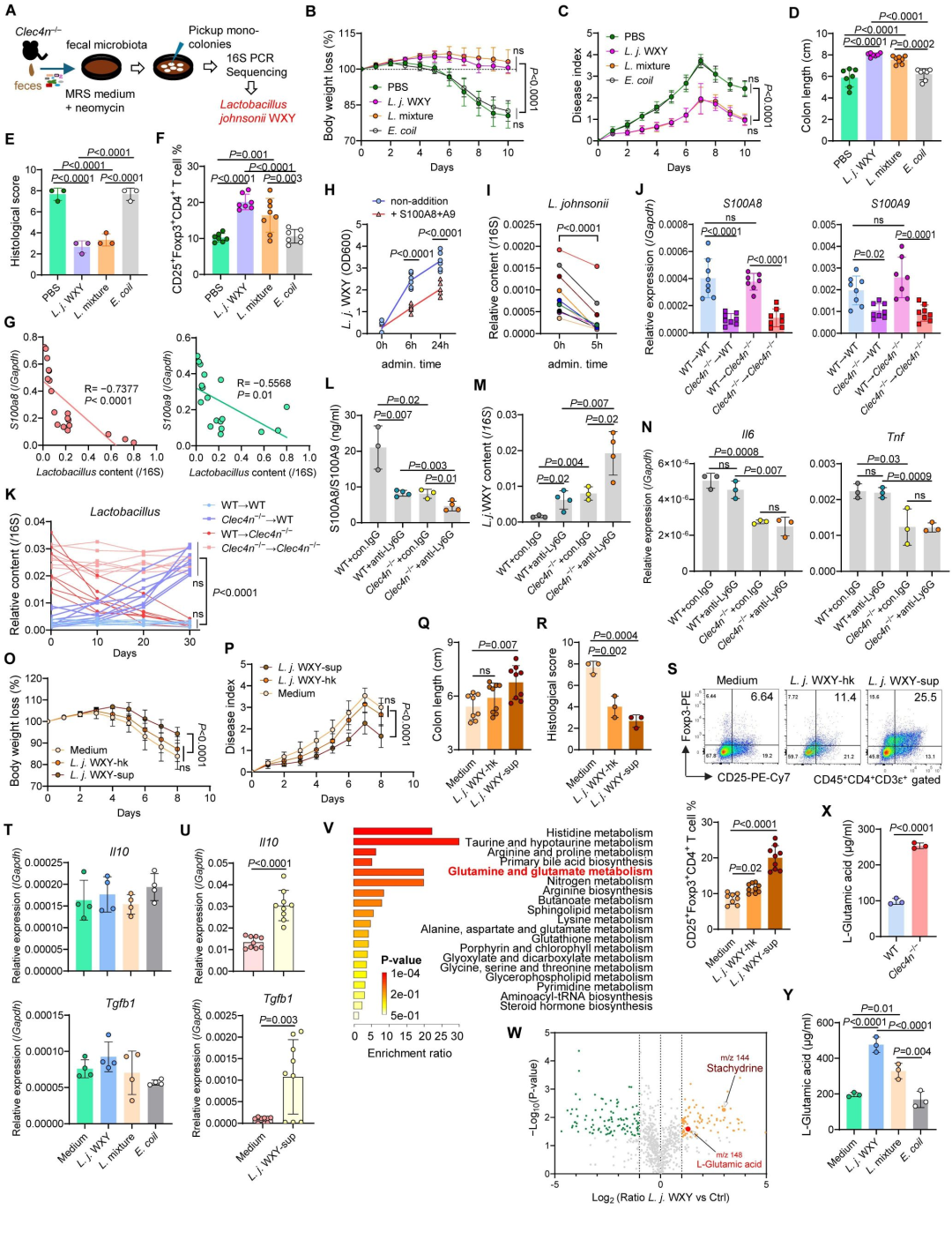
图5. Dectin-2-钙卫蛋白轴限制约氏乳杆菌定植及其衍生代谢物的保护作用。
6. L-谷氨酸通过增强IL-2受体信号维持肠道保护性Treg细胞群
功能验证显示,口服L-谷氨酸可模拟约氏乳杆菌的保护作用,显著缓解结肠炎并提升Treg的占比。机制研究发现,L-谷氨酸能上调T细胞表面IL-2受体CD25的表达,进而增强IL-2信号通路对Treg细胞分化及存活的维持能力。全基因组分析表明,约氏乳杆菌WXY株高表达
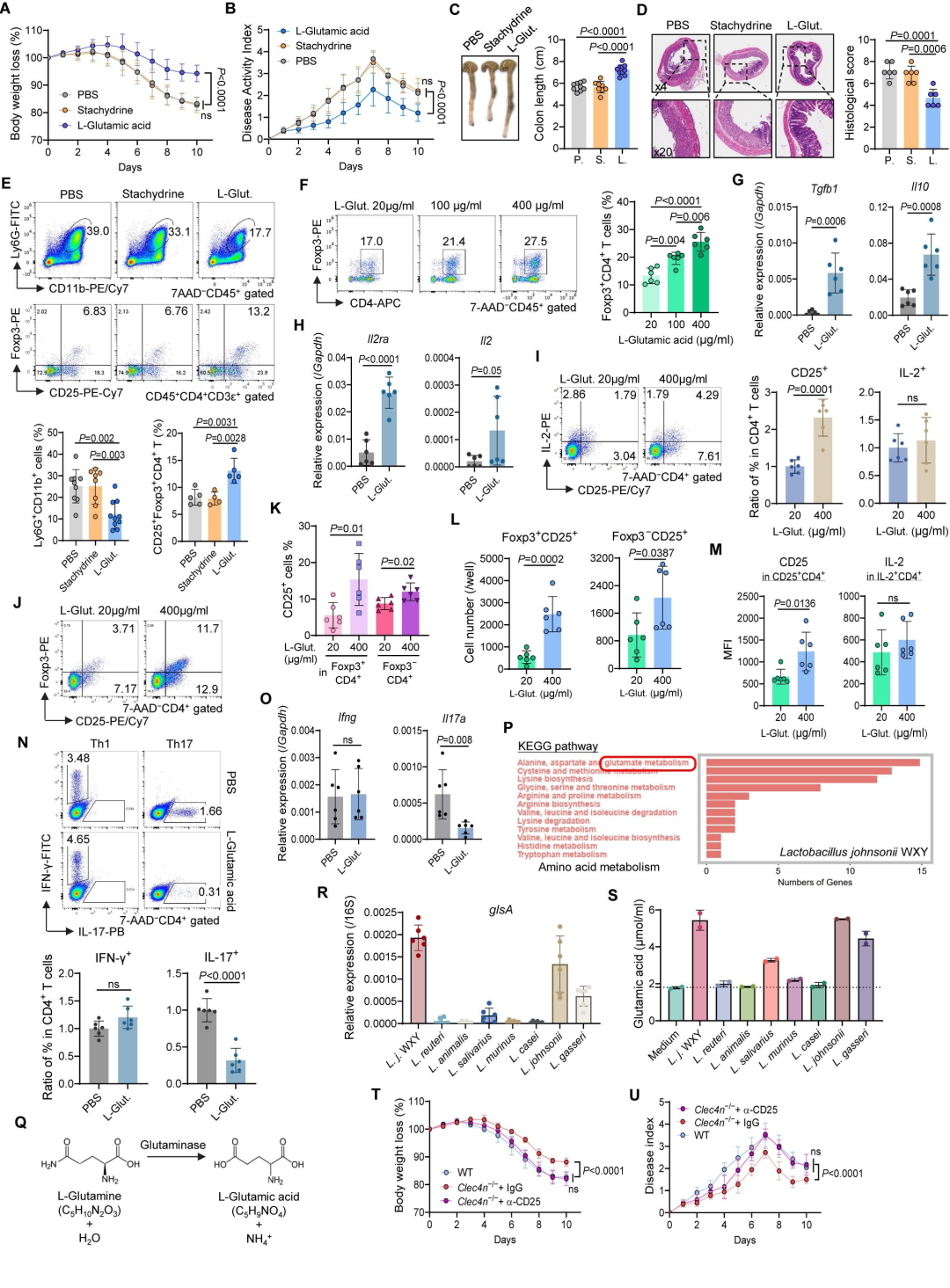
图6. 约氏乳杆菌代谢产生的L-谷氨酸通过增强IL-2受体信号维持肠道Treg细胞群。
7. 临床IBD患者中存在保守的真菌-Dectin-2致病轴与代谢紊乱
在CD和UC患者中,研究者观察到侧齿霉菌丰度显著升高,且与约氏乳杆菌丰度呈显著负相关。患者肠组织中DECTIN-2及钙卫蛋白表达水平与侧齿霉菌含量呈正相关。临床代谢组学同样证实,CD患者粪便中L-谷氨酸水平显著降低。体外实验证实,L-谷氨酸能诱导人类原代T细胞向Treg细胞分化,验证了该机制在人类疾病中的高度保守性 (图7)。
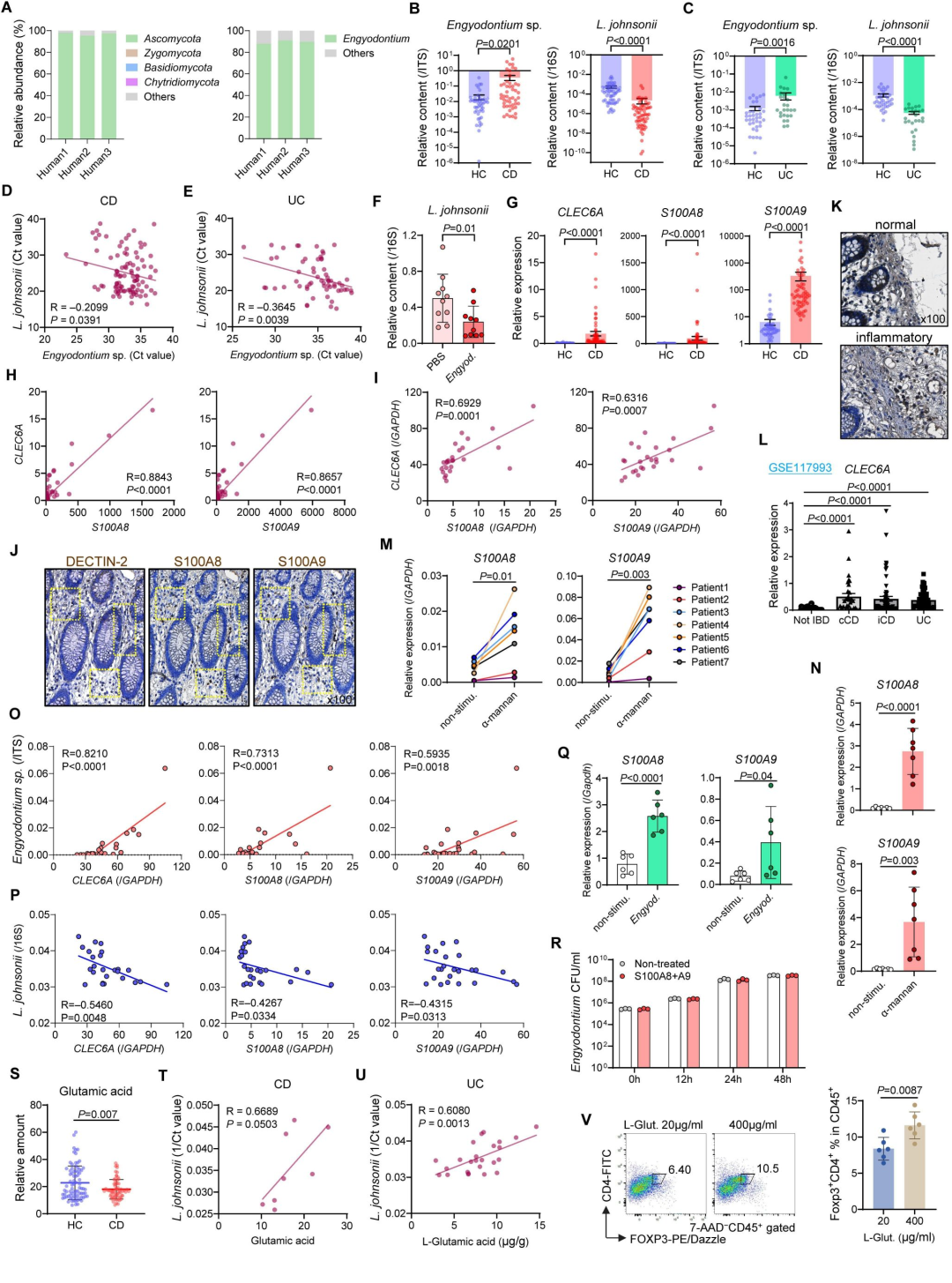
图7. Engyodontium-DECTIN-2-钙卫蛋白致病轴同样存在于IBD患者中。
本研究建立并优化了基于CLR-Fc融合蛋白捕获活体共生微生物的技术体系,为解析“肠道真菌组”功能提供了关键工具。该研究不仅阐明了Engyodontium-Dectin-2-Calprotectin这一全新的致病轴,更明确了微生物代谢产物L-谷氨酸在粘膜免疫稳态中的核心作用,为IBD的精准治疗及营养干预提供了新途径。值得一提的是,该研究与唐策课题组2025年6月发表于《Immunity》的研究成果 (揭示肺部共生真菌通过Dectin-1信号轴诱导
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)