前言
局部晚期
目前,FOLFIRINOX或
患者基本情况
患者信息: 女,65岁。
主诉: 2024年10月因持续一个月上腹部疼痛并放射至背部就诊,疼痛强度评分为4分。
既往史: 家族史和既往病史无显著异常,ECOG体能状态评分为2。
实验室检查: 初始
检查与诊断
影像学检查: 腹部增强CT显示多处胰腺肿块病变,提示胰腺恶性肿瘤,并浸润脾动静脉和脾脏,伴有腹膜后淋巴结转移。
病理诊断: 活检最终确诊为胰腺导管腺癌。根据影像学结果,临床分期为cT4N1M0,III期。 分子标志物: 免疫组化(IHC)显示为错配修复完整(pMMR)状态(MLH1、MSH2、MSH6和PMS2蛋白表达完整)。值得注意的是,PD-L1检测显示患者CPS高达30。

图1 A-B:血清肿瘤标志物水平的时间变化;C-H:胰腺病灶的组织病理学和免疫组化表征;I:肿瘤体积(GTV)勾画,红色轮廓为主要GTV,黄色箭头指示非照射转移灶
治疗策略
考虑到疾病处于局部晚期且患者拒绝手术及标准方案化疗,研究者采用了个性化的BRICS多模态方案,即益生菌(Bifidobacterium)、
立体定向放疗(SBRT): 针对原发胰腺病灶,剂量为24 Gy/3f,旨在促进免疫原性细胞死亡。
系统治疗: SBRT结束后5天启动,每21天为一周期,共6个周期。包括免疫治疗——
益生菌调节: 整个治疗期间持续口服
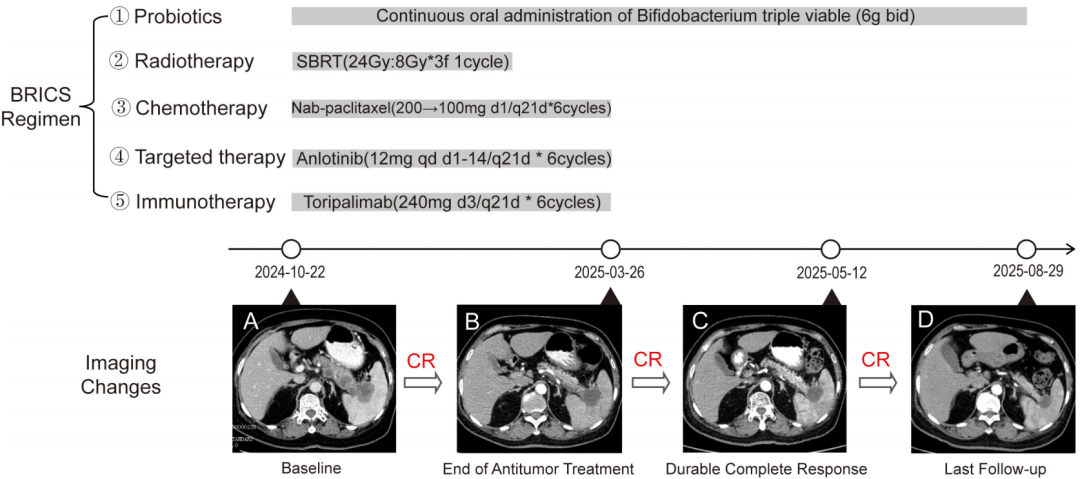
图2 治疗策略、干预时间线及影像学变化
疗效与安全性评估
临床获益: 两个治疗周期后,患者疼痛评分从基线的4分降至0分(从轻中度疼痛转为无痛)。
实验室检查结果: 治疗两个周期后,CA19-9和CEA水平显著降至924.3 ku/L和5.56 ng/mL。2025年3月完成6个周期治疗后,肿瘤标志物恢复正常,CA19-9为31.4 ku/L,CEA为2.67 ng/mL。
影像学评价: 随访CT扫描确认达到CR。截至2025年8月18日,患者仍处于CR状态,肿瘤标志物稳定,且ECOG评分为0。
安全性: 治疗耐受性良好,仅观察到可管理的2级中性粒细胞减少症,无严重不良事件报告。
病例总结与讨论
传统观念认为pMMR/MSS肿瘤对免疫检查点抑制剂(ICIs)反应不佳,本病例对“MMR状态是胰腺癌中ICI疗效的唯一决定性预测指标”这一观点提出了挑战。特别对于胰腺癌这一MSI-H/dMMR发生率较低(<5%),而PD-L1阳性(CPS≥1)的发生率相对较高(13.5%~71%)的癌种,如果仅以MSI-H/d-MMR状态为依据进行筛选,那么相当数量的PD-L1阳性肿瘤患者可能会被排除在ICI潜在获益范围之外。本研究表明,在pMMR胰腺癌中,PD-L1表达可能作为ICI疗效的独立且潜在的主导性预测标志物。
研究者指出,BRICS方案的成功源于五种方式的协同作用:SBRT不仅发挥局部减瘤作用,更利用其“原位疫苗”效应,通过促进免疫原性细胞死亡诱导肿瘤相关抗原释放;白蛋白结合型紫杉醇在直接杀伤肿瘤的同时减少抑制性MDSCs和Tregs;安罗替尼使肿瘤血管正常化以缓解缺氧,并增加效应T细胞浸润;持续补充双歧杆菌则可能增强了系统免疫应答。
总而言之,本文首次记录了一例pMMR/高CPS分子亚型的局部晚期胰腺癌患者通过非手术治疗实现CR的案例。这表明,在精准医学背景下,不应自动将pMMR胰腺癌归类为不适合免疫治疗的“冷肿瘤”。综合PD-L1等分子分型评估以及针对肿瘤微环境量身定制的多模态协同策略,可能为这种极具挑战性的疾病开辟新的治疗途径。
参考文献:
1.Yang S, Shao L, Wu Y, et al. Complete response to BRICS in Locally advanced pancreatic cancer (pMMR, CPS 30): a case report[J]. Frontiers in Immunology, 2026, 17: 1743752.
撰写:Babel
排版:Babel
执行:Babel
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)