引言
在激素受体阳性/人表皮生长因子受体阴性(HR+/HER2-)转移性
研究结果
►患者特征和样本
2018年7月至2023年4月期间,共有51例接受标准ET联合CDK4/6i治疗的HR+/HER2- MBC患者被纳入前瞻性观察性队列(图1a)。在中位随访28.0个月(范围1.6-66.0)期间,收集了279份纵向血液样本,每位患者中位数为5份(2-16份)。最终成功为43例患者(250份样本)构建了肿瘤知情检测panel,构成了分析队列(图1a)。基线患者和肿瘤特征以及治疗轨迹见表1、图1b、c。
大多数患者为
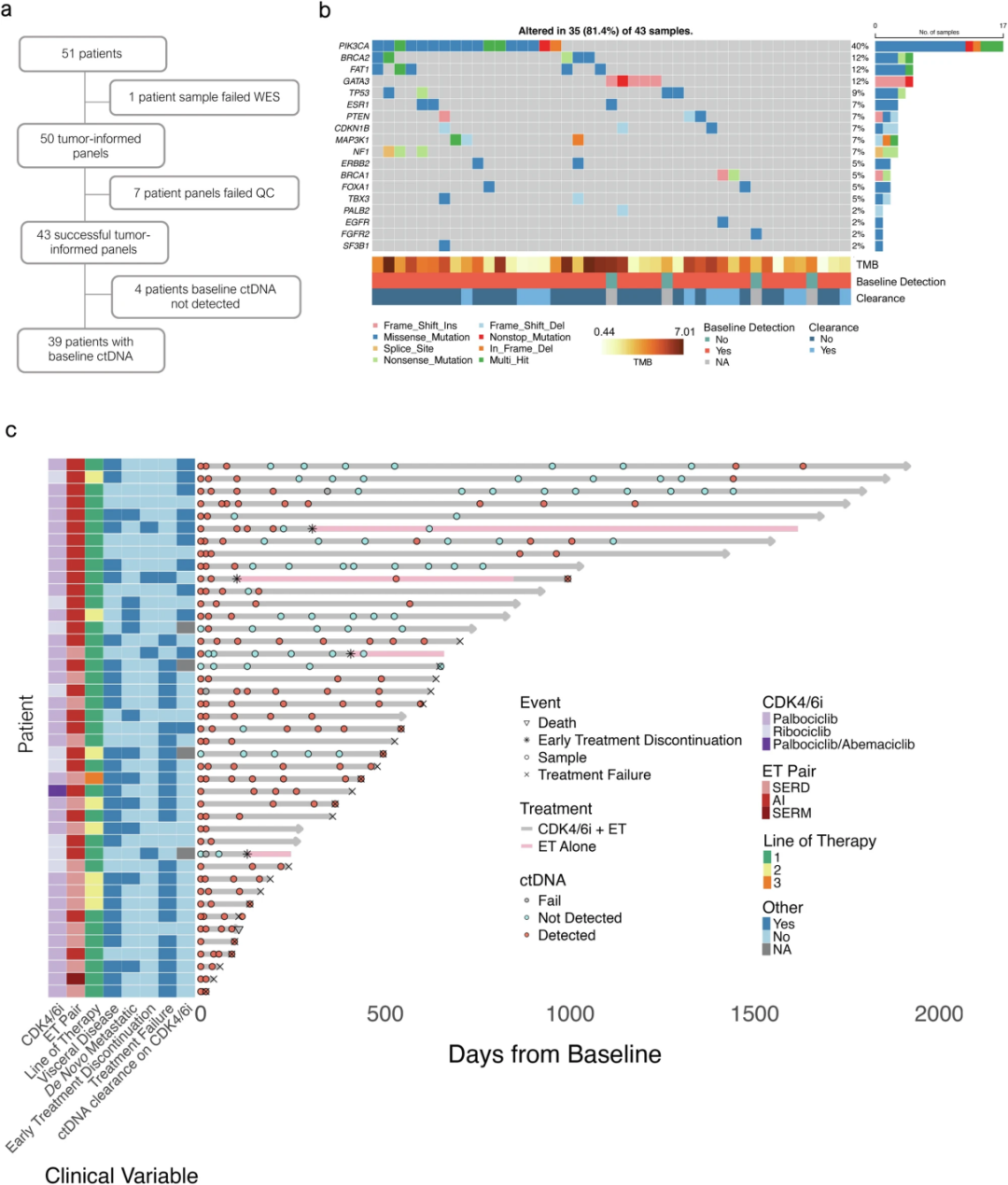
图1. 患者入组流程及基因检测结果[1]
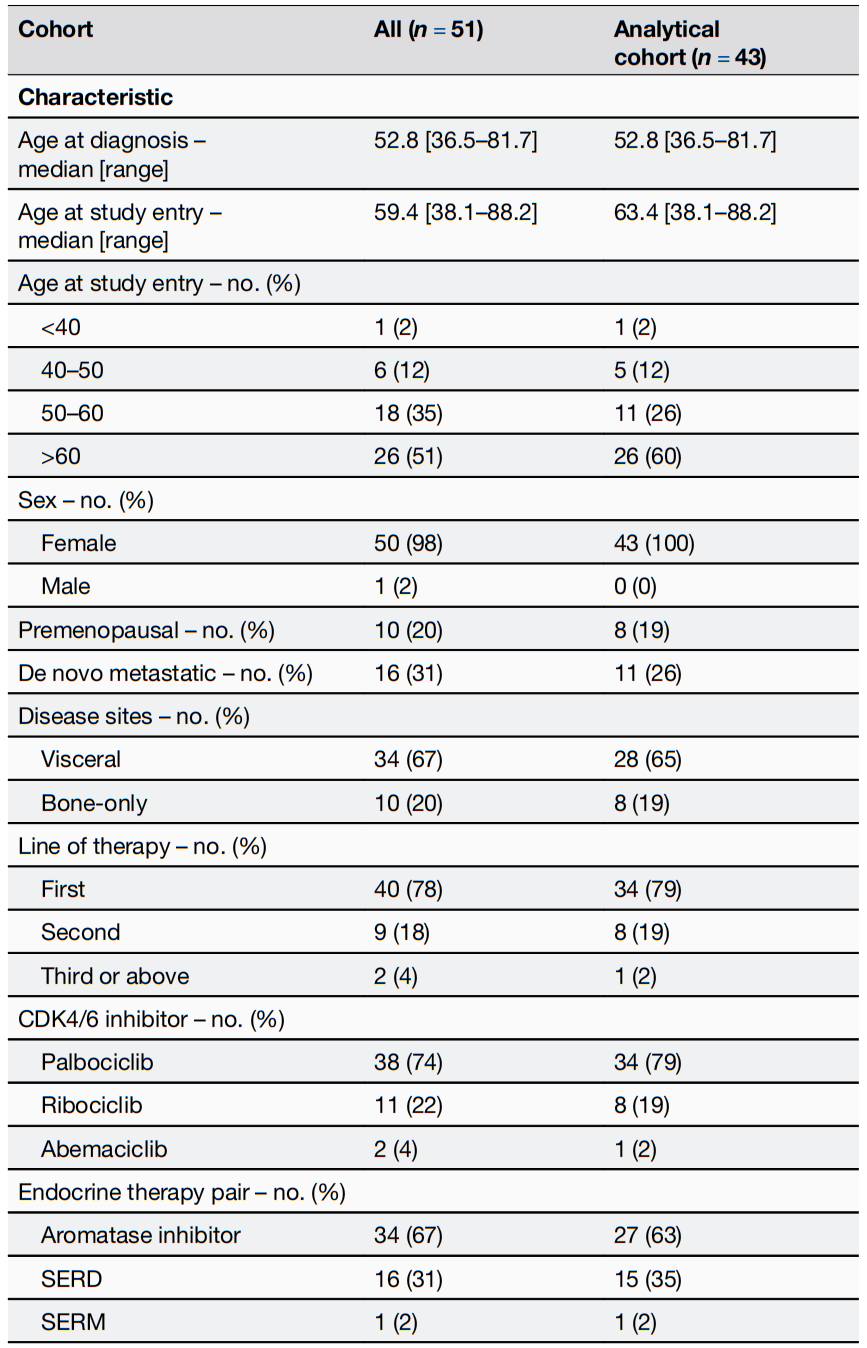
表1. 患者基线特征[1]
►基线ctDNA:临床病理、基因组和预后关联
在43例患者中,共39例(91%)基线检出ctDNA,基线时的中位变异等位基因频率(eVAFBL)为0.5%(0.006-17.9%)。其中,8例(21%)患者<0.1%,有肝转移灶的患者显著更高(2.92% vs 0.32%,p=0.02),但eVAFBL与其他临床病理或基因组协变量均无关(如单纯骨转移、原发性内分泌耐药史、用于panel生成的存档组织与基线血液采样的时间间隔、PI3K通路改变、DNA损伤修复改变、TMB)。此外,eVAFBL在具有RECIST v1.1可测量和不可测量疾病的患者间无显著差异(p=0.43);然而,在有肝病患者中,eVAFBL与最大靶病灶直径呈正相关(rho 0.69, p<0.01),但在总体人群中则无关(rho 0.3, p=0.13)。
所有患者中,较高的eVAFBL可能预示较短的治疗失败时间(TTF,HR=1.15,95%CI,1.06-1.24,p<0.01)和总生存期(OS,HR=1.17,95%CI,1.09-1.26,p<0.01),在调整内脏疾病的存在后,关联仍具有统计学显著性(图2a-b)。在具有可测量疾病的患者中,较高的eVAFBL与较低的部分缓解可能性相关(有应答和无应答患者分别为0.5% vs 5.0%;p=0.12)。
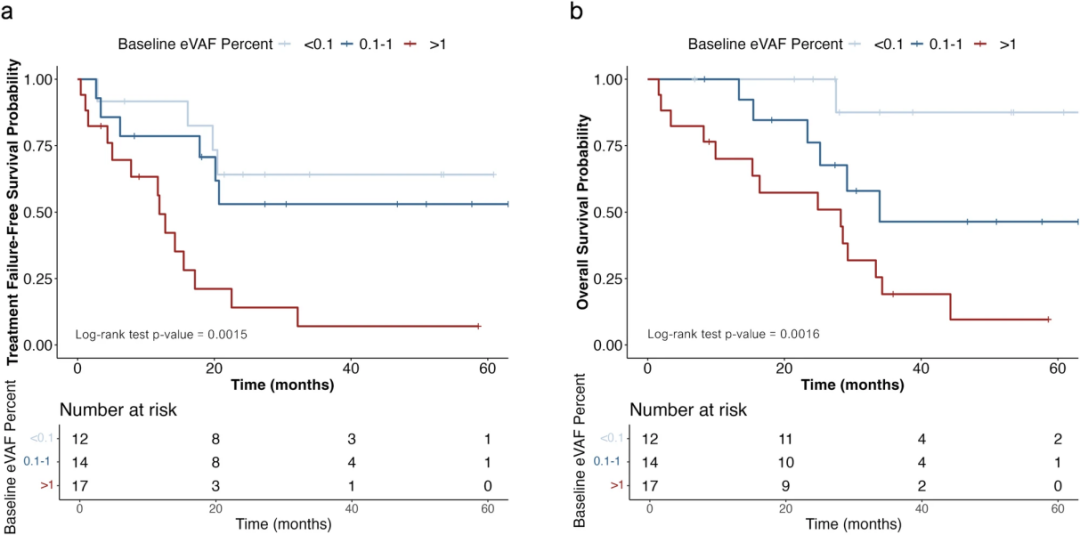
图2. 基线ctDNA检测结果[1]
►ctDNA监测:早期动力学及其与RECIST v1.1指标的关系
250份血液样本中有174份(70.0%)检出ctDNA。所有时间点的中位eVAF为0.29%(0.0008-34.94%),其中67个(39%)阳性时间点eVAF<0.1%,28个(16%)<0.01%。eVAF在治疗期间显著下降,而在影像学进展时增加(中位0.11%和1.43%;p<0.01)。大多数患者(77.8%)在第一个28天周期内eVAF降至低于基线水平,88.9%在首次影像学复查前出现下降(首次检查中位时间为2.9个月,0.8-5.12)(图3a)。6例(13.9%)患者观察到早期(即≤29天)eVAF升高超过基线,但与更差的结局无关;其中3例患者经历了较长的TTF,其eVAF短暂升高后很快降至基线下(图3b)。此外,在经历原发性疾病进展的8例患者中,仅2例出现早期eVAF升高。在27例具有可测量疾病的患者中,ctDNA动态捕捉到靶病灶的Δ直径与ΔeVAF呈现中度相关(rho 0.69, p<0.01)(图3c)。
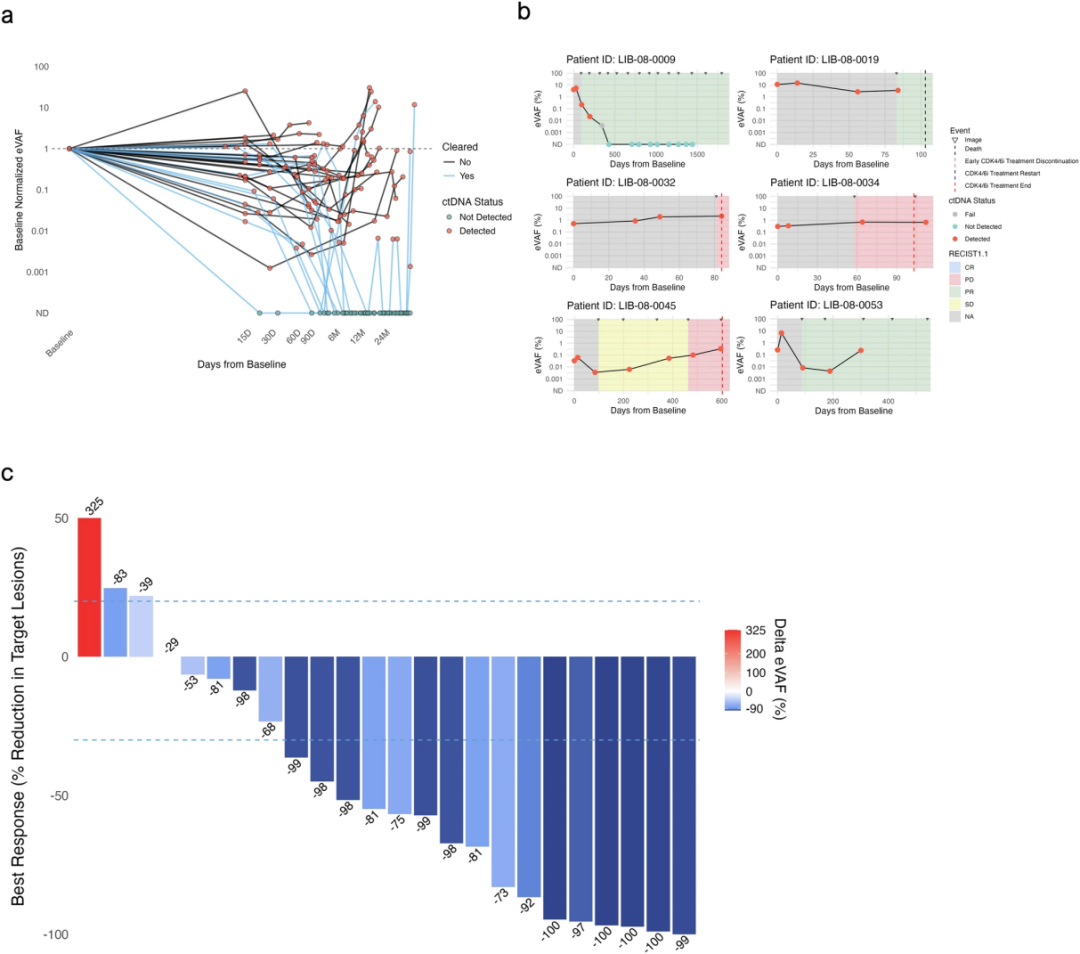
图3. ctDNA监测动态变化结果[1]
►ctDNA监测:分子学缓解的定义
39例基线可检出ctDNA的患者中,11例(28%)在治疗期间发生ctDNA清除,中位发生时间为5.7个月(0.5–13.5个月)(图4a)。ctDNA清除与无清除患者的中位TTF为NR vs 14.3个月,中位OS为NR vs 29.3个月(TTF, HR=0.068,95% CI,0.009-0.52, p<0.01;OS,HR=0.072,95%CI,0.011-0.47, p<0.01,图4b-c)。
为进一步考虑ctDNA清除前的时间间隔以及与其晚期发生相关的潜在生存结局偏倚,在12个月时进行了界标分析,结果显示,ctDNA清除在eVAFBL<0.1%(p<0.01)、研究期间接受AI治疗(p=0.01)以及有影像学反应(p=0.06)的患者中更常见;然而,未观察到与其他相关临床协变量(如疾病部位、治疗线数、CDK4/6i类型、原发性内分泌耐药史)的关联趋势。值得注意的是,获得影像学部分缓解的患者中(n=17)发生ctDNA清除的患者(n=7; 41%)TTF(HR=0.08,95%CI,0.01-0.65, p=0.019)和OS(HR=0.08,95%CI,0.01-0.71, p=0.023)均显著更长。
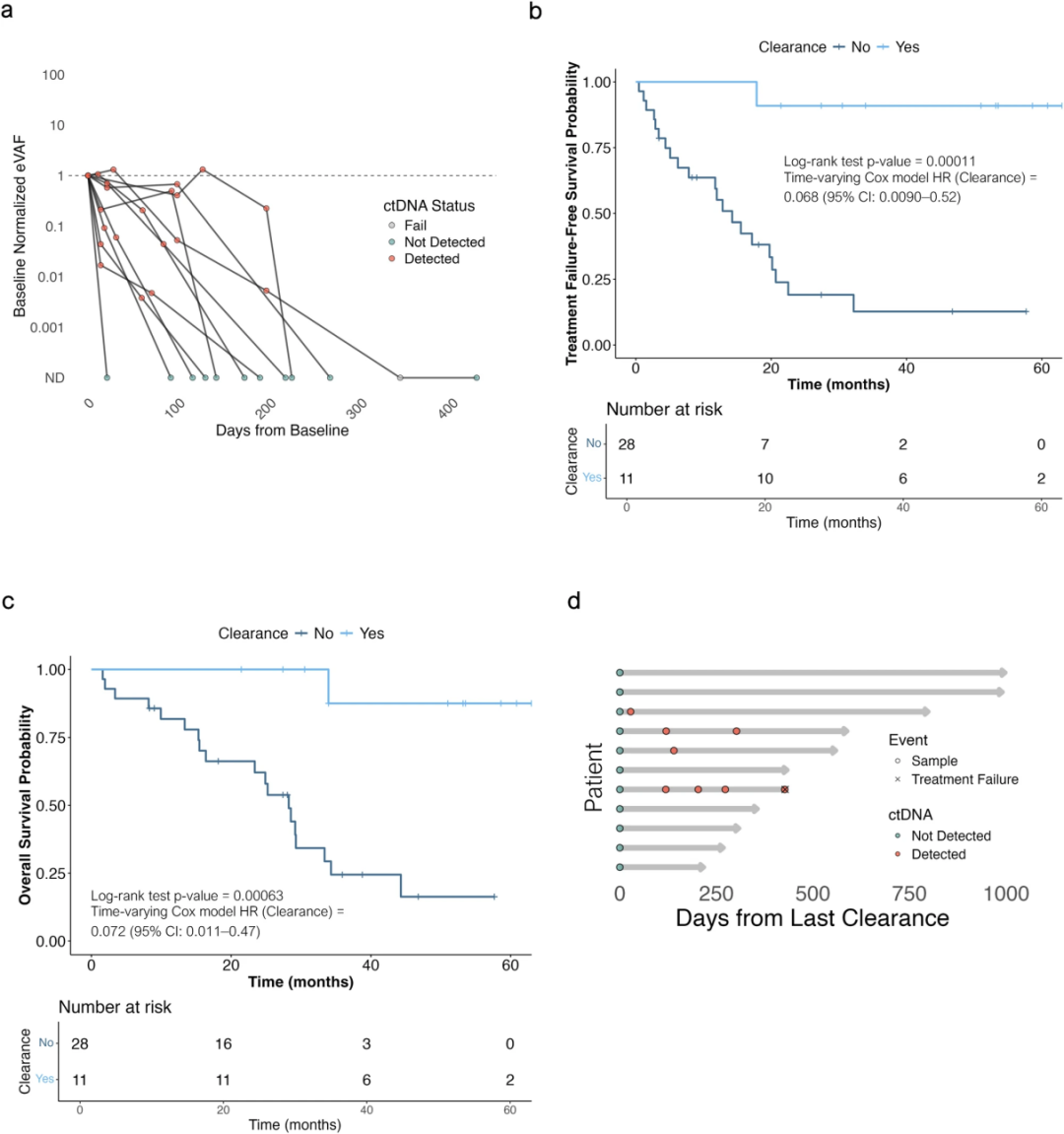
图4. ctDNA清除患者的ctDNA动力学分析[1]
►ctDNA监测:探索分子学进展的定义
随访期间,24例(55.8%)患者治疗失败,其中17例(70.8%)在治疗期间任何时间点出现过ctDNA升高。分析显示,相对于前一次样本的任何eVAF升高(占样本的26%)对于预测放射科医生判定的影像学进展显示出80%的敏感性、86%的特异性、55%的阳性预测值(PPV)和95%的阴性预测值(NPV)(C指数0.83)(图5a,b)。通过将分子进展的阈值限制在eVAF升高>0.01%(占样本的23%),以控制可能归因于技术伪影或生物学变异的小变化,特异性升至89%,PPV升至62%(C指数0.85)。在假阳性病例(7例患者的10个时间点)中,eVAF升高的中位数为0.20%(0.02-7.51),8个时间点被分类为疾病稳定。在中位随访58.9个月(18.6-65.0)后,7例患者中有3例经历了治疗失败,分子学进展的中位领先时间为9.8个月(4.6-13.9),持续治疗的患者中到末次随访的中位时间为9.7个月(8.3-19.2)。
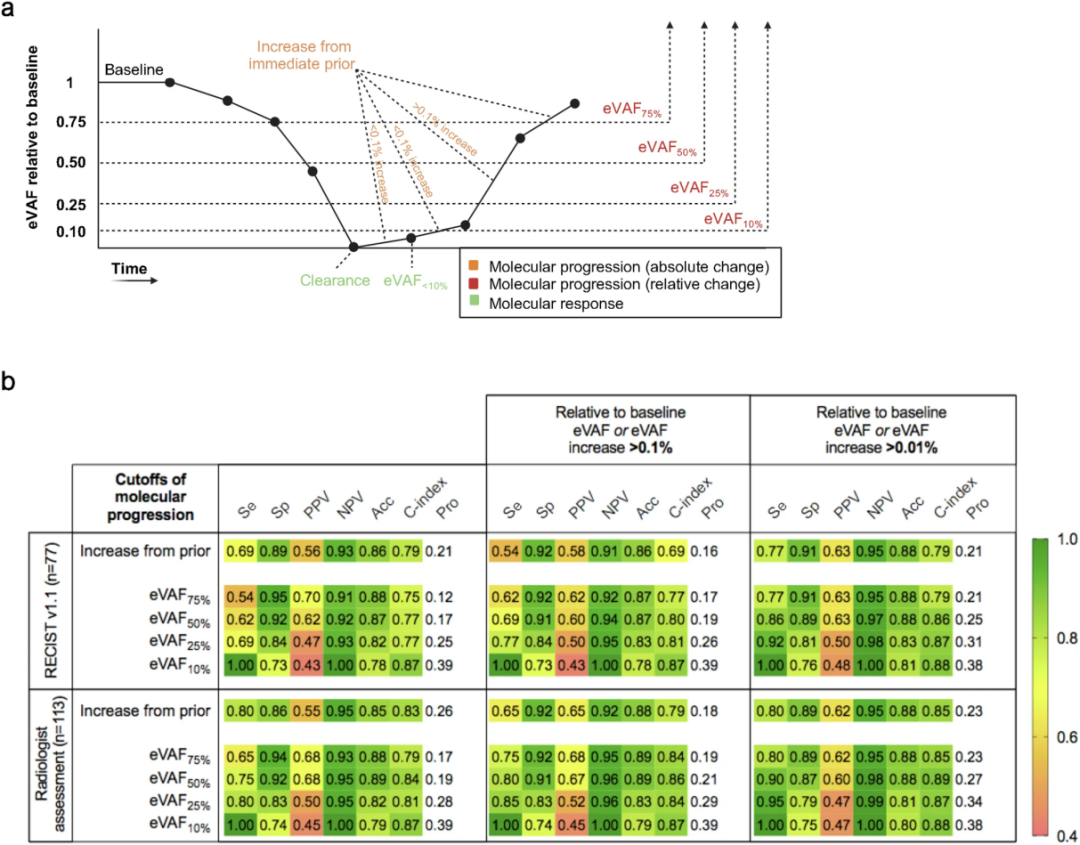
图5. ctDNA随时间变化的动态变化以及分子学进展的不同探索性定义[1]
为了进一步描述分子进展,深入研究了几种基于不同阈值(相对于eVAFBL的相对变化)的探索性定义的性能:包括无下降或下降小于25%(eVAF75%)、50%(eVAF50%)、75%(eVAF25%)和90%(eVAF10%)(图5a,b)。结果显示,eVAF75%(占样本12%)显示出检测影像疾病进展的最高准确性(88%),在可测量人群中(C指数0.75),PPV为70%,NPV为91%,敏感性为54%,特异性为95%。在包括可测量和不可测量患者的完整队列中,PPV为68%,NPV为93%,敏感性为65%,特异性为94%(C指数0.79)。当考虑在研究随访期间经历治疗失败的患者的所有时间点时,eVAF75%显示到治疗失败的领先时间为5.1个月(IQR 3.3-8.3),而eVAF10%(占样本39%)则显示出预测影像学同步进展的最大敏感性(100%),在可测量人群中特异性为73%,PPV为43%,NPV为100%(C指数0.87),在完整队列中敏感性为100%,特异性为74%,PPV为45%,NPV为100%(C指数0.87)。此外,eVAF10%显示到治疗失败的领先时间为7.3个月(IQR 3.9-12.4)。
研究还计算了结合绝对和相对截断值的性能特征(图5b)。将分子进展定义为相对于前一次样本的任何eVAF升高>0.01%和/或eVAF50%(占样本25%)时,在可测量人群中获得了最高的准确性(88%),敏感性为86%,特异性为89%,PPV为63%,NPV为97%(C指数0.86);在完整队列中,敏感性为90%,特异性为87%,PPV为60%,NPV为98%(C指数0.89)。然而,尽管结合绝对和相对变化提高了检测的敏感性和NPV,但反过来导致了更多的假阳性时间点。
►模拟基于血浆检测触发的影像学随访策略
更重要的是,可以从这些数据中制定各种ctDNA知情评估策略。一种合理的方法是对于达到分子缓解(即ctDNA清除或eVAF<10%)的患者实施以血浆检测为先的纵向监测,仅在出现分子进展时才进行影像学确认。具体而言,本队列中采用血液为先的监测可能避免了高达61.1%的用于评估疾病反应的随访影像学检查和/或相关临床访视。
再者,其他分子进展指标如eVAF75%,在分析队列中观察到占治疗中样本的13%(26/207),涉及18/43例(42%)患者,其PPV为70%且到治疗失败的领先时间相对较短(中位5.1个月,IQR 3.3-8.3),可触发紧急影像学检查以排除疾病进展。此外,研究还显示在治疗期间某个时间点出现eVAF10%,在分析队列中观察到占治疗中样本的34%(71/207),涉及31/43例(72%)患者具有更短的TTF和OS,中位到治疗失败的领先时间为7.3个月(IQR 3.9-12.4),可能为早期治疗变更和加强影像学随访提供机会。
小结
本研究证实,高灵敏度肿瘤知情ctDNA检测在接受标准ET联合CDK4/6i治疗的HR+/HER2- MBC患者中具有重要的临床监测价值。研究发现,深度分子缓解(定义为ctDNA清除或eVAF<10%)与显著延长的治疗获益及极低的近期影像学进展风险相关;相反,分子进展(结合绝对升高与相对动态变化)或应答不足(eVAF>10%)则可能有效预测治疗失败。凭借在治疗期间捕捉细微ctDNA变化的能力,这种高灵敏度方法在评估微小残留病灶方面可能优于非肿瘤知情策略。基于此,研究进一步提出“以血浆为先”的监测新模式:对于分子缓解患者,可考虑减少CT扫描频率以降低医疗负担;而对于分子进展患者,则应触发反射性影像学检查或指导治疗升级。
然而,解读研究结果时需考量以下局限性:首先,技术上依赖肿瘤组织进行panel设计限制了无可用组织患者的入组;其次,受COVID-19疫情影响,采样与影像检查间隔的不一致干扰了对分子进展提前量的精确评估;第三,较小的样本量限制了统计效能,尚需大规模前瞻性研究验证;第四,队列主要接受哌柏西利治疗,限制了结论对其他CDK4/6i的普适性;最后,ctDNA作为生物标志物尚不能完全替代影像学和临床访视所提供的关于患者疾病演变的综合信息。
总体而言,尽管受限于部分局限性,本研究数据为未来的适应性治疗策略及个性化临床试验设计提供了重要生物标志物研究证据。
参考文献
[1]Fuentes-Antrás J, et al. Personalized ctDNA monitoring in metastatic HR+/HER2- breast cancer patients during endocrine and CDK4/6 inhibitor therapy. NPJ Breast Cancer. 2025;11(1):74.
审批编号:CN-177657
有效期至:2026-07-26
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)