冠状动脉疾病(CAD)是全球
本文系统综述了血管内成像技术在

血管内成像突破了冠状动脉造影的局限,可清晰显示血管壁分层结构,精准表征斑块成分,为CCS的风险分层和治疗决策提供关键依据,其可将斑块分为富含脂质的斑块、纤维化斑块、钙化斑块三种表型,不同表型的临床意义与干预策略差异显著。
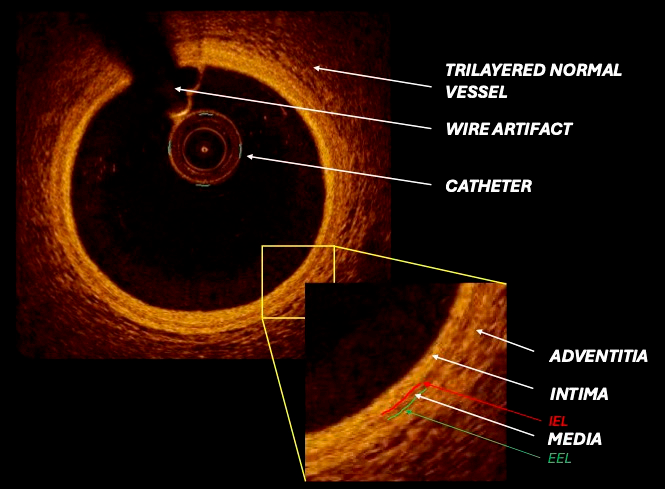
图1 OCT横截面图像
注:本图像为一支健康的冠状动脉,其血管壁结构正常,所有可识别的层和组件都清晰可见。IEL=内弹性层;EEL=外弹性层
•富含脂质的斑块(LRPs)是ACS的病理基础,与斑块易损性和破裂高度相关。在IVUS下可表现为低回声区域及低回声核心,可伴正向重塑;OCT 下为低信号强度区域,由于脂质含量高,信号衰减呈弥漫性(图3 )。当OCT测量的纤维帽厚度(FCT)<65 μm 时,即为薄纤维帽型
•纤维斑块代表稳定的动脉粥样硬化病变,破裂风险低,在IVUS下呈均匀高回声结构,在OCT下为边界清晰的
•钙化斑块是PCI治疗的重要挑战,通常会导致支架扩张不良,增加手术复杂性。在IVUS下,钙化斑块为高反射、明亮区域伴声学阴影,在OCT下为边界清晰、高强度信号区域,且钙化区后伴信号丢失。值得一提的是,钙化程度可影响手术策略:严重钙化病变需行旋磨术或血管内碎石术等策略,OCT引导的支架植入在钙化病变中扩张效果更优。
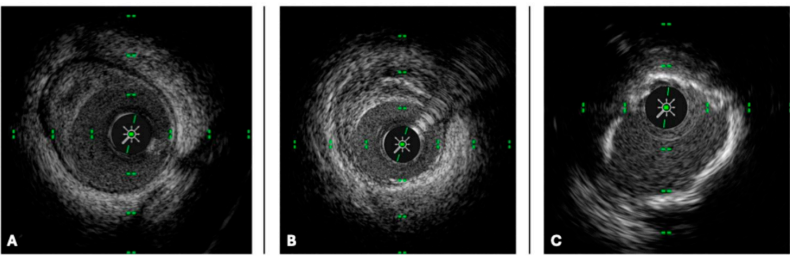
图2 冠状动脉的IVUS横断面图像
注:三种不同类型的动脉粥样硬化斑块:(A)脂质斑块,(B)纤维化斑块,(C)钙化斑块
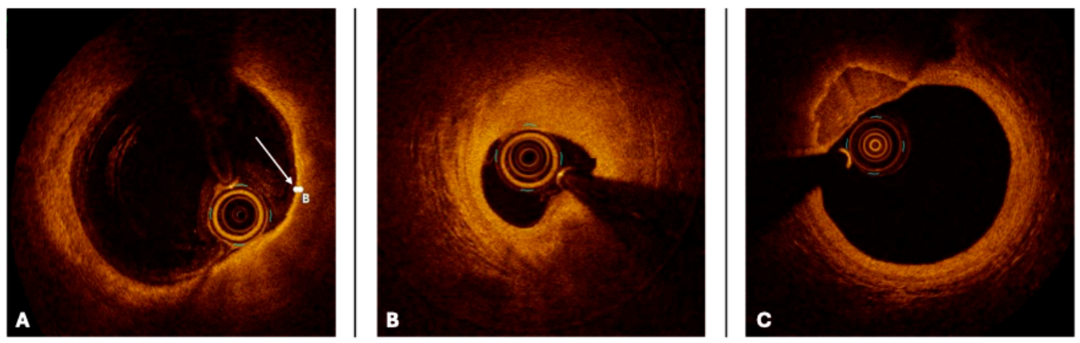
图3 冠状动脉的OCT横截面图像
注:三种不同类型的动脉粥样硬化斑块:(A)脂质斑块(箭头表示薄纤维帽),(B)纤维化斑块,(C)钙化斑块)
除结节状钙化外,OCT还可区分浅表与深层钙化非结节状钙沉积物。浅表钙沉积更有可能影响支架扩张和血管顺应性,而深层钙则主要影响整体斑块硬度。新验证的“3s 规则”(最小钙化厚度>0.3 mm、钙弧 360°、钙段长度>3 mm)能更精准预测严重钙化病变的支架膨胀不足,对手术策略制定具有重要指导价值。
此外,支架膨胀不足(膨胀率<70%)在钙化评分为≥2分的病变中的发生率显著更高,在衍生队列中的阳性预测值为62.5%,阴性预测值为94.4%。该修订评分优于原始的“5s 规则”(采用钙化厚度 0.5mm、长度5mm、弧度>180°作为阈值),尤其适用于严重钙化病变患者。

图4 修订的OCT衍生钙评分(“3s规则”),用于预测钙化病变中的支架膨胀不足
此外,血管内成像可通过临界值判断血流动力学显著狭窄,IVUS提示非左主干冠状动脉最小管腔面积(MLA)<4.0mm²、左主干段 < 6.0mm² 时,需考虑血运重建。
左主干解剖特殊、临床风险高,支架部署不佳易引发灾难性后果,IVUS可提供左主干病变的详细横断面成像,有助于进行精确的病变评估、斑块负荷定量和最佳支架尺寸,是指导PCI治疗的核心工具,最新ESC指南将血管内成像指导左主干病变支架植入列为 I 类推荐,以确保足够的扩张和贴壁,并最大限度地减少了手术并发症。
研究显示,与
LITRO研究提示,可将IVUS测量的MLA为6mm²作为预测缺血的临界值,MLA<6mm²的左主干病变患者不进行血运重建时,2年后的预后较差。随后,Park等确定了MLA为4.5 mm²,IVUS对应于血流储备分数(FFR)≤0.80。根据这些研究,欧洲经皮心血管介入协会(EAPCI)目前建议在MLA<4.5 mm²时对左主干病变进行血运重建,在MLA>6 mm²时不应进行左主干病变的血运重建,并考虑在MLA为4.5~6 mm²时进行功能评估。
除此之外,IVUS还提供了有关斑块形态的信息,以及在钙化斑块的情况下进行病变准备的必要性,从而降低支架贴壁不良、血栓形成等风险。
目前,关于OCT用于左主干病变干预的临床数据有限,因图像采集易受湍流、残留血液伪影影响,暂不推荐用于开口部疾病及左主干病变评估。正在进行的EMPERATRIZ试验,旨在探讨IVUS与OCT衍生的MLA在中度左主干病变中的一致性,或将为二者的临床应用提供更多证据。
血管内成像对病因不明的ACS 患者诊疗价值显著,可检测管腔不规则、斑块破裂及血栓形成等关键病变特征。
OCT是检测管腔内血栓最精准的技术,可依据光学衰减特性区分红色血栓(高反向散射、强信号衰减)与白色血栓(均匀、低衰减),同时能精准鉴别斑块破裂、斑块侵蚀、冠状动脉夹层等罪犯病变形态,为个体化抗栓治疗提供病理生理学依据。然而,高管腔血栓负荷可能掩盖斑块形态,增加OCT鉴别斑块破裂与侵蚀的难度。
IVUS可对ACS罪犯病变的斑块形态和血栓负荷进行标准化评估,将血栓分为急性血栓、亚急性血栓和机化血栓三种亚型,同时量化最大血栓弧、含血栓帧数量,也可通过内膜不连续性、纤维帽破裂等指标判断斑块破裂。
在非阻塞性冠状动脉疾病相关心肌梗死(MINOCA)诊断中,血管内成像可有效区分斑块诱导事件与冠状动脉
CTO
血管内成像在CTO-PCI中具有不可或缺的作用,有助于明确病变近端帽位置,尤其是当病变位置处于分叉水平时。
目前,IVUS是CTO-PCI期间的首选成像方式,可精准指导导丝定位与斑块穿透,从而确认导丝在远端真腔的位置,支持内膜下追踪后的再入操作,同时提供病变长度、斑块形态、血管直径等关键信息,优化支架选择与部署。相比单纯血管造影,IVUS可避免参考血管直径低估,减少支架尺寸选择不当,其引导的CTO-PCI可降低6个月靶病变血运重建(TLR)发生率,改善临床预后。
OCT因缺乏实时成像功能,在CTO-PCI中应用频率较低,但其分辨率优势显著,是支架植入后评估的理想工具,可精准检测血栓、组织脱垂、边缘夹层、支架贴壁不良等术后并发症。目前,OCT主要作为 CTO-PCI后血管愈合评估的研究工具(非临床实践)。此外,OCT 使用易受造影剂注射相关夹层扩展风险限制,顺行血流未恢复时图像质量可能不佳。
易损斑块的典型特征为大型脂质核心伴薄纤维帽,且炎症细胞浸润显著。斑块大小或由其决定的狭窄程度仅可提供斑块脆弱性的部分信息。大多数血栓相关ACS由仅决定轻至中度狭窄的斑块演变而来。
血管内成像技术是识别高危斑块的有效手段,其中OCT 凭借高分辨率优势成为核心工具,其可通过多项特征定义高危斑块:分析节段的MLA<3.5mm²、FCT<75 μm、脂质弧>180°,富含脂质核心,存在巨噬细胞簇。内膜新生血管、胆固醇晶体、钙化结节等也为高危标志物。CLIMA试验证实,FCT<75 µm,脂质弧>180° ,巨噬细胞浸润和MLA<3.5 mm²,这四项核心高危特征共存时,患者1年 MACE 发生率显著升高;COMBINE OCT-FFR研究也表明,即使FFR无缺血表现,
目前,高危斑块的概念已从经典TCFA扩展至易侵蚀斑块、高危钙化结节(eruptive calcified nodules),三者共同构成ACS血栓形成的主要病理基础,临床需整合斑块形态、成分、炎症及血流动力学因素进行综合评估。此外,多血管OCT试验发现,高危斑块常呈多灶性分布,非罪犯部位的易损斑块也是未来不良事件的重要诱因,正在进行的INTERCLIMA试验旨在探讨形态学引导的预防性 PCI对ACS后多支血管疾病患者的获益,或将推动 CAD 治疗从生理学驱动向易损性驱动转变。
值得关注的是,AI的发展实现了OCT对斑块形态与血流动力学的同步评估,可通过脂质纤维帽比值(LCR)、光学流量比值(OFR)等指标,整合形态学与功能学数据,其预测心血管事件的准确性优于单一的OCT易损性特征或生理学指标。
血管内成像可通过提供精准的血管特征、病变评估和手术指导,来进行PCI优化,从而显著减少不良临床事件风险,成为当代PCI的重要支撑。IVUS和OCT是临床核心技术,可有效改善病变准备、着陆段选择、支架尺寸确定及膨胀评估,来优化支架植入,同时可精准检测并管理贴壁不良、边缘夹层等急性并发症。
既往发表的多项研究证实,与血管造影引导的PCI相比,IVUS引导的PCI可实现更准确的血管测量、更大的最小支架面积(MSA),降低支架血栓形成率和TLF。早期OCT相关试验最初使用基于管腔的尺寸测量方法,最终获得的MSA小于IVUS 引导组。然而,包括ILUMIEN III和iSIGHT在内的后续研究表明,基于外部弹性层(EEL)的OCT尺寸测量方案时,其最终MSA 及支架扩张效果均不劣于IVUS引导。
目前,OCT指导PCI的随机数据仍然有限,但现实世界的注册研究表明,与血管造影指导相比,OCT引导的PCI与较低的住院和长期死亡率有关。目前正在进行的ILUMIEN IV试验有望进一步明确OCT引导的PCI是否能改善复杂CAD或糖尿病患者PCI后的管腔尺寸和临床结果。此外,OCTOBER试验表明,与血管造影引导的PCI相比,OCT引导的复杂分叉病变PCI在2年内导致的MACE发生率较低。
此外,研究人员报告称,血管内成像在远端左主干支架置入术中优于血管造影,但OCT和IVUS之间没有显著差异。
理想的支架着陆段应为无病变区域,在临床中应优选斑块负荷<50%(IVUS)或 EEL可见>180°(OCT)的病变远端/近端节段,且优先选择纤维斑块,避免脂质斑块、180°表层钙化区域,降低边缘夹层和远端栓塞风险。血管内成像与血管造影联合配准,可提高着陆段定位精度,减少地理性遗漏风险。
严重钙化病变需在支架植入前行旋磨术、血管内碎石术等病变准备;且精准的参考血管尺寸测量则是支架选择和后扩张的关键,可最大限度提升支架扩张效果和管腔增益。
血管内成像可有效指导支架直径和长度选择,病变覆盖不全是MACE和支架失效的重要预测因素,如支架再狭窄或血栓形成。在高斑块负荷或富含脂质的着陆段部署支架,会显著增加支架边缘再狭窄和术后心肌梗死风险。与血管造影相比,IVUS可精准显示血管真实直径,避免支架尺寸低估,减少支架膨胀不足——而支架膨胀不足是药物洗脱支架(DES)术后早期血栓和再狭窄的核心危险因素。
IVUS数据表明,在非左主干病变中,术后支架横截面积5.5 mm² 是识别不良结局高风险病变的最佳阈值。同样,DOCTORS试验显示,预测PCI后FFR>0.90 的最佳OCT衍生临界值为MSA>5.44 mm²。 此外,Soeda等的研究证实,MSA<5.0 mm²可独立预测1年期面向设备的复合终点(DoCE),包括心源性死亡、靶血管心肌梗死、TLR及支架血栓形成。Prati等的研究发现,MSA<4.5 mm² 与MACE相关。正如预期,左主干病变需要更高的MSA临界值,IVUS 评估时,远端左主干通常需>7 mm²,近端左主干需>8 mm²。
最佳支架扩张的目标包括:MSA大于远端参考管腔面积的100%;MSA大于平均近端和远端参考面积的80%~90%。对于长病变患者,在IVUS引导的PCI中,若MSA超过远端参考管腔面积(即100%以上),患者1年MACEs发生率极低,约为1.5%。据此,EAPCI专家共识提出,需结合绝对标准与相对扩张标准界定支架的理想扩张效果;其中绝对标准为:IVUS测量的MSA>5.5 mm²,或OCT测量的MSA>4.5 mm²,相对扩张标准为MSA/参考管腔面积>80%。
支架贴壁不良与膨胀不足可单独或共存发生,无膨胀不良的急性贴壁不良与短期、长期不良预后无关,且OCT检测贴壁不良的灵敏度是IVUS的2倍以上,其检出的39%~62% 急性贴壁不良中,约半数可在9个月随访时自行缓解。
第一代DES的晚期获得性贴壁不良(LASM)与晚期支架血栓相关,而新一代 DES 因支架支柱更薄、聚合物生物相容性更佳,这种关联显著减弱;但总贴壁不良体积≥7.0mm³的严重贴壁不良,仍与PCI术后严重安全事件相关。临床建议对轴向距离≥400μm 或纵向延伸≥1mm 的急性贴壁不良进行干预。

图5 支架贴壁不良的OCT成像
注:支架贴壁不良,可识别为明亮结构,拖尾阴影位于距离内膜表面一定距离处,不与血管壁接触
OCT可检测到血管造影无法识别的微小边缘夹层,其检出的PCI相关夹层中约 80%无临床意义,且1年随访时可自行愈合,但重度夹层(累及≥60°血管周长、长度≥3mm)是不良预后的预测因素,其中远端夹层宽度>200μm 时,MACE风险升高2.5倍。临床建议对重度边缘夹层行额外支架植入,同时血管内成像可在夹层场景中确认导丝真腔位置,避免夹层扩展和血管急性闭合。
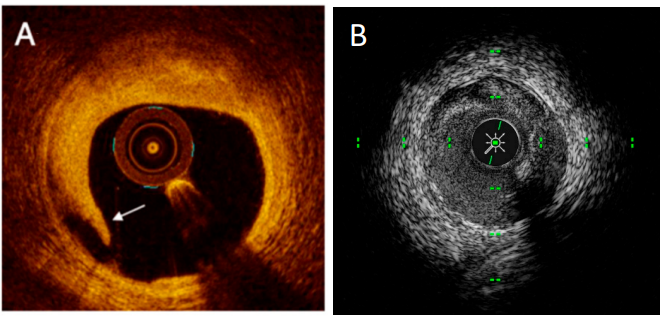
图6 (A)血管内夹层的OCT成像,(B)血管内夹层的IVUS成像
血管内成像技术在阐明支架失败的机制中发挥着关键作用,支架失败主要表现为支架内再狭窄(ISR)和支架血栓形成(ST)。ISR的发生率较高且临床处理难度较大。此外,明确再狭窄的病因是ISR诊疗流程中的关键环节(见表1),而冠状动脉内成像技术在这一诊断过程中具有核心作用。
表1 与ISR相关的临床、解剖和手术因素
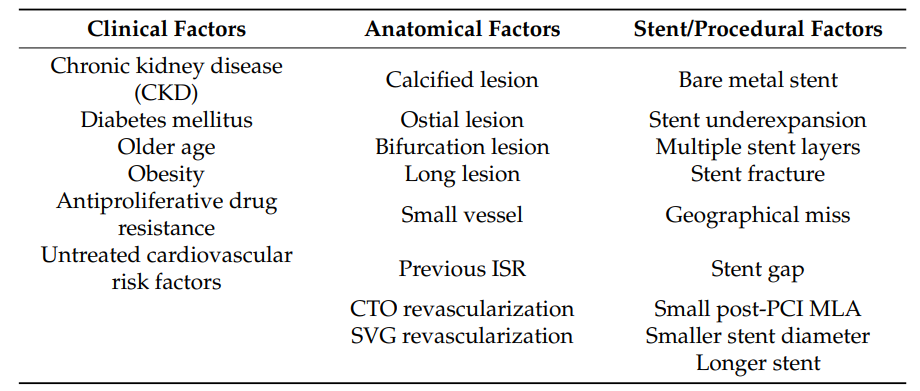
ISR的主要病因为支架膨胀不足(18%~40%),其余原因包括支架断裂(<5%)、新动脉粥样硬化、内膜增生,目前指南建议将血管内成像作为ISR评估的 IIa 类推荐。
按发病时间,ST可分为早期(<30天)、晚期(30~360 天)和极晚期(>360 天),主因贴壁不良、膨胀不足、边缘夹层、新发动脉粥样硬化、支架支柱未覆盖等。IVUS 和 OCT 均可明确支架失败的病因,而OCT在晚期支架失败中诊断能力更优,可精准评估支架支柱覆盖率、识别新动脉粥样硬化,IVUS 则在血栓负荷较高、OCT分辨率受限时更具优势。
表2 ISR的多模态冠状动脉成像特征 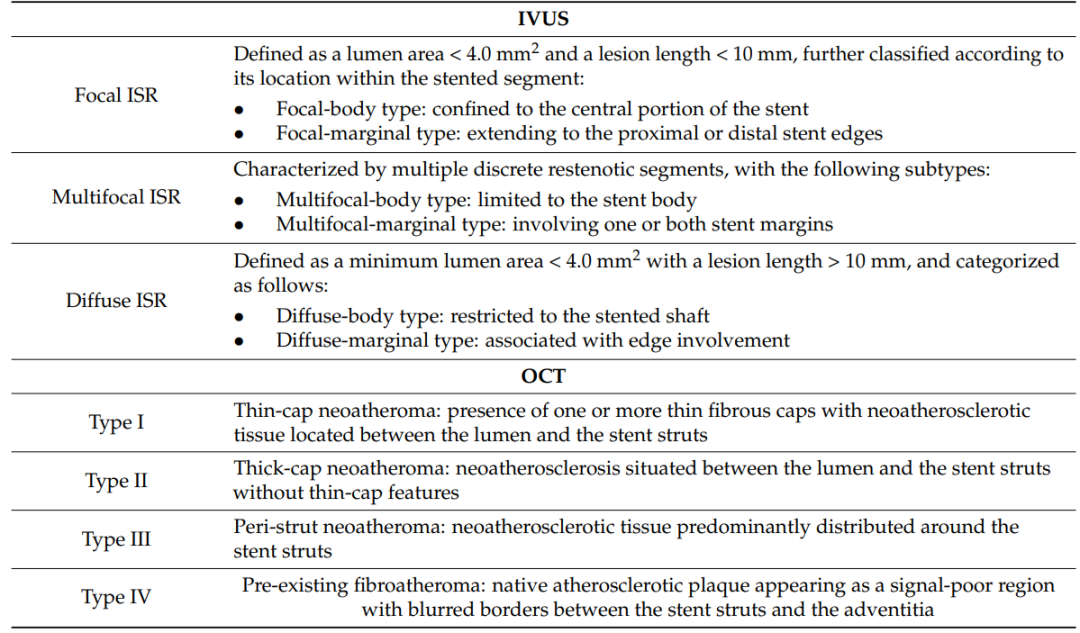
注:该表总结了通过两种主要的冠状动脉内成像方式(IVUS和OCT)评估的ISR的主要形态特征
根据OCT的特征表现,ISR可分为均匀型、异质型、衰减型、分层型四种模式:
•均匀型:呈均匀的高信号强度模式,反向散射极弱,典型对应富含平滑肌细胞的新生内膜组织;
•异质型:信号强度混杂不均,提示为富含蛋白多糖的新生内膜,或存在早期新生动脉粥样硬化改变;
•衰减型:表层呈高信号强度,伴明显反向散射,最符合富含脂质的新生动脉粥样硬化斑块特征;
•分层型:表层高信号带覆盖于深层低信号层之上,该表现常出现在支架支柱周围。
近年来,血管内成像的研究焦点从单纯形态学评估转向斑块生化特征与生物学行为分析,多模态成像与AI技术的结合,成为领域发展的核心方向,各类新型技术不断涌现,逐步弥补传统IVUS和OCT的局限性。
NIRS可定量检测血管壁脂质含量,与IVUS 融合后可实现斑块形态与脂质成分的同步评估,其可通过脂质核心负荷指数(LCBI)量化脂质负荷,临床常用LCBI 4 mm 评估介入目标区域,当 LCBI 4mm>400 时,冠状动脉事件发生率升高4倍。
NIRS-IVUS 可减少脂质定量的个体间差异,目前多项前瞻性试验正验证LCBI或LCBI 4 mm作为冠状动脉事件预测因子的临床价值。
NIRF利用外源性荧光造影剂靶向结合斑块特异性分子,实现斑块生化特征检测,常用造影剂
NIRAF无需外源性造影剂,可检测组织内源性分子的荧光信号,首次人体研究已证实NIRAF-OCT系统安全可行,其信号强度区域与OCT检测的高危斑块高度匹配,可精准识别坏死核心。
IVPA是一种新兴的光谱技术,旨在表征和区分体内血管组织成分。该技术通过向血管壁发射短激光波,接收由组织热膨胀产生的光声波实现成像,并借助对血管壁回波信号的分析,判断斑块的组织构成。
与NIRS技术相同,IVPA利用不同组织的光吸收光谱差异检测斑块成分,但其具备更深的组织穿透深度和更高的成像分辨率。该技术可结合内源性物质或外源性造影剂使用,实现特定分子靶点的靶向检测。
鉴于该技术现阶段的成像速度较慢,且成像探头体积偏大,暂无法开展人体试验。
FLIm与NIRAF的原理相似,均利用组织的自荧光特性鉴别血管壁的组织构成。当斑块组织受到紫外线照射时,可通过检测巨噬细胞、低密度脂蛋白(LDL)、胶原蛋白等斑块成分反射的自荧光寿命,实现对这些成分的识别。血管壁上巨噬细胞、泡沫细胞或胶原蛋白的分布状态会影响自荧光寿命,借此可识别出高危斑块。
FLIm无需使用外源性造影剂,但由于血细胞对紫外线的高吸收性,成像前需进行血管内血液清除处理。此外,紫外线的组织穿透深度有限,仅约200 µm,这也决定了该技术仅能获取动脉血管壁表层的相关信息。
目前,研究人员已研发出已研发出 FLIm-OCT和 FLIm-IVUS 一体化导管;前者已完成动物试验,首次在体人体研究也正在规划中;后者已完成离体人体冠状动脉验证试验。
AI的出现开创了血管内成像精准化新时代,通过自动化图像分析、实时决策支持,克服了传统技术操作复杂、学习曲线陡峭的局限性。
主流AI-IVI系统各具优势:AVVIGO+IVUS的自动病变评估可实现管腔精准分割,与专家球囊尺寸匹配度超92%;Ultreon 2.0 OCT 可自动量化钙化斑块、识别 EEL,提升新手操作的准确性;Gentuity HF-OCT 可在血液清除不全等次优条件下实现实时管腔分割和支架评估;SpectraVAVE HyperVue 整合 DeepOCT 与 NIRS,可自动识别高危斑块,简化手术流程。
当前AI-IVI系统仍存在一定的局限性:对支架夹层、血栓等定性特征检测能力不足,易受图像伪影影响,且训练数据集多基于专家标记而非组织病理学金标准,通用性有限。未来其发展方向为整合计算模拟、扩展现实、血流动力学及基因组学数据,实现高度个性化的 PCI策略制定。
过去数十年间,血管内成像技术极大提升了临床对冠状动脉疾病的认知,以IVUS和OCT为核心的技术可实现斑块形态、病变严重程度及PCI术后血管反应的高分辨率可视化,成为介入手术指导和易损斑块识别的不可或缺的工具,其在临床常规应用中可有效改善患者预后,减少支架血栓、再狭窄等并发症。
目前,该技术的临床推广仍面临成本较高、专业操作人员不足、工作流程繁琐等挑战,同时新型成像技术的临床转化、AI的深度应用仍需进一步研究。
未来,冠状动脉血管内成像的发展核心为多模态技术的整合,在提升诊断精度的同时最大限度减少侵入性;同时需将技术创新纳入临床指南和现实世界实践,推动AI与多学科数据的融合,实现冠状动脉疾病的精准化、个体化诊疗,进一步改善患者长期心血管预后。
参考文献
Iuvara G, Franzino M, Carciotto G, De Ferrari T, Lo Giudice S, Pallante F, Giannino F, Ajello M, Tomasi S, Sciortino L, Monciino G, Licandri W, Caminiti R, Virga V, Costa F, Micari A, Vizzari G.Coronary Intravascular Imaging: Comprehensive Review of
Techniques, Applications, and Future Directions.Medicina (Kaunas). 2025 Nov 12;61(11):2019. doi: 10.3390/medicina61112019.
郑刚 教授
•现任泰达国际心血管病医院特聘专家
•中国高血压联盟理事,中国心力衰竭学会委员,中国老年医学会高血压分会天津工作组副组长、中国医疗保健国际交流促进会高血压分会委员。天津医学会心血管病专业委员会委员,天津医学会老年病专业委员会常委。天津市医师协会高血压专业委员会常委,天津市医师协会老年病专业委员会委员,天津市医师协会心力衰竭专业委员,天津市医师协会心血管内科医师分会双心专业委员会委员。天津市心脏学会理事、天津市心律学会第一届委员会委员,天津市房颤中心联盟常委。天津市医药学专家协会第一届心血管专业委员会委员,天津市药理学会临床心血管药理专业委员会常委。天津市中西医结合学会心血管疾病专业委员会常委
•《中华老年心脑血管病杂志》编委,《中华临床 医师杂志》(电子版)特邀审稿专家,《中华诊断学电子杂志》审稿专家,《华夏医学》杂志副主编,《中国心血管杂志》常务编委,《中国心血管病研究》杂志第四届编委,《世界临床药物》杂志编委、《医学综述》杂志会编委、《中国医药导报》杂志编委、《中国现代医生》杂志编委、《心血管外科杂志(电子版)》审稿专家
•本人在专业期刊和心血管网发表文章948篇其中第一作者759篇,参加著书11部
作者:郑刚教授
审校&排版:GXM
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
