目前已知,抑郁症的认知、情感、精神运动及植物神经症状反映了多个皮层-边缘区域的功能障碍。例如,负责执行功能的背外侧前额叶皮层(dlPFC)、参与决策的膝下前扣带回皮层(sgACC)及调节冲动控制的眶额皮层(OFC),在抑郁症患者中均表现出体积缩小和连接性降低。此外,海马体、杏仁核、伏隔核(NAc)以及前岛叶(aINS)等关键脑区的活动异常共同构建了抑郁症复杂的病理图谱。

一项2月25日在线发表于JAMA Psychiatry(影响因子 17.1)的系统综述中,作者力求整合并重新分析来自抑郁症患者的大脑和血液批量组学及单核组学数据,以确定其是否存在重叠的大脑与血液学紊乱通路,从而为生物标志物的发现和治疗靶点的开发提供依据。
作者对PubMed、Embase和Web of Science进行了全面的检索,纳入了使用人类生物样本、报告抑郁症患者组与对照组差异表达基因(DEGs)或差异甲基化基因(DMGs)、采用RNA测序或甲基化谱分析的高质量研究,并将这些大脑和血液中的分子信号与GWAS关联基因变异进行了交叉验证。
为确保数据的可靠性,研究团队开发了一套质量评估工具,考量指标包括是否共享基因列表、统计分析的严谨性(如协变量的使用、统计阈值、多重检验校正方法等)、样本量大小以及是否按性别报告结果等。随后,作者利用Python脚本查询了Ensembl、UniProt、GeneCards和NCBI等数据库,对提取出的22,897个基因进行了功能注释。最后,通过将这些基因列表与GWAS目录进行整合,作者识别出了那些既存在表达差异又携带遗传风险位点的核心致病因子。
除重及评估质量后,作者共纳入了54篇符合标准的研究。这些研究发表于2014年至2025年,共涉及17,065名参与者,女性占比48.5%。30项研究仅针对大脑组织,20项研究仅针对血液,4项研究同时涵盖了大脑和血液。值得注意的是,现有研究主要源自美国、加拿大和英国,在人群多样性方面存在局限性,报告祖源的研究样本中约80%为白人或欧洲裔。
★ 批量转录组学
分析21项大脑转录组研究后发现,在dlPFC、sgACC、OFC和aINS中,控制代谢、翻译和线粒体功能的通路呈现出显著的上调。具体而言,涉及细胞呼吸、有氧呼吸、线粒体基因表达以及电子传递链的基因表达增加,提示这些脑区在疾病状态下可能处于高代谢应激状态。
与此形成对比的是,涉及神经系统发育、细胞间粘附和轴突引导的通路在上述脑区以及伏隔核中表现出显著下调。这种发育与连接通路的萎缩在不同脑区具有特异性:在腹侧海马下托(vSUB),涉及突触组织、可塑性及学习与记忆的通路严重下调;而在前岛叶,可观察到T细胞和白细胞分化通路的下调。此外,伏隔核表现出独特的上调模式,主要集中在神经胶质细胞生成、神经发生调节和胶质细胞分化上。
以上数据提示,抑郁症患者的大脑在试图进行结构重组的同时,其基础连接功能却在持续恶化。
针对全血,研究识别出472个差异表达基因。基因本体论分析显示,这些基因在抑郁症患者的外周血中同样表现出翻译、核糖体生物合成、细胞呼吸、氧化磷酸化和线粒体功能通路的显著上调。这种在大脑和血液中高度一致的代谢特征提升了「将血液作为大脑代谢状态窗口」的可信度。通过蛋白质互作网络分析,研究进一步锁定了核糖体小亚基组件(如RPL35和RPS11)及与线粒体ATP合成相关的核心枢纽基因(如ATP5F1E和ATP5PO)。
★ 细胞特异性转录组学
单核转录组学数据揭示了更为精细的病理景观。在dlPFC中,兴奋性神经元表现出膜电位调节、突触组装和
与此同时,非神经元细胞则展现出不同的角色。少突胶质细胞表现出线粒体ATP合成、电子传递和蛋白质转运通路的显著上调;星形胶质细胞则在树突形态发生和神经元投影发育通路中表现出上调。这些发现表明,抑郁症中观察到的批量组织代谢水平升高可能主要受少突胶质细胞而非神经元的驱动。此外,小胶质细胞中的核心枢纽基因涉及促炎因子和凋亡调节,进一步证实了免疫激活在脑内的存在。
在不同类型的血细胞中,白细胞表现出RNA剪接、炎症和核转运通路的显著上调。单核细胞中的枢纽基因则主要集中在转录调节和DNA修复上。这些细胞特异性的信号为理解抑郁症的外周免疫紊乱提供了分子证据。
★ 全基因组甲基化分析
甲基化研究在大脑中识别出4,207个DMGs,在血液中识别出8,193个。在大脑中,低甲基化(通常与基因激活相关)基因涉及信号转导、细胞分化和应激反应;高甲基化基因则富集在细胞发育、神经元分化和突触小泡转运通路。
血液中的甲基化模式与大脑呈现出显著的相似性。血低甲基化基因同样涉及轴突生成、细胞分化和神经系统发育。这种跨组织的表观遗传烙印不仅记录了环境压力对基因组的长期影响,也为开发基于甲基化的血液诊断工具提供了科学基础。
★ 血液与大脑共同的转录和表观遗传特征
这是本综述的重要发现之一:大脑和血液数据集共享了744个同向失调的DEGs(716个上调,28个下调),以及544个方向一致的DMGs。
在大脑与血液中共同上调的716个基因主要控制细胞凋亡(如FAM32A和BCLAF1)、自噬(如DRAM1和BECN1)和免疫反应,而共同下调的基因则集中在形态发生和发育(如PTCH1和NPTX1)。此外,共有410个基因在脑与血液中均表现出低甲基化,涉及细胞分裂、转录调节和G蛋白耦联受体信号传导。这些在两种组织中同步震荡的分子信号,正是寻找血液生物标志物的重要突破口 。
★ 转录和表观遗传特征与GWAS遗传变异的整合
通过与GWAS数据的交叉对比,研究发现132个在大脑或血液中失调的差异表达基因位于GWAS风险基因座内。其中,43个基因在脑和血液中表现出方向一致的异常表达,包括调节神经发育的TCF4和MDGA1,以及调节凋亡的CASP8AP2。在甲基化层面,有158个差异甲基化基因与GWAS命中位点重合,涉及神经发育基因RTN1、NRG1以及凋亡基因BLCAP。这些基因不仅携带先天遗传风险,且在疾病状态下确实发生了表达或修饰改变,具有很高的临床转化价值。
综合所有组学证据,抑郁症的病理生理机制可归纳为五个相互交织的通路(图1):
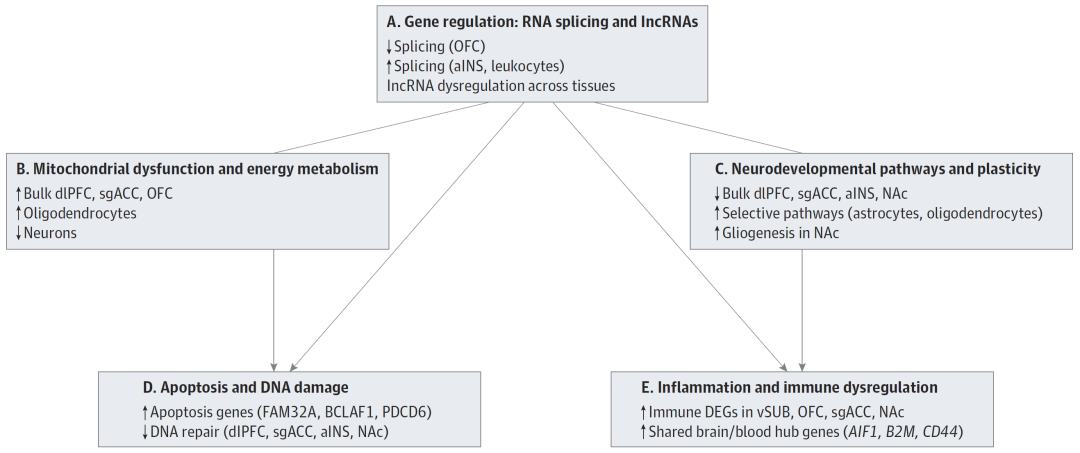
图1 造成抑郁症脑细胞损害的分子通路
1. 线粒体功能与能量代谢失衡
在dlPFC、sgACC和OFC等关键脑区,线粒体功能的整体上调可能反映了代偿性的氧化应激,尤其是在支持轴突功能的少突胶质细胞中。然而,神经元内部的能量缺口可能直接导致了执行功能和决策能力的受损。鉴于这些代谢变化在血液中同样可测定,它们具有成为分层生物标志物的巨大潜力。
2. 神经发育通路与可塑性受损
轴突生成和投射发育基因的广泛下调,提示了抑郁症患者大脑结构连接性的损伤。特定区域(如伏隔核)胶质细胞生成的异常增加则反映了脑区特异性的病理性重塑。
3. 细胞凋亡与DNA损伤
脑与血中凋亡基因的一致性上调,以及凋亡枢纽基因在大脑多个关键区域的富集,为抑郁症中观察到的脑皮层和海马体积缩小提供了分子层面的解释。DNA修复功能的下降进一步加剧了细胞的脆弱性。
4. 炎症与免疫失调
本研究确认,中枢与外周免疫功能障碍是抑郁症的核心特征。无论是在脑组织、血液细胞还是共享的枢纽基因中,免疫信号的激活都清晰可见。
5. RNA剪接与转录控制
RNA剪接通路的失调被视为抑郁症「分子故障」的起点。剪接异常会导致线粒体蛋白、凋亡调节因子和免疫介导因子的功能异构,从而引发连锁的细胞损伤。
本项研究存在一些局限性,如人群祖源的单一性;未来的研究必须纳入更多样化的种族样本,以增强结论的外推性。其次,横断面研究设计无法确定分子改变是疾病的起因还是结果。
空间转录组学等新技术将使我们能够在解剖景观中精准定位基因表达。整合蛋白质组学、大规模遗传变异以及纵向临床随访数据将成为实现精神医学精准诊疗的关键。
综上,抑郁症涉及横跨脑与血的诸多生物学过程的协同紊乱。通过识别这些在大脑和血液中共同存在的分子特征,我们正迈向一个超越症状分类的新时代——利用生物学信息驱动的精准医学,为每一位抑郁症患者提供量身定制的诊断和治疗方案。这不仅是医学研究的突破,更是改善全球精神健康的可持续路径。
2025-07-11

文献索引:Zallar LJ, Dupont MB. Brain and Blood Biomarkers of Major Depressive Disorder: A Systematic Review. JAMA Psychiatry. 2026 Feb 25. doi: 10.1001/jamapsychiatry.2025.4613. Epub ahead of print. PMID: 41739484.
点击「阅读原文」可查看及检索历史文章。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)