文献来源:中华炎性肠病杂志,2026年第10卷第1期
作者:中华医学会消化病学分会
通信作者:朱维铭,南京中医药大学附属医院肛肠科,炎症性肠病诊疗中心;
引用本文:中华医学会消化病学分会炎症性肠病学组,中华医学会外科学分会结直肠外科学组,中华医学会外科学分会胃肠外科学组. 中国




【摘要】 溃疡性结肠炎(UC)患者如果出现药物治疗无效、激素依赖、严重并发症或有癌变风险等情况,需要接受手术治疗。随着治疗目标从单纯控制症状转向达标治疗与改善长期预后,临床上对外科决策的科学性与围手术期管理的规范性也提出了更高要求。本指南由中华医学会消化病学分会炎症性肠病学组牵头,联合中华医学会外科学分会结直肠外科学组和胃肠外科学组专家共同制定,在2020年《炎症性肠病外科治疗专家共识》基础上进行循证更新,融合了最新国际共识、国内研究进展与临床实践需求,旨在为我国UC外科治疗提供标准化、科学化、实用性的临床指导。
【关键词】 溃疡性结肠炎; 外科治疗; 指南;GRADE分级; 德尔菲法
近年来,溃疡性结肠炎(ulcerative colitis,UC)的治疗目标已从单纯控制症状和挽救生命转向达标治疗、诱导深度缓解、改善生活质量及避免疾病致残。尽管生物制剂和小分子靶向制剂等新型药物显著改善了UC的治疗结局,但随着病程延长和UC相关癌变发病率的增加,以及药物治疗存在局限性等原因,仍有相当数量的患者需要接受外科干预[1]。在达标治疗、加速康复外科(enhanced recovery after surgery,ERAS)、损伤控制外科等理念和微创外科技术的引领下,UC手术不断进步,手术方式日益规范,疗效更加满意。全结肠直肠切除(total proctocolectomy,TPC)加回肠储袋肛管吻合(ileal pouch anal anastomosis,IPAA)已成为公认的首选术式。然而,随着IPAA手术的广泛应用,手术相关并发症和储袋功能障碍等问题逐渐成为临床关注的焦点[2]。妥善解决这些问题才能最大程度提高 UC 患者生活质量,改善患者远期结局。
为进一步规范我国UC外科诊疗实践,提高外科治疗决策的科学性与规范化水平,中华医学会消化病学分会炎症性肠病学组联合相关学科专家,基于《中国溃疡性结肠炎诊治指南(2023年·西安)》[3]和最新循证医学证据,对2020年我国首部《炎症性肠病外科治疗专家共识》[4]的 UC 部分进行全面修订,旨在提升我国 UC 外科治疗的整体水平,推动外科诊疗的规范化,确保患者获得同质化高质量的医疗服务。
一、方法
1.指南制定方法:本指南参考循证医学指南制定原则,遵循中华医学会《中国制订/修订临床诊疗指南的指导原则(2022版)》确立的规范化流程与方法论框架、指南研究与评价工具(AGREE Ⅱ)的科学评估标准及卫生保健实践指南报告条目(RIGHT)的规范化报告要求。制定过程中参考了推荐分级的评估、制定与评价(grading of recommendations,assessment,development and evaluation,GRADE)的 理 念 和原则。
2.指南使用者和目标人群:本指南的目标用户是从事炎症性肠病(inflammatory bowel disease,IBD)诊疗工作的临床医务人员,推荐意见的目标适用人群为中国UC患者。
3.指南专家组构成:指南专家组包括临床专家组、方法学组和秘书组。临床专家组由中华医学会消化病学分会炎症性肠病学组、中华医学会外科学分会结直肠外科学组、中华医学会外科学分会胃肠外科学组具有多年IBD内外科治疗经验和学术影响力的医师组成。方法学组由宁波诺丁汉大学GRADE中心专家组成。秘书组由中华医学会消化病学分会炎症性肠病学组外科俱乐部部分成员组成。本指南已在 国 际 实 践 指 南 注 册 与 透 明 化 平 台(Practice Guideline REgistration for TransPAREncy,PREPARE)注 册(注 册 号 :PREPARE⁃2024CN1179)。
4.利益冲突:指南专家组成员的利益冲突管理依据世界卫生组织(WHO)以及国际指南联盟(GIN)对利益冲突管理的指导原则执行。指南专家组向中华医学会报告了个人潜在的利益冲突(包含财务和专业相关的利益冲突)情况,所有成员均无利益冲突。
5. 临床问题的遴选和确定:方法学组与临床专家组对UC外科治疗相关的临床问题通过4次线下专家会议进行探讨。经过对最初临床问题的多轮修改和讨论,最终确定了在本指南中要明确的19个临床问题。
6.证据检索、分级和推荐意见形成:指南专家组在万方、维普、中国知网、PubMed、Embase、Cochrane Library数据库进行了证据检索。文献筛选由两名指南专家组成员依据预先制定的纳入或排除标准进行独立筛查,先根据题目和摘要进行初步筛选,进一步根据全文内容,最终确定纳入文献,并提取研究信息。对于存在争议的文献,通过讨论或咨询第三方最终达成共识。文献纳入标准:(1)研究对象:UC患者,年龄不限定;(2)研究类型:随机对照研究或观察性研究、荟萃分析、系统评价和先前的指南。文献排除标准:(1)重复发表的研究;(2)非中英文语言的研究;(3)综述类无具体数据的研究。
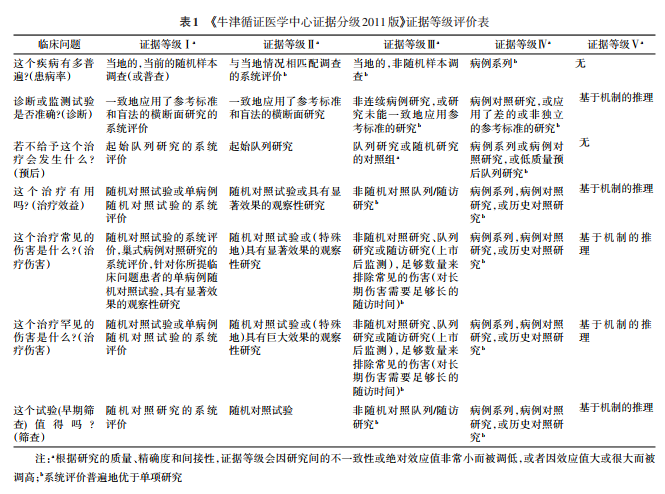
针对纳入研究,采用《牛津循证医学中心证据分级2011版》(OCEBM 2011 Levels of Evidence)来具体执行证据质量评价和分级(表1)[5],综合考虑纳入研究的质量、研究间不一致性、精确度、间接性等,对证据质量评级进行调整。其中Ⅰ级证据为高质量证据,Ⅱ级和Ⅲ级证据为中等质量证据,Ⅳ级和Ⅴ级证据为低质量证据。在形成推荐意见时参考了GRADE 证据到决策(evidence to decision)的理念,结合证据质量将推荐强度分为强和弱两个等级(表2)。强推荐代表指南临床专家组对该推荐意见为最佳临床实践有很高的信心,建议目标用户均采纳该推荐意见。弱推荐代表指南临床专家组对该推荐意见的信心有限,应有条件地应用于目标群体,强调医患共同决策。专家组对研究证据公开讨论后,采用德尔菲问卷调研法结合专家会议法来达成对推荐意见的共识。本指南中的推荐意见在专家组投票后,共识率达到80%,视为达成共识。

7.指南传播和实施:指南的有效传播与落地实施依赖于系统化、多维度的协同努力。本指南发布后,指南工作组将主要通过以下方式对指南进行传播和推广:(1)通过权威医学期刊发表指南全文及摘要,在国家级、区域性学术会议上进行专题解读与推广;(2)利用专业学会网站、医学数据库、移动医疗APP、社交媒体精准推送指南核心推荐意见与解读材料;(3)由医院或科室组织指南培训会,确保临床医师及其他相关专业群体充分了解并正确应用该指南。
二、手术指征
推荐意见 1:在急性重症溃疡性结肠炎中,对于挽救治疗失败的患者,推荐及时手术治疗;个别病情凶险的患者,建议不经过挽救治疗而直接手术;继发中毒性巨结肠患者,推荐尽早进行手术干预。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推 荐 理 由 :急 性 重 症 溃 疡 性 结 肠 炎(acute severe ulcerative colitis,ASUC)病情重、进展快,处理不当或不及时可能危及患者生命。若挽救治疗后病情无明显改善,强烈建议手术治疗;部分进展迅速、病情凶险的ASUC 不一定要经过挽救治疗,可以直接手术,以免耽误宝贵的手术时机,手术时机越延迟,ASUC 死亡率越高。ASUC 伴发中毒性巨结肠是外科急症,尽早施行结肠切除可显著降低并发症风险和死亡率。
ASUC的诊断、评估和药物治疗见《中国溃疡性结肠炎诊治指南(2023年·西安)》推荐意见第35~45条,ASUC和中毒性巨结肠的手术时机见推荐意见第46条[3]。中毒性巨结肠是ASUC罕见但危重的并发症,发生率为1%~5%,住院死亡率达7.9%[6]。研究表明,约30% ~ 40%的ASUC患者最终需要接受结肠切除手术,其中约10% ~ 20%的患者首次住院即需要紧急实施手术[7⁃9]。荟萃分析显示,采用
外科医师在ASUC患者入院早期即应参与治疗决策,以便准确把握手术时机。前瞻性研究对 80 例接受手术治疗的 ASUC 患者进行分析发现,从入院至实施手术的间隔时间是预测术后发生重大并发症的显著相关因素(5 d比 8 d,P = 0.036);多变量分析显示,住院期间药物治疗的持续时间与术后并发症增加呈正相关,是危险因素(OR = 1.12,95%CI:1.00~1.24,P = 0.044)[11]。基于美国外科医师学会国家外科质量改进计划(NSQIP)数据库的回顾性队列研究显示,在508例接受全结肠切除术的ASUC患者中,早期手术组[1.0(1.0,2.0)d]30 d死亡率显著低于延迟手术组[6.0(4.0,9.0)d](4.9% 比 20.3%,P < 0.001),术后并发症发生率亦呈下降趋势,但无统计学意义(64.5% 比 72.0%,P = 0.052);多因素回归分析显示,早期手术可将死亡风险降低 82%(P<0.001),并发症风险降低 35%(P = 0.034)[12]。因此,对于病情进展迅速或药物治疗后没有明显改善的ASUC患者,强烈建议及时手术,以避免紧急手术相关的并发症[3]。
推荐意见 2:药物治疗无效或产生难以耐受的不良反应以及激素依赖的难治性UC患者,推荐择期手术。(证据等级:Ⅲ~Ⅳ,推荐强度:弱推荐)
推荐理由:即使经过充分药物治疗,病情仍未得到满意控制或者产生难以耐受的药物相关不良反应以及
难治性UC的定义:(1)对生物制剂、激素或小分子药物诱导缓解无效;(2)依赖激素维持缓解[13]。难治性UC是最常见的手术指征之一,手术原因包括疾病持续进展、药物疗效或依从性差、病情影响生活质量、希望摆脱持续的医疗干预(如频繁住院、反复
对于充分的药物与营养治疗后仍存在生长
推荐意见3:慢性复发性UC合并结直肠狭窄时,推荐手术治疗。(证据等级:Ⅲ~Ⅳ,推荐强度:弱推荐)
推荐理由:慢性复发性UC合并的结直肠狭窄不但病变本身癌变风险显著增加,而且妨碍内镜对狭窄近端进行监测和活检,推荐尽早手术治疗。
一项纳入439例UC患者的多中心回顾性研究显示,发病 年 龄 ≥ 40 岁(P = 0.008)和 长 期 使 用 激 素(HR = 4.1,95%CI:1.1~16.1)是结肠狭窄的独立危险因素。中位随访时间9.6年,16例(3.6%)发生肠狭窄,6例检出异型增生,其中5例发展为
推荐意见4:UC患者结直肠癌发病风险显著增加,对确诊UC相关癌变或高级别异型增生的患者,推荐遵循肿瘤学外科原则实施全结肠直肠切除术。(证据等级:Ⅱ~Ⅳ,推荐强度:强推荐)
推荐理由:UC 患者发生结直肠癌(colorectal cancer,CRC)的风险显著高于普通人群,主要危险因素包括病程长、炎症持续活动、年轻发病、广泛结肠病变、合并
一项纳入 116 项研究的荟萃分析显示,UC 患者总体CRC患病率为3.7%(95%CI:3.2%~4.2%),累积发生风险分别为10年2%、20年8%、30年18%[25]。针对亚洲人群的系统评价亦提示,UC患者结直肠癌风险随病程延长而增加,总体患病率为 0.85%(95%CI:0.65%~1.04%),累积发病风险10 年时仅为0.02%,20年上升为4.81%,30年高达13.91%,按地区或研究时期进行的亚组分析差异均无统计学意义[26]。UC患者的CRC筛查与监测策略可参考《中国溃疡性结肠炎诊治指南(2023年·西安)》推荐意见第54~55条[3]。
UC相关癌变和高级别异型增生的同时性癌(18%)和异时性癌(17%)发病率远高于散发性 CRC(2.5%)[27⁃28]。前瞻性研究纳入1 225例UC患者,结果显示,初次
三、围手术期处理
推荐意见5:UC患者手术后静脉血栓栓塞症风险显著增加。如无明确禁忌证,推荐实施预防性抗凝治疗,高风险患者建议延续至术后4周。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:UC 患者术后发生静脉血栓栓塞症(venous thromboembolism,VTE)风险显著升高,重症 UC 患者更为显著。术后VTE主要与手术方式、手术时长、急诊手术及术后凝血状态等因素密切相关。建议术前评估患者的血栓形成与出血风险,权衡抗凝治疗的利弊,合理调整抗凝治疗方案。术后依据患者出血与VTE风险及时恢复抗凝治疗,VTE高风险患者建议延长至术后4周。
来自美国NIS数据库3 430例接受结肠切除的UC 患者研究结果表明,术后 VTE 发生率显著高于未行手术患者(4.68% 比1.24%,P < 0.000 1),手术是VTE的独立危险因素(OR = 2.44,95%CI:1.80~3.31)[31]。来自日本的多中心研究显示,UC患者TPC术后VTE发生率为17.1%(24/140),IPAA手术(OR = 17.12,95%CI:1.675~433.7,P = 0.015)、手术时长> 4 h(OR = 28.84,95%CI:1.23~1260,P = 0.036)以及术后第 1 天 D⁃二聚体水平> 5.3 µg/mL(OR = 3.69,95%CI:1.02~14.78,P = 0.045)为 VTE 的独立预测因素[32]。多中心前瞻性研究显示,IBD 结肠次全切除术(subtotal colectomy,STC)和TPC 是术后VTE 的独立危险因素,术后VTE 发生率均超过 3%(最高达 6.3%),其中 CD 与 UC 差异无统计学意义,开腹手术与
VTE的预防措施包括机械预防和药物预防。预防性使用抗凝药物是否会增加活动期UC患者的肠道出血风险,目前仍然存在争议[34⁃35]。如果术后出血风险低,术前口服的抗凝药(如
IBD 术后 38%VTE 事件发生在出院后[33],UC 患者出院后发生VTE的风险比CD更高[37⁃38]。基于美国Optum数据库的回顾性分析显示,约36%VTE事件发生在出院30 d之后,但仅有0.6%患者在出院7 d内接受VTE预防治疗[37]。美国结直肠外科医师协会指南亦指出,UC患者术后VTE风险高于肿瘤患者,41% VTE发生在出院后,但出院后延长VTE预防治疗时间的依从性极低(处方率<2%)[39]。因此,对高风险UC患者,建议参照肿瘤治疗经验,延长预防性抗凝治疗至术后4周[39]。
推荐意见6:在UC外科治疗过程中,推荐遵循加速康复外科路径。择期手术的UC患者,推荐术前进行充分的预康复。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:ERAS 理念强调减少围手术期处理过程给患者造成的应激,并对患者进行充分的预康复和积极的术后康复。虽然针对 IBD 的 ERAS 路径尚待进一步优化与验证,但现有证据已充分表明 IBD 患者能从中获益。激素和
一项纳入16项IBD研究合计2 347例患者的系统综述显示,ERAS能将手术患者住院时间缩短至5.2 d(2.9~10.7 d),手术部位感染率(3.1%~23.5%)、吻合口漏发生率(0~3.4%)、并发症发生率(5.7%~48%)均有显著下降,死亡率均低于1%[40]。另一项纳入 671 例 IBD 患者(包含UC 326例)的单中心队列研究比较了 ERAS 实施前后手术患者的临床结局,结果显示,ERAS组腹腔镜手术率更高(61% 比47.3%,P=0.000 6),住院时间更短,住院费用减少约13%,而术后并发症和再入院率与传统手术组比较差异均无统计学意义[41]。最近一项来自中国UC储袋联盟的216例UC患者IPAA手术多中心回顾性队列研究(中位随访时间8年)进一步证实,与非 ERAS 组相比,ERAS 组患者术后总体并发症指数评分(10.42 比 14.14,P = 0.036)、严重并发症发生率(12.9% 比27.9%,P = 0.019)、住院时间(9 d 比 16 d,P = 0.046)及长期生活质量改善率(79.0% 比 53.2%,P < 0.001)均具有显著优势[42]。
UC患者使用激素的现象比较常见,连续使用
营养风险和营养不良是 UC 术后并发症的独立危险因素,推荐依据《炎症性肠病营养治疗专家共识(第三版)》对拟行择期手术的UC患者进行营养风险筛查和营养状况评估,对有指征的患者及时给予营养治疗[48]。营养治疗首选肠内营养(enteral nutrition,EN)途径,对 EN 失败或不耐受患者,肠外营养(parenteral nutrition,PN)同样有效。回顾性研究分析 235 例 UC 手术患者后发现,尽管 PN 是术后并发症的独立危险因素(OR = 2.32),但在排除静脉导管相关感染后,PN组和不需要PN组术后并发症发生率的差异无统计学意义(OR = 1.5,P = 0.311),提示对严重营养不良的UC手术患者,PN虽然增加静脉导管相关感染的风险,但能够减少严重营养不良所带来的手术并发症[49]。一项纳入61例IBD患者(UC 16例)的前瞻性研究采用不少于4周的术前营养预康复并遵循结直肠肿瘤ERAS 路径,结果显示,术后早期经口进食的患者住院时间明显缩短,肠道功能恢复更快,术后并发症发生率无显著增加[50]。
推荐意见7:生物制剂等药物不增加UC择期手术后感染或其他并发症风险,但可能增加储袋相关并发症风险。因此推荐对计划行 IPAA 的患者,如术前存在抗 TNF 制剂暴露,储袋制作应推迟到二次手术时进行。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:术前使用生物制剂并不增加术后感染或其他并发症风险,不推荐因此推迟择期手术。但拟行IPAA手术的患者,如存在抗肿瘤坏死因子(tumor necrosis factor,TNF)制剂(尤其是IFX)暴露,储袋相关并发症(盆腔感染、吻合口漏等)风险会显著增加,建议采取分期手术策略,避免在使用生物制剂后短期内构建储袋。
一项纳入4 659例IBD患者的荟萃分析显示,术前使用抗TNF⁃α制剂并未显著增加UC术后感染性并发症(OR =1.39,95%CI:0.56~3.45)、非感染性并发症(OR = 1.40,95%CI:0.68~2.85)及总并发症(OR = 1.10,95%CI:0.81~1.47)的风险[51]。PUCCINI 研究进一步证实,即便患者在术前 12 周内接受抗 TNF 治疗或抗 TNF 血清药物浓度处于可检测水平(IFX<1 μg/mL、ADA<1.6 μg/mL),抗TNF暴露组和抗TNF未暴露组术后总感染率(18.1% 比 20.2%,P = 0.469)及手术部位感染率(12.0% 比 12.6%,P = 0.889)差异均无统计学意义[52]。荟萃分析显示,术前使用维得利珠单克隆抗体(vedolizumab,VDZ)、抗TNF制剂及未使用生物制剂者,术后感染性或非感染性并发症发生风险差异均无统计学意义[53⁃54]。研究显示,尽管围手术期应用托法替尼可能与VTE相 关 ,但 与 抗 TNF 制 剂 、VDZ 及 乌 司 奴 单 克 隆 抗 体(ustekinumab,UST)相比,应用托法替尼患者术后总并发症、感染性并发症的发生率差异均无统计学意义[55⁃56]。
然而有荟萃分析显示,术前使用IFX 显著增加IPAA 手术相关并发症(OR = 4.57,95%CI:2.73~7.66)。亚组分析发现,累计使用IFX ≥3次的患者IPAA手术相关并发症风险显著上升(OR = 9.59,95%CI:2.92~31.44,P = 0.000 2),而最后一次输注距手术不足12周并未显著增加IPAA 手术相关并发症风险(OR = 2.35,95%CI:0.98~5.64,P = 0.06),提示IFX累积暴露剂量可能比用药距手术的时间间隔更具临床意义[57]。另一项大型回顾性分析亦证实,术前使用抗TNF制剂显著增加IPAA手术并发症的风险,尤其是吻合口瘘和盆腔感染[58]。因此,鉴于上述结论的不确定性,在接受抗TNF制剂治疗背景下,采取分期实施的结肠直肠切除与回肠储袋肛管吻合手术策略可能有助于降低IPAA手术相关并发症,尤其对于存在手术并发症风险因素的患者[59]。
四、手术方式
推荐意见8:择期UC手术推荐采用微创技术。(证据等级:Ⅱ~Ⅳ,推荐强度:强推荐)
推荐理由:微创手术(如腹腔镜或机器人手术)在UC择期手术中具有显著优势,能够缩小手术创伤程度和范围,降低腹腔粘连与切口疝风险,减少手术并发症,保护性功能与生育功能,促进肠功能恢复,缩短住院时间,提高生活质量。机器人辅助手术具有高清放大的三维视野和防抖设计,操作更为精准,尤其适用于解剖精细、空间狭小的手术操作环境。腹腔镜和机器人手术二者在 IBD 手术治疗中具有同等的疗效。
单中心随机对照试验 LapConPouch 研究显示,尽管腹腔镜IPAA 手术较传统开腹手术时间更长[(313.9 ±52)min比(200.2±53.8)min,P < 0.001],但总体安全性包括主要并发症发生率(9.5% 比 5.0%)和严重不良事件发生率(37.5%比44.0%)差异均无统计学意义;亚组分析显示腹腔镜手术住院时间更短[(11.2 ± 4.8)d比(26.4 ± 4.3)d][60]。病例匹配研究显示,IPAA腹腔镜(404例)与开腹手术(404例)在长期功能结局、生活质量及储袋保留率方面等效,但腹腔镜手术术后1年内夜间排便更少[(2.0 ± 1.4)次比(2.5 ± 1.7)次,P = 0.006],夜间采用防渗漏护理措施比例更低(20.8% 比32.4%,P = 0.04),并且克利夫兰诊所总体生活质量评分(CGQoL)更高[(0.8 ± 0.2)分 比(0.7 ± 0.2)分,P = 0.01][61]。一项针对女性IPAA手术后生育力影响的研究以首次自然妊娠时间为主要终点进行 Kaplan⁃Meier 分析,腹腔镜组的首次自然妊娠率显著高于开腹手术组[70%(19/27)比 39%(9/23),P = 0.023];在37例UC患者亚组分析中,腹腔镜组仍表现出显著优势,差异具有统计学意义(P = 0.033)。在尝试受孕12个月内,腹腔镜组有55%(11/20)成功自然妊娠,而开腹手术组仅为35%(6/17)[62]。
一项系统评价与 Meta 分析纳入了 11 项观察性研究共5 566例IBD患者,比较机器人辅助手术与腹腔镜手术的疗效。结果显示两者在中转开腹率、吻合口漏、腹腔脓肿、术后肠麻痹等方面差异均无统计学意义;尽管腹腔镜组手术时间更短(P = 0.000 01),但机器人辅助手术组术后并发症发生率更低(30.3%比43.1%,P = 0.03),住院时间更短(P = 0.03)[63]。尽管 ASUC 多采用开腹手术,但多项研究证实,腹腔镜或机器人辅助手术在 ASUC 治疗中也具有可行性与安全性[64⁃66]。
在极度狭窄骨盆等特殊情况下,经肛微创手术克服了腹腔镜手术中处理远端直肠面临的困难。多项研究显示,经肛IPAA手术在具备操作经验的中心可获得与腹腔镜IPAA手术相当的长期结果,但其长期疗效与安全性尚缺乏高质量证据支持[67⁃68]。
推荐意见9:推荐IPAA手术作为UC首选术式。对于无重建意愿或存在禁忌的患者,可选择全结肠直肠切除加永久性末端回肠造口术。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:IPAA 手术在切除全部结直肠、永久性避免UC复发的同时,还能保留经肛门排便功能,且大便次数可以被患者接受,显著提升生活质量。因此,该术式是多数UC患者的首选手术方式。但回肠储袋有出现并发症和失败的风险,肛门控便功能差(如括约肌功能差、高龄)或存在严重全身合并症是IPAA手术禁忌证。对没有构建储袋意愿或存在IPAA 手术禁忌的患者,推荐选择 TPC加永久性末端回肠造口术。
IPAA 手术与TPC加永久性末端回肠造口术近期并发症主要与TPC相关,风险相当,但远期并发症差异存在统计学意义。系统回顾与荟萃分析显示,IPAA手术远期并发症主要包括慢性储袋炎(23.0%)、排便失禁(18.6%)及肛门狭窄(10.8%);末端回肠造口术则以造口旁疝(39.1%)、造口旁漏(17.4%)及造口周围皮肤刺激(13%)为主[69]。
一项纳入13项研究的系统综述显示,IPAA手术与TPC加末端回肠造口术在整体生活质量方面效果相当;但在造口生活质量量表(SQOL)评估的分维度中,IPAA手术患者在社交功能(93.4 比79.4,P = 0.01)、身体外观/性功能(93.1比 76.4,P < 0.001)及皮肤舒适度(70.5 比 51.1,P = 0.02)方面的评分均显著优于TPC加回肠造口患者[70]。Meta分析结果显示,≥60 岁的老年患者接受 IPAA 手术后总体并发症风险无显著升高(RR = 1.10,P = 0.41),尽管夜间失禁率略高(RR = 1.91,P = 0.04),但术后满意度超过85%[71]。然而,UC合并PSC的患者在接受IPAA手术后,储袋并发症风险显著升高。一项纳入182例患者的匹配性研究显示,UC合并PSC患者慢性储袋炎(68.1%比 34.1%)及中重度储袋炎(54.9% 比 32.4%)的发生率均显著高于非PSC患者(均P<0.001)[72]。IPAA手术后女性患者的不孕风险显著升高。荟萃分析显示采用药物治疗的UC患者不孕率为15%,而IPAA手术后不孕率高达48%(HR=3.17,95%CI:2.41~4.18)[73]。尽管腹腔镜、机器人辅助手术有助于降低术后盆腔粘连相关生育风险,但仍建议拟行IPAA手术的育龄女性在术前充分知情,并考虑术前妊娠或辅助生殖策略[62,74]。
推荐意见10:推荐根据患者术前状态个体化选择IPAA分期手术。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:IPAA手术复杂,创伤大。个别经过严格筛选的健康状况良好、肠道和盆腔手术条件理想的患者可以一期完成IPAA手术。绝大多数患者在手术时往往处于UC病程后期,常伴有手术并发症危险因素,一期完成手术全过程风险较高。因此,临床多采用分期手术策略:对于手术并发症低风险患者,推荐采用传统二期手术;而对于中高风险患者,建议采用改良二期手术或三期手术。
IPAA 手术分期见表3。一项纳入 14 项研究共 4 973例患者的荟萃分析(其中8项行一期IPAA手术、2项行改良二期手术)比较了IPAA手术是否采用保护性回肠造口的术后结局,结果显示,回肠造口还纳手术与手术并发症相关,未行保护性回肠造口患者的吻合口狭窄率(5.79%比18.08%,OR =0.40,95%CI:0.26~0.62,P<0.000 1)和储袋失败率(2.49%比4.43%,OR = 0.54,95%CI:0.36~0.82,P = 0.003)显著低于造口患者(参见推荐意见16)。尽管未行造口患者再手术率略高(8.55% 比6.18%,OR = 2.51,95%CI:1.12~5.59,P = 0.02),但两组在吻合口漏、腹腔感染及术后小肠梗阻等并发症发生率方面差异均无统计学意义[75]。

一项纳入 212 例活动期 UC 手术患者的回顾性研究显示,三期IPAA手术多为急诊手术(78.6%),而行二期IPAA手术者多为药物治疗失败患者(98.7%),二期与三期IPAA手术在围手术期并发症、吻合口瘘、腹腔感染、储袋炎、储袋失败及长期生活质量方面差异均无统计学意义[76]。Zittan等[77]回顾性比较了单中心二期(223例)和改良二期(237例)IPAA手术结果,发现尽管改良二期手术患者术前激素使用率更高(44.7% 比33.2%)且中重度患者比例更高(86.9%比73.1%),但其吻合口漏发生率仍显著低于传统二期(4.6% 比15.7%,P < 0.01);多因素分析显示,改良二期手术是发生吻合口漏的独立保护因素(OR = 0.27,95%CI:0.12~0.57)。另一项系统综述与荟萃分析比较了改良二期(656 例)与传统二期(777例)或三期IPAA手术(294例)的结局,发现三者总体并发症发生率相当,大多数术后并发症(包括吻合口漏、感染、狭窄、储袋炎、小肠梗阻、深静脉血栓形成等)差异均无统计学意义;但在亚组分析中发现,改良二期较传统二期IPAA手术吻合口漏风险更低(OR = 0.33,95%CI:0.19~0.56)[78]。
推荐意见11:急诊UC 和ASUC 患者,推荐遵循损伤控制理念,首次手术采用结肠次全切除术,后续根据患者情况选择第2次手术方式。(证据等级:Ⅱ~Ⅳ,推荐强度:强推荐)
推荐理由:对于病情危重的急诊UC或ASUC患者,首次手术目的是挽救生命。由于患者伴有手术并发症危险因素,实施确定性手术耗时长、创伤大,不利于患者恢复,建议遵循“损伤控制外科”原则,采用STC去除大部分病灶并保留直肠与盆腔结构,这样既能迅速控制病情,又为后续确定性手术如IPAA创造条件。
ASUC患者的死亡多与术后感染或脓毒症相关,而非直接由肠道本身导致[7]。遵循“损伤控制外科”原则,在UC病情危重时采取分期手术策略可缩小手术创伤范围和程度,有助于术后康复[15]。一项纳入74例接受STC的重症IBD患者回顾性研究显示,术后并发症发生率为 23%,无死亡病例。52 例 UC 患者中,最终 31 例(59.6%)在术后 1 年内接受了IPAA,20例(38.5%)选择保留回肠造口,其中10例切除残留直肠[79]。
首次手术时结肠残端的最佳处理方式目前尚无共识,建议结肠残端位置在腹膜反折以上,便于后续手术。为避免旷置在盆腔的结肠残端因其活动性炎症在术后裂开并引起盆腔感染或出血,临床上常采用以下处理方式:(1)保留部分乙状结肠,残端关闭后将其埋置在皮下,术后如果残端裂开,则切开皮肤,将其变成结肠造口;(2)乙状结肠残端不关闭,直接外置造口;(3)如果残端位置较低,无法埋于皮下或外置,则将其妥善包埋后置于盆腔,并通过肛门放置引流管减压[80]。一项系统综述纳入1 330例因IBD行STC患者,总死亡率为1.7%(95%CI:1.0%~2.8%)、切口感染率为 11.3%(95%CI:7.8%~16.0%)、盆 腔 脓 肿/感 染 发 生 率 为 5.7%(95%CI:4.4%~7.3%)、残端漏发生率为4.9%(95%CI:3.7%~6.6%)。其中,残端埋置皮下的残端漏发生率最高(12.6%),残端置于盆腔的盆腔脓肿发生率最高(11.1%)[81]。另一项纳入476例因ASUC行结肠切除患者的系统回顾显示,乙状结肠外置造口显著降低并发症风险,效果优于留置于盆腔或皮下(总并发症率:12.5% 比 25% 比 27%,盆腔脓肿率:3.1% 比 5.3% 比2%,切口感染率:9.4%比7.9%比14.5%)[82]。
推荐意见12:推荐采用J型储袋,选择管状吻合器行储袋肛管吻合术。(证据等级:Ⅱ~Ⅲ,推荐强度:强推荐)
推荐理由:储袋类型包括J型、S型、H型、W型和D型等。良好的储袋功能取决于适当的储袋容积、良好的储袋顺应性、协调的排便反射和正常的括约肌功能。J型储袋因制作简便、排空效率高,术后并发症少,远期功能不逊于其他类型储袋,是IPAA手术首选的储袋方式。切除直肠过程中远端不能保留过长,以免发生封套炎。选择管状吻合器行储袋肛管吻合操作简便、安全可靠、对控便功能影响小,是首选的吻合方式。
Mukewar 等[83]回顾性比较了 J 型储袋(215 例)和 S 型储袋(45例)的临床效果,尽管J型储袋慢性储袋炎发生率高于S型(36.3%比15.6%,P = 0.002),S型储袋术后并发症发生率(44.4% 比 9.3%)和机械性/结构性并发症发生率(OR = 8.0,95%CI:3.7~17.5,P < 0.001)显著高于J型储袋,但两种储袋失败率差异无统计学意义(7.9% 比6.7%,P = 0.95)。一项纳入18项研究(J形689例、W形306例和S形524例)的荟萃分析显示,J形储袋患者虽然更频繁使用止泻药物,但需要插管协助排空粪便的比例仅为1.8%,显著优于S型储袋(29.6%)和W型储袋(20.0%)[84]。
储袋长度决定其容积,J型储袋的推荐长度为15~22 cm。容积过大易导致粪便淤滞,难以排空,容积过小增加排便频率[84⁃85]。来自中国UC储袋联盟的一项多中心研究显示,长储袋[22.0(20.0,24.0)cm]较短储袋[14.0(14.0,15.0)cm]能显著改善患者的长期生活质量并降低储袋相关并发症风险,短储袋是储袋并发症(OR = 3.1,95%CI:1.519~6.329,P = 0.002)和长期生活质量受损(OR = 2.221,95%CI:1.218~4.050,P = 0.009)的独立危险因素[85]。
储袋肛管吻合方式是影响IPAA手术后功能结局的另一关键因素。齿状线上方2 cm为肛管直肠移行区,在此离断直肠既能去除病变肠管,减少吻合口张力,又保留了直肠残端部分排便感受器,有利于术后维持患者的控便能力[86]。直肠断端超过齿状线上方 2 cm 是 IPAA 手术后发生封套炎的独立危险因素(OR = 2.64,P = 0.018)[87]。一项纳入3 109例IPAA手术患者的多中心研究显示,采用管状吻合器行储袋肛管吻合的术后盆腔感染率(16.9%比21.3%,P = 0.019)、小肠梗阻率(18.6% 比 23%,P = 0.027)、吻合口狭窄率(16.0%比21.7%,P = 0.02)和储袋失败率(4.0%比11.4%,P < 0.001)均显著优于手工吻合[88]。储袋肛管吻合过程中不推荐直肠黏膜剥离术,不仅难以剥除干净,残余直肠黏膜有癌变的风险,而且可能影响术后控便能力[89]。
肠系膜张力是影响储袋下拉及吻合成功的关键因素。一篇包括19项研究的系统评价表明,采用高位血管结扎、肠系膜根部游离、开窗、远端血管分支离断等延长技术可使90%以上的患者实现吻合口无张力,且未增加储袋缺血或功能障碍的风险,吻合口漏与严重并发症的发生率分别为6.1% 和 3.8%[90]。国内也有学者采用 D 型储袋减少吻合口张力的报道,但其长期安全性与疗效有待进一步临床验证[91]。
推荐意见 13:有生育需求和肛门控便功能差、不宜行IPAA手术的UC患者,如果直肠炎症轻微或豁免,并且能够接受术后规范化药物维持治疗和长期内镜监测,依从性良好,经充分术前沟通后可选择回肠直肠吻合术。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:回肠直肠吻合术(ileorectal anastomosis,IRA)能够避免直肠切除导致的盆腔组织粘连以及骶前神经受损,对患者性功能和生育功能影响较小,不影响患者排便功能,术后生活质量良好,适用于直肠豁免或炎症可控、有明确生育需求、不接受IPAA手术后并发症风险且能够严格执行术后药物治疗和随访的UC患者。术前应向患者充分告知残留直肠炎症复发导致手术失败及癌变的风险。
研究显示,不同手术方式对UC患者生育功能的影响存在显著差异,保留直肠对生育功能影响最小[68,92]。瑞典一项6 020例IBD患者(其中UC 3 041例)的队列研究显示,女性接受IRA手术后生育率无明显下降(HR = 0.86,95%CI:0.63~1.17),而IPAA手术后则显著下降(HR = 0.67,95%CI:0.50~0.88,P < 0.001)。对于男性患者,无论采取何种重建方式,术后生育力仅轻度下降(HR = 0.89,95%CI:0.85~0.94)[93]。
与IPAA 手术相比,IRA 术后残留直肠炎症可能反复发作,并且随着病程延长,癌变风险显著升高,术前应充分告知患者的潜在获益与相关风险[94⁃95]。系统评价显示,IRA术后吻合口漏发生率为3.9%(35/907),远期手术失败率为20.4%(498/2 447),10年累积失败率达27.3%,直肠癌变发生率为2.4%(30/1 245)[96]。另一篇包括81项研究的荟萃分析也显示,旷置直肠的患者局部癌变率为 2.1%(95%CI:1.3%~3.0%),IRA为2.4%(95%CI:1.7%~3.0%),均显著高于IPAA手术患者的0.5%(95%CI:0.3%~0.6%)(均P<0.05)[94]。
五、术后病情监测与并发症的处理
推荐意见 14:保留直肠患者推荐术后每年进行内镜监测和定期随访,以降低直肠癌发生风险,但不推荐IPAA 手术后常规进行储袋癌变监测。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:随着病程的延长,保留直肠的患者(包括回肠直肠吻合、直肠旷置及残留直肠封套者)残留直肠癌变风险逐年升高,需每年进行内镜监测。但IPAA手术后储袋相关肿瘤发生率极低,常规内镜监测对无肿瘤危险因素的患者获益有限,推荐根据肿瘤发病风险采取分层的个体化监测策略。
系统评价结果显示,IRA 术后 10 年直肠癌发生率为2.8%,10~15 年内癌变风险呈指数级上升,20 年时上升到7.3%(0~21.7%),需行直肠切除术的比例高达 21%[97]。IPAA手术后储袋相关癌较为罕见(累计发生率<0.4%),但结肠直肠切除标本中存在癌变或异型增生是IPAA术后发生储袋 相 关 癌 变 的 主 要 危 险 因 素(OR=8.8,95%CI:4.61 ~16.80)[98]。Kariv 等[99]对3 203例因IBD行IPAA 手术的患者的随访研究发现,储袋或肛管移行区异型增生发生率为0.72%,癌变总发生率仅为 0.36%,累计发生率在术后第 5、10、15、20 及 25 年分别为 0.9%、1.3%、1.9%、4.2% 和 5.1%,癌变主要发生在肛管移行区或封套部位。术前已确诊直肠癌变或异型增生的患者,术后肿瘤发生率显著高于术前无肿瘤者(6.8% 比 2.7% 比 0.59%),即使行直肠黏膜剥除术也未显著降低肿瘤的发生风险。因此,对储袋或肛管移行区的监测策略应基于风险分层原则,对于术前有结直肠肿瘤史的 IPAA 手术患者,推荐每年进行内镜检查,存在其他危险因素(慢性储袋炎、直肠炎或封套炎)者每 1~3 年检查 1次,无危险因素者可考虑每3年随访1次。储袋相关癌预后较差,一旦确诊建议依据病变性质尽早采取内镜或手术治疗[100]。
推荐意见15:UC相关重度小肠炎是一种少见但病情严重的UC相关并发症,病死率高,一旦发生,应立即采取干预措施。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:UC 相关重度小肠炎(ulcerative colitis⁃related severe enteritis,UCRSE)又称“结肠切除术后小肠炎”,是UC患者在结肠切除术后发生的少见但严重的并发症。UCRSE常表现为消化道大出血、造口高排量及肠穿孔,死亡率高。治疗原则主要是维持循环稳定、降低机体炎症负荷及保护器官功能,激素和生物制剂在 UCRSE 治疗中具有重要作用。
UCRSE 发病机制不明,可能与术后全身高炎症反应状态、肠道感染、肠内容物瘀滞及肠道菌群失衡等因素相 关 。 多 中 心 回 顾 性 研 究 显 示 ,UCRSE 的 发 生 率 为0.8%(42/5 284),中位发病时间为术后28 d。临床表现为肠道大出血(76.2%)、造口高排量(38.1%)和肠穿孔(7.1%),其中35.7%的患者合并低血容量性休克,死亡率达11.9%。激素、IFX 和 5⁃氨基水杨酸的治疗成功率分别为 54.2%(13/24)、60%(9/15)和 60%(3/5)[101]。在难治性出血患者中,内镜止血、介入治疗和手术治疗的成功率分别为70%(7/10)、77.8%(7/9)和 76.9%(10/13)[101]。一项纳入 814 例行结肠切除术UC患者的回顾性研究发现,7例(0.8%)患者发展为UCRSE,中位发病时间为术后33(12,248)d,临床表现为消化道大出血(4例)、造口高排量(3例)和穿孔(1例)。其中3例激素治疗无效的患者转换生物制剂,其他患者直接接受生物制剂治疗,最终5例接受IFX和2例接受戈里木单克隆抗体治疗,均获得改善[102]。
推荐意见16:IPAA手术后早期小肠梗阻推荐非手术治疗,反复发作或非手术治疗无效的患者推荐及时进行手术治疗。(证据等级:Ⅲ,推荐强度:弱推荐)
推荐理由:小肠梗阻是IPAA手术后常见并发症。多数患者尤其是造口相关性小肠梗阻患者,可通过禁食、胃肠减压等保守治疗缓解。对于梗阻反复发作或保守治疗无效的慢性小肠梗阻患者,及时手术可以减少手术并发症,改善预后,提高生活质量。
IPAA 术后小肠梗阻的发生率可达 23%~27%,主要与手术操作导致术后粘连形成有关,约1/3患者最终需要手术治疗[103⁃104]。前瞻性研究纳入1 178例IPAA 手术患者,结果显示,IPAA 手术后小肠梗阻的总发生率为 23%,术后 30 d、1 年、5 年和 10 年累积发生率分别为 8.7%、18.1%、26.7% 和31.4%,需要手术干预的风险分别为 0.8%、2.7%、6.7% 和7.5%,梗阻最常见的原因为盆腔粘连(32%)及造口还纳部位粘连(21%)[101]。长期(平均 9.1 年)随访结果表明,腹腔镜(119 例)与开腹(238 例)IPAA 手术患者术后小肠梗阻的总体发生率差异无统计学意义(29.4% 比 26.1%,P = 0.5),手术率差异亦无统计学意义(11.8% 比 8.5%,P = 0.31)[105]。一项纳入623例患者的回顾性研究比较了IPAA不同分期手术对小肠梗阻风险的影响,结果显示,尽管未达到统计学差异(P=0.062),但Ⅱ期或Ⅲ期手术小肠梗阻发生率(25.6%、26.8%)均高于Ⅰ期和改良Ⅱ期手术(16.3%、13.4%),其中34%患者最终需接受手术处理,保护性回肠造口显著增加小肠梗阻风险[104]。另有研究显示,IPAA手术后造口关闭前小肠梗阻的发生率高达28.8%(59/205),其中 89.8%(53/59)梗阻与造口相关;尽管 98.1% 患者可通过经造口插入导尿管减压获得症状缓解,但仍有 34.0%(18/53)的患者因反复梗阻需提前手术关闭造口[106]。
推荐意见17:IPAA手术后盆腔感染或储袋出血建议积极进行非手术治疗,以免导致储袋失败。(证据等级:Ⅱ~Ⅳ,推荐强度:弱推荐)
推荐理由:IPAA手术后吻合口瘘和继发性盆腔感染是储袋失败的主要危险因素,积极及时的干预是预防病情恶化、避免储袋切除、降低远期储袋失败的关键策略。通过影像学检查(CT/MRI)和内镜评估准确判断病变范围与性质,合理选择引流方式,包括经肛引流或CT引导盆腔穿刺引流、内镜下瘘口夹闭联合抗感染治疗等措施能够有效控制感染,促进瘘口愈合,最大限度降低储袋失败风险。对于储袋出血,首选非手术治疗,必要时行内镜下止血。
一篇纳入 30 项研究共 22 978 例 IPAA 手术患者的荟萃分析显示,术后 5 年和 10 年储袋失败率分别为 7.8% 和10.3%,盆腔感染(r = 0.51,P < 0.05)及储袋瘘形成(r = 0.63,P < 0.01)与储袋失败显著相关[107]。IPAA手术吻合口漏可发生于术后任何时期,常见于术后90 d内,表现为盆腔或腹腔感染。若术中行保护性回肠造口,其临床表现不典型,往往在术后肠道造影、盆腔MRI检查时发现,部分患者甚至在造口还纳后才确诊[100]。研究显示,约6.2%~15.0%IPAA 手术患者会发生吻合口漏及继发性盆腔感染,出现瘘管、脓肿、窦道等结构异常改变,超重(体质量指数≥25 kg/m2)、低白蛋白血症、输血、术前使用激素或抗TNF制剂等是吻合口漏的独立危险因素[108⁃110]。术中经肛门放置减压管是吻合口漏的独立保护因素(OR = 0.37,95%CI:0.14~0.97,P = 0.043),可显著降低术后吻合口漏的发生率(18.5%比7.8%,P = 0.037)[111]。
影像学检查联合内镜评估是诊断储袋吻合口瘘及盆腔感染性并发症的关键手段。急性期首选CT或联合水溶性造影剂储袋造影,识别游离气体、积液及脓肿;慢性储袋瘘或窦道的诊断推荐盆腔MRI,以精确显示解剖结构和感染路径,联合内镜检查后诊断准确率可达100%[112]。早期诊断并积极处理储袋术后吻合口瘘,可有效控制盆腔感染,显著降低储袋失败的风险[107]。吻合口漏相关盆腔脓肿首选麻醉下经肛门探查并置管引流;若未发现漏口,建议CT引导下经皮穿刺引流,并使用广谱抗生素;合并弥漫性腹膜炎者,行腹腔冲洗引流,辅以保护性回肠造口。基于低位直肠癌吻合口漏的经验,尽管未达到统计学差异,但经肛引流造口关闭率为93%,明显高于经腹再手术组(60%)和药物治疗组(67%)[113]。小样本临床研究显示,控制感染后,内镜辅助真空闭合技术、内镜下夹闭技术以及高压氧治疗均有助于吻合口瘘的早期闭合,并降低远期储袋失败率[114⁃116]。
IPAA手术后储袋出血多因肠吻合过程中肠壁组织撕裂或小血管损伤所致,常见于储袋肛管钉合区域,发生率约为1.5%~3.5%,其中 66% 出血发生在术后 7 d 内,确诊主要依赖储袋镜检查[117]。通过袢式回肠造口向远端置入冲洗管,用 1∶200 000 的肾上腺素溶液顺行冲洗可以控制一般的渗血。出血量大或保守治疗效果不佳时,建议尽早行储袋镜检查并内镜下止血。Lian等[118]报道47例IPAA手术后储袋出血患者,其中5例经输血、静脉补液等保守治疗止血;28例患者在储袋镜下行血块清除,包括 15例电凝止血成功(100%,15/15);96%(24/25)经肾上腺素保留灌肠止血成功。
推荐意见18:对IPAA手术后疑似储袋炎的患者,建议行储袋镜检查明确诊断,并根据储袋炎类型进行个体化治疗。(证据等级:Ⅱ,推荐强度:强推荐)
推荐理由:储袋炎症性病变是IPAA手术后常见的并发症,包括急性储袋炎、慢性储袋炎及CD样储袋炎。对所有疑似储袋炎症性病变的患者,建议行储袋镜检查明确病变分型、炎症范围与严重程度,并排除其他可能原因,如吻合口狭窄、瘘管、回肠末端炎以及艰难梭菌与巨细胞病毒等感染。对明确储袋炎患者,可选择抗生素、局部抗炎或生物制剂等治疗手段。
急性储袋炎的发生率高达 70%~80%,其中约 20% 患者可能进展为慢性储袋炎,CD 样储袋炎的发生率约为10.3%,不同类型储袋炎治疗策略差异显著[119⁃120]。根据美国胃肠病学会指南,急性储袋炎治疗首选环丙沙星500 mg 或甲硝唑400 mg、每日2次口服,疗程通常为14 d;慢性储袋炎多采用抗生素轮换口服疗法,如环丙沙星、甲硝唑、替硝唑、利福昔明及阿莫西林⁃克拉维甲酸,每2~4周更换1次,对于抗生素治疗无效的患者,在排除感染因素后考虑生物制剂治疗;CD样储袋炎起始治疗推荐使用抗TNF制剂,抗TNF治疗失败者可更换其他生物制剂治疗[121]。
系统评价与荟萃分析显示,抗TNF制剂治疗难治性慢性储袋炎及 CD 样储袋炎的总体短期(8 周)临床缓解率为50%,长期(12个月)缓解率为52%;亚组分析显示,CD样储袋炎的短期(64%比10%)与长期(57%比37%)缓解率均显著优于慢性储袋炎[122]。EARNEST研究显示,VDZ较安慰剂可以显著提高慢性储袋炎 14 周的溃疡消失率(23.8% 比7.5%)、内镜缓解率(23.8%比7.5%)及黏膜愈合率(16.7%比2.5%)[123]。另一项系统评价显示,UST治疗慢性储袋炎的临床应答率为63%,临床缓解率为10%,内镜应答率为60%;其治疗CD样储袋炎的临床应答率为85%,临床缓解率为27%,内镜应答率为67%[124]。
推荐意见19:建议高度重视IPAA手术远期并发症的诊断与治疗。对于诊断明确的储袋失败患者,推荐在IPAA手术经验丰富的医疗中心进行充分评估,选择储袋切除或储袋重建。(证据等级:Ⅱ~Ⅲ,推荐强度:弱推荐)
推荐理由:IPAA手术后远期并发症复杂多样,应高度重视。发生储袋远期并发症时建议及时采取有效措施,以免导致储袋失败。储袋失败的手术治疗操作复杂,并发症多,建议由具备丰富盆底外科及IPAA手术经验的临床中心充分评估后,个体化选择储袋切除或储袋重建手术。
IPAA手术后患者可能出现营养与代谢改变,贫血、骨质疏松、电解质紊乱和多种维生素缺乏最为常见,其累积发生率可达40%~50%,一旦出现,需要及时治疗[100]。IPAA手术后封套炎发生率约为 30%~45%,可采用美沙拉嗪栓(1 g,每晚1次)纳肛、或者美沙拉嗪或激素灌肠治疗[121]。
IPAA手术后储袋失败发生率约为5%~15%,早期失败多与盆腔感染、吻合口漏相关,远期失败则见于储袋功能障碍(严重失禁、排便困难或储袋容量丧失)、慢性难治性储袋炎、复杂储袋瘘或储袋肿瘤[125⁃126]。在一项纳入664例IPAA手术后患者的研究中,储袋失败发生率为6.2%(41例),主要原因包括 CD 样储袋炎(41.5%,17/41)、慢性储袋炎(14.6%,6/41)、封套炎(12.2%,5/41)及吻合口狭窄(9.8%,4/41)[126]。另一项研究显示,2.0%(45/2 286)的患者IPAA术后发生慢性储袋窦道,其中33.3%(15/45)最终发展为储袋失败[127]。系统综述与荟萃分析显示,储袋相关瘘发生率为4.6%(276/6 014),储袋阴道瘘或储袋会阴瘘最为常见(3.2%,191/6 014)[128]。
单纯慢性储袋窦道或储袋瘘可进行分层处理:通过观察、窦道引流、窦道切开或闭合术等干预,无症状的慢性窦道通常可以愈合(84%),对于症状性窦道应及早评估是否需要手术干预,以防储袋失败[127]。一项纳入152例IPAA手术后出现储袋阴道瘘患者的研究中,97例患者接受手术治疗(经肛门储袋黏膜瓣修补48例、经阴道修补27例、储袋重建手术10例、储袋切除5例、回肠永久性造口2例和挂线引流5例)。中位随访83个月,瘘道愈合率57.7%,储袋失败率35%[129]。内镜治疗(如球囊扩张、针刀切开)在IPAA手术后狭窄处理中技术成功率达 97.4%,临床成功率 81.7%,储袋失败率仅6.8%[130]。系统评价和荟萃分析显示,IPAA手术后储袋狭窄最常见于储袋⁃肛管吻合口部位,指检或器械扩张治疗成功率可达95%,储袋入口狭窄经内镜球囊扩张成功率为67%~75%[131]。
对于IPAA手术后储袋失败且无法重建的患者,建议选择储袋切除术联合末端回肠造口。基于14项回顾性研究共1 601例患者的系统综述显示,仅行回肠转流性造口的患者尽管保留储袋未观察到癌变,但约57.1%患者长期存在肛门渗液,需依赖卫生护垫,提示有必要切除储袋以改善局部不适症状。储袋切除术后并发症发生率为18%~63%,其中持续性会阴窦道(9%~40%)和术区感染(2%~30%)最为常见[132]。储袋切除属于复杂盆腔手术,手术相关并发症发生率高,推荐由具备盆腔手术经验的团队实施[133⁃134]。
储袋重建手术技术挑战与风险更高,仅限在部分具有丰富IPAA手术经验的临床专科中心实施。拟接受储袋重建的患者应当需求明确,心理预期合理,充分了解并能够接受重建失败的风险[125]。一项回顾性队列研究纳入1982–2017年间159例因储袋失败接受经腹储袋重建的患者,3年、5年和10年储袋存活率分别为82.3%、77.2% 和70.6%,35.2% 患者储袋再次失败[135]。
六、展望
随着达标治疗理念的推广,UC外科治疗正逐步迈向早期评估、精准干预与提高生活质量的新阶段。未来将更加注重内外科协同,更加明确手术在整体治疗路径中的时机选择与功能定位,持续推进微创化与标准化手术,不断提升手术质量,实现疾病控制与生活质量改善的双重目标,建立更加科学、系统的功能评价和疾病全周期管理体系,推动UC外科治疗向系统化、标准化、同质化的方向高质量发展。