前言1
传统上,
HER2低表达/超低表达乳腺癌现状及未满足需求1
根据美国临床肿瘤学会-美国病理学家学院(ASCO-CAP)发布的《乳腺癌HER2检测指南(2018版)》,HER2表达状态分为HER2阳性或阴性(图1),其中约80%的浸润性乳腺癌被归类为HER2阴性。然而,HER2表达实际上是一个连续性过程,多数归类为阴性的肿瘤仍可检测到一定水平的HER2蛋白。研究显示,在原发性或转移性乳腺癌患者中,约50%~55%的患者可归类为HER2低表达,15%~20%可归类为HER2超低表达。

图1 当前建议的HER2分类1
由于不可避免的内分泌治疗及化疗耐药,HER2低表达/超低表达的治疗选择均十分有限。对于激素受体(HR)阳性、HER2阴性晚期乳腺癌,一线治疗通常采用内分泌治疗联合CDK4/6抑制剂。然而疾病进展后,二线治疗的疗效下降,中位无进展生存期(PFS)仅为4.2~8.1个月,且不可避免地可能会发生内分泌治疗耐药。与此同时,治疗中断导致能够接受后续治疗的患者比例(即患者退出率)降低,数据显示,从一线进展至二线治疗时,患者退出率为15%~33%,真实世界研究中则高达18%~51%,主要原因为疾病进展及死亡。对于HR阴性、HER2阴性(即三阴性)乳腺癌,标准一线治疗包括化疗、免疫联合化疗(适用于PD-L1阳性患者)或PARP抑制剂(适用于BRCA1/2突变患者),但化疗耐药问题突出,一、二线治疗的中位PFS仅为1.5~10.9个月,因此亟需更有效的治疗手段。
ADC药物在HER2低表达/超低表达转移性乳腺癌中的疗效1
T-DXd作为一种靶向HER2的ADC药物,由人源化抗HER2 IgG1单克隆抗体、可裂解的四肽连接子和拓扑异构酶I抑制剂载荷(DXd)三部分组成。该药物不仅能杀伤表达HER2的肿瘤细胞,其释放的载荷还可扩散至邻近细胞,即通过“旁观者效应”发挥更广泛的抗肿瘤作用。关键Ⅲ期临床试验DESTINY-Breast04(DB-04)和DESTINY-Breast06(DB-06)已证实了T-DXd在HER2低表达/超低表达乳腺癌患者中的临床疗效。
DB-04研究是一项随机、开放标签的Ⅲ期临床试验,旨在评估T-DXd对比医生选择的治疗方案(TPC)在既往接受过1-2线化疗的HR阳性或HR阴性、HER2低表达、不可切除或转移性乳腺癌患者中的疗效和安全性。截至2022年1月,HR阳性队列中,T-DXd组的中位PFS为10.1个月,显著优于TPC组的5.4个月(HR=0.51,P<0.001)。此外,T-DXd组的中位总生存期(OS)为23.9个月,同样优于TPC组的17.5个月(HR=0.64,P=0.003)(表1)。该试验结果表明,对于HR阳性、HER2低表达转移性乳腺癌患者,T-DXd具有统计学显著且临床意义的抗肿瘤活性,且安全性特征良好。此外,该研究对HER2低表达作为一个影响治疗决策的、具有临床相关性的乳腺癌亚型起到积极推动作用。
DB-06研究则聚焦于在转移阶段经内分泌治疗后进展,且既往未接受过化疗的HR阳性、HER2低表达/超低表达转移性乳腺癌患者,对比T-DXd与TPC的疗效。首次中期分析数据显示,截至2024年3月,在HER2低表达队列中,T-DXd组的中位PFS为13.2个月,显著优于TPC组的8.1个月(HR=0.62,P<0.001),且12个月的OS率为87.6%,高于TPC组的81.7%(表1)。
表1 T-DXd在DB-04和DB-06研究中的疗效结果1
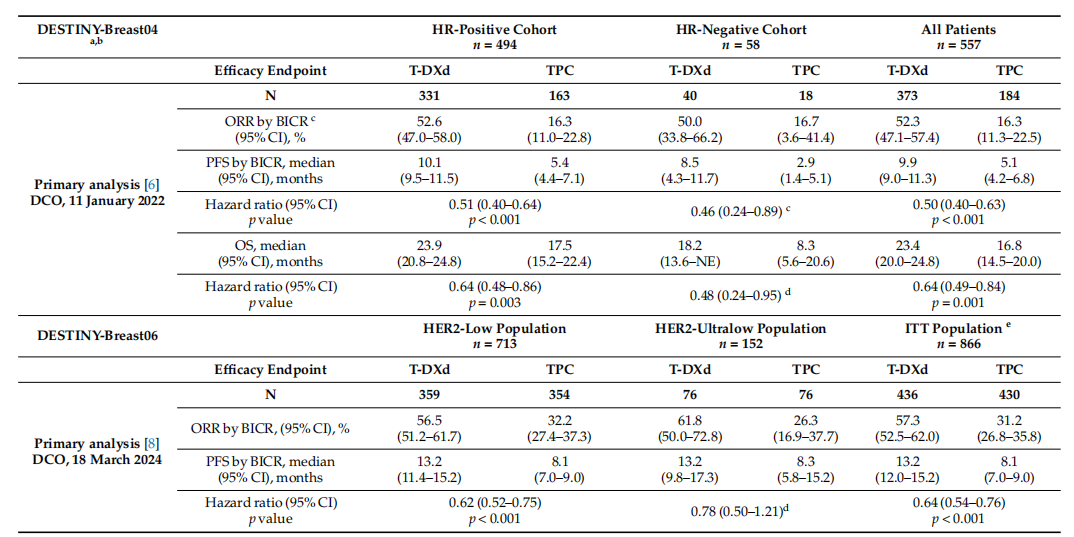
DB-04研究中纳入了58例HR阴性、HER2低表达患者的探索性队列。结果显示,T-DXd组的确认客观缓解率(ORR)为50.0%,高于TPC组的16.7%;中位 PFS为8.5个月,优于TPC组的2.9个月(HR=0.46);中位OS为18.2个月,高于TPC组的8.3个月(HR=0.48),与整体HER2低表达人群的疗效趋势一致。
多项临床试验已纳入HER2超低表达亚组患者,探究T-DXd的潜在疗效。Ⅱ期DAISY试验中,15例HER2 超低表达患者接受T-DXd治疗,确认ORR达40%。DB-06试验亚组分析则纳入了152例HR阳性、HER2超低表达患者,亚组分析显示,T-DXd组的中位PFS为13.2个月,优于TPC组的8.3个月(HR=0.78);ORR为61.8%,高于TPC组的 26.3%。需要注意的是,该亚组分析为探索性研究,未进行统计学检验。
HER2低表达与超低表达晚期/转移性乳腺癌的ADC治疗序贯策略1
基于DB-04研究结果,美国食品药品监督管理局(FDA)批准T-DXd用于在转移阶段接受过至少一种化疗、辅助化疗期间或完成辅助化疗后6个月内复发的HER2低表达晚期成人乳腺癌患者。而DB-06研究的结果则进一步支持T-DXd获批用于治疗既往在转移性疾病阶段经一种或一种以上内分泌治疗进展的、不可切除或转移性HR阳性、HER2低表达或HER2超低表达晚期成人乳腺癌患者。
美国国家综合癌症网络(NCCN)指南推荐:
对于伴有内脏危象或属于内分泌难治性的HR阳性、HER2低表达或超低表达乳腺癌,一线治疗可选择系统性化疗(1类推荐,首选方案)或T-DXd(其他推荐方案)。由于T-DXd的缓解率高于单药化疗,当需要更快速控制症状时,临床医生可考虑优先使用T-DXd。
此外,对于非BRCA1/2突变的HR阴性、HER2 IHC 1+或2+/ISH- 转移性乳腺癌,T-DXd也推荐作为二线治疗的“其他推荐方案”。
►
SG是一种靶向滋养层细胞表面抗原2(Trop-2)的ADC药物,已获批用于治疗既往接受过内分泌治疗且在转移性疾病阶段接受过至少2种其他系统治疗的不可切除局部晚期或转移性的HR阳性、HER2阴性乳腺癌成人患者。此外,基于ASCENT等研究,SG亦获批用于治疗既往接受过至少2种系统治疗(其中至少1种为针对转移性疾病的治疗)的不可切除的局部晚期或转移性三阴性(TNBC)成人乳腺癌患者。
►德达博妥单抗(Dato-DXd):
Dato-DXd是一款新型Trop-2 ADC药物,全球Ⅲ期研究TROPION-Breast01证实,Dato-DXd相较于化疗显著改善了患者的中位PFS(6.9个月 vs 4.9个月,HR=0.63,P<0.0001),Dato-DXd组与化疗组的中位OS分别为18.6个月和18.3个月(HR=1.01,P=0.94)。基于TROPION-Breast01研究,Dato-DXd已获批用于既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的HR阳性、HER2阴性乳腺癌成人患者。NCCN乳腺癌临床实践指南推荐,对于不适合接受T-DXd治疗的HR阳性、HER2阴性患者,Dato-DXd可作为化疗或PARP抑制剂治疗后的二线治疗选择。
回顾性研究提示,HER2阴性转移性乳腺癌患者序贯接受不同ADC治疗时,疗效会下降,中位PFS显著缩短,可能与ADC的抗体靶点或载荷部分产生交叉耐药有关。已获批的DXd类ADC药物与SG所携带的载荷均具有相似的作用机制(拓扑异构酶抑制),因此优化ADC序贯策略尤为关键。然而目前,关于ADC药物的最佳治疗顺序尚无充分的临床证据,仍需进一步研究以明确耐药机制并优化治疗策略。
ADC在HER2低表达转移性乳腺癌脑转移患者中的疗效1
约8.5%~15.0%的HER2低表达转移性乳腺癌患者会发生脑转移,T-DXd对这类患者的全身和颅内疗效已通过亚组分析得到初步验证。DB-04研究的亚组分析显示,基线存在脑转移的患者中,T-DXd组的中位PFS为8.1个月,优于TPC组的4.8个月(HR=0.71)。另一项DB-04研究亚组分析同样证实,与TPC组相比,T-DXd组具有更高的颅内ORR(25.0% vs. 0%)、临床获益率(58.3% vs. 18.2%)和疾病控制率(75.0% vs. 63.6%)。
HER2低表达与超低表达乳腺癌的检测1
NCCN指南和ASCO-CAP临床实践指南推荐,所有新诊断原发性或转移性乳腺癌患者均应进行HER2检测,以指导治疗决策。IHC是检测HER2蛋白表达的常规手段,具有报告周期短、应用广泛,并能评估肿瘤内部的异质性等优势。DB-04和06研究使用的是经临床验证的VENTANA抗HER2/neu(4B5)兔单克隆抗体,是目前FDA批准的唯一用于识别可能适合接受T-DXd治疗的HER2低表达及HER2超低表达转移性乳腺癌患者。此外,目前正在探索替代补充方法,包括基于定量mRNA和蛋白质的检测技术,以及利用人工智能解读结果等。
►判读一致性与标准化:
目前亟需准确区分是否存在细胞膜染色(IHC 1+/IHC 0但存在细胞膜染色/IHC 0且无细胞膜染色),对HER2表达状态进行更加精准的划分。此外,已有研究指出,市售HER2 IHC检测试剂的敏感度与特异度存在差异,可能导致结果判读不一致。而且即使在使用标准化检测流程并严格质控的情况下,评分与判读仍依赖于医生目视观察评估,可能引入额外的主观变异性,导致同一份样本的HER2表达状态在不同实验室或不同病理医生之间出现差异。
►肿瘤异质性与HER2表达的动态变化:
HER2表达状态在肿瘤内(存在异质性)和疾病进展过程中(原发灶与转移灶之间)均可能发生动态变化。因此,重复进行肿瘤检测可能具有合理性,可为治疗决策提供重要依据。
►对既往HER2 IHC 0患者的再评估:
对于既往评分为 HER2 IHC0 的患者,重新检测存档组织或获取新活检样本以评估HER2状态,可能有助于识别从靶向治疗中获益的HER2超低表达患者。因此,应加强肿瘤学医生与病理学医生之间的沟通,并通过多学科团队讨论,优化此类患者评估方案。
安全性:ADC药物不良反应的预防、监测与管理1
在DB-04和DB-06研究中,T-DXd在HER2低表达/超低表达晚期乳腺癌患者中的安全性总体可管理,最常见的药物相关不良事件为低级别的胃肠道或血液学毒性。值得关注的是,
►筛查(Screen):
在使用T-DXd前,必须对患者进行全面评估以识别ILD/肺炎的风险因素(图2)。
►扫描(Scan):
治疗期间应每6-12周进行一次增强胸部CT或高分辨率胸部CT扫描,同时应常规询问患者呼吸系统症状(图2)。
►协作(Synergy):
由护士、肺科医生和放射科医生等组成的多学科团队应共同参与监测,助力患者得到及时的诊断和治疗(图2)。
►暂停治疗(Suspend treatment):
一旦发现疑似ILD/肺炎,应立即中断T-DXd治疗(图2)。
►类固醇(Steroids):
疑似ILD时,应立即启动皮质类固醇治疗,并根据ILD严重程度分级进行对症治疗。

图2 “5S”管理策略早期识别管理ILD/肺炎1
►恶心/
►乏力:
可通过标准化工具对患者进行全面评估,以识别可能导致乏力相关因素进行提前干预。此外,可通过体力活动、优化膳食结构、重视心理健康等措施进行综合管理。
►脱发:
T-DXd相关脱发多为1级(脱发量<50%,无需假发/发片遮盖),目前正在研究采用头皮冷却技术预防化疗所致脱发,但尚无数据支持该技术及药物干预对预防T-DXd相关脱发的有效性。
老年患者接受化疗时,由于年龄相关的生理变化以及化疗药物药代动力学的改变,不良事件发生风险高于年轻患者。因此,针对不同年龄HER2低表达和超低表达乳腺癌患者的T-DXd使用及不良事件管理策略的探索,仍需更多研究支持。
总结与展望1
随着T-DXd在HER2低表达和超低表达转移性乳腺癌中的应用,对HER2表达水平的精准评估与检测标准化提出了更高要求,也使得统一HER2超低表达的定义成为及时识别获益患者的关键。在此背景下,临床医生需综合疗效、患者个体目标、生活质量及治疗毒性,为患者制定最佳的治疗决策。目前,多项临床试验正致力于为晚期HER2低/超低表达乳腺癌的临床实践提供进一步依据。与此同时,其他靶向HER2或TROP2的新型ADC药物也在不断研发中,有望丰富治疗选择。展望未来,研究重点将涵盖ADC序贯策略的优化、耐药机制的阐明、ILD的精准诊断与管理,以及真实世界数据与药物经济学证据的积累,从而全方位推动乳腺癌的精准治疗进程。
参考文献:
1.Nusayba A Bagegni, et al .Cancers (Basel). 2025 Dec 17;17(24):4021
审批编号: CN-177571
有效期至:2027/1/27
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)