一名18个月大女童因发热、咳嗽和呼吸困难1个月就诊于急诊科。咳嗽在1个月内进行性加重,性质为湿性咳嗽。在此次入院前,患者曾在另一家医疗机构住院21天,期间因铜绿假单胞菌肺炎需要气管插管和机械通气8天,并接受了静脉抗生素和雾化治疗。该患儿为非近亲结婚所生第一胎,产前及出生史无特殊。其发育里程碑与年龄相符,并已完成适龄免疫接种,无不良反应。母亲有两次自然流产史,均发生于孕早期。
入院时,患者易激惹。生命体征:心率122次/分,呼吸频率52次/分,血压120/76 mm Hg(>第95百分位),体温正常。人体测量学指标:体重8.5 kg(<年龄第3百分位),身长78 cm(年龄第3-10百分位),身长对应体重正常,头围43 cm(<年龄第3百分位)。一般检查未见苍白、杵状指、发绀或淋巴结病。系统检查显示存在呼吸窘迫,伴有鼻翼煽动、肋间及肋下凹陷,听诊可闻及双侧粗湿啰音。
初始血清实验室检查:血红蛋白12.2 g/dL;白细胞总数13300 个/mm³;中性粒细胞77%;淋巴细胞20%;钠135 mM(正常范围,130-150 mM);钾3.0 mM(正常范围,3.5-5.5 mM);氯83.6 mM(正常范围,98-108 mM);尿素氮2.33 mM(正常范围,1.7-7.1 mM);肌酐0.12 mg/dL(正常范围,0.2-0.5 mg/dL)。
动脉血气分析:pH 7.51;碳酸氢根23.8 mEq/L;碱剩余11 mM;动脉血氧分压(PaO₂)68 mm Hg;二氧化碳分压(PCO₂)86 mm Hg。因此,该患儿存在低钾低氯性代谢性碱中毒伴高碳酸血症性呼吸衰竭。
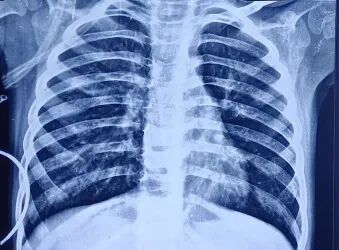
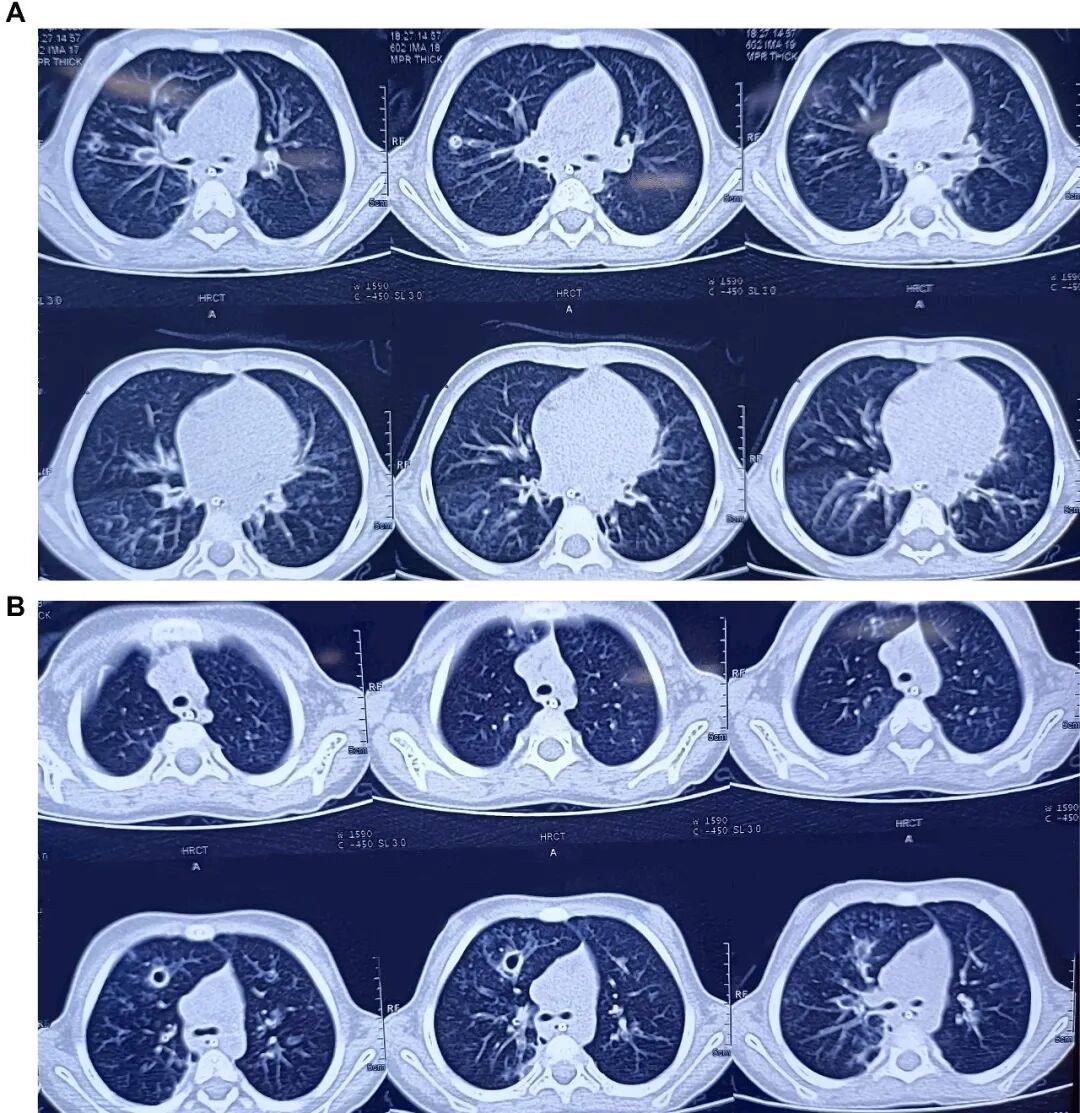
胸片显示双肺野过度充气,伴右肺中野不均匀浸润影及支气管壁增厚(图1)。胸部高分辨率CT扫描显示右肺上叶前段可见厚壁囊腔,可能存在交通,紧邻管壁明显增厚的亚段支气管——提示囊性支气管扩张(图2)。免疫功能缺陷检查已排除:HIV报告正常,免疫球蛋白谱正常,淋巴细胞亚群分析正常。IgA=54.67 mg/dL,IgG=990.32 mg/dL,IgM=404.186 mg/dL,IgE=16.3 IU/mL,CD3(T细胞)=2237.32 个/μL ,62.85% ;CD4 TH细胞=1165.21 个/μL ,32.73% ;CD8 T细胞=1065.26 个/μL,29.92%;CD4/CD8比值1.09,均处于正常范围。
图1 患者入院时胸片。显示双肺野过度充气,左肺中野不均匀密度增高影伴支气管周围增厚。
图2 A.胸部高分辨率CT扫描显示左右肺囊性支气管扩张,伴有空穴病变。B.胸部高分辨率CT扫描显示右肺上叶前段有厚壁囊性腔体,并有囊性支气管扩张的证据。
血管炎相关检查:尿液镜检、抗中性粒细胞胞浆抗体谱、嗜酸性粒细胞计数均为阴性,肾动脉多普勒超声正常。鼻内镜和喉镜检查提示1级声门下狭窄,可能与前次住院期间长期插管有关。
3分钟和5分钟水合试验阳性、粪便脂肪球存在、代谢性碱中毒、深部咽拭子铜绿假单胞菌和肺炎克雷伯菌阳性、以及糖化血红蛋白(HbA1c)为5.9% (5.6%-6.5%) 引起了对囊性纤维化的怀疑。然而,正常的粪便弹性蛋白酶 (464 µg/g) (>200正常) 和阴性的汗液氯离子试验 (收集量156 mg;氯离子,19.51 mM) 不支持该诊断。
持续存在的高血压、正常的肾脏超声和血清醛固酮水平(25.0 ng/dL) (正常 5-90 ng/dL)、以及正常低限的肾素水平 (10.91 ng/mL/h),结合呼吸系统受累,需考虑离子通道病的可能。
诊断:由于持续存在的呼吸道症状、部分提示囊性纤维化的发现以及持续存在的高血压,进行了临床外显子组测序。该检测揭示了一个统一诊断:Liddle综合征-1和伴或不伴汗液氯离子(Cl⁻)升高的支气管扩张症-1,两者均与SCNN1B基因的杂合突变相关(遗传方式——常染色体显性,分类——可能致病)。
儿科人群支气管扩张的病因可能归因于囊性纤维化背景下的反复感染;纤毛清除功能缺陷(原发性纤毛运动障碍);先天性免疫缺陷;麻疹、结核、百日咳或水痘感染后;反复误吸;以及变应性支气管肺曲霉病。伴或不伴汗液氯离子升高的支气管扩张症-1(BESC1)是一种罕见疾病,其临床表现谱和严重程度因基因突变类型而异。其特征是由反复呼吸道感染引起的慢性支气管炎症,最终导致气道异常扩张,伴有慢性咳嗽、脓痰和因呼吸衰竭频繁住院。它也被称为囊性纤维化样综合征或非典型囊性纤维化。囊性纤维化与BESC1的关键区别在于涉及的基因——在囊性纤维化中,致病突变发生在上皮Cl⁻通道,即囊性纤维化跨膜传导调节因子(CFTR),而上皮钠离子(Na⁺)通道(ENaC)的缺陷则与以支气管扩张伴肾脏疾病(I型系统性假性醛固酮减少症和Liddle综合征)为特征的临床表现相关。ENaC的α、β和γ亚单位分别由 SCNN1A、SCNN1B 和 SCNN1G 基因编码。这3个基因属于钠通道(SCN)基因家族。SCNN1B 基因编码ENaC的β亚单位,该亚单位对于包括肾小管和呼吸道在内的多种器官上皮细胞的钠重吸收至关重要。ENaC在钠平衡和气道表面液体水化中起着至关重要的作用,这对于有效的黏液清除至关重要。
Liddle综合征是一种常染色体显性遗传病,由 SCNN1A、SCNN1B 或 SCNN1G 等基因的功能获得性突变引起,导致钠过度重吸收,从而引发低肾素性高血压。在本例特定患者中,SCNN1B 突变同时解释了其肺部(支气管扩张)和肾脏(Liddle综合征)的表现。这两种情况的同时发生突显了ENaC功能失调所带来的多样化临床后果。阿米洛利特异性地阻断肾脏中的这些ENaC通道,减少钠的重吸收和钾的分泌,从而有助于控制与Liddle综合征相关的高血压和低钾血症。研究也表明它可以增加肺部的纤毛清除功能。
在小鼠体内进行的ENaCβ亚单位过表达研究显示,其发展为囊性纤维化样疾病,伴有黏液阻塞和细菌清除不良。气道表面液体容量的正常调节(该功能依赖于ENaC介导的钠吸收和CFTR介导的氯分泌之间的协调)在维持正常纤毛清除功能中起关键作用。因此,任一过程(即主动氯分泌或钠吸收)的缺陷预计都会导致气道表面液体容量减少、纤毛功能障碍和肺部疾病。
临床上,这种情况属于小气道疾病,其特征是呼吸急促、啰音、喘息和低氧血症,症状出现后持续很长时间,如本例患者所示。持续性湿咳和喘息是最常见的症状。胸部CT显示肺不张、支气管周围增厚、空气潴留以及伴有马赛克征的支气管扩张,这使得感染后闭塞性细支气管炎成为该患者重要的鉴别诊断。关于Liddle综合征肺部表型的数据很少,儿科病例也稀少。
患者最初接受了无创通气CPAP、静脉抗生素和雾化药物治疗。由于识别出持续性高血压,开始加用口服阿米洛利和呋塞米。全面的诊断性检查,包括排除免疫缺陷和囊性纤维化等常见病因,结合持续存在的多系统症状,最终促使进行了关键的基因检测,从而提供了明确诊断。
1.本病例强调了基因检测在临床表现复杂的儿科患者中的关键作用,尤其是当存在特征重叠的多系统疾病时。2.SCNN1B 突变的鉴定为支气管扩张和Liddle综合征提供了一个统一的诊断,拓展了已知的支气管扩张基因谱。
3.通过基因鉴定理解如Liddle综合征等疾病的分子基础具有直接的治疗意义,因为靶向阻断上皮钠通道的干预措施有助于控制高血压。
4.本病例主张提高对支气管扩张和高血压罕见遗传病因的认识,鼓励在临床评估和管理中采取个体化方法。
参考文献:Agarwal V, Satija P, Chattopadhyay A, Saikia D. Unraveling the Connection Between Respiratory Distress and Hypertension in an 18-Month-Old Girl. Chest. 2026;169(1):e5-e9. doi:10.1016/j.chest.2025.07.4086
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)