复发或难治性
研究者进一步扩展了该研究并进行了长期随访,共纳入38例R/R AML患者,近日发表于《Journal of Hematology & Oncology》,通讯作者为南开大学附属第一中心医院

设计:Ⅰ期临床试验更新数据,扩大队列并延长随访时间。
对象:38例R/R AML成人患者(中位年龄38岁),既往接受过中位5线治疗,71.05%为多线治疗后复发,31.58%接受过
干预:输注CLL1 CAR-T细胞。
主要终点:安全性(CRS、ICANS、血细胞减少等)及疗效(ORR、MRD⁻ CR率、PFS、OS)。
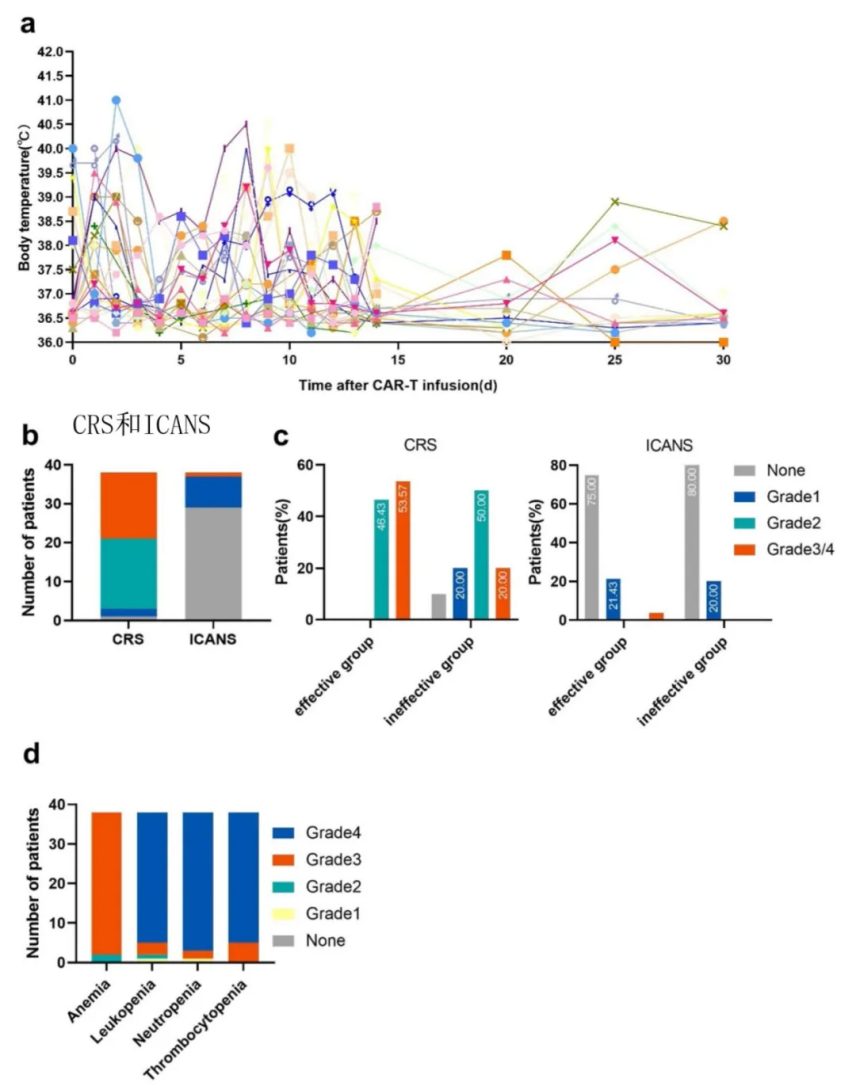
安全性
CRS:所有患者(100%)发生CRS,其中44.7%为3/4级(15例3级,2例4级)。92.10%出现
ICANS:18.4%发生ICANS,其中1例为4级并导致死亡。
血细胞减少:所有患者出现持续性全血细胞减少,中性粒细胞恢复中位时间45天。未桥接移植的患者感染风险高(3例死于脓毒症)。
疗效
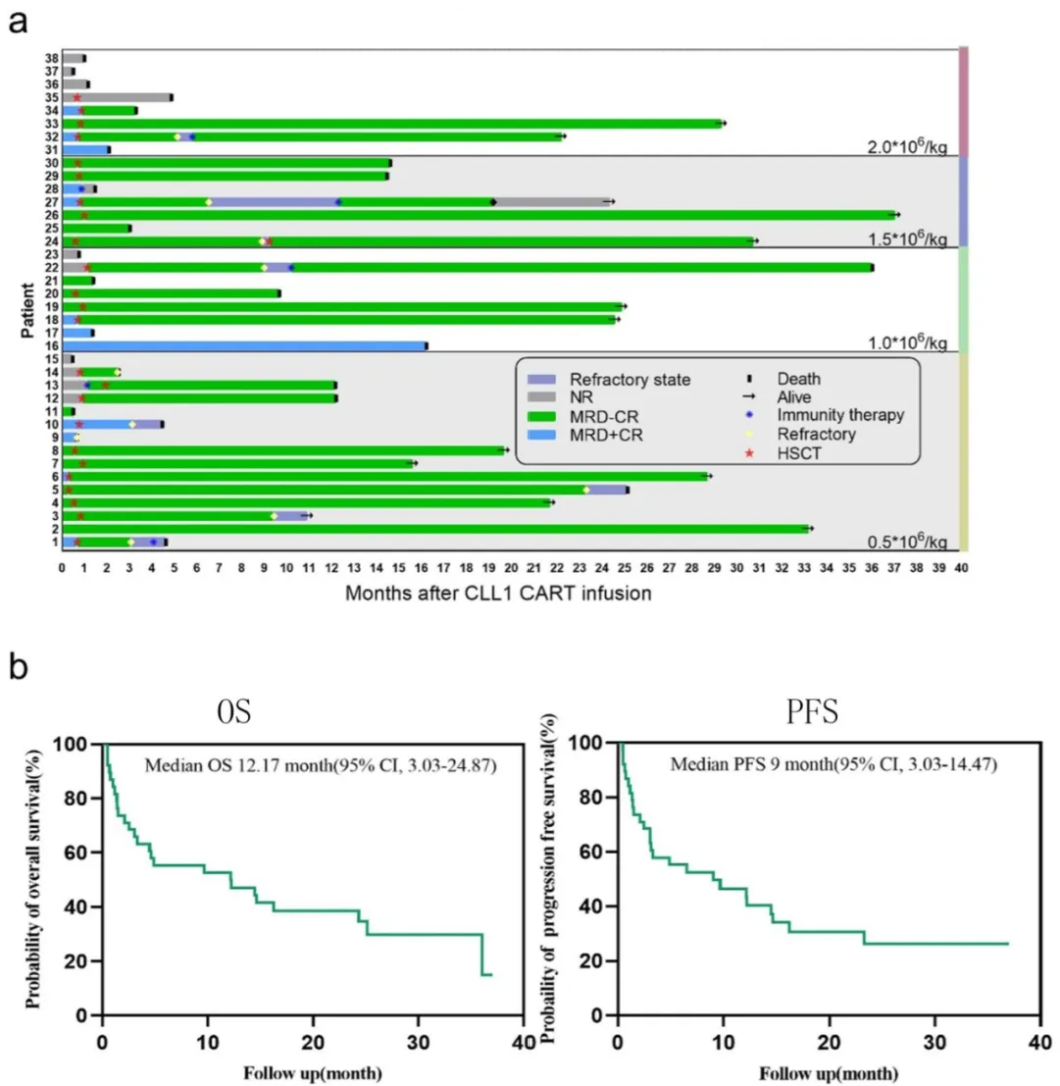
总体疗效:ORR为73.68%,MRD⁻ CR率为42.11%,MRD+ CR率为31.57%。
生存数据:中位PFS为9个月,中位OS为12.17个月;2年PFS率47.94%,2年OS率51.34%。
桥接移植的影响:19例患者在接受CAR-T后桥接了异基因HSCT,其中94.7%(18例)达到MRD⁻ CR。桥接移植组的中位OS(26.25个月 vs. 6.66个月)和PFS(25.16个月 vs. 6.66个月)均显著优于未移植组。
生物标志物分析
应答者血清IL-6和IFN-γ水平显著高于无应答者,且与CAR-T细胞扩增峰值呈正相关。
单细胞转录组测序显示,应答者中增殖性和初始T细胞(尤其CD8⁺ T细胞)比例更高,提示更强的扩增和活化能力。
CLL1 CAR-T疗法在R/R AML患者中显示出有前景的长期抗肿瘤活性,生存数据优于历史基准。
治疗相关毒性(尤其是重度CRS和血细胞减少)较为突出,安全性未优于其他靶向疗法。
桥接HSCT可显著改善血细胞减少并延长生存,是提高疗效的关键策略。
未来需多中心研究进一步验证疗效并评估长期安全性。
参考文献
1.Zhang, X., Lu, W., Zhang, W. et al. Updated data of CLL1 CAR-T cell therapy in adult patients with relapsed/refractory acute myeloid leukemia. J Hematol Oncol 18, 112 (2025). https://doi.org/10.1186/s13045-025-01764-5
2.Jin X, Zhang M, Sun R, Lyu H, Xiao X, Zhang X, et al. First-in-human phase I study of CLL-1 CAR-T cells in adults with relapsed/refractory acute myeloid leukemia. J Hematol Oncol. 2022;15(1):88.
声明:本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。