来源:中华胰腺病杂志

傅德良
复旦大学附属华山医院胰腺外科主任;医学博士、教授、主任医师、博士研究生导师
复旦大学胰腺病研究所所长
上海市中西医结合学会胰腺疾病专委会主任委员
上海市抗癌协会
上海市社会医疗机构协会肿瘤学分会胰腺肿瘤多学科专委会主委
中华医学会肿瘤分会胰腺肿瘤学组副组长
中华医学会普外科分会胰腺学组委员
中国抗癌协会胰腺癌专业委员会副主任委员
中国临床肿癌学会(CSCO)胰腺癌专家委员会副主任委员
中国医促会胰腺疾病分会副主任委员
提 要
胰腺癌发现晚、侵袭性高,药物治疗反应差,手术是目前唯一根治的方法。约3/4的胰腺癌发生在胰头处,而胰头区域解剖结构复杂,血管丰富,肿瘤容易侵犯血管,导致传统的胰十二指肠切除术受到限制。随着胰腺外科的发展,针对胰头癌血管侵犯的各种技术手段不断涌现,血管侵犯已经不再被视为手术禁区,有相当一部分患者可以从手术中获益,但就其具体治疗手段和治疗效果仍存在较多争议。本文系统总结胰头癌血管侵犯的诊断策略与治疗进展,旨在为临床实践提供参考。
全文阅读
胰头是胰腺癌的高发部位,但其解剖位置深在、早期症状隐匿,临床确诊时多数患者已处于晚期阶段。数据显示,约53%的患者已发生远处转移,25%的患者因肿瘤侵犯门静脉‑肠系膜上静脉等重要血管,传统上被列为手术禁忌证,仅15%~20%的患者具备根治性切除的机会。但值得关注的是,近年来临床实践与研究均证实,单纯以解剖学标准定义胰腺癌血管侵犯并不精准,部分影像学提示肿瘤邻近血管的侵犯术后病理检测并没有发现明确的血管侵犯证据,这提醒临床医师必须重视肿瘤生物学属性对诊疗决策的影响。随着胰腺外科技术的精进及与血管外科的交叉融合,在丰富经验的胰腺专科中心,针对胰头癌血管侵犯的根治性手术已成为常规开展的术式,如联合血管切除重建术等,显著扩大了手术适应证和手术切除率。笔者所在复旦大学附属华山医院胰腺外科中心至今已完成超500台联合门静脉系统切除重建的胰腺手术,且率先提出围术期保温在改善此类手术患者近期预后中的重要价值。基于此,本文将系统探讨胰头癌血管侵犯的诊断策略与治疗进展,为临床实践提供参考。
一、胰头癌血管侵犯的诊断
手术是目前治愈胰腺癌的唯一有效方法。根据胰腺癌与血管之间的解剖学关系,美国国家综合癌症网络(National Comprehensive Cancer Network, NCCN)指南将胰腺癌分为可切除、交界可切除、局部进展期和合并远处转移4类,其中交界可切除和局部进展期代表主要血管(包括肠系膜上静脉、门静脉、肠系膜上动脉、肝动脉和腹腔干等)受累(表1)。因此肿瘤与血管的关系评估对确定最初的治疗方案至关重要,目前评估的主要方法仍然是影像学。

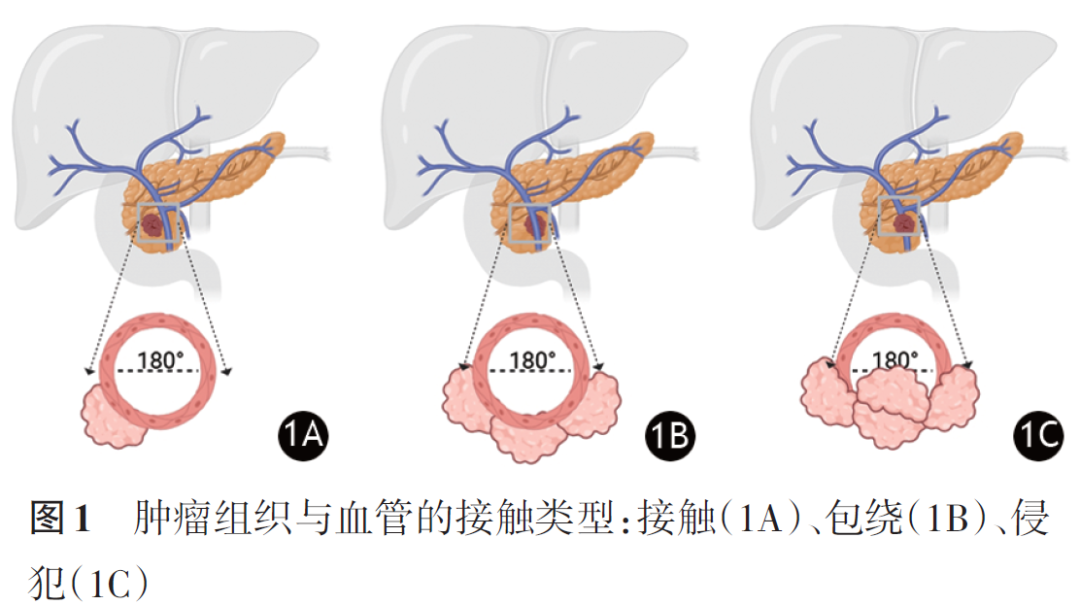
1.血管侵犯的影像学诊断技术:计算机断层成像(computed tomography, CT)是目前检查胰头癌是否血管侵犯的首选检查手段,主要评判标准包括肿瘤‑血管的环向接触程度、接触长度以及血管管径变化等。血管受累程度通过肿瘤组织与血管的解剖学关系界定,依据接触方式分为接触、包绕和侵犯3种类型(图1)。接触指肿瘤与血管的接触范围<180°,通常不被视为血管侵犯;包绕定义为肿瘤与血管接触范围超过180°,该征象诊断血管侵犯具有较高的灵敏度和特异度;而侵犯指肿瘤接触导致血管形态改变,常伴发腔内血栓形成等。ahmed等发现使用圆周界面≥180°且轮廓畸形≥3级伴或不伴肿瘤接触长度>2 cm的标准来预测血管侵犯具有较高的诊断性能。此外,一些特殊的形态学改变也暗示着动脉血管侵犯,如泪滴征(teardrop)、晕征(halo sign)和线样征(string sign)等。胰头癌以侵犯门静脉及肠系膜上静脉最为多见,术前需要充分评估。当胰头癌浸润肠系膜上动脉或腹腔干时,通常被视为不可切除。CT对血管侵犯的评估存在一定的局限:一方面CT难以评估胰腺癌的血管微浸润,这通常是患者术后复发的主要原因;另一方面新辅助治疗后CT难以判断组织坏死、炎症或
近年来超声评估胰头癌血管受累的价值正在被体现。郝思介等对132例CT怀疑胰腺癌血管侵犯的患者行超声内镜(endoscopic ultrasound, EUS)检查发现,在评估静脉侵犯方面,EUS效能优于CT,而评估肠系膜上动脉的侵犯能力则稍弱于CT。Yamada等将CT、EUS和超声内镜联合弹性成像(endoscopic ultrasound elastography, EUS‑EG)对血管侵犯诊断与组织病理学诊断进行比较,结果显示EUS‑EG能显著提高血管侵犯的诊断性能,尤其适用于CT无法清楚评估血管侵犯的情况。此外,一项前瞻性多中心研究评估了化疗后局部进展期患者术中超声评估血管受累的价值。结果发现,与CT相比,术中超声评估可能会改变化疗后多达1/3的局部进展期患者的可切除性状态。未来需要胰头癌术中超声评估血管受累的临床价值的前瞻性研究,以进一步挖掘超声诊断的应用价值。
2.血管侵犯可切除性评估理念的转变:随着胰腺外科学的不断发展,以传统解剖即形态学为基础的分类方法在临床实践中面临着一些挑战,尤其是其无法反映肿瘤异质性、活性、侵袭性等生物学属性。因此,胰腺癌分期标准正逐渐由形态学转向生物学。2017年欧洲癌症研究和治疗组织专家小组指出,胰腺癌可切除性标准不应仅基于血管受累,因为手术技术(血管切除的可行性)和肿瘤学结果[预测R1切除和(或)隐匿性转移的风险]之间可能存在差异。
MD Anderson系统在解剖基础上,引入了生物学指标(血清CA19‑9水平>500 U/ml)和患者状况指标[美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)评分≥2]定义交界可切除,已被采纳为国际共识标准。此外,国家胰腺腺癌解剖临床数据库(National Anatomo‑Clinical Database on Pancreatic Adenocarcinoma, BACAP)联盟最近发布的BACAP评分通过综合解剖学因素(血管血栓形成、肿瘤定位、肿瘤大小)、患者状态评估和临床症状(疼痛、体重减轻),进一步完善了对胰腺癌可切除性的预测。从生物学角度进行分期本质是评估肿瘤属性即“是否应该切除”,进而为患者提供个性化的治疗方案,避免“本不该切除”以及增加“可切除”。
二、胰头癌血管侵犯的外科治疗
1. 静脉侵犯的处理:胰头癌累及大血管曾被视为手术禁区,自1951年首次报道了联合门静脉⁃肠系膜上静脉切除的胰十二指肠切除术(pancreaticoduodenectomy, PD)后,联合静脉切除的胰头癌根治术近年来在不断改善和应用。国际胰腺外科研究组(International Study Group on Pancreatic Surgery, ISGPS)共识推荐,在存在肠系膜上静脉‑门静脉轴受累并可重建的情况下可进行手术切除,并将静脉切除术分为4种类型:1型为可直接缝合的部分静脉切除术(静脉成形术);2型为需使用补片的部分静脉切除术;3型为节段切除术直接端端吻合;4型为节段切除术使用移植物吻合(有两个吻合口)。
静脉切除有几个特殊的情况需要注意。当肿瘤侵犯肠系膜静脉远端的回肠和空肠分支时,通常优先选择回肠分支与近端静脉吻合,因为相比较空肠分支,回肠分支直径更大且解剖位置更容易和肠系膜上静脉吻合。若胰头癌累及肠系膜上静脉⁃脾静脉汇合处,通常需要结扎脾静脉,此时左门静脉系统主要通过胃和食管静脉回流,可能引发
越来越多的证据表明,静脉切除的围术期结果与标准切除相似,但其远期疗效仍需进一步验证。Yu等的荟萃分析显示,尽管联合门静脉‑肠系膜上静脉切除组患者肿瘤直径更大、淋巴结转移率更高,R0切除率(即显微镜下无肿瘤残留)和5年生存率较低,但术后1、3年的生存率与未行联合切除组相比无显著差异,提示两组短期疗效相似而长期生存仍存在争议。Giovinazzo等的荟萃分析则表明,联合门静脉‑肠系膜上静脉切除组患者R0切除率和术后1、3、5年生存率均低于无静脉切除组,这可能与联合静脉切除组纳入较多局部进展期胰腺癌有关。此外,未来研究需进一步细化评估指标,将静脉切除范围、受累血管长度等参数纳入分层分析,以更精准地评估不同手术策略的预后差异。
2.动脉侵犯的处理:动脉切除术作为可能实现根治性切除的重要手段,由于高死亡率、高并发症风险,且患者生存获益有限,其临床应用在指南中存在诸多争议。首先,新辅助化疗后肿瘤退缩与血管周围纤维化很难鉴别,为手术决策带来了不确定性。此外,在技术层面,动脉剥离与切除的选择、血管重建方式和移植物选择以及围术期和术后抗凝管理等尚未达成共识。最重要的是,动脉切除的临床获益尚未完全证实。早期研究证据显示动脉切除预后不良,Mollberg等针对2011年前数据的荟萃分析纳入2 609例患者,其中366例接受动脉切除术,2 243例未行动脉切除术,结果显示接受动脉切除术的患者围术期死亡率显著升高(OR=5.04, P<0.0001),1年生存率(OR=0.49, P=0.002)和3年生存率(OR=0.39, P=0.02)均显著降低,R0切除率亦明显下降(OR=0.44, P=0.004)。Rebelo等对2011—2020年数据的汇总分析进一步证实了这一结论,动脉切除术组术后死亡率显著高于非动脉切除术组(5.3%比1.1%, P<0.001),中位生存期缩短近50%(21.9个月比45.7个月,P=0.008)。值得注意的是,在纳入579例动脉切除术患者的亚组分析中,两组并发症发生率(48%比39%, P=0.1)及死亡率(3.2%比1.5%, P=0.27)差异无统计学意义,提示在部分研究中动脉切除的安全性有所提升。尽管上述研究并未单独针对胰头癌展开,但足以说明动脉切除的临床获益仍有待证实。
目前尚无指南或共识意见推荐将联合血管切除作为常规处理手段。ISGPS指南明确指出,目前尚无有力科学证据支持在标准根治术中常规切除胰头周围的动脉可改善患者预后,因此不推荐常规使用。最新的REDISCOVER指南同样强调胰腺外科医师需要具备血管处理能力,但考虑到动脉切除仍与较高的死亡风险显著相关,因此并不建议在常规实践中推广动脉切除。然而,部分大容量胰腺专科中心的研究表明,对于影像学提示疾病无进展、
胰头癌肝动脉侵犯可以选择血管切除与重建手术,术中应尽量避免由于出血及血栓栓塞导致的肝脏缺血。术后护理同样重要,因为胰肠吻合口周围的血管吻合口受引流
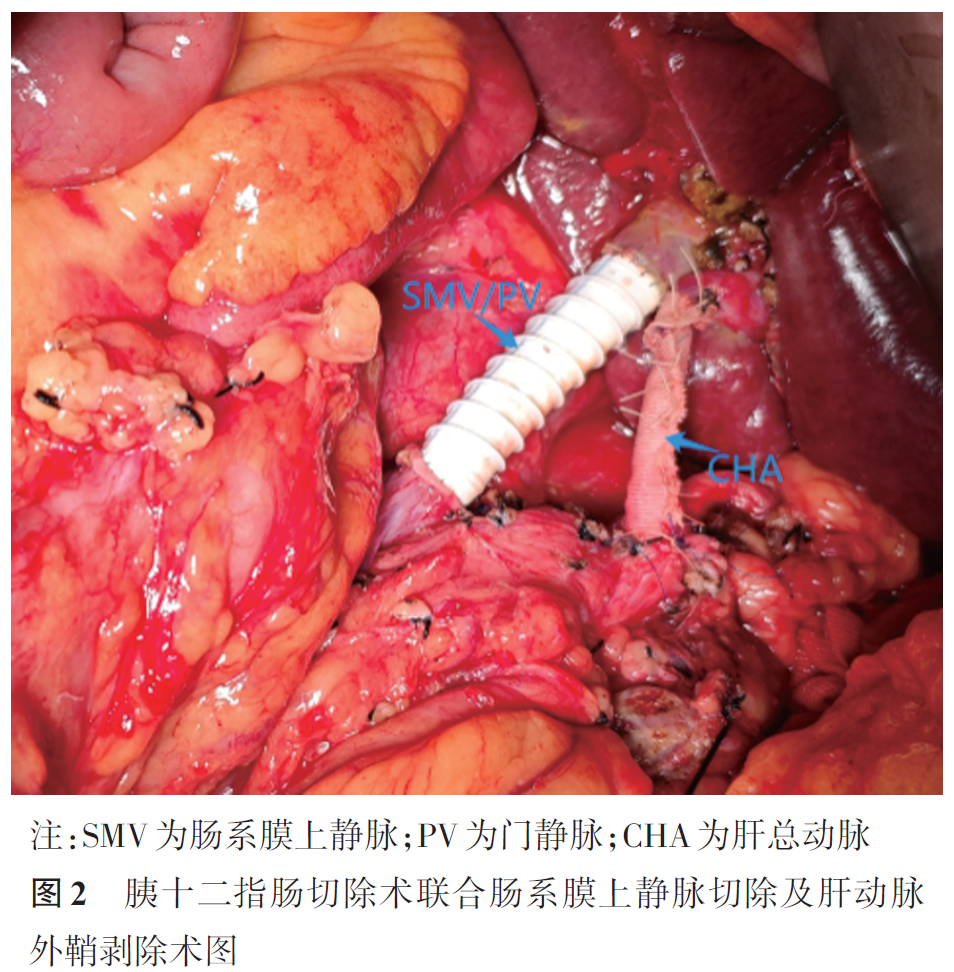
腹腔干血管浸润通常发生在胰体尾部肿瘤,但胰头癌术前仍需仔细评估腹腔干。一方面,需要判断是否存在正中弓状韧带压迫或
肠系膜上动脉受累是导致部分局部进展期胰头癌患者不可切除的主要原因。直接切除后重建手术风险大,术后并发症和死亡率高,因此临床中较少使用。而动脉鞘剥除可以在切除肿瘤的同时保留动脉,减少手术风险。Cai等的回顾性队列研究表明,与标准手术相比,行动脉鞘剥除术的局部进展期患者并发症发生率(40%比37%, P>0.05)和90 d死亡率(8%比3%, P>0.05)略高,但差异无统计学意义,初步证实该术式的安全性。Habib等建议在新辅助治疗后行影像学评估,如果CT表现为晕征(动脉外形正常无缩窄),可以行动脉鞘剥除术,如果表现为线样征(动脉外形有不规则缩窄),则无手术指征。动脉鞘剥除的关键在于在动脉外膜和外弹力层之间建立稳定安全的解剖平面,如果无法识别解剖平面,通常提示肿瘤已侵入动脉中膜平滑肌,此时应考虑动脉切除术。此外,这种血管操作技术会显著增加术中和术后血管并发症的发生率。因此操作时在建立解剖平面的同时要仔细地处理肿瘤侵犯动脉的分支,从而尽量避免术中动脉撕裂和大量出血。笔者团队对125例接受动脉鞘剥除的患者进行回顾性分析,发现动脉鞘剥除后加用补片能够显著降低术后出血风险。
自体小肠移植术是指将肿瘤及受累器官整块移除,在体外灌洗后清除病灶,然后分离小肠并将正常小肠移植回体内。但这种做法存在一定限制:手术时间过长可能会导致严重的小肠缺血再灌注损伤。此外,和肿瘤一起灌洗存在肿瘤细胞扩散的风险。因此,梁廷波团队对该术式做了改进,即在肿瘤切除之前先将小肠切除后单独灌洗保存,随后继续清除病灶。尽管该方法应用较少,但为包绕肠系膜上动脉的胰头癌及其他内脏肿瘤提供了彻底切除的可能性,未来需要更多的临床实践来证实其安全性。
3. 新的手术理念:为更好地实现R0切除并尽量减少术后复发,一些新的切除理念逐步应用于临床实践中,如胰腺全系膜切除、海德堡三角手术等。胰腺系膜被认为是R1切除发生率较高的主要部位,因此基于胰腺系膜理论的切除术在国内外得到广泛关注和应用。
此外,在规划涉及血管的胰头癌切除术时,必须充分考虑患者主要内脏动脉解剖的个体差异性。部分胰头癌血管侵犯的患者主要内脏动脉存在解剖变异或狭窄,需要在切除后进行动脉重建,以避免器官缺血。一项前瞻性试验尝试在化疗和肿瘤切除前先对供应肝脏或肠道的动脉进行重建,在避免术后切除重建的高风险的同时,保证在肿瘤切除后器官的血液供应。该技术被称为“Visceral Debranching”,预计在2026年完成。
4. 手术入路的选择:术前影像学检查难以完全反映胰头癌的实际病灶范围,因此术中探查的手术入路选择显得尤为重要。传统的Whipple手术通常在最后一步分离胰腺颈部时才发现血管受累,影响手术策略和切除效果。为解决这一问题,近年来提出了多种改进的手术入路,例如动脉优先入路、肠系膜入路及钩突优先入路等。
动脉优先入路强调首先分离肠系膜上动脉,便于及早发现肿瘤是否浸润肠系膜上动脉及门静脉‑肠系膜上静脉,从而判断肿瘤是否可切除,同时有利于清扫肿瘤周边淋巴组织和脂肪组织,这一手术入路尤其适用于血管侵犯的胰头癌患者。对于肠系膜上静脉和(或)门静脉受累拟行联合切除重建的患者,动脉优先入路有助于受累静脉的整块切除,减少静脉阻断时间,降低手术风险。此外,多项研究表明动脉优先入路可以提高R0切除率,改善生存率及减少术后并发症。但这一手术理念对术者提出了更高的要求,术者应该熟练掌握动脉优先的几种手术入路:前入路、后入路、左后入路、结肠下入路、钩突内侧入路等,以便根据肿瘤位置和神经丛的切除范围选择最佳入路。
当胰头癌伴有门静脉梗阻和良好的侧支循环时,使用Kocher手法切除可能会导致大量出血,因此,Nakao等基于动脉优先入路的理念,提出了肠系膜入路这一方式。该入路省略了Kocher手法,允许从非癌浸润侧进行解剖,并初步确定无癌切缘和可切除性。它使得早期评估可切除性、实现充分的淋巴结清扫和胰腺系膜切除成为可能。有文献报道,这种技术比PD结合Kocher手法具有更高的R0切除率(100%比87%, P=0.044)和更长的生存时间(P=0.008)。Hackert等于2010年提出钩突优先入路,即由足侧向头侧先游离胰腺钩突,再离断胰颈。其优势在于能够在术中显露胰腺钩突并分离腹膜后组织,获得清晰的肠系膜上血管视野,从而减少血管损伤及术中出血风险。该入路因其技术特点,已被广泛用于
三、其他治疗方法
1. 术前新辅助或诱导治疗:目前新辅助治疗主要适用于具有高危因素的可切除胰腺癌、交界可切除胰腺癌和局部进展期患者,其目标在于降低肿瘤分期、减少微转移、提高可切除性,从而延长患者无病生存期和总生存期。新辅助治疗的优势已经在多篇临床试验中得到验证,最新一项对1 192例患者进行的大型回顾性研究表明,与前期直接门静脉‑肠系膜静脉切除术相比,新辅助治疗后实施手术的R0切除率(57%比47%, P=0.004)和5年生存率(29%比18%, P<0.001)有所提高,对于需要行静脉重建的胰头癌患者,应常规考虑新辅助治疗。Xue等的荟萃分析显示,新辅助治疗后联合大动脉切除可以通过实现R0切除来延长交界可切除或局部晚期胰腺癌患者的生存期,为新辅助治疗的施行提供了新的支持。
然而,新辅助治疗后实施手术仍面临一系列挑战。首先,新辅助治疗可以缩小肿瘤体积并减少血管侵犯,但治疗后难以区分肿瘤浸润与瘤周炎症的纤维化改变。Ahmed等提出了一种肿瘤⁃血管界面标准在预测交界可切除患者新辅助治疗后血管侵犯方面表现出良好的诊断性能,帮助预测R0切除。但考虑到新辅助治疗后肿瘤周围组织的复杂性,有学者提出,新辅助治疗完成后无疾病进展的患者应接受手术探查,因为这是目前可切除性的唯一决定因素。手术方法包括动脉周围活检取样和立即冷冻
2.放疗:由于胰腺癌的放射抵抗性较高,且相邻的空腔器官难以耐受高剂量放射,因此,不能给予胰腺癌患者根治性的高剂量放疗。对大多数胰腺癌患者而言,放疗是一种局部的姑息治疗,其疗效尚未达成共识。目前不推荐根治术后常规行辅助放疗。对于交界可切除胰腺癌的
在新辅助治疗中,放化疗可作为单独化疗的替代或补充方案,但目前仍缺少高质量临床试验证实放化疗的临床疗效。例如,在LAP‑07和CONKO‑007研究中,尽管放化疗显示出R0切除率的改善,但均未能显著提高中位总生存率。在Ⅱ期Alliance A021501研究中,相较8周期的mFOLFIRINOX化疗,7周期的mFOLFIRINOX化疗后加新辅助放疗导致较低的总生存率。提示在新辅助化疗的基础上增加放疗是否会在某种程度上降低新辅助化疗的有效性。ESPAC⁃5试验中也观察到了在新辅助化疗基础上增加放疗的负面影响。因此,关于放疗的疗效和使用人群仍需要进一步探索和验证。
3.消融治疗:消融治疗在局部进展期胰腺癌中逐渐受到重视,其中不可逆电穿孔(irreversible electroporation, IRE)是代表技术之一。这种非热依赖型局部消融技术近年来广泛应用于临床,特别是在肿瘤包绕重要血管的患者中。何朝滨等发现接受IRE和转化手术(conversion surgery)的局部进展期患者生存时间差异无统计学意义,且与转化手术切除比较,IRE在治疗局部进展期具有独特优势,例如无须考虑肿瘤对血管的侵犯程度等,这对于部分无法切除的胰头癌血管侵犯患者而言是一种有效的治疗手段,但其安全性和应用价值仍需要更多的验证。
综上所述,胰头癌血管侵犯的诊断和治疗领域仍面临着诸多挑战。在诊断方面,尽管CT在术前评估中发挥着关键作用,但单纯形态学评估的局限性仍亟需寻找更为精准的评估手段。未来的方向可能包括新型生物标志物和液体活检技术的应用,以更全面地了解肿瘤的生物学属性,帮助优化治疗决策。在外科治疗方面,联合血管切除、动脉鞘剥离等技术的成熟以及新型手术方式的不断提出,为更多胰头癌患者实现根治性治疗提供了可能。然而,这也对胰腺外科医师提出了更高要求和挑战,既需要精湛的技术,也需要科学的术前评估和术中决策能力。未来的工作应重点整合多学科力量,包括影像学、病理学、分子生物学和临床医学的协同合作,推动个性化治疗的发展,为胰头癌血管侵犯患者提供更精准、更高效的治疗方案。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)