弥漫大 B 细胞淋巴瘤(DLBCL)作为最常见的侵袭性
BsAbs 通过同时结合肿瘤细胞表面抗原(如 CD20)与 T 细胞表面 CD3,激活 T 细胞杀伤肿瘤,目前获批用于 R/R DLBCL 的药物包括 epcoritamab、glofitamab 及 odronextamab(EMA 获批),均为 CD20×CD3 双抗,具有 IgG 样结构(延长半衰期、降低中枢毒性)。
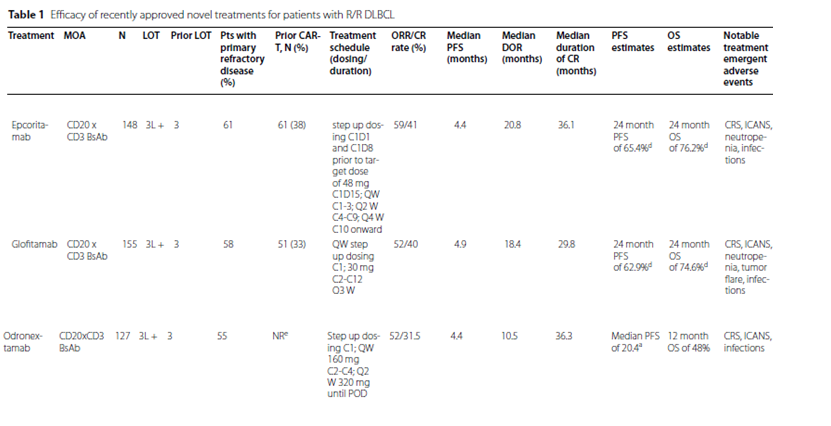
注:Epcoritamab 需逐步加量给药(C1D1、C1D8),后续按 QW(C1-C3)→Q2W(C4-C9)→Q4W(C10+)给药;Glofitamab 需联合 obinutuzumab 预处理以降低 CRS 风险,固定疗程 12 周期。
真实世界数据:REALBITE 研究(n=209)显示,epcoritamab/glofitamab 在真实世界中 ORR/CR 率降至 50.6%/23.8%(低于临床试验),CD20 阴性患者应答率显著降低,且骨髓侵犯、低白蛋白、低中性粒细胞计数与 CRS 风险升高相关。
ADCs 通过靶向递送细胞毒性药物至肿瘤细胞,降低系统毒性,目前获批用于 R/R DLBCL 的 ADC 包括 polatuzumab vedotin(CD79b 靶向)、loncastuximab tesirine(CD19 靶向)及 brentuximab vedotin(CD30 靶向)。
1. Polatuzumab vedotin 联合方案
2. Loncastuximab tesirine
作用机制:CD19 靶向 ADC,载荷吡咯并苯二氮䓬(DNA 损伤剂);
关键数据(LOTIS-2 研究,n=145):ORR/CR 率 48.6%/24.1%,中位 PFS 4.9 个月,中位 OS 9.9 个月;
TEAEs:中性粒细胞减少(40%)、γ- 谷氨酰转移酶升高(40%)、外周
3. Brentuximab vedotin 联合方案
获批方案:brentuximab vedotin +
关键数据(Eschelon-3 研究,n=230):ORR/CR 率 64%/40%(vs R2 组 42%/19%),中位 OS 13.8 个月(vs R2 组 8.5 个月);
TEAEs:周围神经病变(20%,G3 4%)、中性粒细胞减少(46%)。
(三)其他获批方案
1. Tafasitamab + 来那度胺
机制:Tafasitamab(CD19 靶向 Fc 增强型单抗)+ 来那度胺(免疫调节);
关键数据(L-MIND 研究,n=81):ORR/CR 率 57.5%/40%,中位 PFS 11.6 个月,CR 患者 24 个月 OS 90.6%;
TEAEs:中性粒细胞减少(51%,G3+ 49%)、
2. Selinexor
机制:XPO1 抑制剂,抑制 MYC/BCL2 核输出;
关键数据(SADAL 研究,n=127):ORR/CR 率 28%/12%,中位 PFS 2.6 个月,中位 OS 9.1 个月;
TEAEs:血小板减少(61%)、恶心(58%)、疲劳(47%),70% 患者需剂量调整。
(一)CAR-T 细胞治疗
抗 CD19 CAR-T(axi-cel、liso-cel、tisa-cel)已改变 R/R DLBCL 治疗格局,目前 axi-cel 与 liso-cel 获批二线治疗(原发难治或 12 个月内复发),三者均需
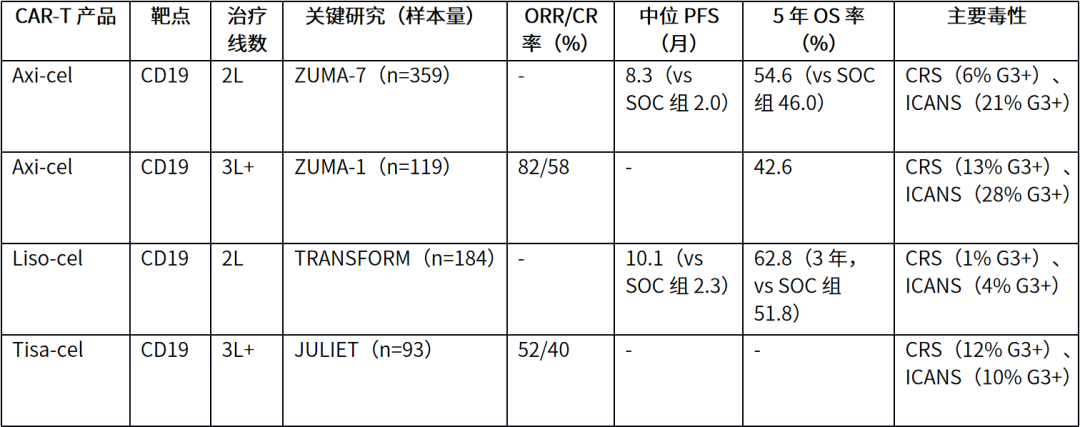
桥接治疗注意事项:
避免使用苯达莫司汀(可能降低 T 细胞采集效率,影响 CAR-T 疗效);
推荐方案:放疗(ORR 67%-100%,可改善 CAR-T 预后)、Pola-R(ORR 42%-54%)、loncastuximab(ORR 40%-63%)。
(二)造血干细胞移植
异基因造血干细胞移植(allo-SCT):适用人群:auto-SCT 或 CAR-T 治疗后进展患者;疗效:CR 患者 3 年 PFS 约 30%-40%,但非复发死亡率较高,需严格评估患者耐受性。
前沿探索:在研疗法与联合策略
(一)在研细胞疗法
双靶点 CAR-T:如 CD19/CD20(zamto-cel)、CD19/CD22(fricabtagene autoleucel),旨在降低抗原逃逸风险;例如fricabtagene autoleucel(CD22 靶向)在 4 线患者中 ORR/CR 率 68%/53%,3 年 OS 率 47%。
通用型 CAR-T/ CAR-NK:如 UCART19-ALLO-501(通用型 CD19 CAR-T)、FT596(iPSC 来源 CAR-NK),无需个体化制备,可快速给药;例如FT596(CD19 CAR-NK)在 I 期研究中 ORR 52%,无 ICANS 发生。
(二)在研非细胞疗法
新型 BsAbs:如新型CD19×CD3,使用低亲和力结合 CD3 以降低 CRS,在 4 线患者中 ORR/CR 率 43%/33%,CRS 均为 G1。新型CD20×CD3双抗plamotamab。
新型 ADC:如 zilovertamab vedotin(ROR1 靶向),在 II 期研究(n=98)中 ORR/CR 率 29%/13%,中位 PFS 2.5 个月。
CELMoD 药物:如 golcadomide(来那度胺类似物,更强降解 Ikaros/Aiolos)、iberdomide;Golcadomide 联合利妥昔单抗在 4 线患者中 ORR/CR 率 48%/30%,中位 DoR 8.3 个月。
(三)联合治疗策略
BsAbs + 化疗:如 glofitamab + GemOx(STARGLO 研究),ORR/CR 率 68.3%/58.5%,中位 OS 25.5 个月(vs GemOx 组 12.9 个月)。
BsAbs + ADC:如 glofitamab + polatuzumab,在 129 例患者中 ORR/CR 率 78.3%/59.7%,DHL/THL 患者 CR 率 65.9%。
多靶点联合:如 ViPOR 方案(venetoclax+ibrutinib +
临床管理建议
(一)治疗决策流程
复发确认:所有疑似复发患者需活检,评估 CD19/CD20 表达(指导治疗选择),排除感染、
分层治疗:
CAR-T/auto-SCT eligible:
12 个月复发:二线铂类化疗,敏感者行 auto-SCT;
原发难治或 < 12 个月复发:优先二线 CAR-T(axi-cel/liso-cel);
CAR-T/auto-SCT ineligible:
2L:Tafasitamab + 来那度胺、Pola-BR;
3L+:BsAbs、loncastuximab、BV-R2。
(二)生物标志物探索
疗效预测:CD20 表达缺失与 BsAbs 应答率降低相关;CD19 表达水平不影响 loncastuximab 疗效;
微小残留病(MRD):ctDNA 检测(灵敏度 10⁻⁶)可早期预测复发,治疗中 ctDNA 清除与 PFS 改善相关。
近 5 年,R/R DLBCL 治疗已从传统化疗转向精准免疫治疗,CAR-T、BsAbs、ADC 等疗法显著改善患者预后。但仍存在未解决问题:如缺乏头对头研究指导测序、高风险患者(DHL/THL、CAR-T 后早期复发)应答率低、生物标志物匮乏。未来需通过前瞻性研究验证联合策略疗效,开发多靶点疗法以克服耐药,推动 ctDNA-MRD 指导的个体化治疗。
参考文献:Allison M Bock, et al. J Hematol Oncol. 2025 Jul 1;18(1):68.
补充声明:本材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批号:CN-173905
过期日期:2026-03-15
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)