
本期配图来自2025年9月29日发表在European Journal of Medicinal Chemistry(IF 5.9)上的文章《Rational design of copper ionophores for efficient induction of cuproptosis via simple n-alkyl modification》[1]
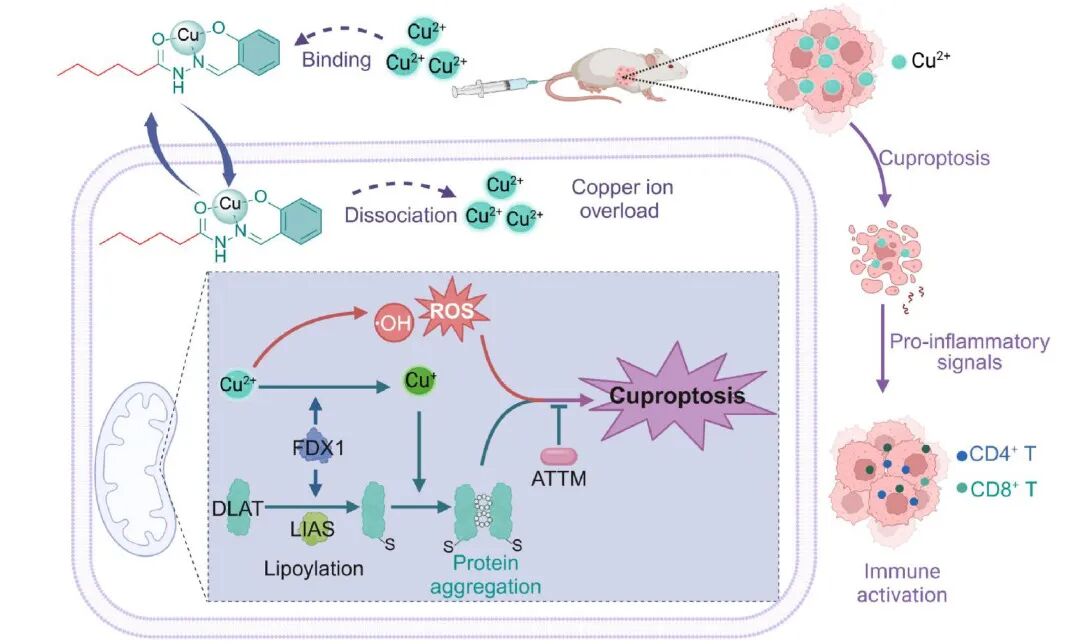
图1 N -烷基化修饰铜离子载体抗癌机制示意图[1]
图片展示了通过N -烷基化修饰设计高效铜离子载体(C6),借助铜离子超载(Copper ion overload)启动铜死亡(Cuproptosis)级联反应,同时联动肿瘤免疫激活(immune activation),为基于铜死亡的抗三阴性
铜离子的结合与释放
C6铜离子载体先与细胞外的Cu²⁺结合(Binding ),随后进入细胞并解离释放(Dissociation)Cu²⁺,导致细胞内铜离子超载(Copper ion overload)。
铜死亡的级联反应
Cu²⁺在线粒体这一强还原性环境内被还原为Cu⁺,进而产生羟基自由基(·OH)等活性氧(ROS)。该过程依赖FDX1(铁氧还蛋白 1)、DLAT(二氢脂酰胺 S - 乙酰基转移酶)、LIAS(脂酰胺合成酶)等蛋白,触发蛋白质脂酰化(Lipoylation),最终导致蛋白质聚集(Protein aggregation)。ROS的氧化损伤和蛋白质聚集的物理/代谢干扰共同作用,从结构和功能层面抑制了ATTM通路,最终引发铜死亡(Cuproptosis)。
免疫激活效应
铜死亡的肿瘤细胞会释放促炎信号(Pro-inflammatory signals),招募并激活CD4⁺ T细胞、CD8⁺ T细胞等免疫细胞,实现肿瘤免疫激活(immune activation)。
背景补充
金属稳态对维持细胞平衡至关重要。在本研究中,通过改变正烷基链长度设计了一系列铜离子载体,以探究其离子转运效率。在该系列载体中,C6即使在低外源铜浓度下也表现出最高的细胞离子转运效率。值得注意的是,C6通过铜离子诱导铜死亡发挥强效抗肿瘤活性,其机制与ROS水平升高及线粒体功能障碍相关。体内实验进一步表明,C6不仅具有强大的肿瘤抑制作用,还具备显著的免疫调节效应。综上,本研究提出了一种优化金属离子载体的简便策略,为开发靶向金属稳态的癌症免疫治疗药物提供了新见解。
参考文献:
Yu, L., Shen, Q., Xie, X., Ai, M., Li, Z., Wang, P., Zhu, Z., & Tan, C. (2025). Rational design of copper ionophores for efficient induction of cuproptosis via simple n-alkyl modification. European Journal of Medicinal Chemistry, 2025(5.9), 10.1016/j.ejmech.2025.118257. DOI: 10.1016/j.ejmech.2025.118257

往期推荐
阿帕替尼与
编辑:Sophia
审校:Luna
排版:Sophia
执行:Luna
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
