
译者|吴秋萍
编辑|秋天

关键词
抗真菌;生物膜;白色念珠菌;低温微针;药物递送;鼠李糖乳酸杆菌;益生菌。
1.引言
白色念珠菌(C.albicans,CA)是一种机会性真菌病原体,通常定植于健康个体的粘膜表面和皮肤。虽然它通常作为共生生物存在,但过度使用抗生素、
对益生菌日益增长的兴趣推动了对其治疗应用的研究,特别是在预防和治疗感染方面[12,13]。世界卫生组织将益生菌定义为活微生物,当摄入足够量时,可以提供健康益处,包括抗菌活性、免疫调节和增强的营养生物利用度[14]。益生菌与宿主微生物群相互作用,并通过免疫调节信号影响各种器官,包括肠道、大脑、肝脏、肺、皮肤和阴道。研究人员也在精神病学中探索它们在治疗情绪障碍、焦虑和抑郁方面的潜力[15]。益生菌,主要是
益生菌,如植物乳杆菌和
微针(MN)技术是一种新兴的微创透皮和靶向药物输送方法[25]。MN通过在角质层中创建临时微通道来促进小分子、蛋白质、外泌体、基因、金属离子、气体和纳米粒子的给药[[26],[27],[28]。然而,MN制造通常需要具有足够机械强度的材料才能成功穿透,通常是通过在相对较高的温度下(至少室温,通常为40°C,甚至更高)缓慢干燥来实现的。然而,细菌等活细胞对这些条件高度敏感,因此保持其存活率具有挑战性[29,30]。
冷冻微针(cryoMN)提供了一种有前景的替代方案。与传统的微针不同,冷冻微针由水或低浓度的水凝胶材料(如明胶和基质胶(细胞外基质模拟物))制成,不需要干燥过程,使其能够保持传统微针的成型保真度和渗透能力[31,32]。用冷冻培养基制成的冷冻微针已被探索用于输送活细胞,包括枯草芽孢杆菌和蛭弧菌[33,34],以及用于
在这项研究中,我们开发了装载有筛选出的益生菌菌株的延迟熔融冷冻微针,以克服现有益生菌制剂和冷冻微针递送方法的局限性(图示1)。益生菌菌株最初从乳制品、保健品和药品中分离出来,然后进行体外筛选,以鉴定对白色念珠菌具有抗真菌活性的最强菌株。然后将筛选出的益生菌通过明胶-透明质酸水凝胶支架装入新型延迟熔融冷冻微针系统中,形成双网络结构。这种创新的配方显著延迟了微针的熔化,在室温下保持尖端完整性超过10分钟,同时在4°C下保持结构完整性和细胞活力长达5天,从而实现了冷冻微针的无链运输。筛选出的益生菌显示出很强的抗真菌活性,通过直接抑制真菌或预防生物膜形成,有效抑制白色念珠菌生物膜。此外,在基于细胞的检测和深部白色念珠菌感染的小鼠模型中,负载益生菌的微针表现出很高的治疗效果和生物安全性,为抗真菌治疗提供了一种微创、冷冻链独立的替代方案。本研究建立了一种新型的基于益生菌的冷冻微针平台,提供了一种有前景的下一代抗真菌疗法,具有更高的稳定性、疗效和易用性。
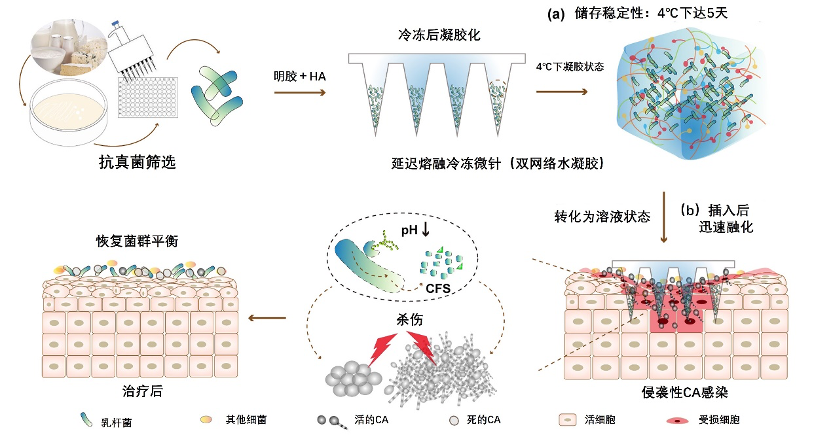
方案图示: 用于皮肤递送优化益生菌以对抗侵袭性白色念珠菌(CA)感染的延迟熔化冷冻微针(cryoMNs)的图示。冷冻微针是使用明胶与透明质酸(HA)作为支架材料结合形成交织的双网络水凝胶制成的,在冷藏条件下保持结构完整性和细胞活力长达5天(4°C)(a),允许进行冷冻无链运输。一旦插入皮肤,热响应性水凝胶针尖会迅速融化,将优化的益生菌输送到皮肤中,以有效治疗侵袭性白色念珠菌感染(b)。
2. 材料和方法
2.1 材料
明胶(来自牛皮,220PS8)是罗赛洛(温州)明胶有限公司(中国)赠送的礼物。透明质酸(HA,Mw 100-200 kDa)购自麦克林生化有限公司(中国)。沙氏
2.2 细菌种类和生长条件
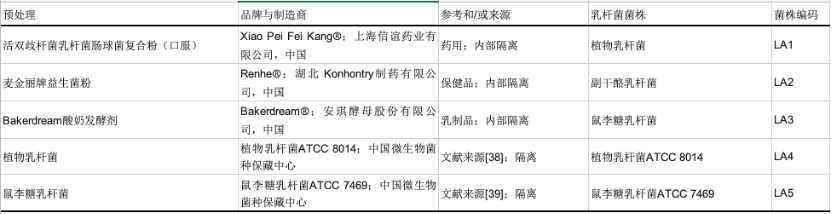
收集乳杆菌物种(列于表1中),并在37°C的厌氧条件下在MRS肉汤中培养。五种益生菌菌株中有三种是从常见来源分离出来的,包括牛奶、保健品和药品,而两种以白色念珠菌抑制特性而闻名的乳杆菌菌株[38,39]是从中国工业文化收藏中心获得的。通过添加
表1 益生菌菌株。
2.3 抗白色念珠菌益生菌菌株的筛选及生物活性
益生菌菌株在37°C下厌氧培养48小时。培养后,在4°C下以4000 rpm离心细菌培养物15分钟,然后通过0.22μm注射器过滤器过滤以消毒上清液,从而获得无细胞上清液(CFS)。根据临床和实验室标准研究所(CLSI)指南[42],通过微量滴定肉汤稀释法测定每种益生菌CFS对白色念珠菌的最小抑菌浓度(MIC)。在96孔板中,制备每种CFS的连续稀释液,并将其加入微孔板中培养的白色念珠菌(10^5菌落形成单位(CFU)/mL)中。将平板在37°C下孵育24小时,通过目视评估,MIC被确定为完全抑制白色念珠菌生长的最低浓度。此外,使用Synergy 2微孔板读数器(美国Bio-Tek)测量OD600,并计算抑制率。通过琼脂扩散法(牛津杯法)进一步评估抗真菌作用[43],其中将200μL CFS(100%,未稀释)加入预先接种白色念珠菌的SDA琼脂上的6mm直径牛津杯中。在37°C下孵育24小时后,测量抑制区的直径。
2.4 16S rDNA序列分析
每株菌株至少经过三轮纯化以确保其纯度,并通过16S rDNA测序进行鉴定。将得到的序列与国家生物技术信息中心(NCBI)的GenBank进行比对。为了构建系统发育树,使用MAGA 12程序通过邻居连接法对检索到的序列进行分析。该树基于16S rRNA核苷酸序列构建,整合了通过NCBI数据库中的BLAST搜索确定的最接近的同源序列。
2.5 MN PDMS模板的制作
不锈钢铜MN母模的基部直径为460μm,尖端间距为900μm,顶端高度为1000μm,排列成10×10阵列。为了制作阴模,将PDMS浇注在主模板上以复制其结构。在真空炉中脱气后,将PDMS在60°C下固化2小时,然后小心地从模板上剥离。
2.6 延迟熔融冷冻微针的制备
如文献[36]所述,CryoMN(延迟熔融冷冻微针)是通过离心法制造的。简而言之,将明胶和HA溶解在磷酸盐缓冲盐水(PBS)中,通过以4000 rpm离心3分钟将溶液倒入PDMS模具中。然后将模具在-20°C下冷冻过夜,并在相同温度下储存直至使用。使用不同的浓度和不同成分的明胶与HA质量比制备微针,以评估其熔融和机械性能。室温下微针尖端的熔化曲线由Cannon微距相机记录。通过测试微针穿透四层石蜡膜的能力来评估微针的机械强度。
2.7 益生菌负载冷冻微针的制备和表征
乳杆菌LA3菌株在体外表现出最佳的抗真菌效果,被选为制备负载益生菌的冷冻微针。简而言之,将LA3在MRS肉汤中培养24小时,然后通过离心(4000rpm,10分钟)收获。将细胞沉淀重新悬浮在含有2%明胶和1%HA混合物的微针培养基中。然后将所得悬浮液装入微针模具(每个阵列200μL),然后离心填充(4000 rpm,3分钟),以确保针腔内的精确分布。由于霉菌的空腔体积有限,部分益生菌沉淀物自然沉降到微针贴片的背衬层中。在给药过程中,将整个贴片(包括针阵列和背衬层)贴在感染的皮肤上。随着冷冻微针的融化,背衬层溶解,使其中的益生菌能够均匀地分布在治疗区域。因此,背衬层中的益生菌含量得以保留。填充模具后,加入适量的背衬层基质(2%明胶+1%HA),将完成的贴片在-20°C下冷冻直至使用。对于凝胶对照(LA3凝胶),将200μL相同的LA3悬浮液直接分配到无菌EP管中,并在-20°C下冷冻。两种制剂都含有相同浓度的LA3(超过109 CFU)。通过Cannon微距相机记录了人类手臂皮肤上微针尖端的熔化时间。根据制造商的说明,通过在MRS琼脂上平板并使用带有DMAO和PI的活/死细菌染色试剂盒来评估冷冻前后的细胞存活率。
2.8 穿透测试
用拇指将微针贴片压入1.5%(w/w)琼脂糖凝胶中,并在体外和体内小鼠皮肤中。渗透后,通过佳能数码相机对琼脂糖凝胶和小鼠皮肤进行成像。然后用4%多聚甲醛固定经微针处理的皮肤,并用苏木精和伊红(H&E)染色,以观察针通道。
2.9 运输稳定性模拟
通过模拟试验评估了LA3-微针在冷藏运输过程中的稳定性。为了复制冷藏运输条件,在整个冷冻过程中,将微针在4°C不同持续时间(0、1、3和5天)下运输。通过Cannon微距相机记录微针的形态,并通过将LA3细胞铺在MRS琼脂上评估其存活率。
2.10
收集新鲜大鼠血液,以1500rpm离心10分钟以分离红细胞(RBC),然后用PBS洗涤三次并重新悬浮以制备10%(v/v)RBC悬浮液。微针培养基(包含2%凝胶和1%HA)负载不同浓度的LA3,以PBS作为阴性对照,以蒸馏水作为阳性对照。接下来,将100μL的RBC悬浮液加入到900μL的每种样品混合物中,充分混合,在37°C下孵育2小时。然后将样品在3000 rpm下离心5分钟并拍照,在540 nm下测量吸光度以计算溶血率[29]。
2.11 自动聚集和共聚集分析
为了评估LA3是否可以与白色念珠菌共聚集,将2 mL白色念珠菌酵母(1×108 CFU/mL)和菌丝(1×106 CFU/mL)重新悬浮在PBS中,并将2 mL LA3在PBS中的悬浮液(109 CFU/mL)混合,在37°C下孵育4小时。还测试了LA3和白色念珠菌酵母和菌丝的自聚集性。在时间0(A0)和4小时后(A4)测量600nm处的吸光度。自聚集百分比通过方程式(1-A4/A0)×100%计算,共聚集通过以下方程式计算:
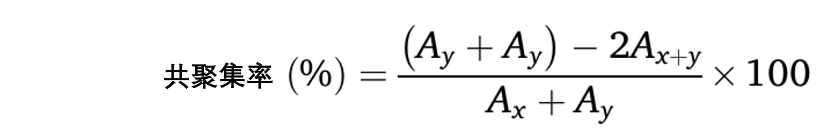
其中Ax和Ay表示每种微生物单独的吸光度值,Ax+y表示LA3和白色念珠菌的混合物的吸光度值[44]。
2.12 LA3对白念珠菌菌丝形成和聚集的影响
使用BeyoGold 35 mm共聚焦皿(直径14 mm;Beyotime,中国)进行丝状化分析[15]。简而言之,将1 mL添加了20%FBS的DMEM中的白色念珠菌接种到每个培养皿中,然后加入1 mL不同浓度的CFS,并补充MRS肉汤。作为阴性对照,白色念珠菌单独与MRS一起孵育。将培养皿在37°C和5%CO2中孵育4小时。孵育后,用200μL 荧光白(CW)过滤白色念珠菌细胞10分钟,并用PBS轻轻洗涤两次。通过奥林巴斯FV31-SPCOV共聚焦激光扫描显微镜(CLSM)观察真菌荧光。
对于聚集试验,将分散在含有10%FBS的YPD肉汤中的白色念珠菌与分散在含有10%FBS的MRS肉汤中的LA3细胞混合。阴性对照由白色念珠菌悬浮液组成,与仅含10%FBS的MRS肉汤一起孵育。将混合物在37°C下孵育4小时。然后按照与丝状化试验相同的方案观察白色念珠菌聚集体的形成。通过ImageJ软件计算每个样品中白色念珠菌聚集的面积(每个实验条件至少分析三个场)。
2.13 共培养试验
通过共培养试验评估LA3对白色念珠菌生长的影响[45],在该试验中,真菌与LA3一起或不与LA3孵育。简而言之,将5 mL MRS培养基中的LA3(107 CFU/mL)加入到EP管中,EP管中含有5 mL YPD肉汤中的白色念珠菌(105 CFU/mL。作为对照,白色念珠菌用无菌MRS肉汤(不含LA3)孵育,LA3用YPD肉汤(不含有白色念珠菌)孵育。培养物在37°C下孵育,CFU在0、12、24和48小时的时间点计数。以下培养基用于计数:白色念珠菌补充100mg/L
2.14 抗白色念珠菌生物膜试验
为了形成成熟的生物膜,将白色念珠菌(105 CFU/mL)分散在每100 mL补充3.453 g MOPS的RPMI 1640培养基中,并在37°C下静置培养24小时,以促进生物膜的形成[41]。通过0.1%结晶紫染色评估生物膜的形态,并进一步用钙氟白对真菌细胞进行染色,以便通过CLSM显示微观结构[46]。
对于生物膜破坏试验,成熟生物膜用不同浓度的CFS(0、0.4%、0.8%、1.6%、3.125%、6.25%、12.5%和50%)处理,MRS调节至pH 4.0(MRS pH 4.0),中和CFS(pH 6.5,50%)24小时。所有处理溶液均通过等体积混合MRS和RPMI 1640制备。处理后,用PBS轻轻洗涤孔3次,然后向每个孔中加入100μL 10%CCK-8,在黑暗中孵育4-8小时。通过酶标仪在450 nm处测量吸光度,以计算白色念珠菌生物膜的抑制率。此外,生物膜在共聚焦培养皿中培养24小时,用不同浓度的CFS处理24小时,然后用PBS洗涤三次,用活/死细菌染色试剂盒过滤。通过CLSM获取Z-stack图像,量化生物膜厚度,并通过ImageJ软件量化生物膜面积。
2.15 单层阴道和角质形成细胞模型的建立
使用两种人类细胞系,A431阴道上皮
2.16 细胞毒性试验
将白色念珠菌酵母(1×106 CFU/mL)、白色念珠菌菌丝(1×105 CFU/mL)和不同浓度的LA3(1×106,1×107和1×108 CFU/mL)共培养,采用CCK-8试验测试细胞毒性。以DMEM用作阴性对照。测量450nm处的吸光度以确定细胞存活率。此外,用含有钙黄绿素AM和PI的活/死细胞染色试剂盒对用LA3(1×108 CFU/mL)和MN培养基(2%明胶/1%HA)处理的细胞进行染色,并通过CLSM观察细胞活力。
2.17 基于HaCaT和A431细胞的粘附试验
粘附试验按照Santos等人[44]的描述进行。简而言之,收获微生物,用PBS洗涤两次,并重新悬浮在DMEM中,使LA3的最终浓度达到108 CFU/mL,白色念珠菌的最终浓度为106 CFU/mL。将每种悬浮液的1000μL等分试样加入相应的孔中,分组如下:LA3单培养对照、白色念珠菌单培养对照和LA3+白色念珠菌共培养组合。将平板在37°C和5%CO2中孵育2小时。孵育后,用PBS洗涤孔三次,去除非粘附微生物。然后用1 mL 0.05%Triton X-100裂解细胞,并将裂解物的系列稀释液分别接种在白色念珠菌的SDA琼脂和LA3的MRS琼脂上,以定量粘附微生物。细菌粘附定量为每孔lg(CFU)。对照组由单独与白色念珠菌孵育2小时的细胞组成,LA3处理的细胞的粘附率表示为相对于对照的百分比,对照设定为100%粘附。
2.18 体外感染试验
根据文献报告的程序进行体外感染试验,并稍作修改[44]。HaCaT或A431细胞在24孔板中培养至90%融合,然后分为五组:NC(阴性对照,仅DMEM)、CA菌丝(白色念珠菌菌丝感染)、LA3(单独使用益生菌LA3)和CA+LA3-sim。(同时添加LA3和白色念珠菌)和CA+LA3预处理。(白念珠菌感染前用LA3预处理2小时)。选择白色念珠菌菌丝进行感染是因为它们具有更强的侵袭能力和较低的增殖率,最大限度地减少了与益生菌对营养的竞争。对于感染程序,每个孔以1:1的感染复数(MOI)(白色念珠菌与细胞比)接受500μL的白色念珠菌菌丝悬浮液,然后在37°C、5%CO2下孵育6小时。在LA3治疗组中,按照两种不同的方案给药500μL益生菌悬浮液(MOI 100:1,细菌与细胞比):在真菌攻击前与宿主细胞预孵育2小时,或在感染开始期间与白色念珠菌接种物同时给药。孵育后,用PBS洗涤细胞三次,通过CCK-8测定法评估细胞存活率,细胞损伤以相对于NC组的百分比表示(设置为100%存活率)。此外,通过CLSM观察活性氧(ROS)水平,并用ImageJ进行半定量,以评估各组的抗氧化作用。
2.19 体内抗白色念珠菌感染试验
所有
2.20 统计分析
通过GraphPad Prism 8.0.1进行统计分析和绘图。数据以平均值±标准差的形式呈现。通过Student t检验对两组差异进行统计分析,并通过单因素方差分析(ANOVA)对多重比较进行统计分析。p<0.05的值被认为具有统计学意义(*p<0.05、**p<0.01、***p<0.001和****p<0.0001)。
结果
3.1 抗白色念珠菌益生菌的分离、纯化和筛选
3.1.1 益生菌候选菌株的分离纯化
益生菌被定义为给宿主带来健康益处的活微生物,如病原体拮抗、免疫调节和可持续的宿主定植,在面对日益增加的抗菌素耐药性时,益生菌已成为传统化学抗真菌药物的有前景的替代品[44]。为了鉴定具有最佳抗白色念珠菌功效的菌株,建立了一个全面的筛选平台(图1a)。选择了五种候选菌株,包括三种从乳制品来源分离的菌株和两种具有抗真菌活性的参考乳杆菌菌株(表1)。每株菌株都经过至少三代传代培养以确保纯度,随后通过16S rDNA测序进行鉴定。
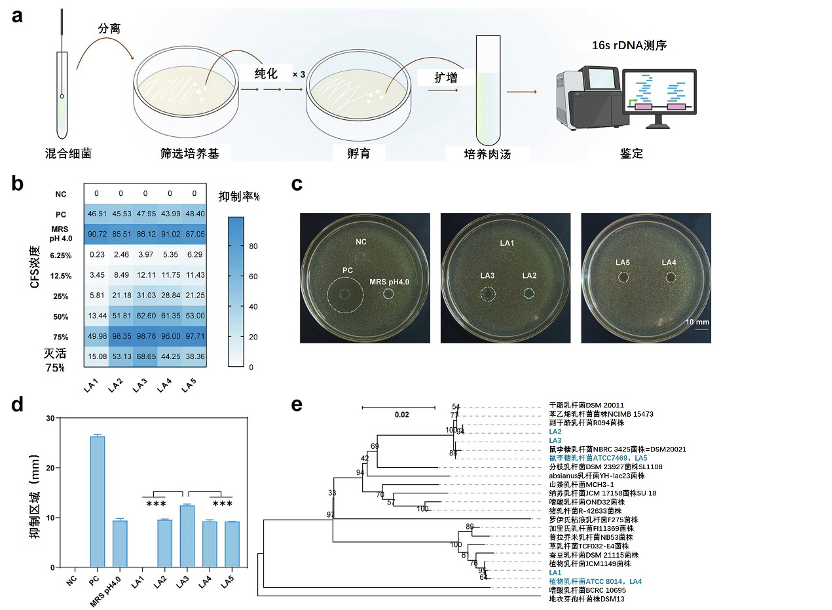
图1 抗白色念珠菌候选益生菌的筛选、纯化和鉴定。a)益生菌菌株的分离、纯化和鉴定的工作流程示意图。b-d)使用五种益生菌候选物的无细胞上清液(CFS)评估抗真菌潜力:b)通过肉汤微量稀释法测定对白念珠菌浮游物的最低抑菌浓度(MIC)值。相应的MIC图像如图S1所示;c)代表性图像(蓝色虚线圆圈表示杯放置,白色虚线圆圈表示抑制区)和d)通过牛津杯法对未稀释CFS的抑制区进行定量测量。原始测量数据列于表S2中。e)候选益生菌的系统发育分析:基于全长16S rDNA序列的邻居连接树。与NCBI参考菌株的同源性匹配详见表S1。未接种De Man、Rogosa和Sharpe(MRS)肉汤作为阴性对照,而用乳酸(MRS pH 4.0)和氟康唑(2.5μg/mL)调节至pH 4.0的肉汤作为阳性对照。数据以平均值±标准差表示(MIC测定n=5;抑制区测定n=3)。通过双侧非配对Student t检验确定统计显著性(***p<0.001,**p<0.01,*p<0.05)。(如需解释此图例中对颜色的引用,请参阅本文的网络版本。)
3.1.2 白念珠菌抗真菌活性筛选
鉴于其出色的安全性,针对白色念珠菌的体外抗真菌活性被优先作为关键筛选标准。从五种候选菌株中初步筛选CFS显示出浓度依赖性的抗真菌作用(图1b)。当浓度≥50%时,四株菌株(LA2-LA5)表现出强大的抗真菌活性,实现了超过50%的生长抑制,而LA1的效果很小(50%时抑制率为13.44%)。值得注意的是,即使在25%的浓度下,LA3和LA4也保持了显著的活性。通过牛津杯试验进行的进一步评估确定,LA3是最有希望产生12.46±0.21 mm抑制区的菌株,其表现优于LA4(植物乳酸杆菌ATCC 8014),后者的抑制区为9.24±0.23 mm(图1c和d)。由于主要筛选目标是确定最佳抗真菌菌株,因此跨浓度的综合MIC测试(图1b)证明了LA3的优越疗效。因此,抑制区评估采用100%CFS作为标准化浓度,以最佳地显示菌株特异性抗真菌潜力。
3.1.3 LA3的鉴定和系统发育特征
系统发育分析显示,鼠李糖乳酸杆菌(L.rhamnosus)分支中的LA3与角质形成细胞粘附参考菌株DSM 20021具有99.79%的16S rDNA同源性(表S1),已被证明可以减少
3.2 工程化制造延迟熔融冷冻微针支架用于益生菌递送
3.2.1 延迟熔融冷冻微针的制备与优化
虽然传统的冷冻微针能够通过冷冻以高存活率保留表皮益生菌,但它们的临床转化往往受到严格的冷冻链要求的限制。为了克服这一局限性,我们开发了一种延迟熔融的冷冻微针系统,该系统在标准制冷(4°C)下保持结构完整性和益生菌存活率(>90%),消除了冷冻的需要(图2)。创新之处在于仿生交织的双网络水凝胶设计,它模仿了天然生物膜基质。这种设计结合了蛋白质基质(明胶)和胞外多糖(HA)。明胶充当热响应支架,而HA动态调节水合作用。此外,水凝胶的RGD(Arg-Gly-Asp)基序(来自明胶)和CD44受体相互作用(来自HA)可能进一步促进成纤维细胞募集,这可以加速感染组织的伤口修复[50,51],作为抗真菌载体提供了另一个关键优势。

图2 延迟熔融冷冻微针支架的制备和表征。a)明胶-HA双网络水凝胶系统的结构设计示意图。b-d)明胶基质(2%w/v)中HA(0、0.5%、1%和2%w/v)的浓度优化:b)不同时间点熔融MN的代表性照片;c)室温下微针尖端熔化时间的定量分析;d)不同HA浓度下石蜡膜层渗透效率的比较评估。补充影片S1-4分别展示了含有0%、0.5%、1%和2%HA的微针在2%明胶基质中在室温下的熔化行为,而影片S5展示了2%明胶-1%HA制剂在人体手臂皮肤上的熔化动力学。对于模拟冷藏运输评估:e)模拟运输测试的示意性工作流程,f)微针的结构完整性分析,g)MRS琼脂平板上LA3的CFU计数,h)实验组之间LA3 CFU计数的统计比较,以及i)不同冷藏时间(0、1、3和5天)下LA3的存活率。数据以平均值±标准差的形式呈现(n=3)。通过双侧非配对Student t检验确定统计显著性(***p<0.001,**p<0.01,*p<0.05)。
牛源明胶因其天然来源、热可逆凝胶化和生物相容性而被选为主要的蛋白质基质。与合成水凝胶不同,明胶为细菌定植提供了最佳的微环境,同时在冷冻后保持了结构的稳健性[52]。明胶浓度的系统评估揭示了聚合物含量与功能性能之间的非线性关系(图S2)。在环境温度(25°C)下,将明胶浓度从0%(PBS对照)增加到2%(w/v),将针尖熔化时间从0.44分钟延长到2.07分钟。然而,将明胶浓度进一步增加到5%(w/v)仅略微改善了抗熔化时间(3.02分钟),但降低了石蜡膜测定中的渗透效率,第一层的成功率从99%降至77%。
为了在不影响机械强度的情况下增加抗熔化时间,我们将HA(100-200kDa)(一种具有内在水合调节特性的糖胺聚糖)掺入明胶基质中。由此产生的物理互穿网络表现出协同稳定作用(图2a)。渐进式HA掺入(0-2%,w/v)显著延长了尖端熔化时间,从2分钟(单独使用明胶)延长到室温下的10分钟以上(图2b、c和电影1-4),比PBS对照组提高了20倍。明胶和透明质酸之间的竞争性氢键被确定为关键的稳定机制,过量的透明质酸(2%透明质酸:2%明胶)会破坏冷冻凝胶化,使耐融化时间缩短56.1%。重要的是,这些增强并没有损害机械性能,正如石蜡膜分析中99%的渗透效率所证明的那样(图2d)。此外,优化的2%明胶/1%HA配方表现出优异的热响应性,在37°C下实现快速融化(皮肤温度;图S3和电影5),同时在环境温度下保持延迟融化(图2b),并在4°C下保持凝胶状态(图2f)。
3.2.2 模拟冷藏运输可行性评价
为了评估延迟熔化微针系统的冷藏运输可行性,我们进行了模拟运输研究,在最初的48小时冷冻期后,将微针置于4°C的冷藏中不同的时间(1-5天),然后恢复冷冻储存,直到累计9天的测试终点(图2e)。如图2f所示,针尖和背衬层在4°C下保持结构完整性长达5天。通过LA3的CFU计数评估的益生菌存活率显示出极好的保存效果(图2g-i):在4°C下放置一天后,存活率几乎保持不变(0.23 lg CFU/mL),仅在3天后略有下降(0.46 lg CFU/mL),5天后明显下降(0.64 lg CFU/mL)。值得注意的是,即使在冷藏5天后,存活率仍超过90%(9.16 lg/9.70 lg=94.4%),符合世界卫生组织益生菌稳定性指南,而对数比例减少率(0.13 lg CFU/天)与商业冷链依赖性制剂一致[53]。这些结果证实,延迟熔融冷冻微针可以承受冷藏运输至少24小时,而不会明显损失益生菌,在优化条件下稳定性延长至5天。
3.2.3 负载LA3的冷冻微针的制备与表征
针对益生菌装载,收获鼠李糖乳杆菌LA3,重新悬浮在微针培养基(2%明胶/1%HA)中,然后通过离心加入PDMS模具中(图3a)。大多数益生菌集中在微针尖端(图3b),用DiD标记细菌细胞膜进一步突显了它们的优先分布(图2f),这提高了药物输送的效率。在-20°C或-80°C下冷冻48小时后,与冷冻过程前相比,益生菌的存活率没有显著降低(图3c和d)。CFU计数显示,微针有效地保持了LA3的存活率,使CFU计数与冷冻前相当(图3c)。活/死细菌染色分析进一步证实了碘化丙啶(PI,死细胞)的最低荧光,而几乎所有细菌都显示出来自N,N-二甲基苯胺N-氧化物(DMAO,活细胞)的绿色荧光信号,这与冷冻前对照一致(图3d)。值得注意的是,即使没有冷冻保护剂,LA3在冷冻后仍保留了约90%的存活率,突显了LA3在基于冷冻微针的递送中的内在优势。

图3 负载LA3的冷冻微针的制备、穿透效率和表征。a)冷冻微针制造工作流程示意图。b)LA3-微针贴片(10×10阵列)的数字图像,图S4提供了微针模板的详细信息。c)在-20°c或-80°c下冷冻48小时前后LA3的CFU计数。d)通过活/死应变评估LA3细胞的存活率(活细胞:DMAO/绿色;死细胞:PI/红色)。e)琼脂糖凝胶渗透试验的代表性图像,显示微针介导的递送。f-g)冷冻微针在f)离体和g)体内小鼠背部皮肤模型中的透皮渗透曲线。h-i)h)离体和i)体内皮肤切片的组织学分析(h&E染色),显示LA3在微针产生的微通道内聚集。j)10分钟内负载LA3的冷冻微针在人体手臂皮肤上的熔化行为。k)不同浓度(0、107、108和109 CFU/mL)的负载LA3冷冻微针的溶血试验。数据以平均值±标准差的形式呈现(n=3)。通过双侧非配对Student t检验确定统计显著性(***p<0.001,**p<0.01,*p<0.05)。(如需解释此图例中对颜色的引用,请参阅本文的网络版本。)
此外,图3(e-i)显示了装载LA3的微针的卓越皮肤穿透能力。在琼脂糖凝胶平台上,DiD标记的益生菌负载微针保持了明确的阵列结构,正面和侧面清晰可见,证实了均匀的渗透(图3e)。当应用于离体小鼠皮肤时,微针会产生明显的微孔,在体内应用于小鼠背部皮肤会导致有效的插入和保留(图3f和g)。施用后,在皮肤上观察到可见的微针融化痕迹,H&E染色的组织切片显示了不同的插入通道,在递送部位有局部的益生菌簇(图3h和i)。进一步研究了微针在人体手臂皮肤上的熔化行为。如图3j所示,微针背衬层在5分钟内开始熔化,到10分钟时,与皮肤接触的大部分背衬层几乎完全熔化,导致针头塌陷。这一过程的发生速度明显快于室温下微针的熔化速度。鉴于皮肤的生理温度较高,微针针的尺寸较小,插入后的实际体内熔化速率预计会显著加快。此外,溶血试验和体内刺激性试验证实了明胶HA基质的优异生物相容性。即使在高LA3浓度(109 CFU/mL)下,溶血水平也保持在5%以下,与PBS对照组相比没有显著差异(图3k)。冷冻微针插入后,皮肤出现轻度发红,5分钟内明显消退,30分钟后几乎完全消退。微针留下的穿刺痕迹在应用10分钟后仅显示出轻微的压力痕迹,没有冻伤或皮肤损伤的迹象(图S5)。
总而言之,我们的延迟熔融冷冻微针系统比传统输送系统具有几个优点。与难以保持益生菌稳定性的传统凝胶或乳霜不同,我们的系统在冷冻条件下保持活力,确保益生菌的长期稳定性。此外,这种方法通过在针尖集中益生菌进行精确有效的沉积,克服了这些制剂的低输送效率。与目前的冷冻微针相比,我们的平台采用了含有明胶和HA的仿生双网络水凝胶设计,提高了冷冻条件下的稳定性和生物利用度。主要优点包括冷藏运输(0°C以上)长达5天,高局部输送效率,以及与生理条件一致的温度触发融化,使其成为皮肤局部益生菌输送的优越解决方案。
3.3 LA3对白色念珠菌的多模式抗真菌机制
3.3.1 共培养模型中的直接杀菌作用
鼠李糖乳杆菌(LA3)代表了一种双重作用的抗真菌策略,涉及营养竞争和代谢物介导的抑制。共培养实验表明,LA3直接抑制白色念珠菌的生长(图S6),在48小时内白色念珠菌CFU逐渐减少,从12小时的0.36 lg CFU/mL降至48小时的1.01 lg CFU/mL。有趣的是,虽然白色念珠菌生长受到抑制,但LA3本身增殖,表明营养耗竭和LA3代谢物(如短链脂肪酸和抗菌肽)的积累有助于这种抗真菌作用。
3.3.2 抗生物膜作用
为了进一步评估抗真菌活性,我们测试了48小时LA3培养物中的CFS对白色念珠菌浮游生长和生物膜破坏的抑制作用。如图1b-d所示,CFS有效地抑制了白色念珠菌的浮游生长。主要关注的是它破坏白色念珠菌生物膜的能力。结晶紫染色证实,在37°C的RPMI 1640培养基(3.453 g MOPS/100 mL)中培养24小时后,白色念珠菌形成了成熟的生物膜(A595>2),CLSM分析验证了生物膜的显著厚度和复杂形态(图S7)。用浓度增加的CFS处理成熟生物膜24小时,导致白色念珠菌生物量呈剂量依赖性减少(图4a-e)。CCK-8测定表明,随着CFS浓度从1.6%增加到50%,抑制率从18%增加到85%(图4c)。CLSM分析进一步表明,6.25%至50%的CFS浓度降低了生物膜面积和厚度,在50%CFS时,生物膜几乎完全破坏(图4a、b、d和e)。50%CFS下的活/死染色显示出最小的绿色(DMAO,活细胞)和主要的红色(PI,死细胞)信号,证实了广泛的细胞死亡。值得注意的是,中和CFS(pH 6.5)显著降低了其抗生物膜活性,而其对白色念珠菌浮游生长的抑制作用也出现了类似的减弱(图1b),这强烈表明有机酸是产生抗真菌作用的主要原因。此外,CFS表现出浓度依赖性选择性:虽然对浮游白色念珠菌表现出适度的抑制作用(12.5%CFS时存活率降低12%),但它实现了明显的生物膜破坏,导致相同浓度下66%的代谢抑制(CCK-8测定),并伴有明显的三维结构坍塌(与阴性对照相比,厚度减少40%,生物膜面积减少84.5%)。
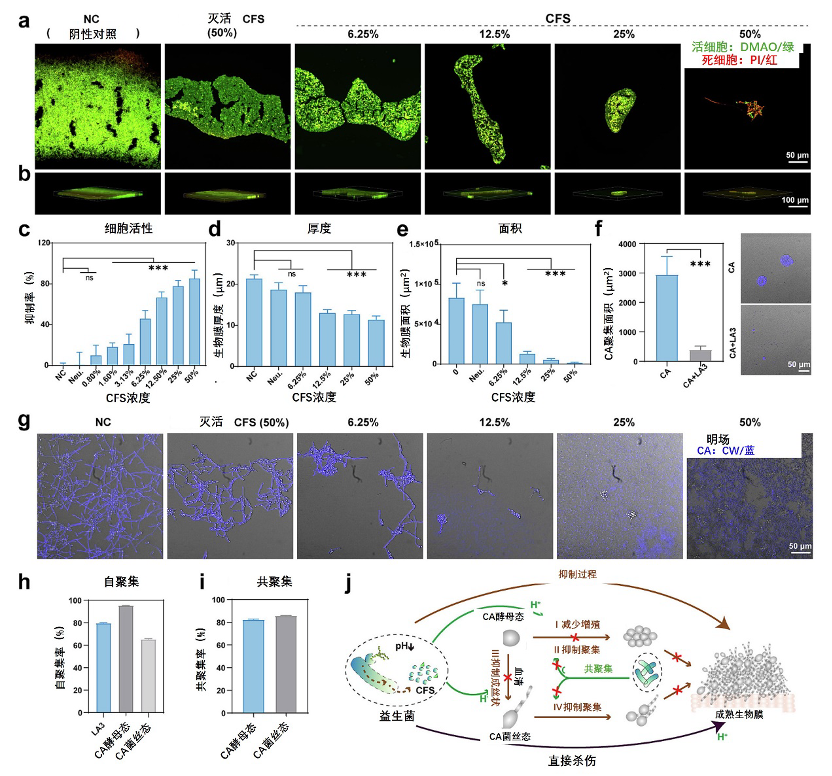
图4 LA3体外抗白色念珠菌的多模式抗真菌机制。a)代表性CLSM图像和b)用活/死存活试剂盒染色的生物膜的相应3D重建(活细胞:DMAO/绿色;死细胞:PI/红色)。c)通过CCK-8试验评估的用CFS(0-50%v/v)处理的成熟生物膜的代谢活性。生物膜的生物物理参数:d)厚度分布(Z轴量化)和e)投影面积(ImageJ分析)。f)在生物膜诱导条件下(在含10%FBS的培养基中37°C下4小时)白色念珠菌单培养物和与LA3共培养物的聚集特征。用荧光白(CW)对真菌细胞壁进行应变。g)不同CFS浓度(0、6.25%、12.5%、25%和50%)对共同培养4小时(37°C,5%CO2)后白色念珠菌菌丝形成的影响。h)自动聚集能力的定量分析和i)LA3、酵母和菌丝细胞之间的共聚集模式。j)说明LA3对抗白色念珠菌生物膜的生物学作用机制的示意图。数据以平均值±标准差的形式呈现(n=3)。通过双侧非配对Student t检验确定统计显著性(***p<0.001,**p<0.01,*p<0.05)。注:图4g中所有面板上观察到的微弱丝状结构可能是CLSM系统光路产生的成像伪影。这些伪影的位置是一致的,不会干扰数据解释。(如需解释此图例中对颜色的引用,请参阅本文的网络版本。)
3.3.3 LA3抗真菌活性的机制研究
除了破坏成熟的生物膜外,LA3还有效地抑制了白色念珠菌生物膜的形成,这主要与其形态发生锁定机制有关(图4f-j)。在生物膜诱导条件下共培养4小时,单独培养的白色念珠菌倾向于形成大聚集体和一些菌丝结构。相比之下,LA3的存在导致更小的簇或单个白色念珠菌酵母细胞,将白色念珠菌聚集面积减少到13.3%(图4f)。白色念珠菌酵母与LA3的共聚集率(82.4%)低于白色念珠菌自身聚集率(95.3%),表明LA3强烈粘附在白色念珠菌上,从而阻止了进一步的聚集和沉淀(图4h和i)。此外,用不同浓度的CFS处理白色念珠菌,并补充10%FBS(5%CO2,37°C),有效地防止了酵母向菌丝的转变(图4g)。在对照条件下(DMEM:MRS,1:1),几乎所有白色念珠菌在4小时后都转变为菌丝形式。随着CFS浓度的增加,菌丝结构减少。在6.25%CFS时,仅观察到少数具有几乎菌丝结构的酵母细胞;在12.5%的CFS中,酵母形式占主导地位;在25%的CFS时,几乎所有的白色念珠菌都保持酵母形式,并存在一些细胞片段。在50%的CFS时,发生了广泛的细胞破碎,只留下少数完整的酵母细胞。然而,中和CFS组与阴性对照组没有显著差异。这些观察结果强烈表明,白色念珠菌细胞活力的抑制和酵母向菌丝的转变主要是由于CFS中存在的有机酸。为了进一步确认有机酸的作用,我们使用用乳酸调节至pH 4.0的MRS肉汤来模拟CFS。如图S8所示,虽然高浓度(50%)酸化MRS肉汤显著抑制了白色念珠菌的形态转变,但与等浓度的CFS相比,低浓度(≤25%)MRS(pH 4.0)的抑制活性较弱。这种不同的疗效表明,CFS中的非酸性成分对其抗真菌作用的贡献超出了pH介导的抑制。
图4j展示了鼠李糖乳酸杆菌LA3对抗白色念珠菌的主要机制。LA3不仅通过酸性代谢物的直接作用破坏成熟的白色念珠菌生物膜,而且通过“粘附阻断”抑制生物膜的形成→pH值紊乱→代谢协同效应”级联。通过减少白色念珠菌酵母的自聚集和减少生物膜聚集,LA3有效地阻断了生物膜成熟所需的初始定植。这一发现与乳杆菌表面粘附素(如S层蛋白)竞争性抑制病原体与宿主相互作用的证据相一致[54,55]。LA3的CFS通过浓度依赖机制进一步抑制白色念珠菌的毒力。当浓度≥25%时,LA3-CFS抑制白色念珠菌丝状化并直接破坏膜的稳定性,导致真菌裂解,而较低浓度(<25%)抑制酵母到菌丝的转变。将MRS培养基调节至pH 4.0(模拟CFS)仅部分复制了低浓度CFS的效果,表明非酸性代谢物(如细菌素和过氧化氢)可能通过靶向麦角甾醇生物合成在群体感应干扰和氧化应激诱导中发挥作用[56]。这种多模式作用在50%CFS浓度下实现了强效的抗生物膜疗效,导致85.2%的代谢抑制,同时成熟生物膜生物量覆盖率降低了98.2%,超过了克霉唑等唑类药物的生物膜耐药性限制[8,10]。
3.4 LA3对白色念珠菌诱导的细胞损伤的保护作用
3.4.1 细胞相容性评价
从抗真菌检测过渡到细胞感染模型对于评估益生菌的治疗潜力至关重要。为了评估LA3对白色念珠菌诱导的细胞损伤的保护作用,我们利用了阴道上皮细胞(A431)和皮肤角质形成细胞(HaCaT)模型。与不同浓度的LA3共孵育8小时后,通过CCK-8试验评估细胞存活率和细胞毒性(图5a)。在1×106至1×108 CFU/mL的浓度范围内,LA3表现出优异的生物相容性,在两种细胞系中都保持了93%以上的存活率。相比之下,白色念珠菌感染诱导了形态依赖性细胞毒性:酵母细胞(1×106 CFU/mL)将HaCaT细胞的存活率降低到84.5%,将A431细胞的生存率降低到91.5%,而菌丝形式(1×105 CFU/mL)加剧了细胞损伤,将存活率分别降低到78.9%和85.3%。这些发现与之前强调菌丝形式更大毒力的报告一致[8,10]。活/死染色进一步证实了LA3的安全性(图5b),LA3处理组(1×108 CFU/mL)和微针培养基组均显示出主要的绿色荧光(钙黄绿素AM,活细胞)和最小的红色荧光(PI,死细胞),与阴性对照组相当。这种强大的安全性支持LA3作为减轻白色念珠菌相关角质形成细胞损伤的有前景的候选者。
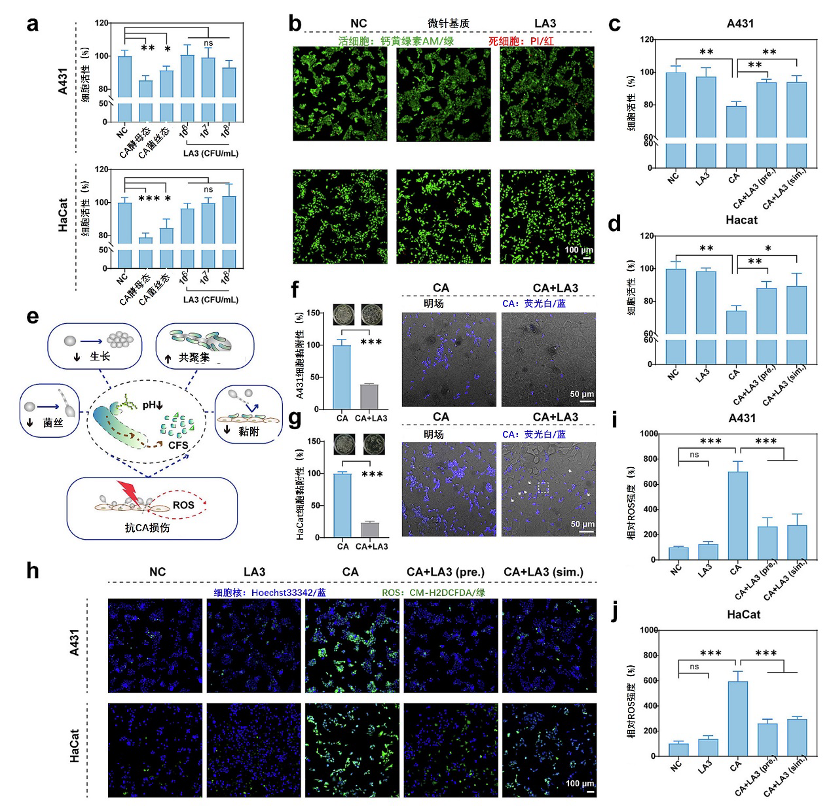
图5 LA3对白念珠菌诱导的细胞损伤的保护作用。a)A431和HaCaT细胞与LA3和白色念珠菌共培养8小时后的存活率和细胞毒性特征。b)A431和HaCaT细胞的活/死菌株与LA3或MN培养基共培养8小时(活细胞:钙黄绿素AM/绿色;死细胞:PI/红色)。在C)A431和d)HaCaT细胞中感染白色念珠菌菌丝6小时后,通过CCK-8试剂盒对每组进行存活率分析。e)LA3对抗白色念珠菌感染的拟议作用机制的示意图。LA3和白色念珠菌在f)A431和g)HaCaT细胞上的竞争性粘附试验:定量CFU计数显示微生物粘附竞争;显示真菌粘附的代表性CLSM图像(细胞壁用钙氟白色(CW)、蓝色染色)。h-j)感染上皮细胞中LA3对ROS的调节:h)A431和HaCaT细胞内ROS水平(CM-H2DCFDA,绿色)的CLSM可视化,以及i)A431与j)HaCaT的相对ROS强度的定量分析。数据以平均值±标准差的形式呈现(n=3)。通过双侧非配对Student t检验确定统计显著性(***p<0.001,**p<0.01,*p<0.05)。(如需解释此图例中对颜色的引用,请参阅本文的网络版本。)
3.4.2 防止白色念珠菌感染
鉴于白色念珠菌菌丝的细胞毒性作用比酵母形式更明显,我们选择了菌丝形式进行后续感染研究。白色念珠菌感染6小时后,A431细胞中的宿主细胞存活率降至80%以下(图5c),HaCaT细胞中降至75%(图5d)。然而,同时或作为2小时预处理的LA3给药,在HaCaT细胞中将菌丝诱导的存活率损失逆转至88%以上,在A431细胞中逆转至93%以上。这些发现突出了LA3的预防和治疗潜力。
3.4.3 细胞保护-黏附竞争和减轻ROS机制
LA3的保护作用似乎是多方面的,图5e阐明了这些保护作用的主要机制。与仅用白色念珠菌治疗的对照组相比,LA3显著降低了70-75%的白色念珠菌上皮黏附图5f和g),表明竞争性排斥是主要的防御机制。值得注意的是,HaCaT细胞比A431细胞表现出5%的真菌黏附,这与更大的存活率损失有关(78.9%对85.3%),表明细胞特异性受体相互作用可能会影响感染结果。共聚集试验表明,LA3对菌丝具有很强的亲和力,聚集率从65%(自动聚集,图4h)增加到86%(共聚集,图4i)。这种对菌丝入侵的物理阻断补充了之前证明的LA3对酵母向菌丝转变的抑制作用,LA3共同抑制了形态毒力因子。此外,DCFH-DA荧光定量显示,与感染相比,LA3治疗使HaCaT细胞中感染诱导的细胞内ROS减少了50%以上,A431细胞中减少了60%以上(图5h-j)。重要的是,单独使用LA3不会增加基线ROS水平,这证实了其具有靶向抗氧化活性,而不是非特异性细胞调节。
综上所述,这些发现表明,LA3通过多种机制保护宿主细胞免受白色念珠菌诱导的损伤,包括病原体排除、黏附介导的毒力抑制、酵母向菌丝过渡的抑制以及降低氧化应激。这种多模式的保护作用在预防和治疗背景下都能保持上皮细胞的活力。这些结果强调了LA3的治疗潜力,特别是当它通过延迟熔融冷冻微针系统输送时。
3.5 体内疗效
3.5.1 体内抗真菌疗效评估
这些体外益处在小鼠深部组织念珠菌感染模型中转化为显著的治疗效果。为了评估体内治疗效果,我们通过在背部区域多部位皮内注射白色念珠菌悬浮液(108 CFU/mL,50μL/小鼠)建立了一种侵袭性感染模型(图6a)。48小时后,通过真菌负荷定量(约7×107 CFU/g组织)、组织病理学分析显示PAS染色显示真皮菌丝入侵,以及h&E染色切片中明显的炎症浸润,证实感染成功(图S9)。LA3-微针实现了优异的真菌清除率,将真菌负担降低了98.3%(与模型相比,p<0.001),显著优于LA3凝胶(86.2%)和克霉唑乳膏对照(80.6%)(图6b和c)。大体形态评估支持了这些发现(图6d),因为微针治疗的小鼠表现出脓疱完全消退和最小的表皮鳞屑,而LA3凝胶组出现了一些残留鳞屑,克霉唑乳膏组出现了大量的表皮鳞垢。组织学分析进一步证实,LA3-微针恢复了近乎正常的皮肤结构,角质层完整,真皮胶原蛋白排列良好,而LA3凝胶治疗没有(H&E染色;图6e)。PAS染色(图6f)显示,微针处理样品中的白色念珠菌仅限于角质层(<20μm),而凝胶和克霉唑组均表现出更大的真菌穿透力(>80μm)。相比之下,未经治疗的模型组表现出广泛的皮肤侵袭(>500μm)。

图6 LA3-微针对白色念珠菌诱导的侵袭性感染的体内抗真菌效果。a)在小鼠中建立皮肤念珠菌病的实验时间线示意图。b-c)真菌负荷定量:b)对在沙氏葡萄糖琼脂(SDA)上培养的均质皮肤组织中的CFU进行统计分析,c)每组中具有代表性的SDA平板图像。d)显示各治疗组组织形态变化的代表性宏观图像。e)通过H&e染色进行组织病理学评估,揭示炎症浸润。f)过碘酸希夫(PAS)染色显示真菌菌丝渗透到真皮层。g-j)促炎细胞因子分析:g)IL-1β,h)TNF-α,i)ELISA定量的IL-6水平,j)相应的热图可视化,比较各组之间的细胞因子表达模式。数据以平均值±标准差的形式呈现(n=6)。通过双侧非配对Student t检验确定统计显著性(***p<0.001,**p<0.01,*p<0.05)。
3.5.2 直接抗真菌作用和免疫调节的潜在治疗机制
值得注意的是,LA3显示出抗真菌和免疫调节的双重治疗作用(图6g-j)。微针组的促炎细胞因子显著降低,IL-1β降低了74.6%(199.2至50.5 pg/mL),TNF-α降低了59.4%(45.4至18.4 pg/mL。与局部凝胶应用相比,这些增强的免疫调节作用与LA3皮肤定植增加10倍相关(图S10)。综合安全性评估证实,主要器官(心脏、肝脏、脾脏、肺和肾脏;图S11)没有组织病理学异常。
本研究介绍了一种双重创新策略:优化鼠李糖乳杆菌LA3作为多模式抗真菌药物的机制阐明,以及开发一种延迟熔融冷冻微针(MN)平台,该平台能够针对侵袭性白色念珠菌感染提供益生菌。虽然唑类药物仍然是一线抗真菌药物,但它们的局限性(包括肾毒性和对生物膜的疗效差)突显了对替代疗法的迫切需求[57]。相比之下,基于益生菌的干预措施具有独特的临床优势。LA3是体外筛选的五种乳杆菌中最有效的抗真菌菌株,通过多种多靶点机制表现出很强的抗真菌活性,特别是对生物膜。值得注意的是,根据报告[58],益生菌疗法可以选择性地抑制白色念珠菌,而不会破坏共生菌群,这是长期治疗安全性的关键特征。我们设计的延迟熔融冷冻微针平台通过使运输不依赖于冷冻链,进一步推进了传统的冷冻微针技术。这种综合策略为解决深部真菌感染提供了一种创新的解决方案。
尽管有这些优点,但仍然存在一些局限性。首先,尽管负载LA3的冷冻微针显示出优异的治疗效果,但其贴片尺寸(约1.2×1.2 cm2)小于感染病变面积(2×2 cm2)。虽然贴片一直应用于病变中心以最大限度地增加治疗接触,并且熔融背衬层的扩散可能有助于扩大益生菌的暴露面积,但这种空间不匹配仍然是一种方法学限制,需要在未来的设计中进行优化。其次,应该用额外的益生菌进一步评估冷冻微针平台,以评估其更广泛的适用性。此外,由于CFS活性部分依赖于pH值,因此需要全面的代谢组学分析来鉴定非酸性生物活性化合物(如细菌素)。此外,应进行宏基因组测序,以阐明LA3在念珠菌病治疗期间对皮肤微生物群的调节作用。通过将机理见解与创新的交付策略相结合,本研究为能够破坏生物膜和靶向深层感染的精确抗真菌干预奠定了基础。
4. 结论

*注:本文非广告,仅供专业人士作为学术交流目的阅读和参考,不具有商业推广或者服务目的。本文著作权归作者所有,如需转载,请联系编辑人员,对未经许可而进行复制或传播本文内容的行为,将依法追究责任。部分封面图像来源于网络,如有侵权,请联系删除。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)