
目录
1.1 肝细胞癌治疗进展:临床医生当前和不断发展的治疗方法概述 1.2 |
2.1 检查点抑制剂联合化疗对比单纯化疗在PD-L1低表达晚期胃癌患者一线治疗中的比较:系统综述与荟萃分析 2.2 Claudin-18亚型2特异性CAR T细胞疗法(satri-cel)对比医生选择的治疗方案治疗既往经治的晚期胃癌或胃食管交界处癌的疗效(CT041-ST-01):一项随机、开放标签、Ⅱ期临床试验 2.3 胃癌 2.4 一线免疫检查点抑制剂联合化疗治疗晚期胃癌和胃食管交界处癌:一项Ⅲ期临床试验的荟萃分析 |
Advances in the treatment of hepatocellular carcinoma: An overview of the current and evolving therapeutic landscape for clinicians
肝细胞癌治疗进展:临床医生当前和不断发展的治疗方法概述
Moris D, et al. CA Cancer J Clin. 2025 May 20.
中科院分区:1区 医学
IF:232.4
原文网址:https://acsjournals.onlinelibrary.wiley.com/doi/10.3322/caac.70018
肝细胞癌(HCC)是全球第六大常见恶性肿瘤,也是癌症相关死亡的第三大原因。近年来,全身治疗和局部区域治疗的进展推动了同行评审指南中关于系统治疗的更新,同时也带来了疾病分期降期的可能性,使部分晚期患者有机会接受肝部分切除术或移植达到根治的目标。本综述聚焦于HCC的所有治疗方式,以当今改变实践的随机数据为指导。本文讨论了HCC的外科治疗方法,包括肝切除和
Nivolumab plus ipilimumab versus lenvatinib or sorafenib as first-line treatment for unresectable hepatocellular carcinoma (CheckMate 9DW): an open-label, randomised, phase 3 trial
纳武利尤单抗+伊匹木单抗对比仑伐替尼或索拉非尼作为无法切除的肝细胞癌(Checkmate 9DW)的一线治疗:一个开放标签,随机,Ⅲ期试验
Yau T, et al. Lancet. 2025 May 24;405(10492):1851-1864.
中科院分区:1区 医学
IF:88.5
原文网址:https://linkinghub.elsevier.com/retrieve/pii/S0140-6736(25)00403-9
背景:对于不可切除的,预后评估较差的肝细胞癌患者而言,急需能够长期获益的治疗方案。此处报告CheckMate 9DW研究中的一项预先计划好的中期分析结果,评估了在不可切除的肝细胞癌的一线治疗中使用纳武利尤单抗+伊匹木单抗对比使用仑伐替尼或者索拉非尼的效果。
方法:这项开放标签、随机分组的Ⅲ期临床试验在亚洲、澳大利亚、欧洲、北美和南美的25个国家共163家医院和癌症中心招募了18岁及以上、未接受过系统治疗的不可切除肝细胞癌患者。入组患者需要至少具有一处根据实体瘤疗效评估标准(RECIST)1.1版可测量,未经治疗的病灶,Child-Pugh评分为5或6分,且东部肿瘤协作组(ECOG)体能状态评分为0或1。患者通过交互式响应技术系统按1:1比例随机分配至接受以下治疗:纳武利尤单抗(1 mg/kg)+伊匹木单抗(3 mg/kg)静脉注射,每3周一次,最多4次;之后继续给予纳武利尤单抗480 mg,每4周一次;或由研究者选择口服仑伐替尼(按体重每日8 mg或12 mg)或口服索拉非尼(每日两次,每次400 mg)。随机分组按病因学、是否存在大血管侵犯、肝外转移或两者兼有,以及基线甲胎蛋白水平进行分层。主要终点为总生存期,在所有随机分配的患者中评估。探索性终点为安全性作,在所有至少接受过一剂研究药物的随机分配的患者中评估。该试验注册于 ClinicalTrials.gov,注册号 NCT04039607(研究进行中)
结果:在2020年1月6日至2021年11月8日期间,共纳入668例患者随机分配至纳武利尤单抗+伊匹木单抗组(n=335)或者仑伐替尼/索拉非尼组(n=333)。在试验开始后的前6个月内,纳武利尤单抗+伊匹木单抗组的Kaplan-Meier总生存曲线早期出现交叉,反映出该组早期死亡人数较多(风险比1.65,95% CI 1.12–2.43),但随后曲线持续分离,呈现出纳武利尤单抗+伊匹木单抗组生存优势(风险比 0.61,95% CI 0.48–0.77)。中位随访35.2个月(四分位距:31.1–39.9个月)后,纳武利尤单抗+伊匹木单抗组的总生存期明显优于仑伐替尼/索拉非尼组,(中位总生存期23.7个月[95% CI 18.8–29.4] vs 中位总生存期20.6个月 [95% CI 17.5–22.5],风险比为0.79 [95% CI 0.65–0.96],双侧分层对数秩p=0.018),在24个月时总生存率分别为49%(95% CI 44–55)vs 39%(95% CI 34–45);在36个月时为38%(95% CI 32–43)vs 24%(95% CI 19–30)。总体而言,纳武利尤单抗+伊匹木单抗治疗组的332例患者中有137例(41%),以及仑伐替尼/索拉非尼治疗组的325例患者中有138例(42%)出现了3–4级治疗相关不良事件。纳武利尤单抗+伊匹木单抗组出现12例因治疗相关不良事件导致的死亡,仑伐替尼/索拉非尼组出现3例。
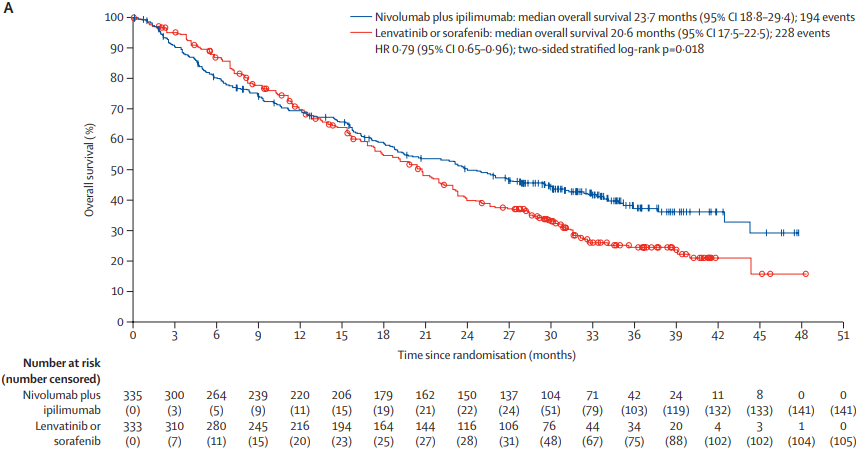
阐释:在既往未接受过系统治疗的不可切除肝细胞患者中,与仑伐替尼/索拉非尼相比,纳武利尤单抗+伊匹木单抗显示出显著的总生存期获益,且安全性可控。此研究结果支持纳武利尤单抗+伊匹木单抗作为这种情况下的一线治疗方案。
Toripalimab plus bevacizumab versus sorafenib as first-line treatment for advanced hepatocellular carcinoma (HEPATORCH): a randomised, open-label, phase 3 trial
特瑞普利单抗联合贝伐珠单抗对比索拉非尼一线治疗晚期肝细胞癌(HEPATORCH):随机、开放标签、Ⅲ期试验
Shi Y, et al. Lancet Gastroenterol Hepatol.
中科院分区:1区 医学
IF:38.6
原文网址:https://linkinghub.elsevier.com/retrieve/pii/S2468-1253(25)00059-7
背景: 尽管已经有几种PD-1或PD-L1抑制剂联合抗血管生成药物获批作为晚期肝细胞癌的一线治疗,但由于肝细胞癌的高发病率和死亡率,以及区域批准状态、医疗保险限制和成本考虑等因素,治疗需求仍未得到满足。在本项III期HEPATORCH研究中,旨在比较特瑞普利单抗联合贝伐珠单抗与索拉非尼在初治晚期肝细胞癌患者中的疗效和安全性。
方法:在中国大陆、台湾和新加坡的57家医院开展了一项随机、开放标签、III期研究。通过中央交互式网络响应系统,符合条件的18至75岁的不可切除或转移性肝细胞癌患者按1:1随机分配。通过分层区组随机化方法,接受240 mg特瑞普利单抗(静脉注射,每3周一次)联合15 mg/kg贝伐珠单抗(静脉注射,每3周一次)或400 mg索拉非尼(口服,每日两次)。随机分组按以下因素进行分层:大血管侵犯或肝外转移(有 vs 无)、ECOG体能状态评分(0 vs 1)以及局部区域治疗史(有 vs 无)。共同主要终点为无进展生存期(由独立评审委员会根据实体瘤疗效评估标准(RECIST)1.1版评估)和总生存期。在意向性治疗人群中进行疗效分析(即所有随机分配至治疗组的患者)。在所有至少接受过一剂研究药物的患者中评估安全性。该研究已在ClinicalTrials.gov注册,编号NCT04723004,并已完成。
结果:在2020年11月23日到2022年1月21日期间,545例患者接受了研究入组筛查,其中219例不符合筛查标准。326例患者被随机分配接受干预治疗:162例患者被分配至特瑞普利单抗联合贝伐珠单抗组,164例患者被分配至索拉非尼组,两组患者的中位年龄分别为58.0岁(四分位距50.0-66.0)和56.0岁(四分位距49.0-61.0)。所有326例患者均被纳入意向治疗人群以及安全性分析人群。282例(87%)为男性,44例(14%)为女性。在首次无进展生存期分析时(数据截止2022年8月10日),中位随访时间为9.4个月(四分位距7.0-12.0)与索拉非尼相比,特瑞普利单抗联合贝伐珠单抗显著延长了无进展生存期(中位时间 5.8个月 95% CI 4.6-7.2 vs 4.0个月 95% CI 2.8-4.2,风险比HR=0.69 95% CI 0.53-0.91; p=0.0086)。
在最终总生存期分析时(2024年5月31日),中位随访时间为16.4个月(四分位距 7.1-29.5) 特瑞普利单抗联合贝伐珠单抗组显著延长了总生存期(中位时间 20.0个月 95% CI 15.3–23.4 vs 14.5个月 95% CI 11.4–18.8,风险比 HR=0.76 95% CI 0.58–0.99;p=0.039)。特瑞普利单抗联合贝伐珠单抗组中有102例(63%)发生3级及以上治疗相关不良事件,索拉非尼组中有100例(61%)。特瑞普利单抗联合贝伐珠单抗组有21例(13.0%)导致停药,索拉非尼组有20例(12%)。治疗相关致死性不良事件的发生率在两组间相似,特瑞普利单抗联合贝伐珠单抗组发生2例(1%),索拉非尼组发生1例(1%)。特瑞普利单抗联合贝伐珠单抗组中,发生率≥5%的3–4级常见不良事件包括:
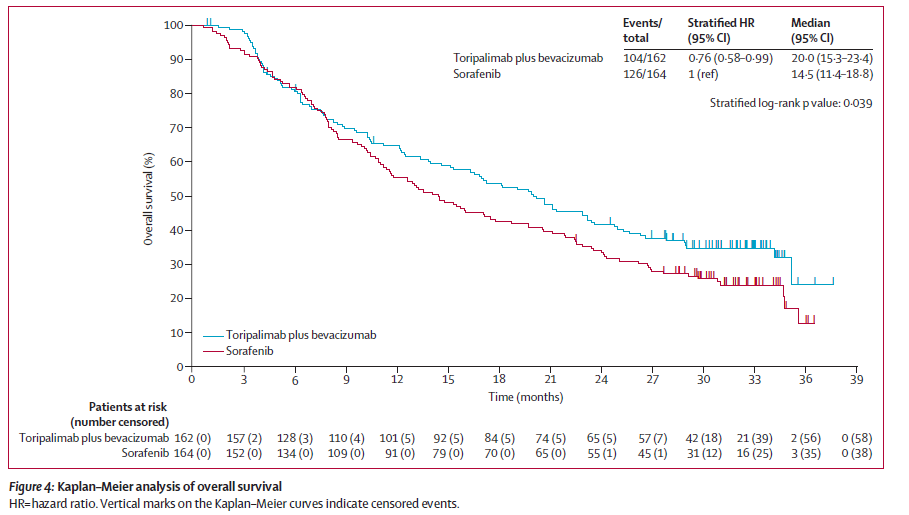
阐释:在初治的晚期肝细胞癌患者中,特瑞普利单抗联合贝伐珠单抗的无进展生存期和总生存期显著长于索拉非尼,且安全性可控。基于这些结果,国家医药产品监督管理局已批准该方案在中国使用。
Comparison of immune checkpoint inhibitors in combination with chemotherapy versus chemotherapy alone in the first-line treatment of advanced gastric cancer patients with low PD-L1 expression: a systematic review and meta-analysis
免疫检查点抑制剂联合化疗对比单纯化疗在PD-L1低表达晚期胃癌患者一线治疗中的比较:系统综述与荟萃分析
Wang Y, et al. Ther Adv Med Oncol. 2025 May 8;17:17588359251336627.
中科院分区:2区 医学
IF:4.2
原文网址:https://pmc.ncbi.nlm.nih.gov/articles/PMC12062602/
背景:免疫检查点抑制剂(ICI)联合化疗已成为人表皮生长因子受体2(her2)阴性胃癌(GC)的一线标准治疗方案。
目的:本研究旨在探讨ICI联合化疗是否能使程序性死亡配体1(PD-L1)低表达的患者获益。
设计:本研究是一项系统综述和荟萃分析。
数据来源:我们检索了PubMed、Embase、Web of Science和Cochrane图书馆,以及2019年至2024年欧洲肿瘤内科学会、美国癌症研究协会、美国临床肿瘤学会(ASCO)、ASCO胃肠道肿瘤研讨会(ASCO-GI)的年会资料,还有ClinicalTrials.gov数据库。
方法:本系统综述纳入了比较晚期胃癌一线免疫治疗联合化疗对比单纯化疗的III期随机对照试验。对于未报告PD-L1低表达人群数据的试验,采用KMSubtraction法估算生存数据。
结果:我们共纳入了九项随机临床试验。在综合阳性评分(CPS)<1和CPS<5的患者中,单克隆抗体联合化疗在总生存期(OS)或无进展生存期(PFS)方面未显示出改善(CPS<1 OS:风险比(HR)=0.91,95%置信区间[CI]:0.77-1.08;PFS:HR=0.88,95% CI:0.73-1.07.CPS<5 OS:HR=0.92,95% CI:0.79-1.08;PFS:HR=0.78,95% CI:0.53-1.14)。然而,在使用双抗体的试验中,PD-L1 CPS<5的患者在PFS方面有所改善(HR=0.64,95% CI:0.52-0.80)。在使用肿瘤区域阳性率(TAP)评分的试验中,TAP<5%的亚组在免疫治疗联合化疗后,OS或PFS未获益(OS:HR=0.92,95% CI:0.75-1.13;PFS:HR=0.91,95% CI:0.74-1.13)。
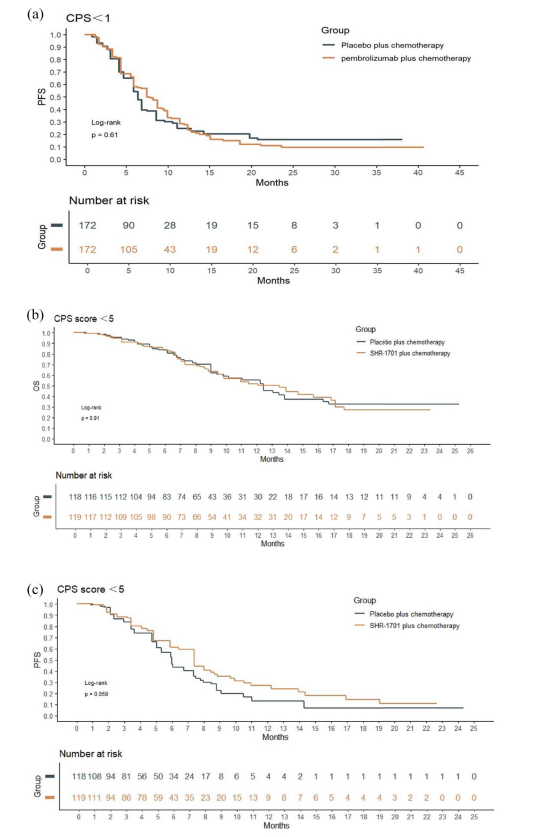
结论:我们的研究结果表明,在晚期胃癌的一线治疗中,与单纯化疗相比,单克隆抗体联合化疗不能使PD-L1低表达患者获得生存获益。然而,值得注意的是,在COMPASSION-15试验中,CPS<5的患者在OS和PFS方面有显著改善,这可能与双特异性抗体相关,需要进一步研究验证。
Claudin-18 isoform 2-specific CAR T-cell therapy (satri-cel) versus treatment of physician's choice for previously treated advanced gastric or gastro-oesophageal junction cancer (CT041-ST-01): a randomised, open-label, phase 2 trial
Claudin-18亚型2特异性CAR T细胞疗法(satri-cel)对比医生选择的治疗方案治疗既往经治的晚期胃癌或胃食管交界处癌的疗效(CT041-ST-01):一项随机、开放标签、Ⅱ期临床试验
Qi C, et al. Lancet. 2025 Jun 7;405(10494):2049-2060.
中科院分区:1区 医学
IF:88.5
原文网址:https://linkinghub.elsevier.com/retrieve/pii/S0140-6736(25)00860-8
背景:Claudin-18亚型2(CLDN18.2)已成为胃癌或胃食管交界处癌颇具前景的治疗靶点。Satricabtagene autoleucel(satri-cel;又名CT041)是一种自体CLDN18.2特异性嵌合抗原受体(CAR)T细胞疗法,在I期临床试验中,对既往接受过治疗的晚期胃癌或胃食管交界处癌患者显示出了显著疗效。在本文中,我们报告了II期关键试验(CT041-ST-01)的主要结果,该试验旨在研究satri-cel治疗胃癌或胃食管交界处癌的疗效和安全性。
方法:在中国开展的这项开放标签、多中心、随机对照试验中,将CLDN18.2阳性(免疫组化表达强度≥2 +且阳性肿瘤细胞≥40%)且既往对至少两线治疗耐药的晚期胃癌或胃食管交界处癌患者按2:1的比例随机分组,分别接受satri-cel治疗或医生选择的治疗方案(TPC)。在satri-cel组,satri-cel最多输注三次,每次剂量为250×10⁶个细胞。在TPC组,医生根据情况选择使用一种标准治疗药物(纳武利尤单抗、紫杉醇、多西他赛、伊立替康或Rivoceranib[阿帕替尼])。TPC组中出现疾病进展或药物不耐受的患者,若符合条件,可接受后续的satri-cel治疗。主要终点是意向治疗人群中由独立审查委员会评估的无进展生存期。本研究已在ClinicalTrials.gov注册(NCT04581473),不再招募新患者。
结果:2022年3月22日至2024年7月29日期间,共筛选了266例患者,其中156例被随机分配至satri-cel组(n=104)或TPC组(n=52)。satri-cel组88例(85%)患者和TPC组48例(92%)患者接受了研究药物治疗。在satri-cel组中,28例(27%)患者既往接受过三线或以上治疗,72例(69%)患者有腹膜转移。在TPC组中,10例(19%)患者既往接受过三线或以上治疗,31例(60%)患者有腹膜转移。根据反向Kaplan-Meier法,satri-cel组无进展生存期的中位随访时间为9.07个月(95%置信区间[CI] 6.21 - 13.01),TPC组为3.45个月(2.89-不可评估)。在意向治疗人群中,satri-cel组的中位无进展生存期为3.25个月(95% CI 2.86-4.53),TPC组为1.77个月(1.61-2.04)(风险比为0.37[95% CI 0.24-0.56];单侧log-rank检验p<0.0001)。在安全性分析集(所有至少接受过一剂研究药物的患者)中,satri-cel组88例患者中有87例(99%)发生了3级或以上治疗期间不良事件,TPC组48例患者中有30例(63%)发生了相关事件。satri-cel组中最常见的3级或更严重的治疗相关不良事件为淋巴细胞计数减少(88例患者中有86例[98%])、白细胞计数减少(68例[77%])和中性粒细胞计数减少(58例[66%])。satri-cel组88例患者中有84例(95%)发生了细胞因子释放综合征。
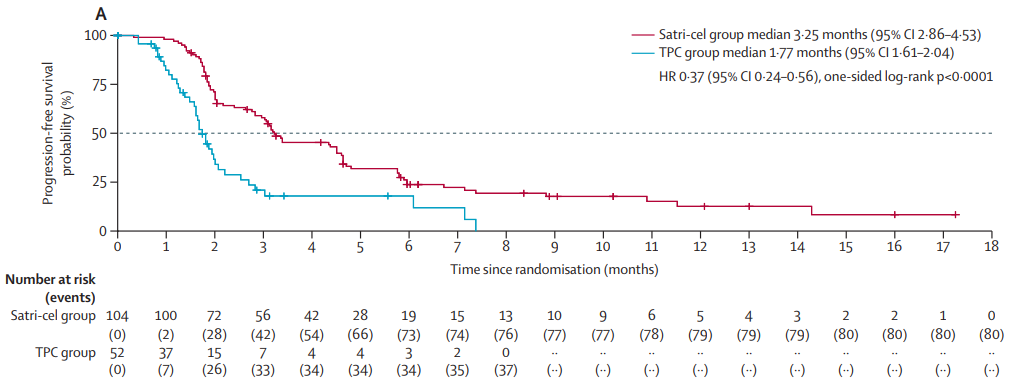
解读:这是全球首个在实体瘤中开展的CAR T细胞疗法随机对照试验。Satri-cel治疗显著改善了无进展生存期,且安全性可控。这些结果支持satri-cel作为晚期胃癌或胃食管交界处癌患者的新型三线治疗方案。
Gastric cancer
胃癌
Sundar R, et al. Lancet. 2025 Jun 7;405(10494):2087-2102.
中科院分区:1区 医学
IF:88.5
原文网址:https://www.sciencedirect.com/science/article/pii/S0140673625000522?via%3Dihub
胃癌仍然是全球重大的健康挑战,每年新增病例近100万例,导致超过65万例死亡。从流行病学角度来看,胃癌的发病率存在显著的地域差异,在亚洲、南美洲和东欧地区发病率较高,且50岁以下人群中早发性病例迅速增加。胃癌的主要危险因素包括幽门螺旋杆菌感染、饮食、肥胖、吸烟和遗传易感性。通过全面的诊断程序进行早期检测对于优化治疗结局至关重要。局部晚期胃癌的标准治疗方法包括手术切除,特别是D2淋巴结切除术,并辅以化疗和放疗。对于可切除的疾病,越来越多地采用微创手术技术;对于晚期疾病,则将免疫检查点抑制剂和靶向治疗相结合。新兴疗法,如新型靶向治疗和下一代免疫疗法,有望改善患者的生存率和生活质量。未来胃癌治疗的方向侧重于精准医学、免疫疗法的持续发展、新型早期检测方法以及多学科综合治疗。这些策略旨在提高全球范围内治疗的整体疗效和改善预后。
First-line immune checkpoint inhibitors with chemotherapy in advanced gastric and gastroesophageal junction adenocarcinoma: a meta-analysis of phase 3 trials
一线免疫检查点抑制剂联合化疗治疗晚期胃癌和胃食管交界处癌:一项Ⅲ期临床试验的荟萃分析
Lin Y, et al. Front Immunol. 2025 May 2;16:1564604.
中科院分区:2区 医学
IF:5.9
原文网址:https://pmc.ncbi.nlm.nih.gov/articles/PMC12081356/
背景:在过去几年中,免疫检查点抑制剂(ICI)与化疗(CT)方案的联合应用已成为晚期胃癌和胃食管交界处(G/GEJ)腺癌临床研究的关键焦点。近期III期试验得出了差异化的结果,引发了肿瘤学界的广泛讨论。针对这些不同的研究结果,我们进行了一项荟萃分析,以评估该策略的疗效和安全性特征。
方法:截至2024年12月15日,我们对PubMed和主要会议记录开展了系统性文献检索。对于疗效评估,计算了无进展生存期(PFS)和总生存期(OS)的汇总风险比(HR),以及客观缓解率(ORR)的比值比(OR);对于安全性评估,评估了不良事件(AE)的相对风险(RR)。
结果:分析了九项III期临床试验,包括KEYNOTE-062、CheckMate 649、ATTRACTION-4、ORIENT-16、GEMSTONE-303、KEYNOTE-811、KEYNOTE-859、RATIONALE-305和COMPASSION-15,共纳入7825例患者。与单纯CT治疗相比,ICI联合CT治疗的PFS(HR,0.71;95%置信区间[CI],0.65-0.79)、OS(HR,0.79;95% CI,0.75-0.83)显著延长,ORR(OR,1.57;95% CI,1.43-1.72)更高。然而,这种联合治疗增加了3-5级AE(RR,1.15;95% CI,1.09-1.22)和严重AE(RR,1.44;95% CI,1.21-1.70)的发生风险。
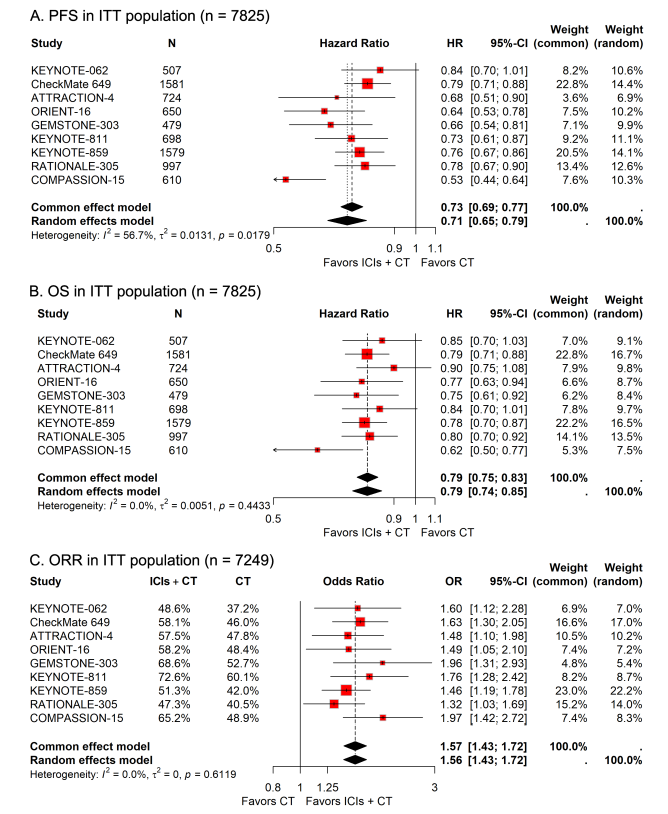
结论:对于晚期G/GEJ腺癌患者,在CT方案中联合ICI作为一线治疗相较于单纯CT的疗效更具优效性,但会增加毒性风险。在有多种治疗策略可供选择的情况下,药物安全性特征可以指导临床医生为更有可能从特定治疗策略中获益的患者选择更合适的干预措施。
声明:本材料由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
审批号:CN-170031
有效期:2026-10-27
审核:Aurora
排版:Aurora
执行:Aurora

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)