前言
随着表皮生长因子受体(EGFR)突变晚期
唐可京 教授
中山大学附属第一医院
呼吸与危重症医学科副主任、药学部主任/党总支部书记、感染性疾病科主任
医学博士,主任医师,博士生导师,博士后合作导师
中山一院肺癌MDT首席专家,Ⅲ期肺癌多学科联合规范化诊疗中心、肺癌诊疗一体化中心、肿瘤免疫治疗不良反应MDT团队负责人
美国范德堡(Vanderbilt) 大学医学中心访问学者
美国德州大学西南医学中心(UTSW) Harold C. Simmons综合癌症中心访问科学家
中国医师协会呼吸医师分会肺癌工作委员会委员
中国肺癌防治联盟免疫治疗委员会常委
中国抗癌协会个案管理专业委员会常务委员
中国初级卫生保健基金会胸部肿瘤精准治疗专委会常务委员
广东省医学会呼吸病学分会副主任委员
广东省医学会临床药学分会副主任委员
广东省医学会肺部肿瘤学分会常务委员
广东省临床试验协会(GACT / CTONG)理事
广东省医师协会临床试验专业委员会副主任委员
广东省医师协会呼吸科医师分会常务委员,感染与重症专业工作组组长

多线布局,多点突破:埃万妥单抗斩获EGFR突变NSCLC领域多项适应证
随着精准诊疗的逐步深入,NSCLC的治疗已进入基于驱动基因突变的分子分型时代。EGFR突变是NSCLC最常见的驱动基因突变,围绕着EGFR突变患者的精准治疗策略不断丰富。在这一进程中,埃万妥单抗以其独特的EGFR/c-MET双重阻断机制,突破了传统EGFR-TKI治疗的局限性。通过同时结合EGFR与c-MET受体,埃万妥单抗同时阻断EGFR和MET信号通路,同时可介导EGFR和MET的内化和降解、且具有免疫细胞导向活性等多重作用机制,不仅能够抑制EGFR常见敏感突变及20号外显子插入突变(EGFR 20ins)的相关信号通路,还可有效克服部分耐药机制,展现出广谱且持久的抗肿瘤活性[1-2]。
基于这一创新机制,多项关键临床研究进一步验证了埃万妥单抗在EGFR突变晚期NSCLC中的临床价值。MARIPOSA研究评估了埃万妥单抗联合兰泽替尼对比
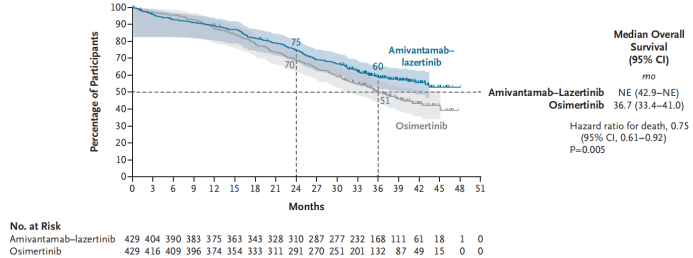
图1. MARIPOSA研究OS结果
基于这些坚实的循证证据,埃万妥单抗在2025年收获颇丰,在中国陆续获批三大适应证:联合化疗一线治疗EGFR 20ins突变晚期NSCLC、联合化疗治疗EGFR-TKI耐药的EGFR突变晚期NSCLC,以及联合兰泽替尼一线治疗EGFR敏感突变晚期NSCLC。三项获批覆盖了EGFR突变晚期NSCLC患者的多个亚型及治疗阶段,不仅为临床提供了疗效显著、安全性可管理的治疗新选择,也进一步明确了埃万妥单抗在EGFR突变NSCLC精准治疗领域的核心地位。

剂型优化,高效便捷:埃万妥单抗皮下注射剂型开启临床管理新篇章
《“健康中国2030”规划纲要》明确指出,到2030年,要实现全人群、全生命周期的慢性病健康管理,同时将总体癌症的5年生存率提高15%。其中,推动肿瘤慢病化管理成为国家医疗改革的核心议题。在EGFR突变晚期NSCLC患者生存获益不断提升的同时,如何进一步优化治疗体验并推动肿瘤治疗逐步向慢性疾病管理模式转变,已成为当前临床关注的重点。在肿瘤治疗领域,皮下注射剂型的开发已成为重要的发展趋势,目前已有多款免疫检查点抑制剂、抗HER2抗体开发了皮下注射剂型。通过简化给药操作、缩短治疗时间,皮下给药方案不仅优化了患者的治疗体验,也提升了临床管理的效率和治疗的可及性,将“以患者为中心”的治疗理念转化为更加可行的临床实践。埃万妥单抗皮下注射剂型的推出契合这一趋势,该剂型基于ENHANZE药物递送技术,通过重组人
PALOMA-3研究是一项国际多中心Ⅲ期临床研究,旨在评估埃万妥单抗皮下注射(SC)vs 静脉注射(IV)联合兰泽替尼治疗奥希替尼和铂类化疗后进展的EGFR突变晚期NSCLC患者的药代动力学(PK)、疗效和安全性[9]。
SC组(n=206)对比IV组(n=212)具有非劣效的PK及客观缓解率(ORR)。SC组与IV组在C2D1以及C4D1时稳态谷浓度的几何平均比(GMR)分别为1.15和1.43。两周期(第1天至第15天)曲线下面积(AUCD1-D15)GMR为1.03,达到非劣效标准;SC组与IV组ORR分别为30%和33% (RR=0.92,P=0.001)。此外,相较IV组,SC组在中位缓解持续时间(DoR)上数值更优(11.2个月 vs 8.3个月),SC组中位PFS也呈现获益趋势(6.1个月 vs 4.3个月,HR=0.84,95%CI:0.64-1.10,P=0.20),且SC组较IV组降低了38%死亡风险(12.9个月 vs NE,HR=0.62,95%CI:0.42-0.92,P=0.02)(图2)。
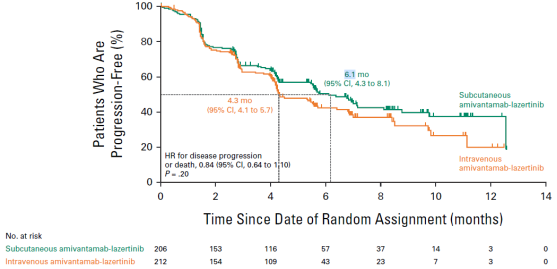
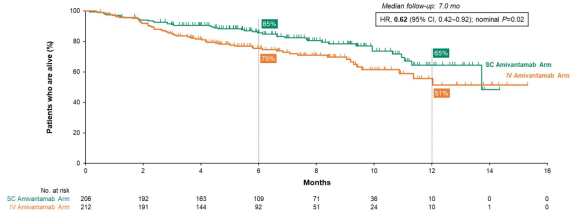
图2. PALOMA-3研究OS结果
在安全性方面,SC组的输液相关反应(IRR)发生率仅为IV组的五分之一(13% vs 66%),且SC组的静脉血栓栓塞症(VTE)发生率为9%,预防性抗凝治疗安全可行(图3)。
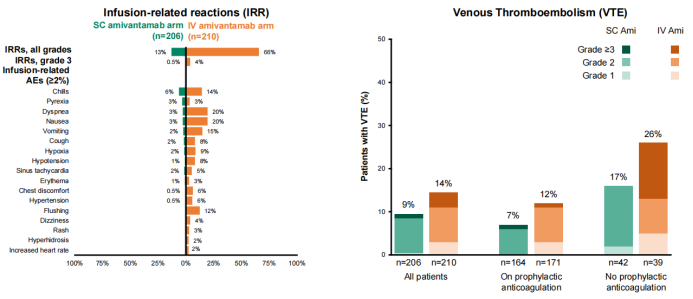
图3. PALOMA-3研究IRR及VTE
在给药便利性方面,SC组的平均给药时间小于5分钟,显著短于IV组的5小时。SC组的患者在输液椅上的停留时间更短(C1D1:0.4 vs 6.5小时;C3D1:0.6 vs 3.4小时)(图4)[10]。研究中85%患者认为SC剂型“方便”或“非常方便”。此外,亚洲人群亚组中SC剂型取得了与总人群一致的疗效和安全性获益[11]。
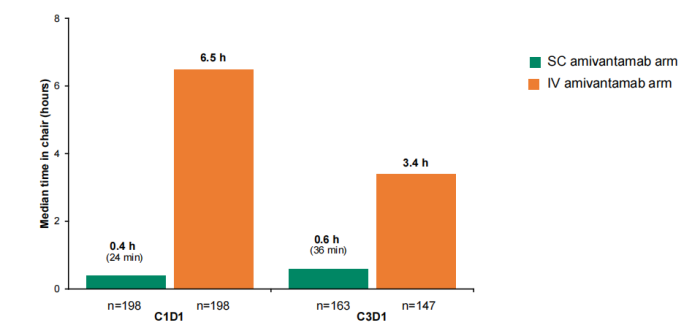
图4. PALOMA-3研究:坐在输液椅上的时间
PALOMA-2研究则评估了埃万妥单抗SC剂型(联合化疗和/或兰泽替尼)用于不同EGFR突变晚期NSCLC的疗效、药代动力学和安全性。该研究计划入组约520例EGFR突变晚期NSCLC患者,覆盖EGFR突变NSCLC的多个亚型及治疗阶段。其中,队列1纳入EGFR敏感突变一线治疗患者(对应MARIPOSA研究人群);队列2纳入EGFR 20ins突变一线治疗患者(对应PAPILLON研究人群);队列3和3b纳入经奥希替尼治疗后进展的EGFR突变患者(对应MARIPOSA-2研究人群);队列4观察了从IV剂型转换至SC剂型的疗效和安全性;队列5评估了埃万妥单抗SC剂型Q4W给药方案一线治疗EGFR敏感突变患者(对应MARIPOSA研究人群);队列6评估了埃万妥单抗SC剂型联合兰泽替尼在强制预防性抗凝条件下一线治疗EGFR敏感突变患者(对应MARIPOSA研究人群);队列7评估了埃万妥单抗SC剂型联合化疗治疗MARIPOSA方案一线治疗后的EGFR敏感突变患者(图5)。
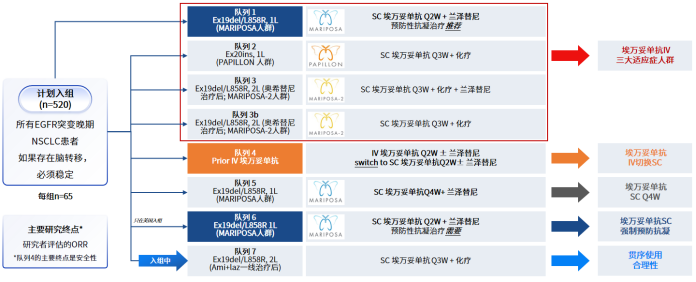
图5. PALOMA-2研究设计
在队列1及队列6中(对应MARIPOSA研究人群)[12],采用埃万妥单抗SC剂型(Q2W)联合兰泽替尼一线治疗EGFR敏感突变晚期NSCLC患者,显示出与MARIPOSA研究中埃万妥单抗IV剂型联合兰泽替尼相当的应答率,同时安全性进一步改善,给药相关反应(ARR)和VTE发生率显著降低至15%和13%,提示皮下注射给药在保持疗效的同时具备更佳的临床便利性和耐受性。
在队列5中(对应MARIPOSA研究人群)[13],采用埃万妥单抗SC剂型Q4W给药方案联合兰泽替尼一线治疗EGFR敏感突变晚期NSCLC患者同样显示出疗效、安全性和便捷性优势。研究者评估的ORR达82%,独立中心审查(ICR)评估ORR为87%。
在队列2中(对应PAPILLON研究人群)[14],采用埃万妥单抗SC剂型联合化疗一线治疗EGFR 20ins突变晚期NSCLC患者,研究者评估ORR为76%,ICR评估ORR为77%,显示出与PAPILLON研究中埃万妥单抗IV剂型联合化疗一致的应答率,且ARR发生率仅为6%。
在队列3b中(对应MARIPOSA-2研究人群)[15],采用埃万妥单抗SC剂型联合化疗治疗奥希替尼治疗后进展的EGFR突变晚期NSCLC患者,研究者评估的ORR为47%,ICR评估的ORR为53%;中位PFS为7.9个月,中位OS尚未达到。该结果与MARIPOSA-2研究中埃万妥单抗IV剂型联合化疗的疗效相当
在队列4中[16],患者从埃万妥单抗IV剂型转换至埃万妥单抗SC剂型,其安全性特征与既往观察到的相似,且未发现新的安全性信号,表明从IV剂型转换为SC剂型治疗是安全可行的。此外,PK模拟结果显示,在Q2W、Q3W及Q4W的给药方案下,埃万妥单抗IV剂型与SC剂型的暴露量总体上具有非劣效性,进一步支持了IV到SC转换的可行性。
总体而言,埃万妥单抗SC剂型在PALOMA系列研究中不断被验证。Ⅰ期研究主要评估了埃万妥单抗SC剂型的剂量和安全性,为后续研究奠定基础。而PALOMA-2 & 3则分别评估了埃万妥单抗SC剂型不同联合方案的可行性,以及对比IV剂型的药代动力学和疗效,形成了从剂量安全性探索到疗效验证的完整循证链条。
PALOMA系列研究显示,埃万妥单抗SC剂型在保持IV剂型疗效和安全性的同时,实现了显著的给药便捷性和优化了患者体验,为埃万妥单抗SC剂型的临床应用提供了坚实的循证支持。传统的静脉输注需时较长且存在输注相关反应风险,而SC给药仅需几分钟即可完成,大幅缩短治疗时间(C1D1:4.8分钟 vs 5.0小时)[9],减轻患者就医负担,显著提升了治疗的便捷性和可及性。这一创新剂型不仅优化了临床操作流程,也有助于推动肺癌管理向“慢病长期管理”模式转型。更为关键的是,这一便利性建立在MARIPOSA研究、PAPILLON研究和MARIPOSA-2研究已验证的卓越疗效基础之上,SC剂型的推出不仅使高效治疗更易于长期坚持,也有助于提升整体依从性和疗效,有望为患者带来更持久、更可及的生存与生活质量改善。
此次埃万妥单抗SC剂型在我国的获批有望深刻改变EGFR突变晚期NSCLC的治疗模式,助力国家“健康中国2030“战略目标的实现,推动肿瘤慢病化管理与患者生存质量的双重提升,开启EGFR突变NSCLC临床管理的新篇章。
本资料为强生创新制药所有,仅供医学药学专业人士参考,未经批准,严禁翻印、转载及传播。
本资料仅用于医学、科学交流,可能涉及尚未在中国获批的产品和适应症。强生创新制药不支持、不鼓励任何未被批准的药品/适应症使用。
本资料中涉及的AE/SS/PQC已按照公司的要求上报。(适用于含AE/SS/PQC的资料)
CRC Code:EM-196170
Approved Date:2025-12-24
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)