

1核因子E2相关因子2(Nrf2)在急性肝损伤中的保护机制
Nrf2是CNC家族中的一种碱性亮氨酸拉链转录因子,是细胞中的一组保护转录因子。在机体受到氧化应激时,Nrf2通过与抗氧化响应元件(ARE)结合,激活下游多种抗氧化因子及谷胱甘肽氧化还原系统,从而保护细胞免受氧化应激损伤,是细胞抗氧化应激的关键因子。
Nrf2能够诱导
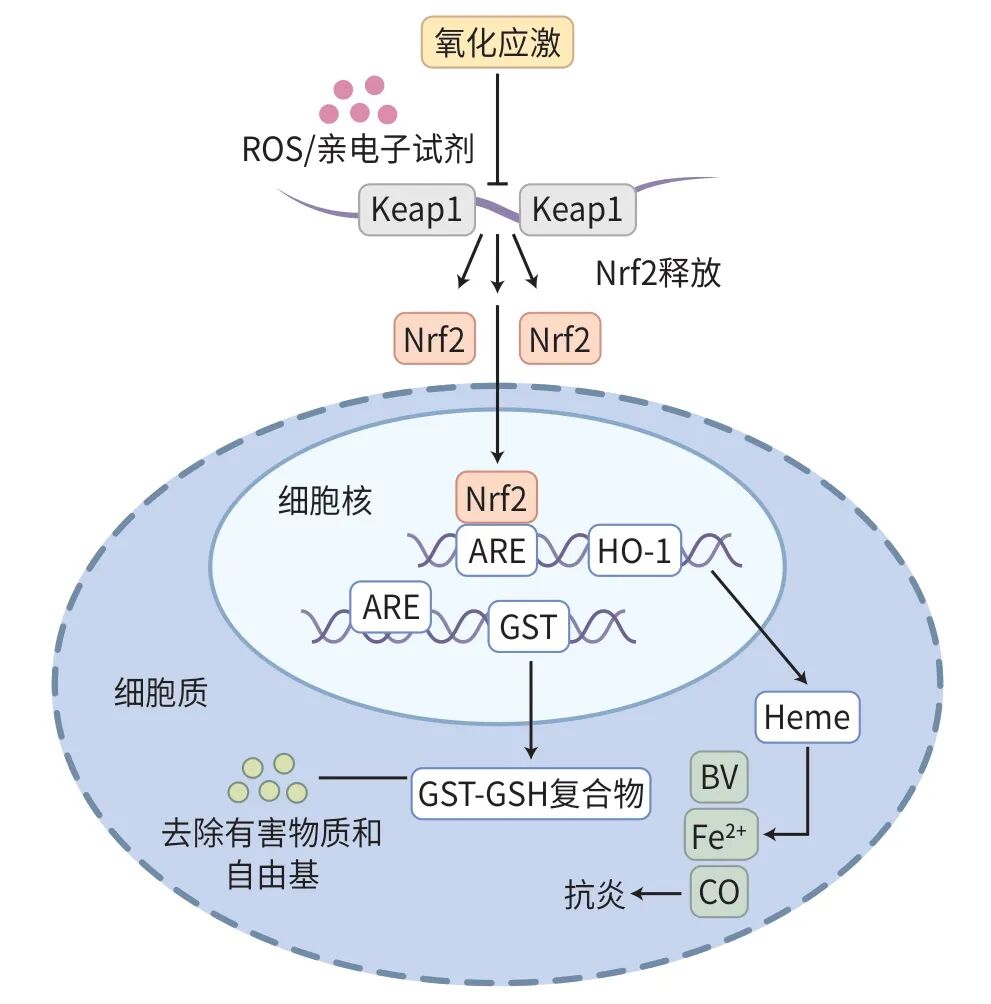
注: Nrf2,核因子E2相关因子2;Keap1,Kelch样ECH相关蛋白1;ROS,活性氧;ARE,抗氧化响应元件;HO-1,血红素氧合酶1;Heme,血红素;GST,
图1 氧化还原信号中的Nrf2/HO-1/GST信号通路
Nrf2通过调控与铁代谢相关的基因表达,影响铁的储存和吸收。Nrf2的活化可以促进铁的储存,减少细胞对铁的吸收,从而限制ROS的产生。此外,Nrf2还可以通过上调NQO1和血红素氧合酶1(HO-1)等与铁和ROS代谢有关的靶基因表达,从而抑制铁死亡。
Nrf2通过调节核基因组编码的线粒体蛋白,并改变ROS和其他影响线粒体功能相关代谢物的平衡,从而影响线粒体功能。研究表明,Nrf2过表达可以促进线粒体生物合成,改善线粒体功能,减少细胞坏死和凋亡。
在
Nrf2能通过干扰核因子κB(NF-κB)p65转录,抑制诱导型

2Nrf2在急性肝损伤中的调节机制
Nrf2信号通路是细胞应对氧化应激和毒性物质的重要机制。该通路的核心转录因子Nrf2通过调控多种抗氧化因子和诱导解毒酶的表达,保护细胞免受氧化应激和毒性物质的伤害。在正常生理状态下,Nrf2被Keap1锚定在细胞质中,而Keap1作为Cullin3依赖性E3泛素连接酶复合物的作用底物,能够促使Nrf2发生泛素化且被蛋白酶体快速降解。但当细胞受到ROS或亲电体的攻击时,Nrf2从Keap1中解离且快速转位进入细胞核。细胞内存在多种抵御氧化应激的抗氧化因子,包括维持细胞稳态的调节性和结构性蛋白以及Ⅱ相解毒酶,如SOD、CAT、GSH-Px、
Nrf2/HO-1信号通路是人体内重要的抗氧化应激通路,主要通过调节HO-1的活性来发挥其功能。如图1所示,在氧化应激条件下,Nrf2被激活并促进HO-1的表达,从而催化血红素氧化为胆绿素(BV)、一氧化碳(CO)和游离铁离子,这些代谢产物具有抗氧化和抗炎作用。Nrf2/HO-1信号通路亦是一种器官保护通路,在多种实验性动物模型中均被证实对各种炎症性疾病具有核心调控作用,包括
一项针对小鼠肝和小肠的研究显示,Nrf2缺陷会导致GST表达显著下降,提示Nrf2在调节GST基因表达中具有关键作用。GST是一类与肝脏解毒功能密切相关的酶,主要分布于肝脏内,当肝细胞受到损伤时迅速释放入血,引起血清GST活性升高。除通过ARE调控GST基因的表达外,Nrf2还可能通过其他途径发挥作用,例如Nrf2的小型Maf异二聚体形式也能直接结合ARE并激活下游基因。如图1所示,GST通过结合细胞内的GSH等抗氧化剂,帮助清除体内的有害物质和自由基,从而保护肝脏免受氧化应激的损害。Nrf2信号通路在癌症、
研究显示,肠道菌群与急性肝损伤之间存在密切联系,能通过肠-肝轴影响引起炎症反应。如图2所示,当
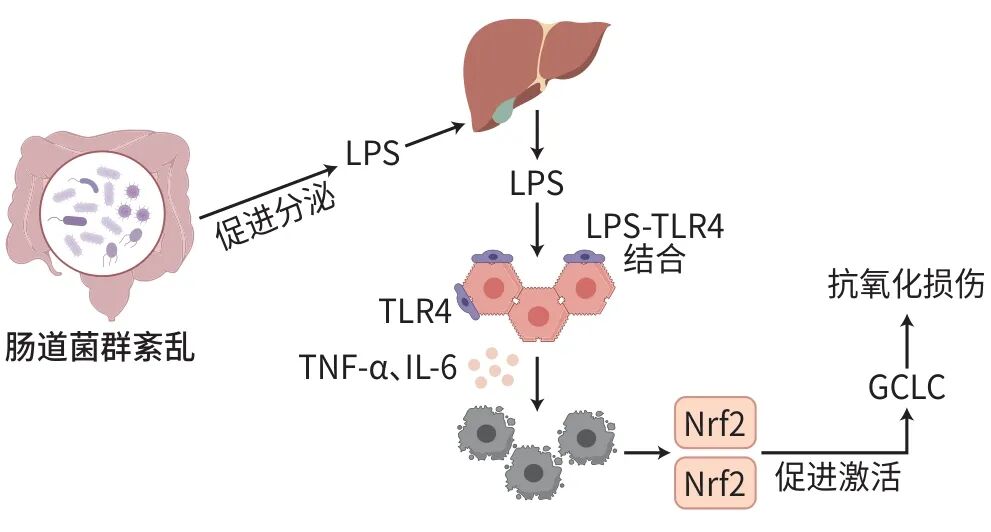
注: LPS,脂多糖;TLR4,Toll样受体4;TNF-α,肿瘤坏死因子-α;IL-6,白细胞介素-6;Nrf2,核因子E2相关因子2;GCLC,谷氨酰半胱氨酸连接酶。
图2 Nrf2/GCLC信号通路

3Nrf2在不同病因急性肝损伤中的作用
DILI是临床上常见的急性肝损伤类型之一,其中对乙酰氨基酚(APAP)过量服用是引发急性肝衰竭的重要原因。研究表明,Nrf2在APAP诱导的急性肝损伤中发挥关键的保护作用。在APAP中毒早期,Nrf2被迅速激活,进而上调一系列抗氧化和解毒酶基因的表达。例如,Nrf2可诱导HO-1的表达,HO-1催化血红素降解生成BV、CO和游离铁离子。BV在胆绿素还原酶作用下进一步生成TBil,两者均具有强抗氧化活性,能够清除自由基、抑制脂质过氧化;CO则可通过激活鸟苷酸环化酶-环磷酸鸟苷信号通路,抑制炎症细胞的浸润和炎症因子的释放。同时,Nrf2可促进GSH的合成,增强细胞的解毒能力,并抑制肝细胞凋亡信号通路的激活,有效减轻APAP诱导的急性肝损伤程度,提高肝脏的再生修复能力。
长期酗酒可导致酒精性肝病,其中酒精性肝损伤(ALI)是其早期阶段的主要表现。ALI的病理研究表明,氧化应激是其主要发病机制之一,酒精代谢过程中细胞色素P4502E1产生的ROS是发生氧化应激的主要原因。研究表明,Nrf2是抗氧化反应的关键调节因子,其通过调节HO-1、NQO1等抗氧化基因的表达,增强细胞对氧化应激的抵抗能力,从而预防ALI。在酒精暴露的小鼠模型中,Nrf2的激活能够显著降低血清中的ALT和天冬氨酸氨基转移酶水平,减少肝组织中的丙二醛(MDA)等氧化应激标志物的含量,并提高SOD等抗氧化酶的活性。
病毒性肝炎是由多种肝炎病毒感染引起的肝脏疾病,其中甲型、乙型和丙型等肝炎病毒感染可导致急性肝损伤。病毒感染过程中会产生大量的ROS和炎症因子,加剧肝脏的氧化应激和炎症反应,进一步加重肝细胞损伤。在病毒性急性肝损伤的模型中,Nrf2信号通路被广泛研究。例如,在LPS/D-Galn诱导的小鼠急性肝炎模型中,Nrf2与TLR4/NF-κB信号通路共同参与调控炎症反应和肝损伤进程。此外,Nrf2在脓毒症急性肝损伤中也显示出显著的抗氧化应激作用,能够降低血清ALT水平并提高肝组织中Nrf2的表达。同时,Nrf2还可能通过调节细胞内的信号通路,影响病毒的复制和传播。
发生败血症时,免疫系统过度反应释放大量TNF-α、IL-6等炎性因子,直接损伤肝细胞,Nrf2的激活可通过增强谷胱甘肽过氧化物酶4(GPX4)等抗氧化酶的表达,清除ROS,并抑制NF-κB等促炎通路,从而减轻肝细胞损伤。此外,败血症可诱发肝细胞铁死亡(一种铁依赖性脂质过氧化导致的细胞死亡)。Nrf2通过上调下游基因SLC7A11(溶质载体家族7成员11)和GPX4的表达,维持细胞氧化还原平衡,阻断铁死亡进程。例如,Maresin1通过激活Nrf2/SLC7A11/GPX4通路,可显著减轻败血症所导致的急性肝损伤。
四氯化碳经细胞色素P450代谢产生三氯甲基自由基,引发脂质过氧化和氧化损伤。Nrf2激活后,转入细胞核并结合ARE,诱导下游SOD、GSH-Px、HO-1、NQO1等抗氧化酶的表达,从而减轻氧化损伤。同时,Nrf2也能促进排毒,通过调控GST、尿苷二磷酸葡萄糖醛酸转移酶等Ⅱ相解毒酶的表达,加速四氯化碳代谢产物的解毒过程。

4Nrf2激动剂在急性肝损伤治疗中的研究
Nrf2激动剂通过激活Nrf2信号通路,上调多种抗氧化酶的表达,从而抑制氧化应激和炎症反应,在急性肝损伤治疗中展现出潜在价值。
姜黄素在急性肝损伤中的保护机制主要通过多靶点协同作用实现,主要包括以下3个方面:(1)激活抗氧化通路:姜黄素作为一种强效Nrf2激动剂,可促进Nrf2核转位,诱导下游HO-1、SOD、CAT等抗氧化酶的表达,增强机体清除ROS、MDA等自由基的能力,减轻脂质过氧化损伤。(2)抑制炎症级联反应:通过阻断NF-κB活化及核苷酸结合寡聚化结构域样受体蛋白3炎症小体通路,降低TNF-α、IL-1β和IL-6等促炎因子释放,并抑制环氧化酶-2、诱导型一氧化氮合酶等炎症介质生成,减轻肝组织炎性浸润。同时,姜黄素通过激活线粒体自噬清除受损线粒体,阻断核苷酸结合寡聚化结构域样受体蛋白3/半胱天冬蛋白酶-1介导的炎症爆发。(3)保护细胞结构与功能:在线粒体保护方面,姜黄素可维持呼吸链复合物Ⅰ活性,修复谷胱甘肽系统,减少线粒体ROS产生;在抗凋亡调控方面,其可上调B细胞淋巴瘤-2基因/细胞凋亡调控因子比值,抑制半胱天冬蛋白酶-3/9活化,减少肝细胞凋亡。在治疗急性肝损伤中,姜黄素具有高安全性,显著优于传统肝保护剂Ⅰ期临床试验的验证安全性:口服剂量高达12 g/d时未见肝肾毒性或严重不良反应,血液生化指标保持稳定。
白藜芦醇是一种天然多酚类物质,广泛存在于葡萄、蓝莓等植物中,具有强大的抗氧化和抗炎特性。白藜芦醇通过p38丝裂原活化蛋白激酶通路磷酸化Nrf2的Ser40位点,阻断Keap1-Cullin3泛素化降解系统,使Nrf2在10 min内入核启动抗氧化基因转录,进而上调GCLC促进GSH合成,恢复细胞内抗氧化储备,并激活NQO1以稳定抗氧化酶活性。在LPS诱导的ALI小鼠模型中,白藜芦醇可使肺组织SOD活性提升40%、GSH水平增加35%,同时使MDA水平降低50%。在抗炎作用方面,白藜芦醇可阻断TLR4活化,抑制人NF-κB抑制蛋白α降解和NF-κB核转位,下调TNF-α、IL-1β和IL-6等促炎因子表达,在缺血再灌注和脓毒症模型中可使炎症因子水平降低40%~60%。尽管白藜芦醇多靶点特性具有临床潜力,但其生物利用度低和缺乏人体数据的问题仍待解决。未来研究应聚焦于剂型优化、联合用药方案及严谨的临床试验验证。
SFN是一种异硫氰酸酯类化合物,广泛存在于西兰花、卷心菜等十字花科蔬菜中,是由硫代葡萄糖苷在内源性芥子酶作用下水解生成的。作为一种高效的Nrf2激活剂,SFN能够特异性地与Keap1蛋白上的半胱氨酸残基发生共价结合,使Keap1构象发生改变并释放Nrf2,进而诱导大量抗氧化和解毒酶的表达,有效清除体内的ROS和有害化学物质。在DILI模型中,SFN预处理可显著提高肝组织中Nrf2、HO-1和NQO1等蛋白的表达水平,降低APAP诱导的血清ALT水平升高,减轻肝组织的病理损伤程度,提示SFN可能成为预防和治疗DILI的新型天然药物。目前其临床潜力主要集中于药物性肝损伤、缺血再灌注损伤及脓毒症相关肝损伤的辅助治疗,但仍需进一步开展人体研究验证安全性与有效性。
CGA是一种富含于杜仲、金银花等植物中的多酚酸,具有免疫保护、抗氧化和抗炎等特性。CGA可以通过调节细胞内的氧化还原状态激活Nrf2:一方面,通过清除细胞内的ROS,减少氧化应激对Keap1-Nrf2复合物的影响,促进Nrf2与Keap1解离;另一方面,通过激活细胞内的磷脂酰肌醇3激酶/蛋白激酶B信号通路等抑制糖原合成酶激酶-3β的活性,有助于Nrf2的稳定和激活。在化学物质诱导的急性肝损伤模型中,CGA可以激活Nrf2,上调其下游抗氧化酶基因的表达,减轻肝脏的氧化损伤和炎症反应,降低血清ALT水平,保护肝细胞。目前临床主要将CGA用于中成药辅助治疗(如茵栀黄口服液),但需注意剂量控制以避免潜在毒性,未来需深化临床研究以明确其最佳治疗窗和长期安全性。
近年来研究发现,奥替普拉具有显著的Nrf2激活作用。其通过与Keap1蛋白的特定半胱氨酸残基结合,抑制Keap1对Nrf2的泛素化降解,促进Nrf2的积累和活化。同时,奥替普拉还可以通过激活肝细胞核因子-1,直接上调谷胱甘肽S-转移酶A1等解毒酶的表达,加速对APAP产生的N-乙酰-对苯醌亚胺等毒性代谢物的结合与清除。在急性肝损伤模型中,奥替普拉可有效激活Nrf2,诱导肝组织中抗氧化酶和解毒酶基因的表达,增强肝脏的抗氧化能力,降低氧化应激水平,减少肝细胞损伤和炎症反应。奥替普拉通过抗氧化、促解毒对急性肝损伤发挥显著保护作用,尤其在APAP模型中效果明确。尽管存在剂量限制性毒性及临床数据缺失等不足,但奥替普拉仍为DILI治疗的重要候选药物,未来需通过剂型改良和联合策略推动其临床转化。
CDDO-Me是一种合成的三萜类化合物衍生物,具有强大的抗炎、抗氧化和抗肿瘤活性。其可通过抑制Keap1与Nrf2的相互作用、促进Nrf2的磷酸化修饰以及增强Nrf2与ARE的结合能力等多种方式激活Nrf2。在急性肝损伤模型中,CDDO-Me可显著提高肝组织中Nrf2及其下游靶基因(如HO-1、NQO1、GSH合成酶等)的表达水平,降低血清中炎症因子和ALT的含量,减轻肝组织的病理损伤,对药物性、酒精性等多种急性肝损伤均表现出良好的保护效果。其独特的化学结构和高效的Nrf2激活作用使其成为开发新型肝脏保护药物的潜力候选化合物。
DMF作为工业化学中常用的化合物,价格低廉且易于获得,具有抗氧化、抗炎、抗肿瘤、神经保护和免疫调节等特性。DMF通过共价修饰Keap1的半胱氨酸残基,阻断Nrf2泛素化降解,促进其核转位;同时通过抑制NF-κB信号通路的抑制蛋白IκB激酶,减少IκB的磷酸化和降解,从而抑制NF-κB的核转位及基因表达,进而减轻炎症反应。此外,DMF还可能通过修饰Keap1或者调节细胞内的氧化还原状态促进Nrf2与Keap1的解离,进而激活Nrf2。在急性肝损伤治疗中,DMF呈现“风险-获益”双面性:风险管控方面,需严格监测患者的肝功能,建立基于基因筛查的个体化用药方案;治疗潜力方面,通过剂型优化和精准给药,其在酒精性、缺血性及自身免疫性肝损伤中具有明确保护价值,尤其适用于N-乙酰半胱氨酸禁忌患者。未来需重点推进肝靶向制剂和适应证拓展的临床研究。

5小结与展望
Nrf2在急性肝损伤治疗中具有重要作用和应用前景,其在细胞抗氧化、解毒代谢、抗炎及抗凋亡等环节中具有核心调控功能,并在多种病因导致的急性肝损伤中显示出明确的保护作用。目前,已有多种Nrf2激动剂具备临床应用转化潜力。然而,目前针对Nrf2在急性肝损伤治疗中的研究仍面临诸多挑战:首先,尽管Nrf2的基本作用机制已初步明确,但在体内复杂的生理病理环境下,其与其他信号通路之间的相互作用网络尚未完全阐明,限制了对Nrf2作用的全面认识以及针对Nrf2治疗策略的精准设计。其次,尽管Nrf2激活剂的开发已取得了一定进展,但大多数仍处于实验研究阶段,其在人体中的安全性、有效性、药代动力学特性以及最佳使用剂量和疗程等问题仍需进一步研究和临床试验验证。未来的研究方向应聚焦于进一步解析Nrf2信号通路的精细调控机制,深入挖掘Nrf2与其他细胞内信号通路之间的相互作用关系,以期发现更多潜在的治疗靶点和药物作用位点。同时,积极推进对Nrf2激活剂的临床前研究和临床试验,优化药物设计与研发策略,提高药物的疗效和安全性,为急性肝损伤患者提供更为有效、精准的治疗方案。

https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH260127

陶辉跃, 杨娜, 刘杨. 核因子E2相关因子2在急性肝损伤中的作用机制与治疗潜力[J]. 临床肝胆病杂志, 2026, 42(1): 209-216
来源:临床肝胆病杂志
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)