医脉通肝病科“肝注「药」闻”栏目聚焦肝病领域全球新药研究进展和资讯,旨在及时传递前沿诊疗理念供临床参考。本文整理了近期新药研发进展。
➤Linerixibat获美国食品药品监督管理局(FDA)批准,用于治疗
➤羟尼酮胶囊拟纳入国家药品监督管理局药品审评中心(CDE)优先审评程序,适应症为慢乙肝
➤Cell重磅:揭示肝纤维化新机制,首创新药TDI01展现治疗潜力
3月19日,葛兰素史克(GSK)宣布,美国FDA已批准 Lynavoy(linerixibat) 用于治疗PBC成年患者的胆汁淤积性瘙痒。linerixibat是一种回肠胆汁酸转运体(IBAT)抑制剂,通过抑制胆汁酸重吸收,减少血液循环中多种瘙痒介质,从而发挥作用。据新闻介绍,这是美国首个获批用于该适应症的药物。

此次获批主要基于Ⅲ期GLISTEN试验的结果。GLISTEN 研究为一项随机、双盲、安慰剂对照的 Ⅲ 期临床试验,该研究达到主要终点及关键次要终点。与安慰剂组相比,linerixibat可显著、快速(治疗第2周)且持续(治疗24周)改善患者的胆汁淤积性瘙痒症状(p≤0.001)及瘙痒相关睡眠干扰(p=0.024)。
研究主要终点为每月最严重瘙痒数字评定量表(WI-NRS)评分自基线的变化值;结果显示,治疗 24 周时,linerixibat组(n=119)瘙痒症状较安慰剂组(n=119)显著改善,最小二乘均值差为-0.72(95% CI:-1.15, -0.28;p=0.001)。
Linerixibat 的安全性特征与过往研究及 IBAT 抑制机制一致。最常见不良事件为
加州大学戴维斯分校胃肠病学和肝病学主任Christopher Bowlus教授在新闻稿中表示:“linerixibat的获批为改善PBC患者的生活质量提供了重要机遇,这些患者长期饱受难以控制且常常令人衰弱的瘙痒之苦。瘙痒对PBC患者的影响可能非常深远,而迄今为止治疗方案十分有限。此次获批标志着PBC瘙痒治疗领域迎来重要里程碑,填补了这一关键的未被满足的临床需求”。
此前,Linerixibat已在美国、欧盟和日本获得孤儿药资格认定,并在中国获得优先审评资格。目前,该药在欧盟、英国、加拿大及中国的上市申请工作正在推进中。
近日,CDE公示,北京康蒂尼药业研发的羟尼酮胶囊拟纳入优先审评程序,该药适应症为慢性乙型肝炎肝纤维化及早期肝硬化。目前全球尚无获批用于慢性乙型肝炎肝纤维化治疗的特效药物,若其最终获批上市,将为慢乙肝肝纤维化及早期肝硬化人群提供新的治疗选择。

图源:CDE官网
羟尼酮是一种新型抗纤维化药物,可抑制转化生长因子 β(TGF-β)信号通路及肝星状细胞(HSC)活化并促进HSC凋亡。此前,旨在评估其疗效与安全性的为期52周随机、双盲、安慰剂对照 Ⅲ 期临床试验结果,已于2025 年在美国肝病学会年会(AASLD 2025)上公布。主要终点显示:羟尼酮组实现纤维化逆转比例显著高于安慰剂组:羟尼酮组有65名患者(52.85%)达到纤维化逆转,而安慰剂组为37名(29.84%),绝对差异为23.01%(P=0.0002)。尽管接受ETV抗病毒治疗,安慰剂组仍有25.81%的患者出现纤维化进展,而羟尼酮组仅8.94%。关键次要终点(肝炎症改善≥1级且无纤维化进展)的达成:羟尼酮组为 49.57%,安慰剂组为34.82%(P=0.0246)。
安全性方面,两组在HBV DNA不可测率(81.74% vs. 85.47%)和ALT复常率(80% vs. 88.89%)表现相当。不良事件谱相似;严重不良事件发生率羟尼酮组为4.88%、安慰剂组为6.45%,无因不良事件停药者。
肝纤维化是导致代谢相关脂肪性肝炎(MASH)等肝脏疾病患者死亡的重要病理过程,目前针对肝纤维化的治疗手段十分有限。识别可成药的促纤维化靶点并开发基于机制的治疗方法具有重要的意义。

近日,四川大学
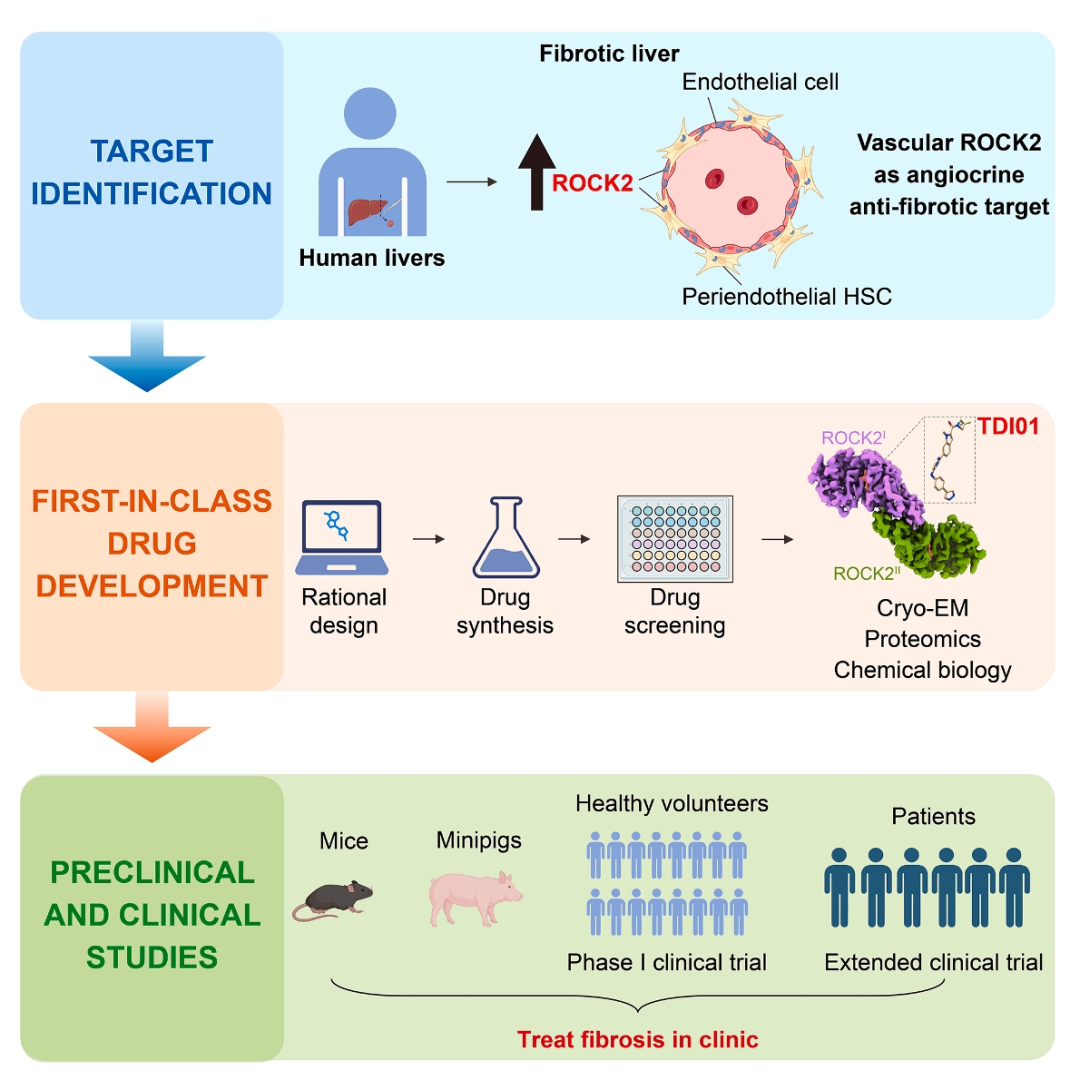
TDI01在啮齿类及小型猪MASH模型中,可恢复血管表型并减轻纤维化程度。在Ⅰ期临床试验中,共纳入62名健康志愿者,评估TDI01单次(400mg、800mg、1200mg)和多次给药(200mg或400mg,每日一次,共7天)的安全性、耐受性及药代动力学。结果显示未观察到严重不良事件,整体耐受性良好,TDI01 具有良好的药代动力学(PK)特征和安全性。
在扩展临床试验中,纳入6例肝纤维化患者,予以200 mg TDI01每日一次口服治疗24周,结果显示5例患者观察到肝脏硬度值持续下降、胶原沉积均明显减少、纤维化评分改善。免疫组化证实,TDI01治疗后患者肝组织中pROCK2水平降低,而pROCK1水平无明显变化,进一步验证其靶向特异性。
综上,研究明确了ROCK2为促肝纤维化血管表型的可成药靶点。与现有ROCK抑制剂相比,ROCK2抑制剂TDI01的选择性指数显著更高,在治疗肝纤维化方面具备独特临床潜力。该研究从靶点和机制发现、药物研发到临床研究,为抗纤维化药物研发提供了一个全链条研究范式。
参考资料:
1.GSK官网
2.Hu Y, Yang B, Xiao C,et al. Selective targeting of endothelial and perivascular angiocrine ROCK2 treats liver fibrosis. Cell. 2026 Mar 6:S0092-8674(26)00166-2.
3.CDE官网
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)