Metadata Card
文献题目:Tofacitinib repairs inflammation and mitochondrial dysregulation in GM-CSF-reprogrammed RA macrophages
发表期刊:Cellular & Molecular Immunology
发表时间:26.3.4
影响因子:19.8(中科院1区)
通讯作者/单位:Shiva Shahrara @ 伊利诺伊大学芝加哥分校
一句话总结:本研究揭示了GM-CSF如何通过重塑线粒体代谢诱导RA巨噬细胞致病,并证明
Graphical Abstract

Abstract
中文摘要:
英文摘要:
Rheumatoid arthritis (RA) exhibits heterogeneous endotypes, complicating treatment strategies. GM-CSF and GM-CSFRα are enriched in RA synovial CD68⁺macrophages (MΦs), and are implicated in acute and chronic disease stages. Since anti-TNFi and anti-IL6R therapies did not effectively suppress GM-CSF/GM-CSFRα expression or the GM-CSF-associated landscape, we explored alternative therapeutic strategies to target GM-CSF function using RA blood, synovial tissues, and preclinical models. We demonstrate that GM-CSF-MΦs reprogrammed in RA blood and synovial tissue share a distinct IL1β⁺S100A⁺HIF1⁺IL10ˡᵒNFIL3/6ˡᵒ expression profile, manifested by mitochondrial oxidative stress and fragmentation. To correct the metabolic imbalance of GM-CSF-MΦs, cells were treated with a complex I inhibitor (i) or a glucose uptake blocker. Complex Ii did not broadly alter the inflammatory or metabolic networks or affect the mitochondrial dynamics remodeled by GM-CSF-MΦs. While the glucose uptake inhibitor (HK2i) reduced glycolysis-derived ATP, it had limited efficacy in restricting the inflammatory signature or restoring TCA enzymes in GM-CSF-MΦs. In contrast, tofacitinib achieved broad-spectrum effects by downregulating GM-CSFRα expression and inhibiting STAT5 signaling. Moreover, tofacitinib redirected RA blood and synovial IL1β⁺S100A⁺HIF1⁺IL10ˡᵒNFIL3/6ˡᵒMΦs into a regulatory phenotype, reversing oxidative stress and mitochondrial fragmentation. In preclinical models, local GM-CSF overexpression induced MΦ-directed joint inflammation and metabolic dysregulation. Consistently, Tofacitinib reversed GM-CSF-differentiated murine IL1β⁺HBEGF⁺HIF1⁺MΦs by impeding STAT5 signaling, correcting metabolic dysregulation, and repairing mitochondrial fragmentation. In conclusion, anti-TNFi, anti-IL6R, and metabolic-targeted therapies were largely ineffective in modifying GM-CSF-MΦ pathology. Conversely, tofacitinib deactivation of STAT5 attenuates GM-CSF-MΦ-triggered inflammation and mitochondrial malfunction by restoring regulatory markers and rebalancing oxidative phosphorylation in RA specimens and/or preclinical models.
Background & Problem
背景:类风湿关节炎(RA)是一种自身免疫性疾病,滑膜巨噬细胞是炎症细胞因子的主要来源。粒细胞-巨噬细胞集落刺激因子(GM-CSF)在RA滑膜液和血液中显著升高,与临床病理密切相关。
痛点:尽管生物制剂(如抗TNF、抗IL-6R)已广泛应用,但仍有部分RA患者反应不佳。研究发现,这些传统制剂无法有效抑制GM-CSF及其受体的表达,也无法逆转受其驱动的巨噬细胞代谢病理,导致疾病持续发展。
Methodology
策略:作者采用了“从临床到实验室再到动物模型”的全方位策略,重点研究GM-CSF如何调控RA巨噬细胞的免疫代谢。
逻辑:首先,利用单细胞测序(scRNAseq)和免疫组织化学(IF)分析RA患者滑膜组织中GM-CSFR的表达;其次,体外诱导GM-CSF重编程的巨噬细胞(GM-MOs),并使用Seahorse代谢分析和Confocal成像检测线粒体功能;最后,建立腺病毒介导的GM-CSF诱导小鼠关节炎模型,评估托法替布的治疗潜力。
Key Results & Interpretation
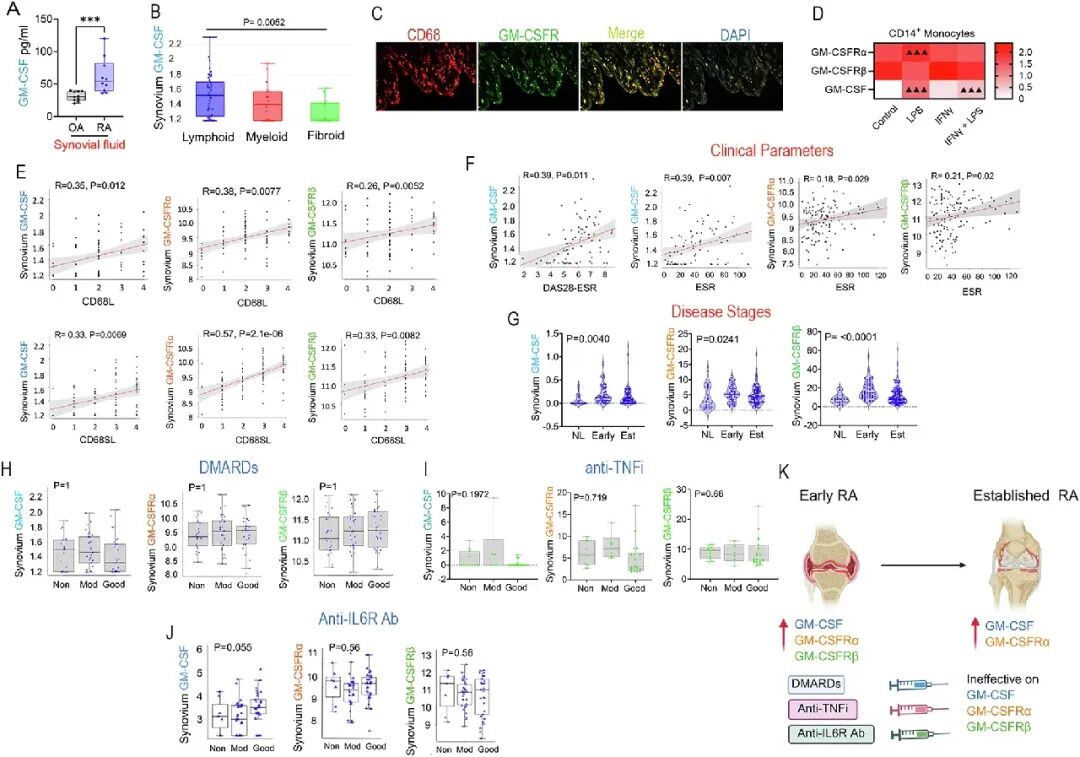
[A-C]:通过ELISA和免疫荧光发现,RA滑膜液中GM-CSF水平显著高于OA,且GM-CSFR与CD68+巨噬细胞在滑膜组织中高度共定位,确立了巨噬细胞作为其主要靶细胞的地位。
[D-G]:实验显示LPS可诱导单核细胞高表达GM-CSF及GM-CSFRα,且其表达水平与患者的DAS28-ESR评分及ESR临床指标呈显著正相关。
[H-J]:核心挑战在于,无论是DMARDs、抗TNFi还是抗IL-6R疗法,均无法有效降低滑膜组织中GM-CSF及其受体的转录水平,即使临床好转的患者其表达依然顽固。
[K]:逻辑总结模型图显示,GM-CSF系统贯穿RA发病期,且是现有标准治疗的盲区。
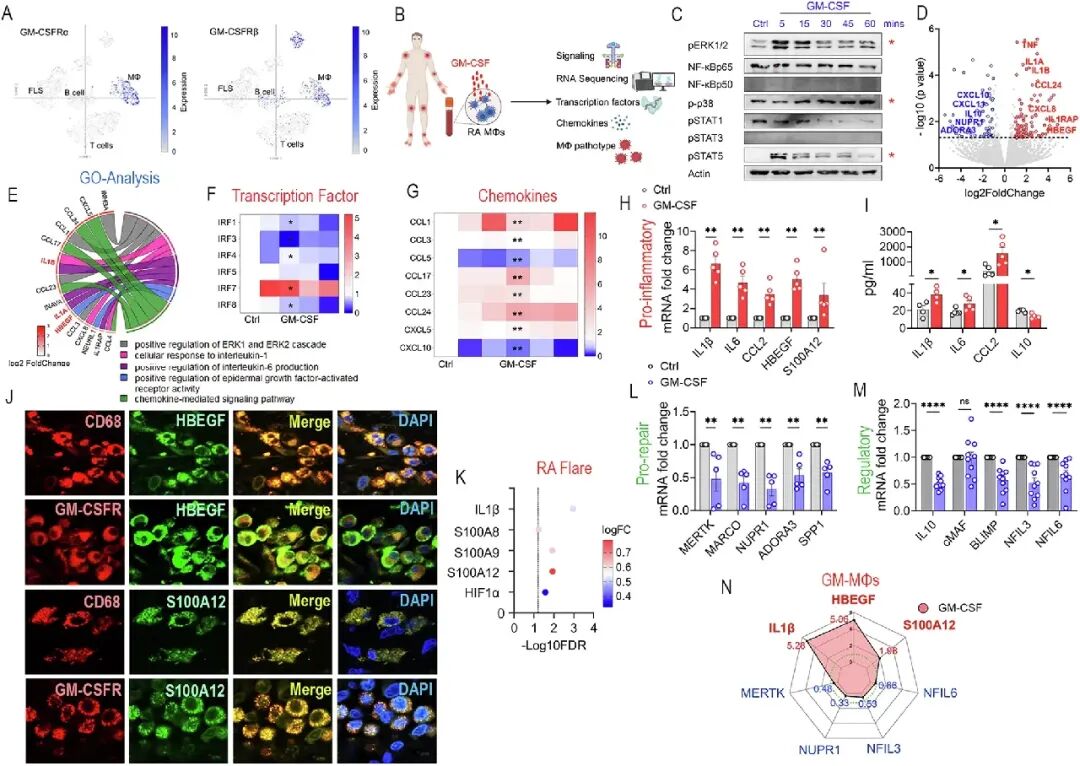
[A-C]:单细胞测序证实GM-CSFRαβ特异性簇集在巨噬细胞中,刺激后迅速激活ERK、p38及关键的STAT5通路,而STAT1/3则无反应。
[D-G]:RNAseq显示GM-MOs展现出促炎基因(如IL1β、IL6)的显著上调及修复基因的下调,并伴随趋化因子CCL1、CCL17及CCL24的特异性爆发。
[H-K]:验证发现GM-MOs分泌大量IL-1β和CCL2,且该特征基因群(如S100A12、HIF1α)在RA病情活动期的血液标本中同样显著升高。
[L-N]:雷达图综合分析显示GM-MOs处于高度致病状态:炎症因子极高(HBEGF+、S100A+),而调节性分子(MERTK、IL-10、NFIL3/6)被全面抑制。
发现点3:GM-CSF导致代谢重编程:糖酵解增强与线粒体碎片化
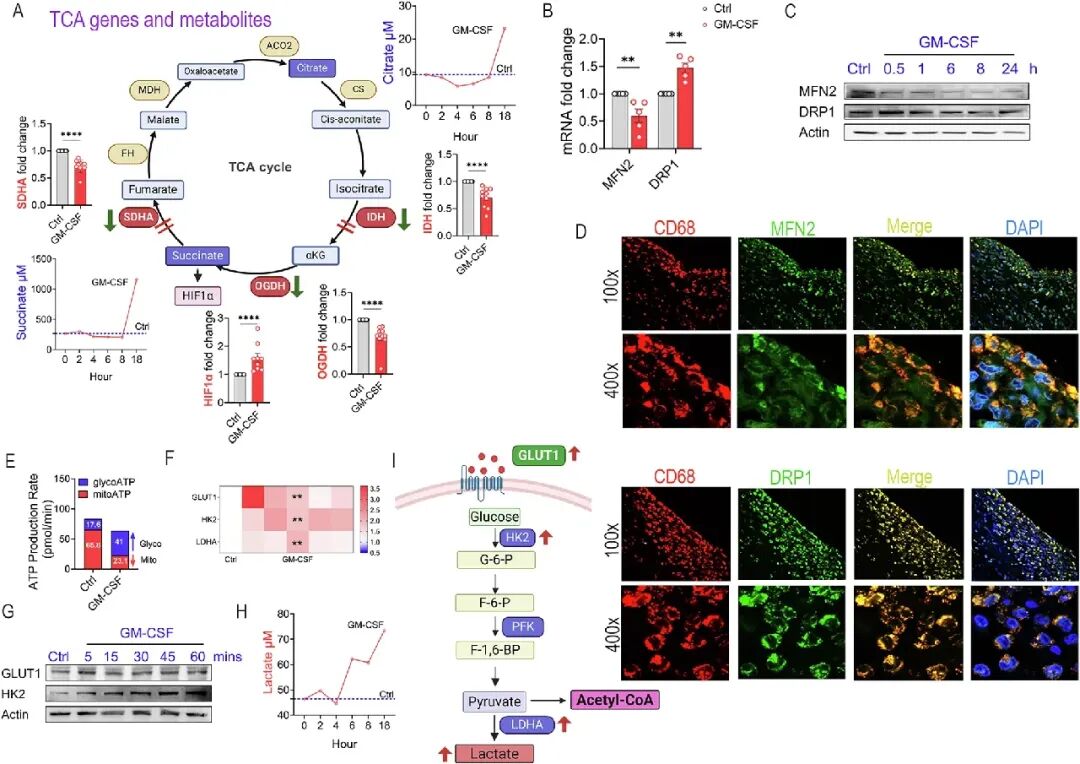
[A]:GM-CSF显著抑制TCA循环关键酶(IDH、OGDH、SDHA)的表达,导致柠檬酸(Citrate)和琥珀酸(Succinate)代谢物积聚,进而诱导HIF1α水平升高。
[B-D]:线粒体形态发生巨变,裂变蛋白DRP1升高而融合蛋白MFN2降低,在RA滑膜组织中观察到线粒体呈现严重的碎片化状态。
[E-H]:Seahorse检测证实GM-MOs的能量产出从氧化磷酸化切换到了糖解(glycoATP比例从17%上升至41%),并伴随GLUT1、HK2水平及乳酸(Lactate)分泌的显著增加。
[I]:代谢路径总结图描绘了GM-CSF如何强制细胞进入“高糖酵解、低氧磷”的促炎能量循环。
发现点4:糖解抑制剂及传统生物制剂仅能实现局部修复
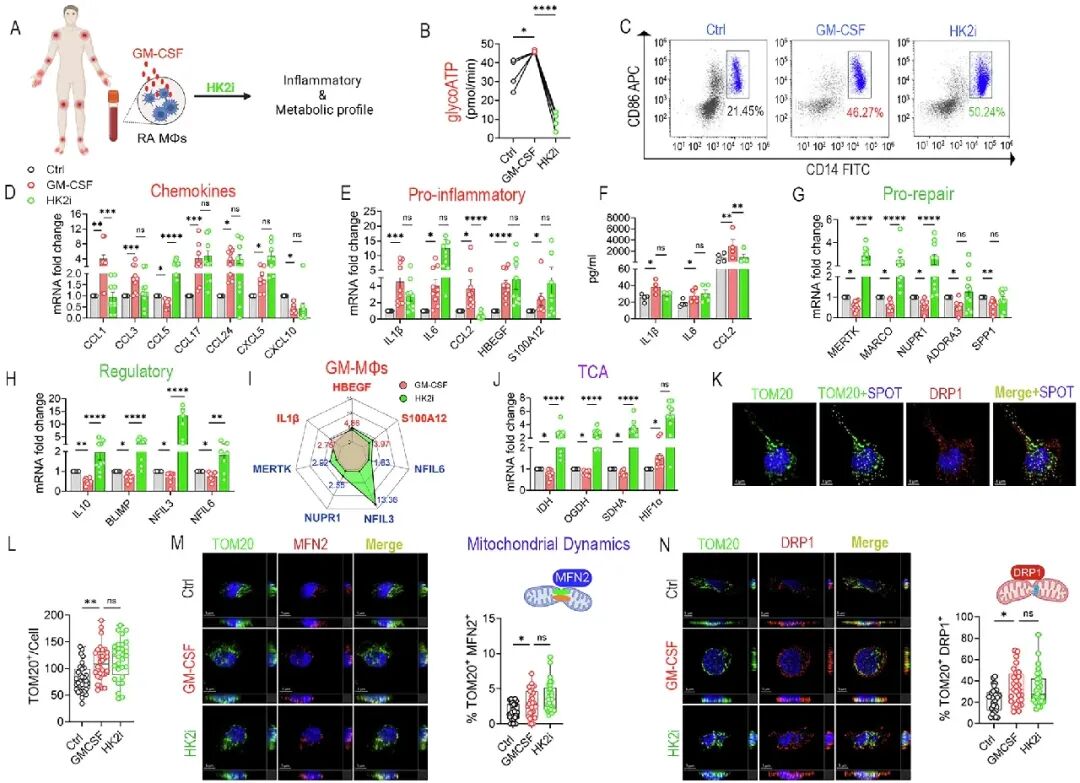
[4A-C]:糖解抑制剂(HK2i)虽能阻断glycoATP的产生,但无法阻止单核细胞向CD14+CD86+炎症表型分化。
[4D-J]:HK2i虽能微调部分修复基因,但对核心炎症信号(IL1β、HBEGF、S100A12等)及主要趋化因子群几乎没有抑制作用。
[4K-N]:尤为关键的是,HK2i无法纠正线粒体的碎片化趋势,DRP1/MFN2的失衡依然存在。
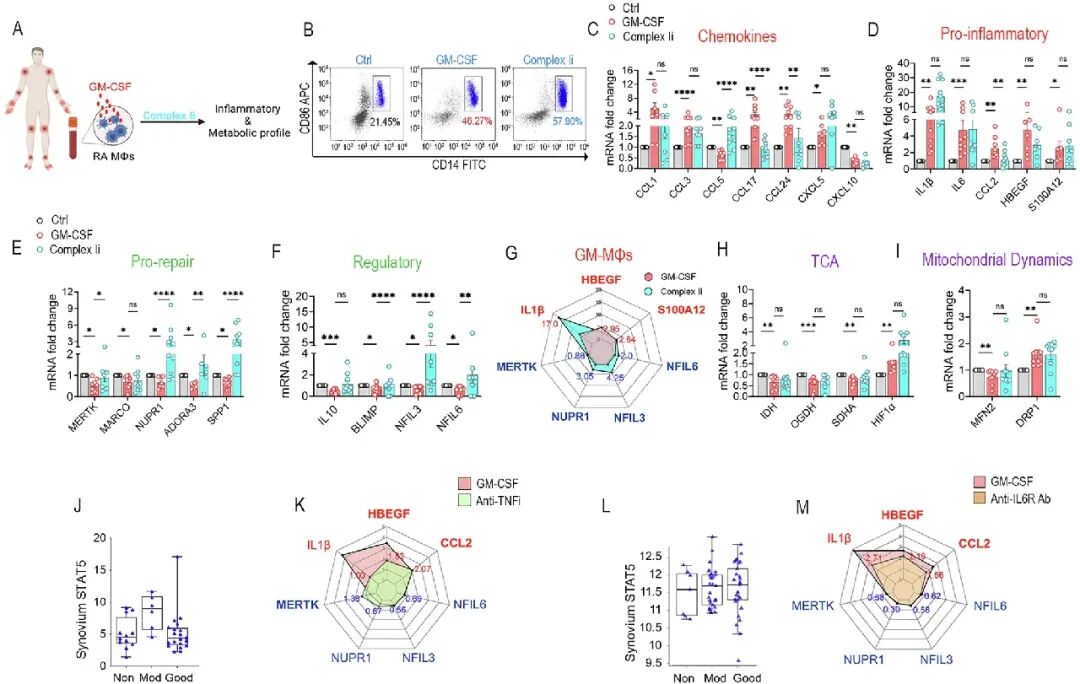
[5A-I]:另一代谢干预——线粒体复合物I抑制剂(Complex Ii)在恢复代谢酶和抑制炎症方面同样表现乏力。
[5J-M]:雷达图直观对比显示,抗TNFi和抗IL6R药物在调控GM-CSF诱导的STAT5信号及修复调节基因方面收效甚微。
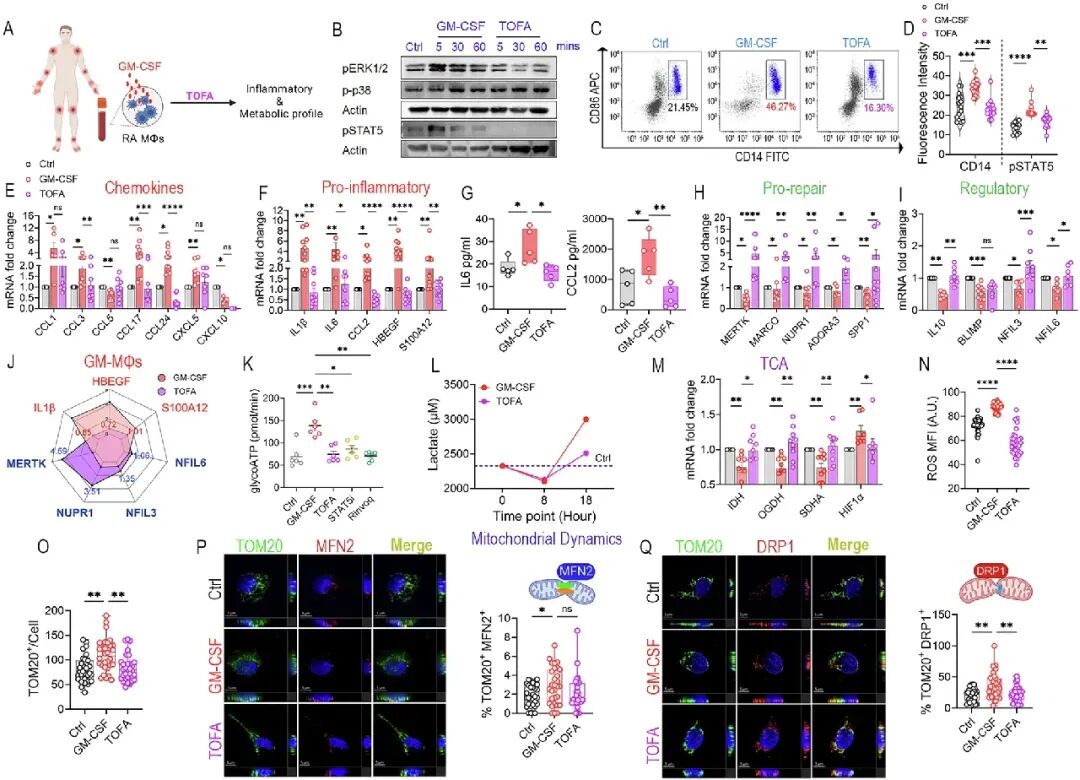
[6A-D]:托法替布精准切断STAT5信号磷酸化,并显著抑制了促炎性单核细胞的重构。
[6E-J]:与代谢药物不同,托法替布实现了“地毯式”修复:大幅下调IL1β、HBEGF、S100A12和趋化因子群,同时强力上调了MERTK、IL-10和NFIL3/6等调节性基因。
[6K-M]:代谢机能被纠偏,细胞能量由糖解重新导向氧化磷酸化,TCA酶(IDH、SDHA)活性得以恢复,并成功抑制了乳酸和HIF1α的累积。
[6N-Q]:托法替布成功修复了线粒体动力学,显著降低了细胞内的ROS水平及线粒体碎片化程度。
发现点6:托法替布在RA滑膜组织水平展现出比代谢抑制剂更广泛的修复能力
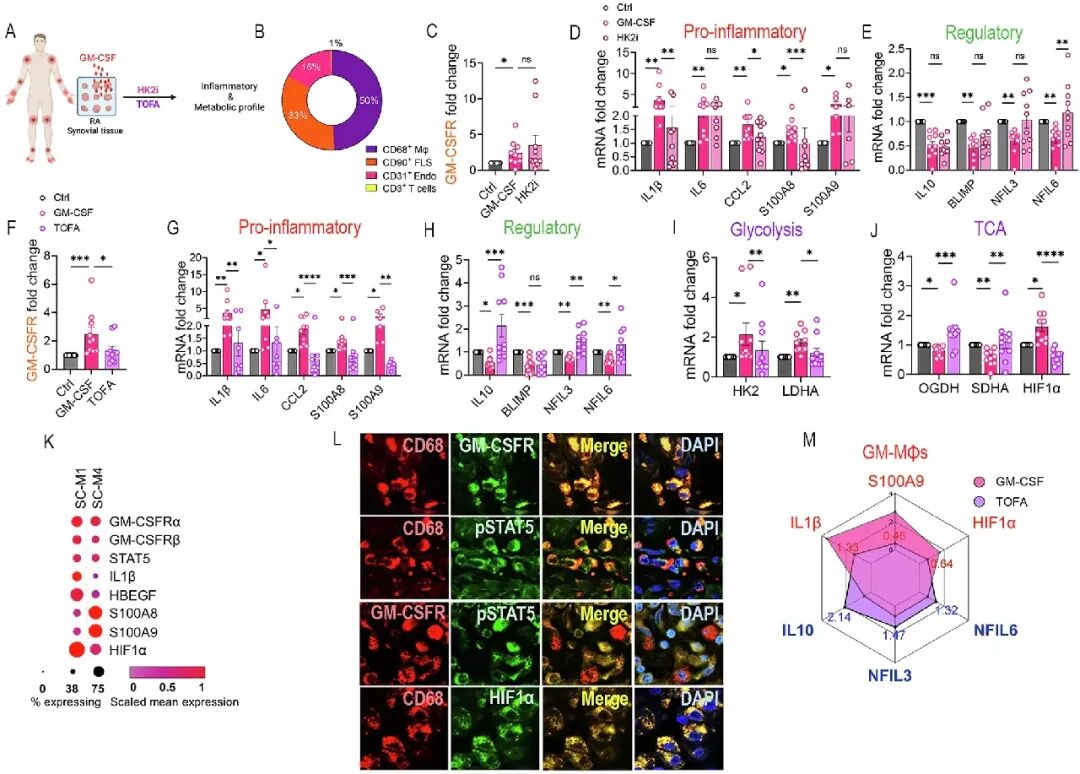
[7A-B]:Pathotyping分析所选取的RA滑膜组织为“髓系富集型”,其中CD68+巨噬细胞占比高达50%。
[7C-E]:糖解抑制剂(HK2i)在组织中能抑制IL1B和CCL2并提升NFIL6,但对核心靶点GM-CSFR以及关键炎症因子IL-6、S100A9几乎无效。
[7F-J]:托法替布显著下调了GM-CSFR的表达,还全面抑制了促炎基因(IL1B, IL6, S100A8/9)、糖解基因(HK2, LDHA)及缺氧因子HIF1a。同时挽救了被GM-CSF减低的IL-10、NFIL3/6等调节基因及OGDH、SDHA等氧化磷酸化关键酶。
[7K-L]:单细胞测序回顾性分析与免疫荧光验证一致显示,GM-CSFR、pSTAT5、HIF1a富集在RA滑膜的M1(IL1β)和M4(IFN)巨噬细胞亚群中,明确了托法替布在组织中的靶点。
[7M]:综合雷达图清晰地刻画了托法替布对滑膜组织的“重编程”效果:将组织状态从由GM-CSF驱动的促炎、高糖解模式,强力扭转为高修复、高氧磷的稳态模式。
发现点7:托法替布在滑膜组织及临床前模型中验证疗效
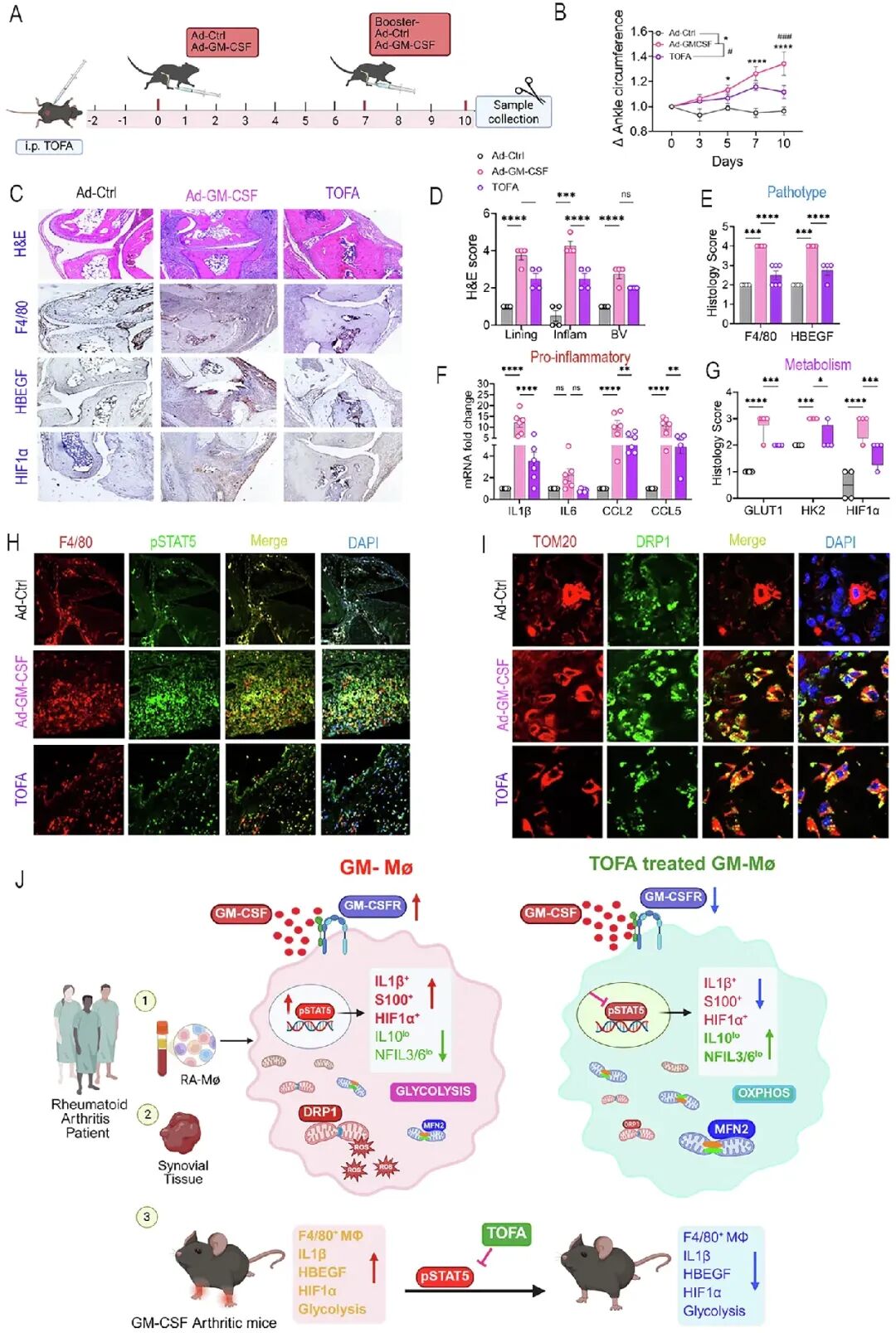
[8A-B]:在腺病毒驱动的GM-CSF诱导小鼠关节炎模型中,托法替布预防性治疗显著遏制了踝关节的肿胀进程。
[8C-E]:组织病理显示,托法替布能显著降低滑膜增厚、炎症细胞浸润以及致病性F4/80+HBEGF+巨噬细胞的频率。
[8F-G]:分子层面观察到促炎因子mRNA表达骤减,且GLUT1、HK2和HIF1α等糖解/缺氧标记物被同步抑制。
[8H-I]:托法替布通过降低pSTAT5水平,在组织原位修复了线粒体失调(减少TOM20+DRP1+细胞)。
[8J]:托法替布通过阻断GM-CSFR/STAT5轴,将高糖解的碎片化线粒体巨噬细胞,重编程为高氧磷的稳态巨噬细胞,从而控制关节炎症。
Innovation & Takeaway
✨ 创新点
1、首次定义了GM-CSF驱动的IL1β⁺S100A⁺HIF1⁺IL10ˡᵒNFIL3/6ˡᵒ致病性巨噬细胞内型 。
2、证明了JAK抑制剂(托法替布)在修复代谢-线粒体失调方面的广谱优势,填补了传统生物制剂无法触及的治疗盲区。
✨ 科研启示
炎症不仅仅是细胞因子的过量,更深层的动因在于细胞内的“代谢紊乱”和“线粒体崩塌”。研究免疫代谢重编程是寻找RA新药的关键。
✨ 临床/应用价值
对于那些对传统抗TNF或IL-6R疗法不敏感的“难治性”RA患者,如果其关节表现为高GM-CSF/STAT5特征,及早转换使用JAK抑制剂(如托法替布、
局限性
研究主要聚焦于STAT5信号轴,可能忽略了其他JAK家族成员或其他通路的交互作用。虽然小鼠模型结果积极,但仍需在更多样化的RA临床样本中验证其长期代谢修复效果。虽然文章极力宣称抗TNF/IL-6R“无效”,但这更多是基于其对GM-CSF通路的调控层面。在临床实践中,这些制剂对非GM-CSF驱动型RA依然有效。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。