盐皮质激素受体拮抗剂(MRA)通过减轻醛固酮诱导的炎症、纤维化和容量潴留的有害影响,在
针对盐皮质激素受体和/或醛固酮生成的新兴疗法可能为干预醛固酮-盐皮质激素受体轴提供替代策略。例如,非甾体类MRA(nsMRA)因其结构组成、药代动力学、药效学和组织分布差异可能具有更高的受体选择性,
近期,JACC: Heart Failure(IF:11.8)发表的一篇综述阐述了非甾体类和甾体类MRA以及盐皮质激素受体调节剂和醛固酮合酶抑制剂之间的结构和机制区别;总结了其在心力衰竭、糖尿病和CKD人群中的现有证据。
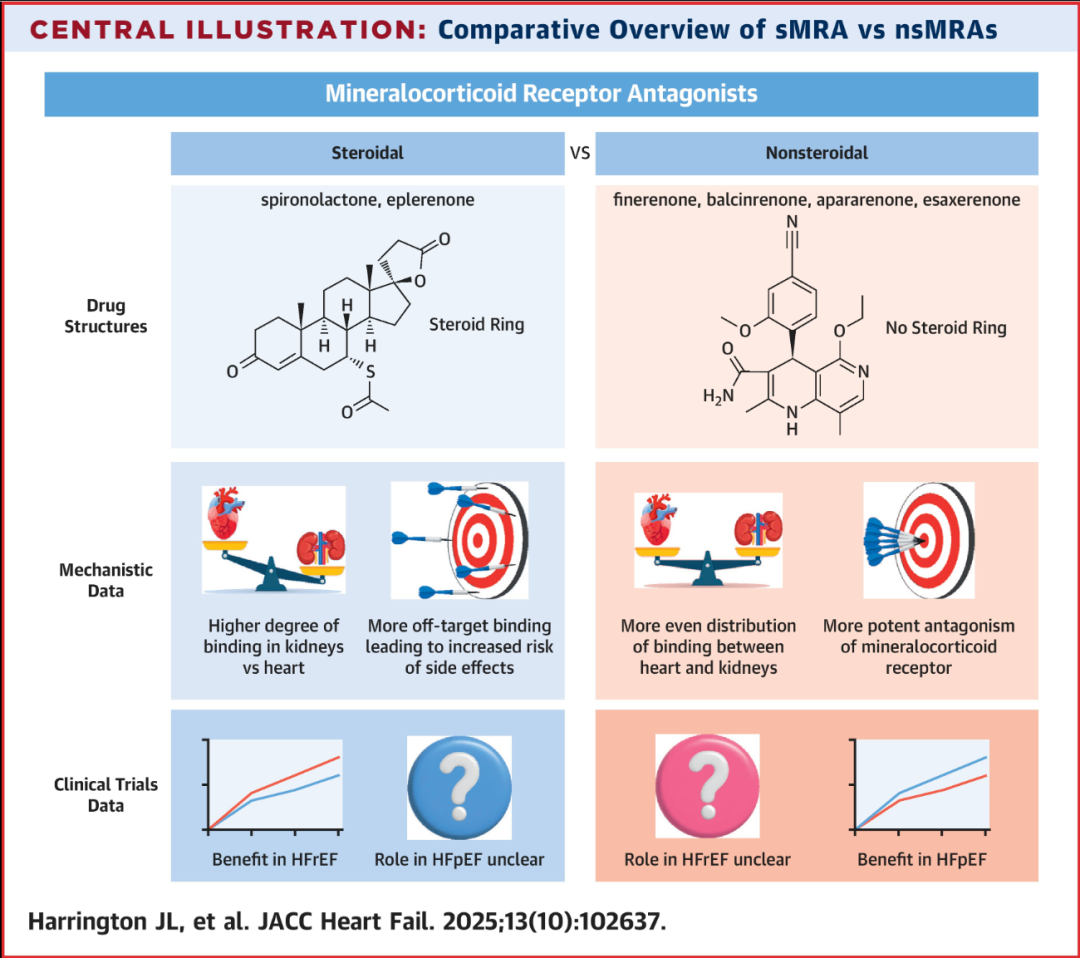
中心插图:sMRA与nsMRA概览
结构类别决定了传统sMRA(例如,螺内酯、依普利酮)与新兴nsMRA(例如,非奈利酮、Balcinrenone、Apararenone、Esaxerenone)之间的关键药理学差异。nsMRA中无甾体核,产生了更均衡的心-肾受体亲和力分布曲线和更精准的靶点拮抗作用,从而在心力衰竭谱系中转化为独特的疗效-安全性特征。HFpEF = 射血分数保留的心力衰竭;HFrEF = 射血分数降低的心力衰竭;nsMRA = 非甾体类盐皮质激素受体拮抗剂;sMRA = 甾体类盐皮质激素受体拮抗剂。
充分的数据支持在HFrEF患者中的使用sMRA,因此,心力衰竭管理指南一致推荐其用于HFrEF,且为 I A 类推荐(表1,图1)。
表1 sMRA治疗心力衰竭的证据
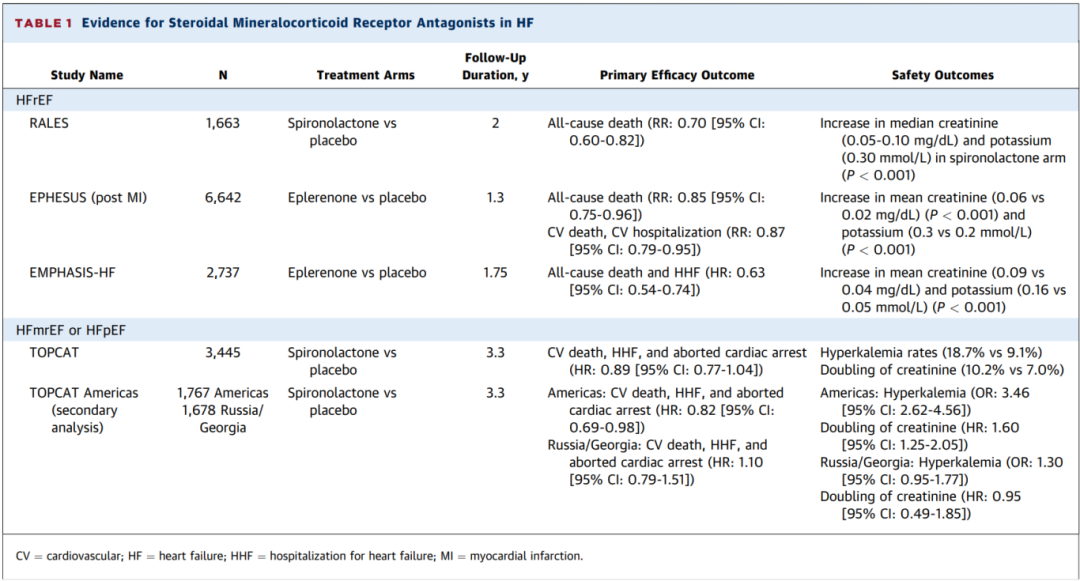

图1 当代心力衰竭指南对MRA的推荐
在随机临床试验中,螺内酯和依普利酮均被证明能显著降低HFrEF患者的全因死亡(螺内酯)或心血管死亡(依普利酮)及心力衰竭住院风险,包括近期发生
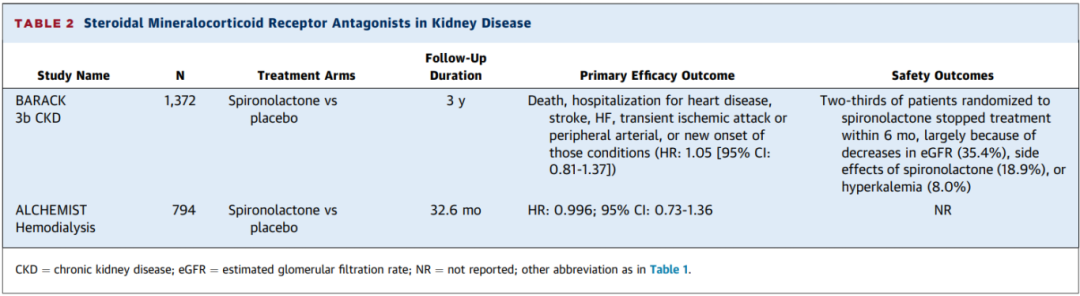
表2 sMRA治疗CKD的证据
多类靶向醛固酮-盐皮质激素受体轴治疗心力衰竭和CKD的新型药物正在涌现。nsMRA和盐皮质激素受体调节剂都能拮抗盐皮质激素受体,临床前模型表明这些药物在盐皮质激素受体上的作用方式可能与sMRA不同。与许多膜结合受体不同,盐皮质激素受体直接与基因组相互作用,通过募集不同的辅助因子肽来触发多种通路。在临床前模型中,已证明盐皮质激素受体调节剂Balcinrenone改变了核辅助因子肽的募集,选择性完全拮抗促纤维化和炎症基因,同时保留MRA的益处,并部分拮抗电解质调节基因,从而降低
在结构上,sMRA具有核心甾体骨架,这使它们能够与盐皮质激素受体结合,但也导致与其他甾体激素受体(如雄激素、
表3 sMRA与nsMRA的关键差异
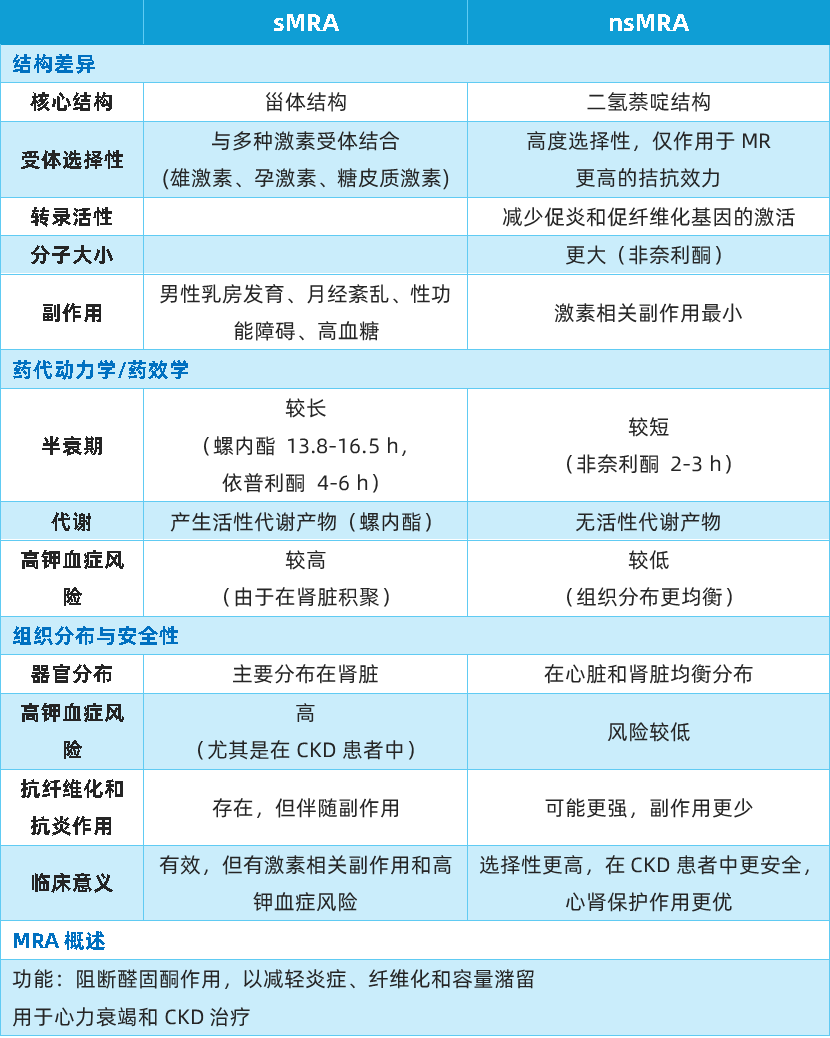
备注:MRA = 盐皮质激素受体拮抗剂;nsMRA = 非甾体类盐皮质激素受体拮抗剂;PK/PD = 药代动力学和药效学;sMRA = 甾体盐皮质激素受体拮抗剂。
当前有大型3期结局试验支持在CKD合并T2MD患者以及HFmrEF/HFpEF患者中使用nsMRA非奈利酮(表4)。来自其他小型2期和3期试验的数据总体表明,其他nsMRA(包括Apararenone和Esaxerenone)以及盐皮质激素受体调节剂Balcinrenone在CKD患者中也具有临床获益且耐受性良好。
表4 nsMRA和MRM在心力衰竭和肾脏病试验中的现有证据
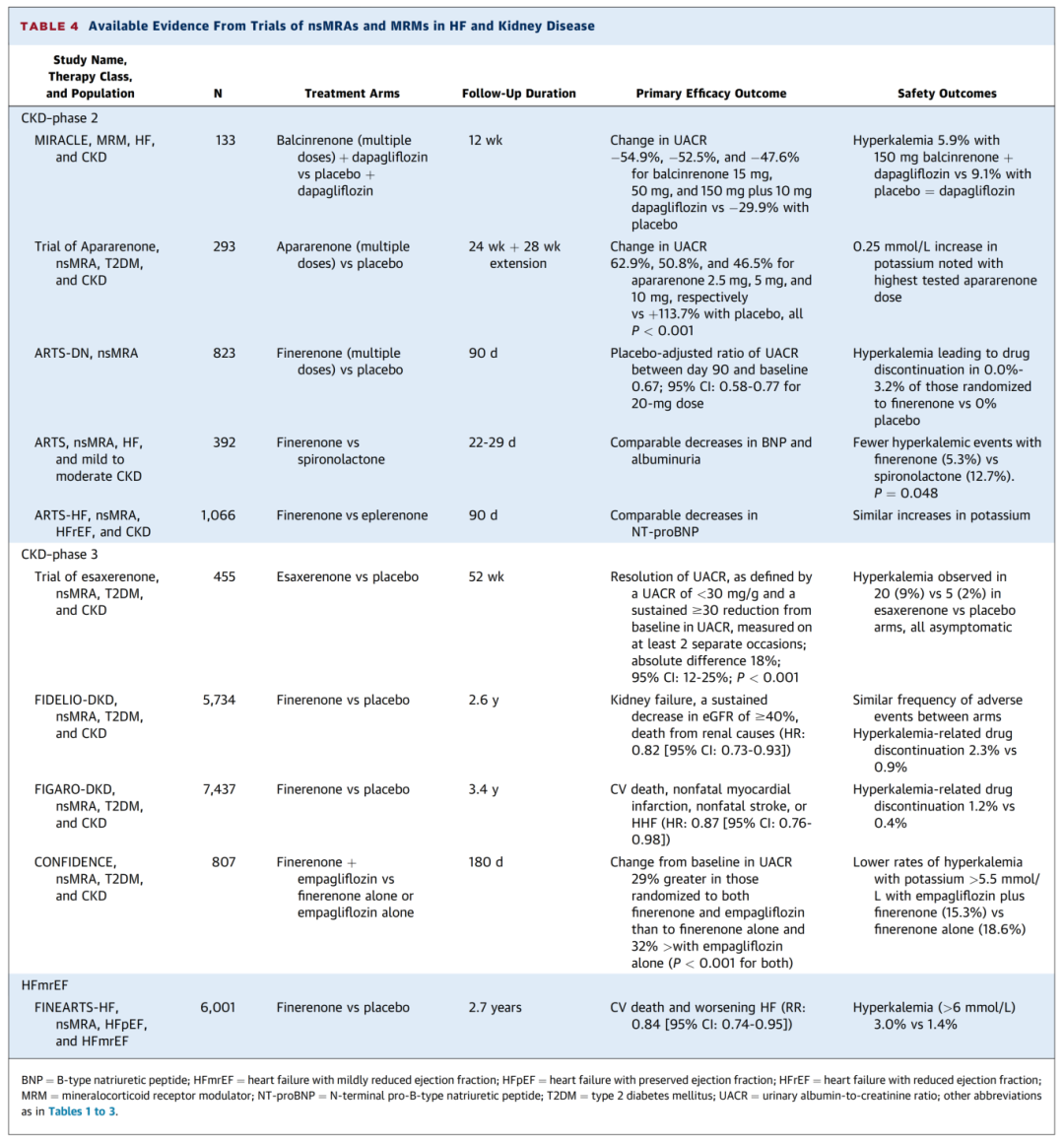
关于nsMRA在临床实践中的作用,关键未解问题仍然存在,包括哪些人群能从中获益等。即将进行的试验所产生的证据将有助于确立这些新型疗法的总体作用。此外,多项正在进行的试验将有助于进一步阐明sMRA的作用(表5)。
表5 nsMRA、sMRA、MRM和醛固酮合酶抑制剂在心力衰竭和肾脏病中正在进行的试验
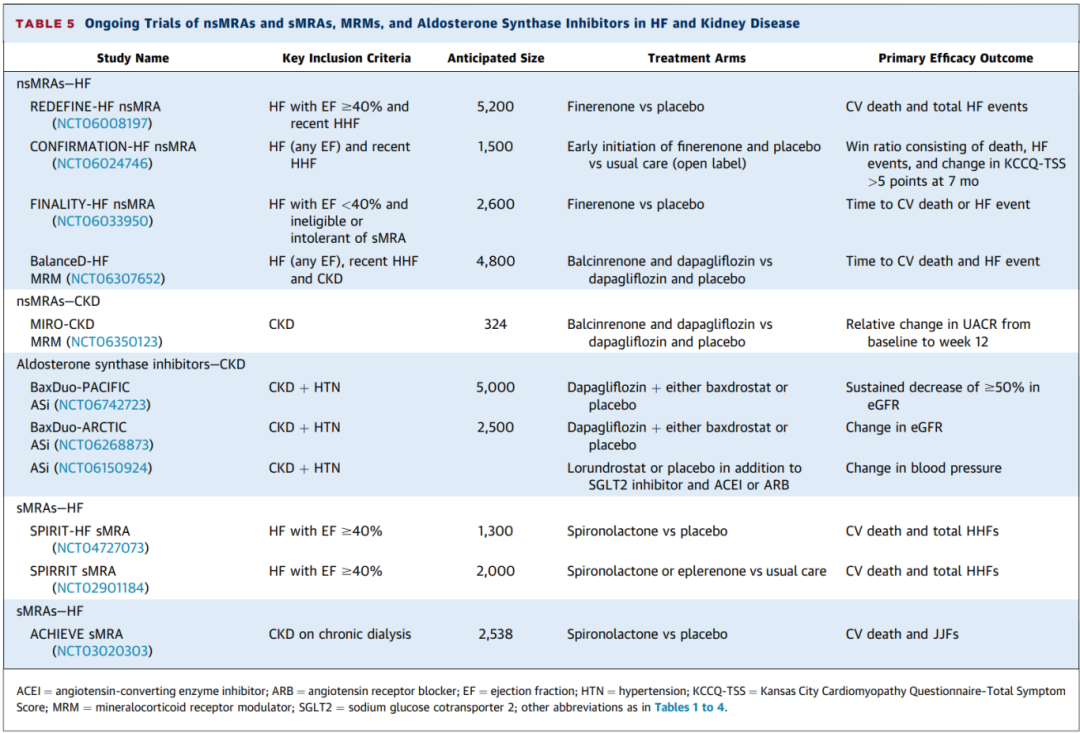
现有证据强力支持sMRA用于HFrEF治疗,但其临床应用常因耐受性而受到限制。nsMRA受体选择性更优、组织分布均衡和脱靶效应更少。越来越多的临床证据支持nsMRA使用,特别是对于HFmrEF/HFpEF以及T2DM合并CKD患者。其他新兴疗法,如MRM和ASi,调节盐皮质激素受体或减少醛固酮产生,并可能在该领域提供额外的潜在替代治疗策略。
然而,重大的未解问题仍然存在,正在进行的临床试验对于弥补这些空白并阐明nsMRA、MRM和ASi在心力衰竭治疗中的未来作用至关重要。
文献索引:Josephine L. Harrington, Mario E. Canonico, Abdelghani El Rafei, et al. Nonsteroidal and Steroidal Mineralocorticoid Antagonists: Rationale, Evidence, and Unanswered Questions. JACC: Heart Failure, Volume 13, Number 10. 4 September 2025.
编辑:Kbh
审校:siqili
排版:siqili
医脉通是专业的在线医生平台,“感知世界医学
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)