
一年一度的肿瘤领域盛会——2025年欧洲肿瘤内科学会年会(ESMO 2025)于10月17日至21日在德国柏林隆重举行。在这场肿瘤领域的年度盛事中,一系列前沿临床研究成果得以公布,全球顶尖专家齐聚一堂,为促进临床肿瘤学的进步共襄盛举。
Claudin 18.2(CLDN18.2)在
ATG-022是一种靶向CLDN18.2的ADC,由人源化HER2单抗通过可裂解连接子与vc-MMAE偶联而成。前期临床数据显示,该药物在多种CLDN18.2表达水平下均显示抗肿瘤活性潜能。
CLINCH是一项Ⅰ/Ⅱ期研究,包含剂量递增和剂量扩展两个阶段。剂量递增阶段的纳入标准为晚期实体瘤患者,无论CLDN18.2的表达状态。所有患者均接受ATG-022治疗(0.3-3.0 mg/kg,Q3W),以评估药物的安全性、耐受性和药代动力学。在剂量扩展阶段,CLDN18.2阳性(≥IHC 1+,1%)的GC/GEJC患者被纳入研究,分别接受2.4mg/kg或1.8 mg/kg剂量的ATG-022治疗。研究的主要终点包括剂量限制性毒性(DLT)和不良事件(AE),疗效终点包括客观缓解率(ORR)和疾病控制率(DCR)。
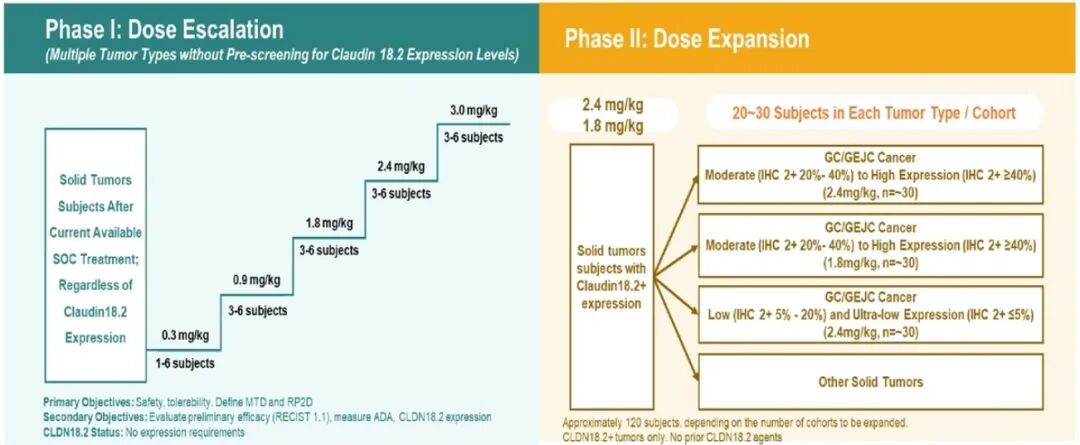
图1 研究设计
截至2025年6月20日,共入组56例晚期GC/GEJC患者(8例来自递增阶段,48例来自扩展阶段)。递增阶段中,患者的药物剂量范围为0.3-3.0 mg/kg;扩展阶段中,患者接受的药物剂量为2.4 mg/kg。其中32例患者的CLDN18.2表达≥IHC 2+/20%,此类患者的中位年龄为60.5岁,基线ECOG评分包括0分(8例)和1分(24例),65.5%的患者既往接受过≥2线全身治疗,71.9%的患者既往接受过抗PD-1/PD-L1治疗,56.3%的患者既往接受过紫杉烷类治疗。
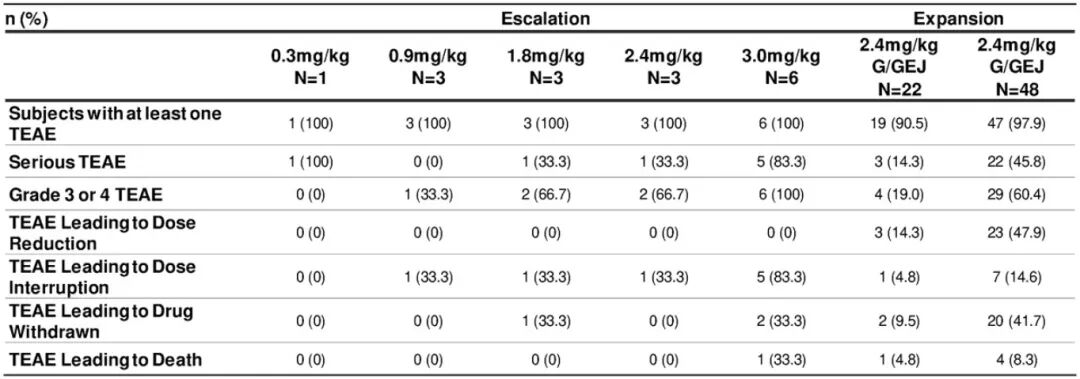
安全性分析显示,在剂量扩展阶段的2.4 mg/kg治疗组中,严重TEAE的发生率为45.8%,≥3级TEAE的发生率为60.4%,未观察到眼毒性或神经毒性。
表1 安全性分析
疗效分析显示,对于剂量扩展阶段中曾接受≥1次肿瘤评估且CLDN18.2表达≥IHC 2+/20%的患者,30例患者接受了2.4 mg/kg药物治疗,其中1例出现完全缓解(CR)、11例出现部分缓解(PR),ORR为40%,DCR为90%,中位无进展生存期(PFS)为6.97个月,12个月总生存(OS)率为66.2%。25例患者接受了1.8 mg/kg药物治疗,其中1例出现完全缓解(CR)、9例出现部分缓解(PR),ORR为40%,DCR为84%。18例患者接受了1.8-2.4 mg/kg药物治疗,其中1例出现完全缓解(CR)、5例出现部分缓解(PR),ORR为33.3%,DCR为50%。
对于CLDN18.2高表达、低表达和超低表达的GC/GEJC患者,ATG-022显示出可控的安全性特征和令人鼓舞的初步抗肿瘤效果,研究者建议开展进一步的临床研究。
SKB315是一种靶向CLDN18.2的新型ADC,载荷药物为拓扑异构酶1抑制剂。研究者开展了一项I期临床试验,以评估SKB315单药治疗在晚期实体瘤患者中的安全性、耐受性和抗肿瘤活性。
研究的纳入标准为标准治疗失败的晚期实体瘤患者,患者接受SKB315单药治疗。研究终点包括DLT、安全性以及研究者根据RECIST v1.1评估的疗效。在此,研究者首次报告了所有入组患者的安全性结果,并分析了表达CLDN18.2的晚期GC/GEJC患者的疗效结果。
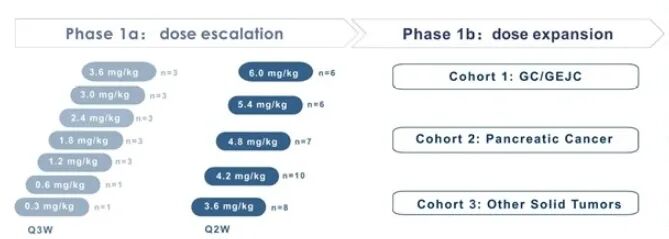
图2 研究设计
截至2025年4月21日,共入组83例患者(其中Q3W组17例,Q2W组66例),安全性分析基于所有83例患者进行,疗效分析基于42例CLDN1.2中/高表达且治疗剂量≥2.4 mg/kg的GC/GEJC患者进行。
表2 患者基线
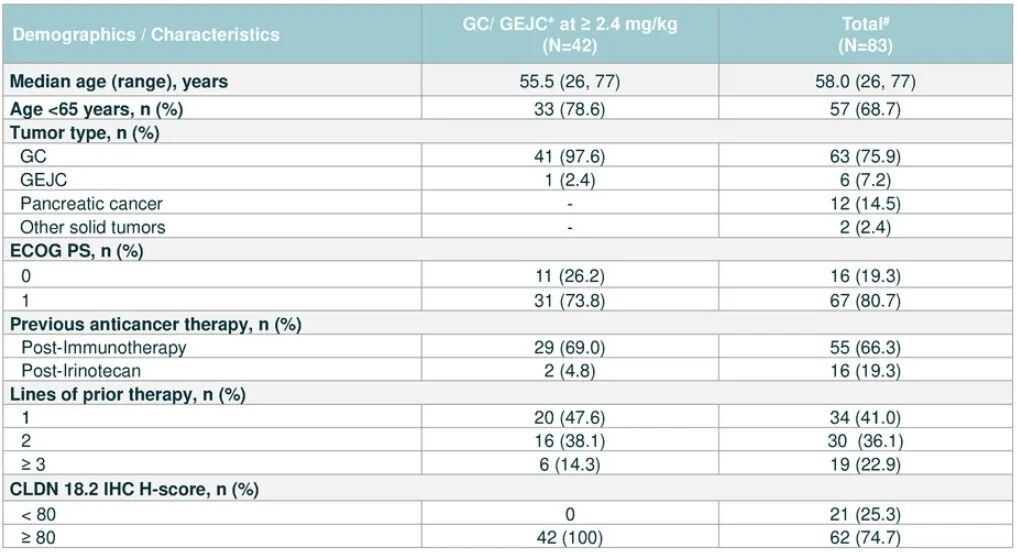
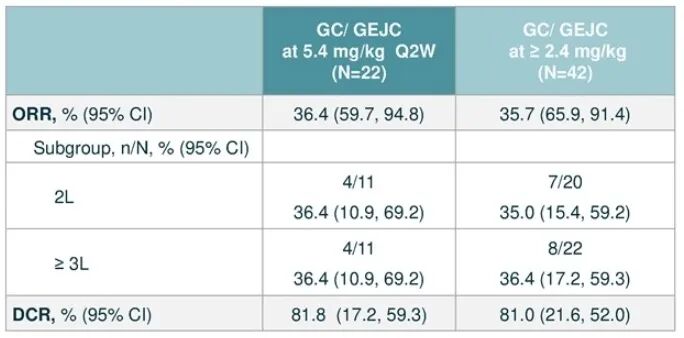
中位随访4.1个月时,42例患者的ORR为35.7%,DCR为81.0%,中位DOR为7.9个月,中位PFS为6.8个月,中位OS为11.8个月。
表3 疗效分析
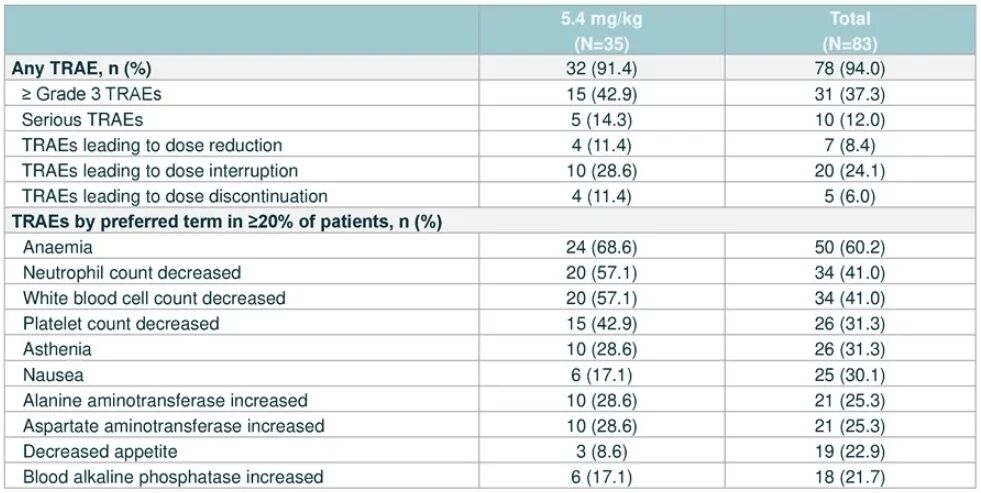
安全性分析显示,任意级别治疗相关不良事件(TRAEs)的发生率为94.0%,≥3级TRAEs的发生率为37.3%,未发生TRAE导致的死亡。
表4 安全性分析
SKB315在晚期实体瘤患者中表现出可控的安全性,对于表达CLDN18.2的晚期GC/GEJC患者中,治疗显示出有前景的抗肿瘤活性。这些研究结果支持在表达CLDN18.2的实体瘤患者中对SKB315进行进一步评估。
参考文献(向上滑动查看):
1. Jinfeng Ma, et al. Phase I/II study of claudin 18.2 ADC ATG-022 in patients with advanced gastric/gastroesophageal junction cancer (CLINCH). 2025 ESMO 2113P
2. Ting Deng, et al. SKB315, a novel claudin 18.2 (CLDN18.2) antibody-drug conjugate (ADC), in patients (pts) with advanced solid tumors including gastric/ gastroesophageal junction cancer (GC/GEJC): A phase I study. 2025 ESMO 2139P
撰写:Babel
排版:Babel
执行:Babel

(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)