2021年美国圣安东尼奥

背景:Datopotamab deruxtecan(Dato-DXd)是一种靶向Trop2的ADC药物,由人源化抗TROP2 IgG1单克隆抗体与有效载荷强效拓扑异构酶I抑制剂通过稳定的四肽可裂解连接子偶联而成。I期TROPION-PanTumor01研究的初步结果表明,Dato-DXd在非小细胞肺癌(NSCLC)患者(Meric-Bernstam,ASCO 2021)和三阴性乳腺癌(TNBC)患者(Bardia,ESMO BC 2021)中具有令人鼓舞的抗肿瘤活性和可管理的安全性特征。此处公布了TNBC队列的更新结果。
方法:TROPION-PanTumor01(NCT03401385)是一项在既往接受过治疗的实体瘤患者中评价Dato-DXd的I期、多中心、开放标签、多队列研究。根据NSCLC患者的剂量递增结果,研究对于既往接受过标准治疗后复发/进展的转移性TNBC和HR+/HER2-乳腺癌患者中给予Dato-DXd,6 mg/kg,每3周一次,静脉给药。2例TNBC患者在选择6 mg/kg进行剂量扩展前接受了8 mg/kg Dato-DXd。由盲态独立中心审查委员会(BICR)根据RECIST第1.1版评估安全性和疗效,包括客观缓解率(ORR)。
结果:截至数据截止日期2021年4月6日,44例TNBC患者接受了≥1次Dato-DXd,中位年龄为53岁(范围:32-82岁)。30例患者(68%)既往接受过≥2线治疗;19例患者(44%)既往接受过免疫治疗,7例患者(16%)既往接受过PARP抑制剂治疗。中位治疗持续时间为2.8个月(范围:0.7-6.9个月)。中位随访3.9个月(范围:0.3-9.2个月)。
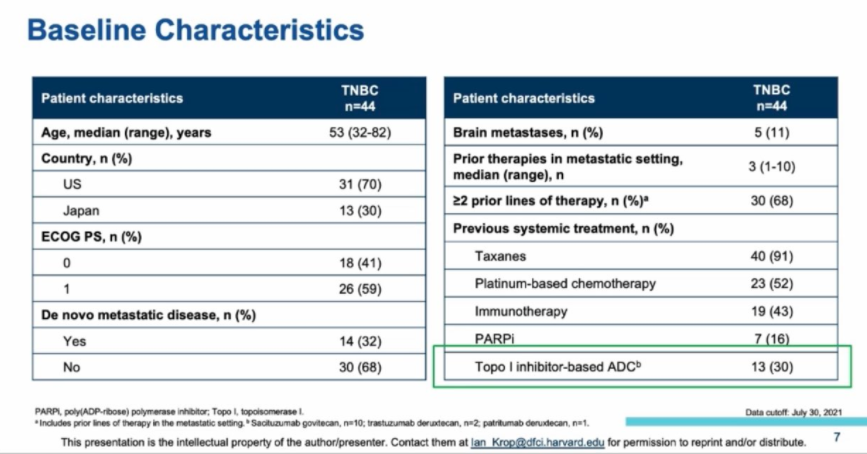
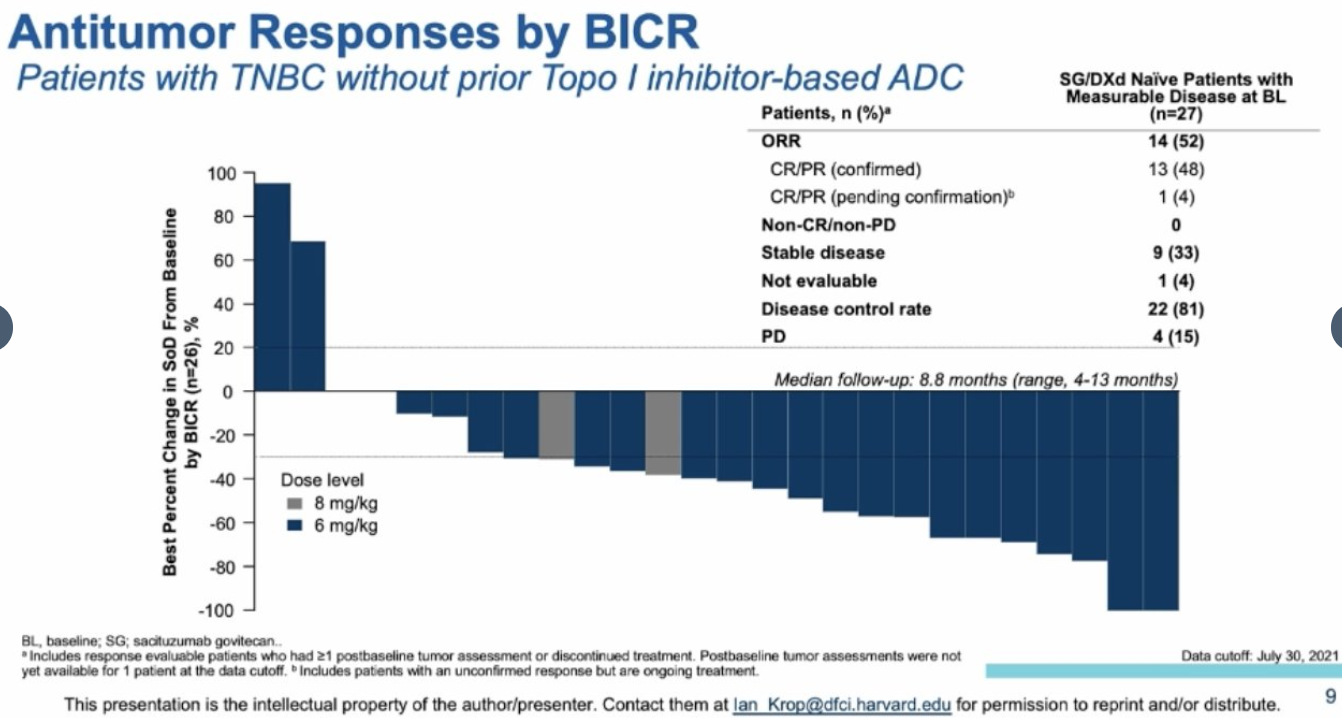
疗效数据显示,在整体患者中BICR评估的ORR为34%,疾病控制率(DCR)为77%(34/44)。

既往未接受过拓扑异构酶Ⅰ抑制剂为基础的ADC药物治疗的患者ORR为可达52%。
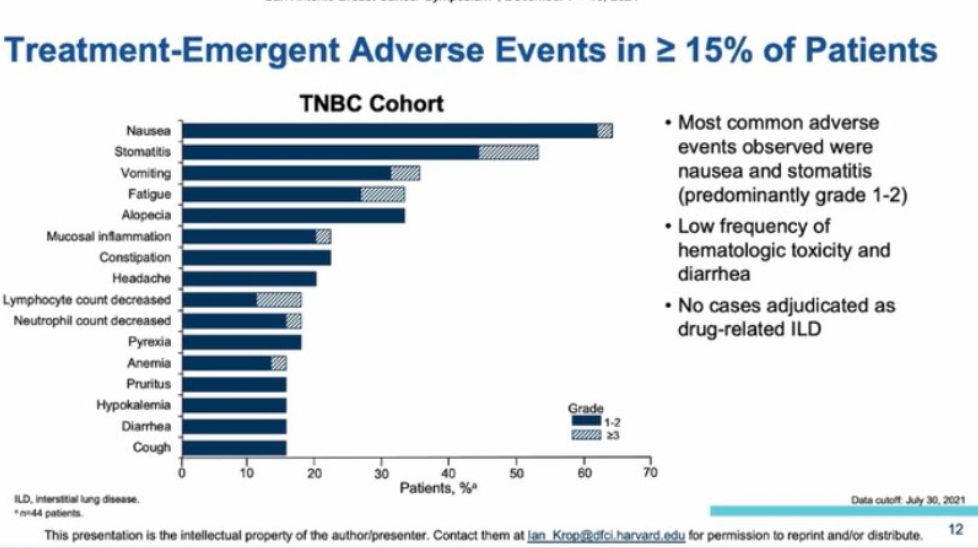
安全性方面,在95%和35%的患者中分别观察到因治疗导致的任何等级和≥3级的不良事件(TEAE);2例为4级。最常见(≥30%)和≥3级的TEAE包括恶心(58%,0%)、口腔炎(53%,9%)、脱发(35%,N/A)、呕吐(35%,2%)和疲乏(33%,7%)。1例患者发生3级中性粒细胞计数降低;未观察到≥3级
结论:该研究初步结果表明,Dato-DXd在既往接受过治疗的晚期/转移性TNBC患者中表现出有前景的抗肿瘤活性和可管理的安全性特征,需要在乳腺癌患者中进一步进行验证。
参考文献:
GS1-05 Datopotamab deruxtecan in advanced/metastatic HER2- breast cancer: Results from the phase 1 TROPION-PanTumor01 study.Presented at: 2021 San Antonio Breast Cancer Symposium; December 7-10, 2021; San Antonio, TX.
(本网站所有内容,凡注明来源为“医脉通”,版权均归医脉通所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:医脉通”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们。)