
编者按
眼科医生并不陌生这些场景:
但《Progress in Retinal and Eye Research》2026年发表的这篇综述,把问题往前推进了一步:眼睛并不是大脑之外的孤立器官,视觉输入、眼表感觉、视网膜神经节细胞投射、炎症反应等功能都可能参与情绪调控。换句话说,眼病与情绪障碍之间,不只是“患病后心情不好”,而可能存在一条更深的眼-脑轴。
这篇综述由眼科、精神科、神经生物学和计算机科学团队共同完成,聚焦抑郁和
哪些常见眼科疾病容易合并情绪障碍?
摘要
眼-脑轴的核心,是把“眼睛看见”理解为一种神经、免疫和行为共同参与的调节事件。例如,视网膜可通过RGCs(视网膜神经节细胞)和ipRGCs(内在光敏视网膜神经节细胞)把光信号投射到与昼夜节律、恐惧、奖赏、睡眠和情绪有关的脑区;眼表疼痛和干涩可经三叉神经进入脑干,参与慢性疼痛和中枢敏化;眼内炎症、血眼屏障和血脑屏障异常,则可能通过体液和免疫通路影响中枢状态。
从临床角度看,青光眼、AMD、DR、干眼和
正文
01:眼睛为什么不只是“视觉器官”?
视觉系统之所以特殊,是因为它既承担环境信息输入,又与大脑多个情绪相关网络直接相连。综述指出,RGCs和ipRGCs可投射到约42个脑区核团。这些投射并不只通往传统意义上的视觉中枢,也包括SCN(视交叉上核)、杏仁核、BNST(终纹床核)、缰核、上丘和下丘脑等区域。
这些脑区对应的功能非常关键:SCN调节昼夜节律,杏仁核和BNST参与恐惧和焦虑反应,缰核与奖赏/厌恶加工有关,上丘参与快速定向和警觉反应。也就是说,光线和视觉信息进入眼内后,并不是只生成一幅图像,还会参与睡眠、警觉、应激和情绪状态的调节。
这也解释了为什么某些眼病患者的表现不只限于视力下降。慢性视觉输入减少或异常,可能影响睡眠节律、活动范围、社交参与和奖赏反馈;眼表疼痛和畏光则可能让患者进入长期警觉和回避状态。眼病造成的情绪负担,既有生活层面的原因,也有神经通路层面的基础。
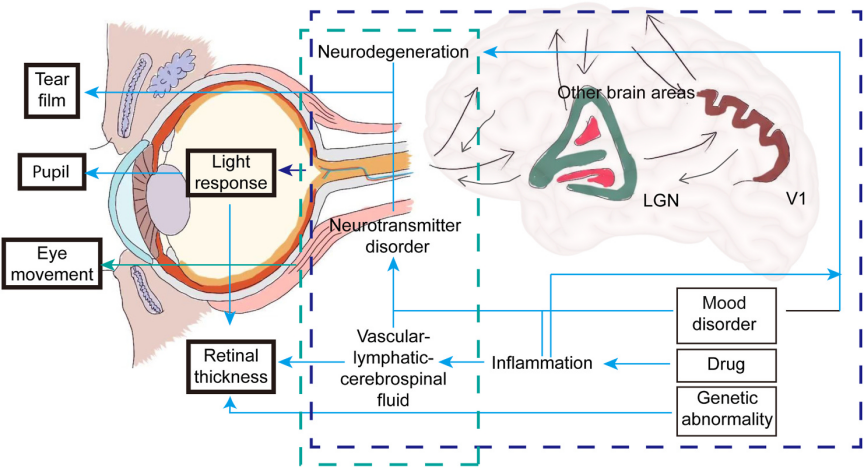
原文 Fig. 12:视觉输入、眼部信号与情绪调控通路的关系示意
02:三条通路,把眼病和情绪障碍串起来
第一条通路是视觉输入异常或视觉剥夺。青光眼、AMD、糖尿病视网膜病变和
第二条通路是眼表感觉和慢性疼痛。干眼、神经病理性眼痛和葡萄膜炎等疾病,常伴随烧灼感、异物感、畏光和反复疼痛。长期外周刺激可诱发中枢敏化,使患者出现“症状重、体征轻”的不匹配。此时,眼表不适已经不只是局部表面病变,而是进入了疼痛调节和情绪调节系统。
第三条通路是炎症和血管-脑脊液循环。AMD、DR、葡萄膜炎、干眼和高度近视等疾病,都可能伴随局部或系统炎症。炎症因子、血眼屏障和血脑屏障改变、血管-淋巴-脑脊液循环异常,可能把眼部病变与中枢炎症联系起来。综述也强调,目前许多细节仍来自动物和基础研究,不能简单等同于临床因果,但这条方向已经值得重视。
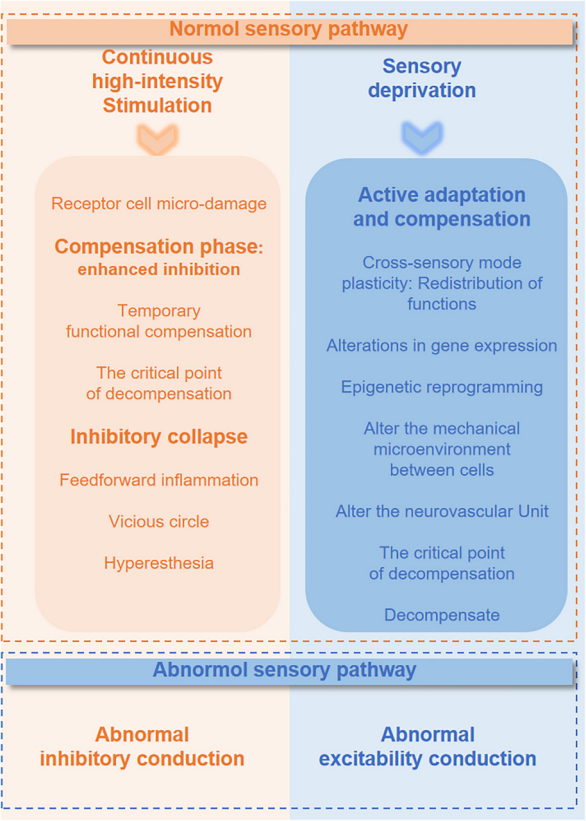
原文 Fig. 8:眼与脑之间的血管、淋巴和脑脊液循环联系
03:不同眼病的情绪风险,并不是同一种逻辑
综述汇总显示,约25%眼病患者会经历
干眼患者抑郁风险可升高约2.9倍,部分研究显示29%~40%干眼患者存在抑郁症状。这里的重点不是“眼干让人烦躁”,而是疼痛、睡眠、神经敏化、症状体征不匹配和用药因素共同作用。葡萄膜炎患者的抑郁比例约17%,非感染性葡萄膜炎研究中可达35%,复发、疼痛、激素治疗和视力预后不确定性都会参与。
视网膜退行性和血管性疾病则更多牵涉慢性视觉剥夺和代谢炎症。AMD患者抑郁比例在不同研究中约7.2%~38.6%;糖尿病视网膜病变与抑郁呈双向关系,抑郁会影响血糖、血压、自我管理和随访依从性,反过来加重眼病管理难度。高度近视、斜视和白内障还叠加外观、社交和生活质量因素,不能只从屈光或晶状体混浊本身解释。
表1:眼-脑轴视角下,眼病与情绪障碍的主要连接方式
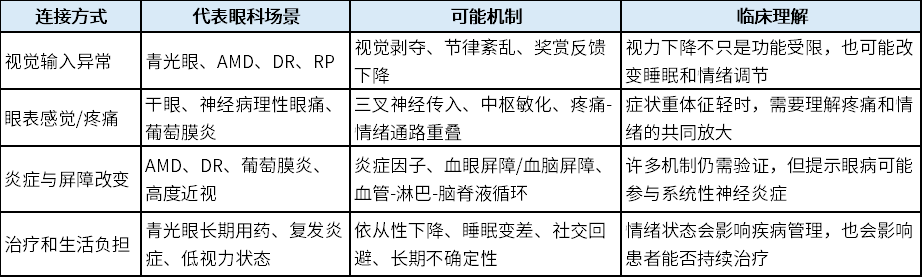
AMD:年龄相关性黄斑变性;DR:糖尿病视网膜病变;PR:视网膜色素变性
04:情绪障碍也会“反写”到眼睛上
这篇综述很重要的一点,是强调关系并非单向。抑郁症患者可出现模糊或波动性视物、对比敏感度下降、
眼表方面,抑郁与睑板腺功能障碍(MGD)和干眼关系密切。SSRIs、SNRIs等药物可能减少泪液分泌或加重眼表不适;自主神经和神经内分泌改变也可能影响泪腺和睑板腺功能。换句话说,精神心理状态、药物、泪膜和眼表炎症之间可能互相影响。
视网膜结构和血管参数也可能成为观察窗口。综述提到,情绪障碍患者可出现RNFL、GCL和黄斑区厚度变化,双相障碍患者还可能存在深层视网膜血管密度和脉络膜厚度改变。这些变化目前还不能作为独立诊断标准,但提示眼科影像可能参与精神疾病的辅助评估和风险分层。
05:从
综述提出,未来跨学科管理可以从两端推进。一端是筛查和评估:对视觉受损、慢性干眼、长期用药、复发炎症或主诉与体征不匹配的患者,可考虑使用PHQ-9、HADS、GAD-7等工具进行初步情绪筛查。同时,OCT、OCTA、角膜共聚焦显微镜、ERG、FLIO和眼动分析,可能成为观察情绪障碍眼部表现的客观工具。
另一端是干预。光疗通过ipRGCs和SCN调节昼夜节律,常用强度约10,000 lux,每天30~60分钟或1~2小时。视觉皮层刺激、眼动训练、EMDR、VR/AR、视觉生物反馈和脑机接口结合的沉浸式干预,也被综述纳入未来方向。
更稳妥的理解是:视觉系统既可能被眼病破坏,也可能成为调节情绪网络的入口。未来真正有价值的,可能是眼科、精神科、神经科学、康复和人工智能共同建立一套更完整的评估和干预路径。
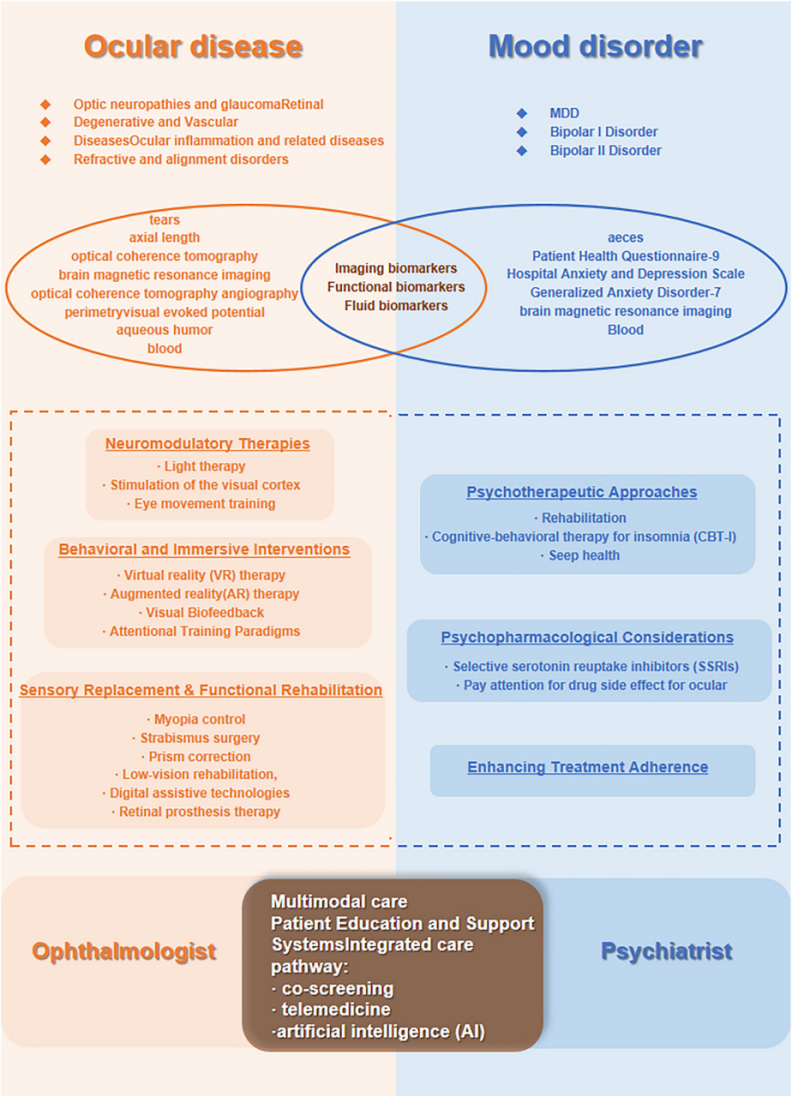
原文 Fig. 15:眼病与情绪障碍的跨学科诊疗框架
结语与展望
眼-脑轴最值得重视的地方,是它把眼科慢病从“局部器官疾病”重新放回神经、免疫、代谢和心理的整体网络中。眼病带来的焦虑和抑郁,既可能来自视力下降后的生活受限,也可能来自视觉输入紊乱、慢性疼痛、炎症因子、屏障改变和长期治疗负担。
当然,综述也反复提醒,目前许多机制证据仍来自动物模型、细胞实验或间接临床观察,不能把所有相关性都写成因果。更合理的态度,是把它看作一个正在形成的解释框架:它帮助我们理解为什么同样的眼病,不同患者会有完全不同的疼痛、睡眠、依从性和生活质量表现。
一句话总结:眼-脑轴不是一句概念,而是提醒我们,眼科结局不只取决于视力、
参考文献
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。