
2026年欧洲肿瘤内科学会
医脉通特此选取两项口头报告,围绕ctDNA在临床监测与检测方法学的最新研究进展展开解读。
1O|TRAK-ER研究中高危HR+/HER2-乳腺癌监测期间ctDNA的检出率[1]
既往研究显示,在HR+乳腺癌辅助内分泌治疗(ET)期间检测ctDNA,可较高准确度地预测疾病复发。TRAK-ER研究旨在评估高危HR+/HER2-乳腺癌患者接受辅助ET期间开展ctDNA动态监测的可行性及其在分子复发预警中的应用价值。
TRAK-ER是一项随机、多中心研究,计划纳入1100例高危HR+/HER2-乳腺癌患者,在辅助ET期间每3个月进行一次ctDNA监测,持续3年。(注:入组患者需已接受至少6个月、且不超过7年的辅助ET治疗。)
该研究采用基于全外显子测序ctDNA检测技术(Labcorp),追踪18~50个患者特异性突变位点。若检测到ctDNA阳性,患者需接受影像学评估;如未发现影像学转移,则随机接受
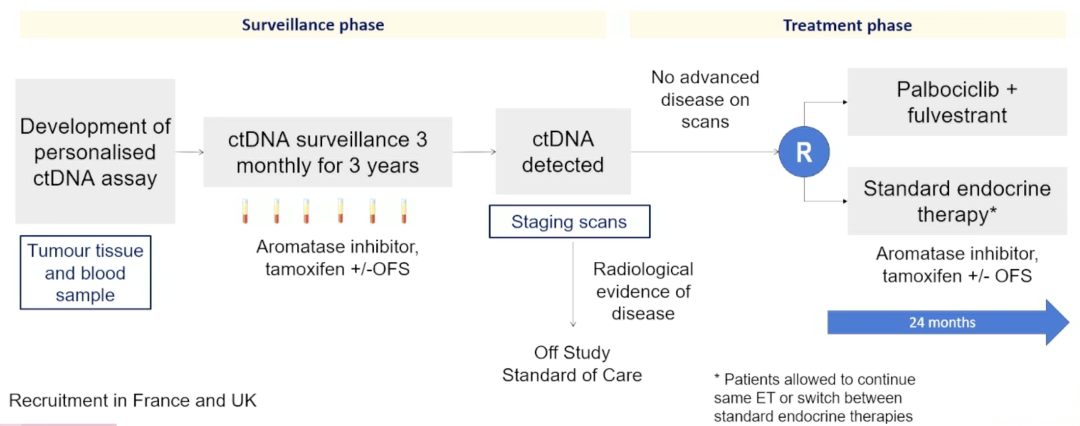
图1 研究设计[1]
截至2025年9月1日,共1104例患者完成注册,研究共计对901例患者进行了5724次ctDNA监测,总体检出率为1.9%(107/5724);11.6%(105/901)的患者在至少一个时间点检测到ctDNA阳性。
首次监测(M0)ctDNA检出率显著高于后续监测(M3+)(5.0% vs. 1.3%,p<0.0001)。
在进行ctDNA检测时,42.9%的患者出现疾病复发,其中M0组中65.9%的患者已存在转移性疾病,而M3+组为26.2%。从数值趋势来看,ctDNA检出率随淋巴结分期升高逐渐提升,IIIc 期患者ctDNA检出率较高,1级肿瘤患者ctDNA检出率则相对更低。
此外,按时间分层分析显示,术后ctDNA年度检出率分别为:第1年6.1%,第2年5.3%,第3年7.2%,第4年4.5%,第5年5.6%,第6年3.5%,第7年5.4%。
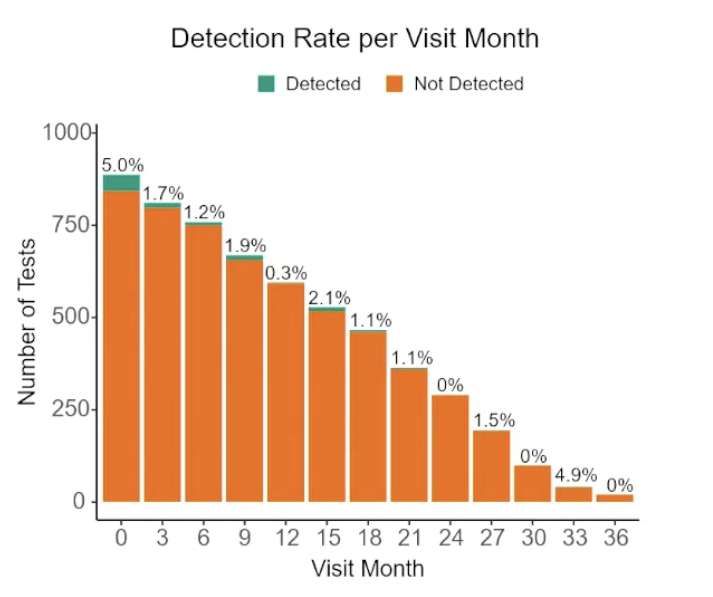
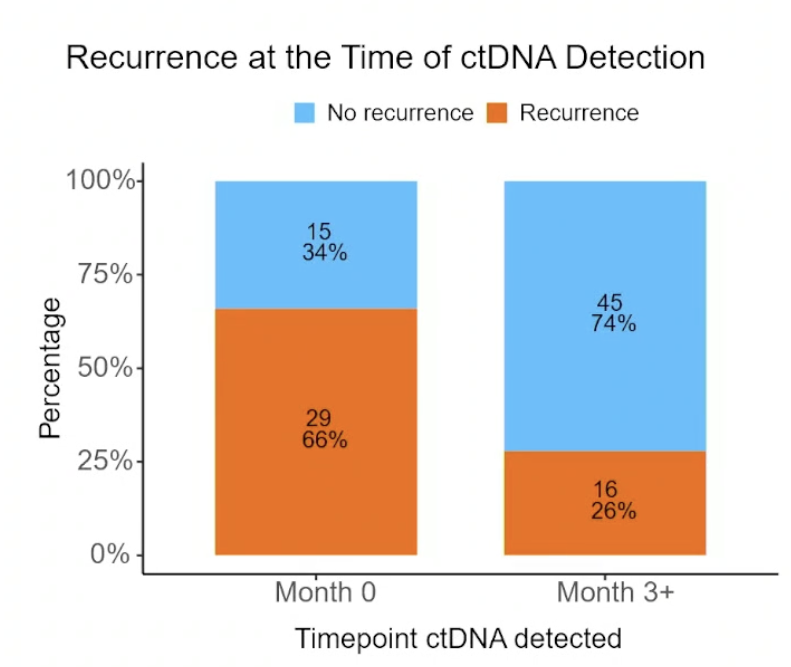
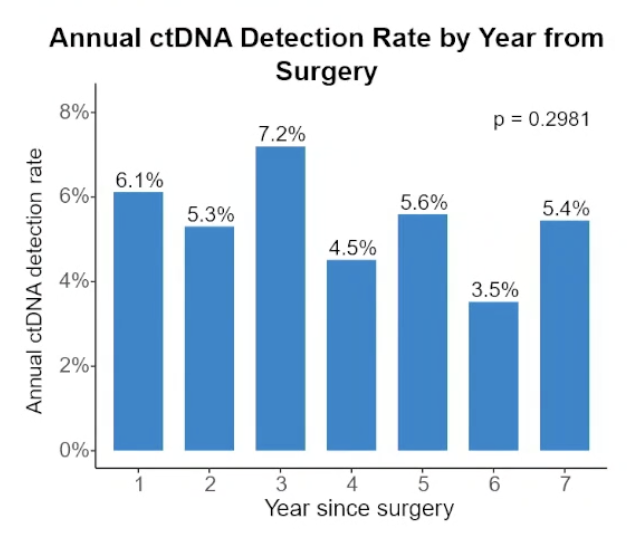
图2 研究结果:不同时间节点ctDNA检出率及乳腺癌复发率[1]
TRAK-ER研究显示,ctDNA连续动态监测可在高危HR+/HER2-乳腺癌患者中实现分子复发的早期识别,进一步支持ctDNA在MRD监测及风险预警中的临床应用潜力。
4RO|早期三阴性乳腺癌中无组织ctDNA检测与多变异肿瘤知情型检测方法的比较分析[2]
ctDNA检测已成为微小残留病灶(MRD)监测的重要工具。传统肿瘤知情型检测依赖原发肿瘤测序信息,而基于肿瘤与非肿瘤DNA差异表观遗传特征的“无组织”检测方法,有望在无需肿瘤样本的情况下实现ctDNA识别,从而简化检测流程,并在性能相当时为MRD监测提供更具可及性的替代方案。本研究基于cTRAK-TN试验数据,对无组织检测与肿瘤知情型检测进行回顾性比较。
本研究利用cTRAK-TN(NCT03145961)前瞻性队列中采集的样本开展回顾性分析。该研究共纳入161例高危三阴性乳腺癌(TNBC)患者,在完成辅助治疗后接受每3个月一次ctDNA监测,最长随访2年。
既往ctDNA检测采用肿瘤知情型多变异检测方法(RaDaR),通过原发肿瘤全外显子测序追踪最多48个个体特异性突变。本研究进一步使用无组织检测方,基于甲基化差异特征分析159例患者共计1062个样本,并在其中133例患者的809个样本中进行两种方法的对比分析。
研究结果
133例患者的809个样本中,两种检测方法结果一致率为95.2%(770/809)。
在患者层面,61.7%(82/133)的患者为ctDNA阴性;30.8%(41/133)在两种检测方法下均呈ctDNA阳性;另有7.5%(10/133)检测结果不一致。41例ctDNA阳性患者中,29.3%(12/41)的患者接受肿瘤知情型检测较无组织检测更早检出ctDNA阳性,而2.4%(1/41)则由无组织检测率先检出阳性结果。
此外,从首次检出ctDNA阳性到临床复发的中位时间为:肿瘤知情型检测7.1个月(95% CI 5.7–10.0个月),无组织检测7.6个月(95% CI 4.6–10.5个月),两者差异无统计学意义(HR 1.46,95% CI 0.87–2.44;p=0.154)。
无组织ctDNA检测与肿瘤知情型检测在整体检测性能及疾病预警时间方面具有高度一致性。该结果支持无组织检测方法在临床试验中的应用潜力,尤其适用于缺乏可用肿瘤组织样本的情境,但其临床应用价值仍需进一步前瞻性研究验证。
参考文献:
1.Niamh Cunningham,et al.ctDNA detection rates during surveillance in high-risk HR+/HER2 negative breast cancer from the TRAK-ER study.2026 ESMO BC 1O.
2.Niamh Cunningham,et al.A comparative analysis between tissue-free ctDNA detection and a multivariant tumour-informed assay in early triple-negative breast cancer.2026 ESMO BC 4RO.
撰写:Ocean
审校:Ocean
排版:Ocean
执行:Ocean
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。