
前言
肺癌是全球发病率与死亡率双高的恶性肿瘤。生物标志物的持续发现与临床转化,为肺癌全周期精准防控、早期诊断及个体化治疗开辟了全新路径。本综述立足最新研究进展,系统梳理肺癌生物标志物的核心分类、临床应用价值及未来发展趋势,以期为临床诊疗决策与科研探索提供参考依据。
研究背景与核心分类
肺癌主要分为
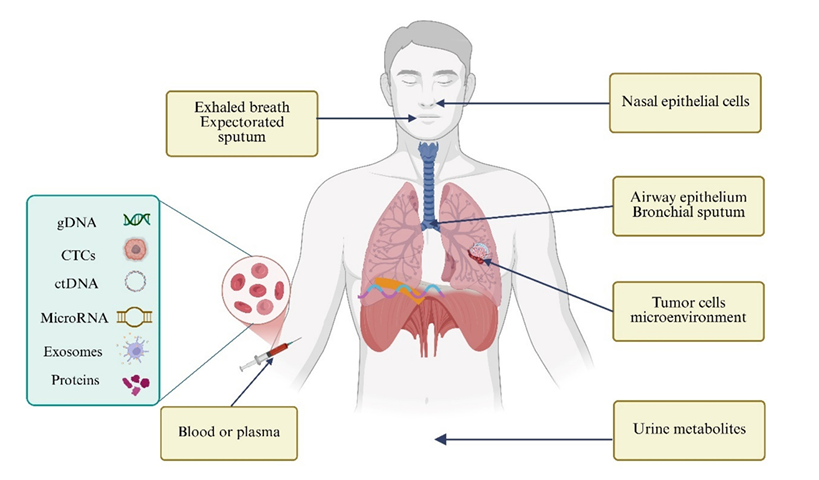
图1. 生物标志物的不同来源
依据临床功能,生物标志物可划分为三类,在诊疗决策全流程中各司其职、精准赋能。
预测性标志物:核心价值在于预判患者对特定治疗的应答效果,为个体化治疗方案的选择提供科学依据。例如,NSCLC中的鳞状分化特征,可提示患者对
诊断性标志物:通过可重复验证的生物学特征(如基因变异、蛋白表达水平等)实现疾病的精准诊断,兼具快速、准确、无创或微创等优势。典型代表包括
预后性标志物:不依赖具体治疗方案,可独立预测疾病的自然进展轨迹与临床结局,同时为解析疾病潜在分子机制提供重要线索。例如,B型脑钠肽(
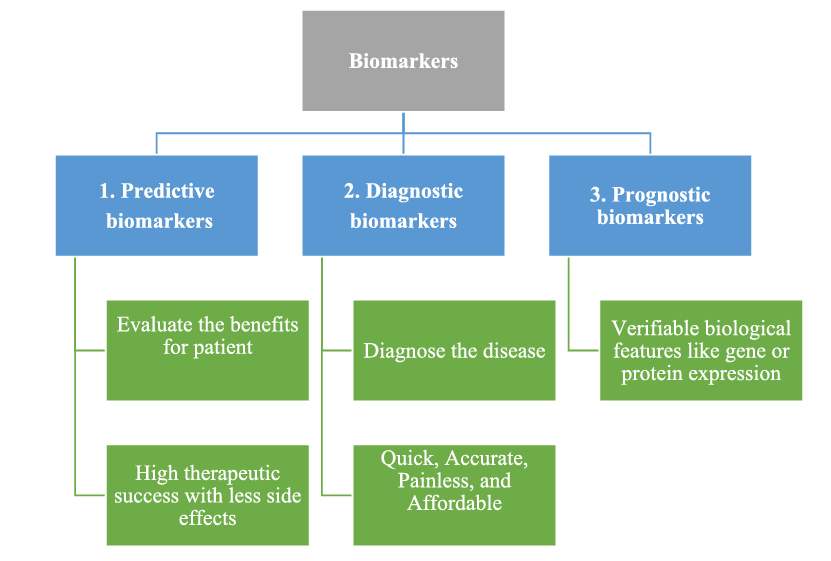
图2. 基于预后的生物标志物
肺癌生物标志物的主要类型
目前,肺癌生物标志物已形成覆盖分子、蛋白质、游离核酸、细胞及微生物等多维度的完整体系,各类标志物凭借独特优势适配不同临床场景。
分子标志物:作为靶向治疗的核心依据,已明确的可行动靶点包括EGFR(常见突变Del19、L858R;罕见突变T790M、G719X等)、ALK融合、ROS1融合、MET exon14跳跃突变、BRAF V600E、NTRK融合等。此外,HER2扩增、PIK3CA突变、FGFR融合等新兴标志物的临床价值正逐步验证,有望进一步丰富靶向治疗的适用人群。
蛋白标志物:癌胚抗原(CEA)、细胞角蛋白19片段(CYFRA21-1)、神经元特异性烯醇化酶(NSE)、
循环肿瘤DNA(ctDNA):作为液体活检的核心指标,ctDNA可通过非侵入性方式精准检测肿瘤基因突变、甲基化模式。其在临床中具有多重关键价值,既能监测靶向治疗耐药(如EGFR T790M突变),为方案调整提供依据;也可评估微小残留病(MRD)状态、预警肿瘤复发。其浓度变化与肿瘤负荷、患者预后密切相关,是动态反映疾病进展的重要分子标尺。
无细胞DNA(cfDNA):除肿瘤源性ctDNA外,cfDNA的片段长度特征(肿瘤来源片段通常更短)、特异性甲基化图谱(如SHOX2、RASSF1A位点甲基化)已成为肺癌早期筛查的重要补充手段。基于cfDNA片段组分析开发的DELFI评分等算法,能有效区分良恶性病变,进一步提升早期诊断的精准度。
非编码RNA:微小RNA(miRNA)通过调控基因表达参与肿瘤发生发展,以13-miRNA组合为代表的检测面板,可辅助肺癌风险分层与筛查。长链非编码RNA(lncRNA)如lncMMP-2,已被证实与肺癌脑转移密切相关,其表达水平具有潜在的诊断与预后评估价值,为这类高危转移人群的精准管理提供了新方向。
循环肿瘤细胞(CTCs):SCLC患者的CTCs数量显著高于其他肺癌亚型,其基线计数及治疗后的动态变化是重要的预后预测指标。此外,CTCs的上皮-间质转化(EMT)表型与肿瘤转移潜能密切相关,为评估疾病侵袭性、指导治疗强度提供了关键参考。
免疫细胞与炎症标志物:中性粒细胞-淋巴细胞比值(NLR)、预后营养指数(PNI)、系统性免疫炎症指数(SII)等可综合评估机体免疫状态与营养水平,精准预测患者生存结局。程序性死亡配体1(PD-L1)表达水平是免疫检查点抑制剂(ICIs)治疗的核心预测标志物,高PD-L1表达的患者接受ICIs单药治疗时,往往能获得更优疗效。
外泌体:作为携带DNA、RNA、蛋白等生物分子的功能性囊泡,外泌体的表面整合素(如ITGβ3)已被证实与肺癌脑转移密切相关,其非侵入性检测特性使其成为肺癌诊断、转移风险评估及预后判断的潜在工具。
影像标志物:基于CT、MRI的影像组学技术,结合机器学习算法,能够深度挖掘肿瘤影像学特征,实现肿瘤组织学类型的精准区分、驱动基因突变状态的无创预测及治疗响应的提前预判,为临床决策提供可视化支撑。
微生物标志物:肺与
自身抗体:针对p53、NY-ESO-1等肿瘤抗原的自身抗体,可在肺癌临床症状出现前被检测到,其早期预警特性为肺癌超早期筛查开辟了新方向,有助于提升高危人群的早诊率。
表1. 各类生物标志物的优缺点
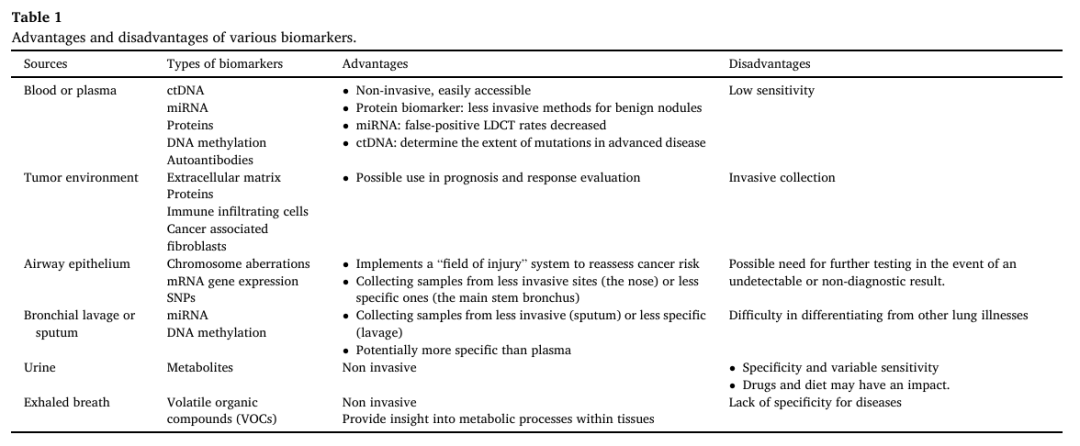
潜在的新兴生物标志物
通用新兴标志物:HER2扩增、PIK3CA突变、BRCA1/2突变、MAP2K1突变、NRG1融合等标志物,目前多与二线治疗相关临床试验紧密结合,其临床价值正逐步验证,未来有望纳入常规检测体系,进一步拓宽精准治疗的覆盖范围。
鳞状NSCLC特色标志物:以FGFR融合、突变或扩增为核心的特色标志物,为这一亚型肺癌的精准治疗提供了全新方向,有望破解其治疗选择有限的困境。
ADC相关标志物:随着抗体偶联药物(ADCs)在胸部肿瘤领域的广泛应用,c-MET、TROP2、CEACAM5、DLL3、HER3、HER2、B7-H3等标志物的临床意义日益凸显,可通过分子检测或免疫组化(IHC)技术明确表达状态,为ADC药物的个体化选择提供依据。
耐药相关标志物:STK11、KEAP1、SMARCA4、NOTCH突变及MTAP表达缺失,已被证实与ICIs原发性耐药密切相关。通过下一代测序(NGS)技术分析EGFR突变肿瘤的共突变情况(如p53突变),有望发现靶向治疗耐药及部分响应的新型标志物,为耐药后治疗方案调整提供支撑。
肿瘤突变负荷(TMB):作为免疫治疗响应的探索性标志物,TMB目前在美国的临床应用中已得到一定认可,但欧洲暂未推荐其常规使用,相关研究结果仍存在争议,其临床价值有待更多前瞻性数据进一步验证。
表2. 用于NSCLC免疫治疗与靶向治疗的生物标志物

表3. 肺癌生物标志物相关的在研临床研究
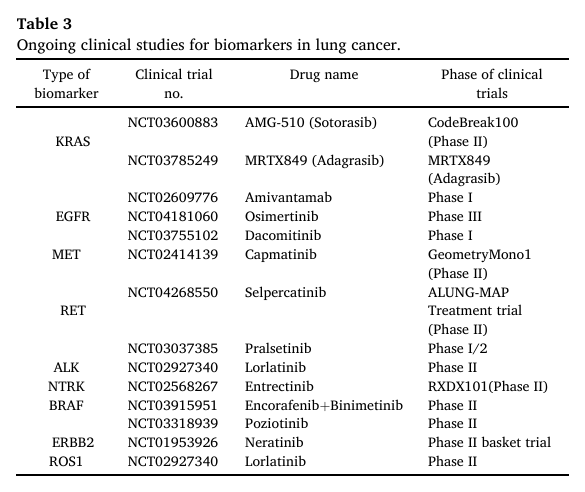
临床应用场景
生物标志物贯穿肺癌风险评估、诊断、治疗、预后监测全流程,在各阶段发挥关键作用。
结合吸烟史、肺癌家族史等临床高危因素,联合miRNA检测面板、cfDNA甲基化等生物标志物,可精准筛选低剂量螺旋CT(LDCT)筛查目标人群,有效降低LDCT的高假阳性率,显著提升早期肺癌检出效率。
针对肺癌患者一级亲属、长期吸烟者等高危人群,采用多模态标志物组合策略(如蛋白标志物+cfDNA甲基化检测),可进一步强化筛查灵敏度,助力超早期肺癌的发现。
肺结节良恶性鉴别:对于中等风险肺结节,将CEA、CYFRA21-1等血清标志物与影像学特征联合分析,可精准评估恶性风险,减少良性结节的不必要活检与手术干预,降低医疗负担与并发症风险。
分子分型确诊:通过NGS技术检测EGFR、ALK等驱动基因突变,为靶向治疗提供明确依据。液体活检作为组织活检的重要补充,尤其适用于无法获取组织样本的晚期患者,实现分子分型的无创化与快速化。
预后分层:EGFR突变、ERRC1高表达通常提示患者预后较好,而KRAS突变、p53突变及高中性粒细胞-淋巴细胞比值(NLR)则与不良预后相关。ctDNA检测提示的MRD阳性,是患者复发风险升高的强力预警信号,可较影像学提前预判复发。
治疗响应监测:靶向治疗期间,ctDNA突变丰度的动态下降提示治疗有效,若检测到EGFR C797S等新的耐药突变,则提示需及时调整治疗方案。ICIs治疗中,动态监测PD-L1表达水平及TMB变化,可实时评估疗效,指导治疗决策。
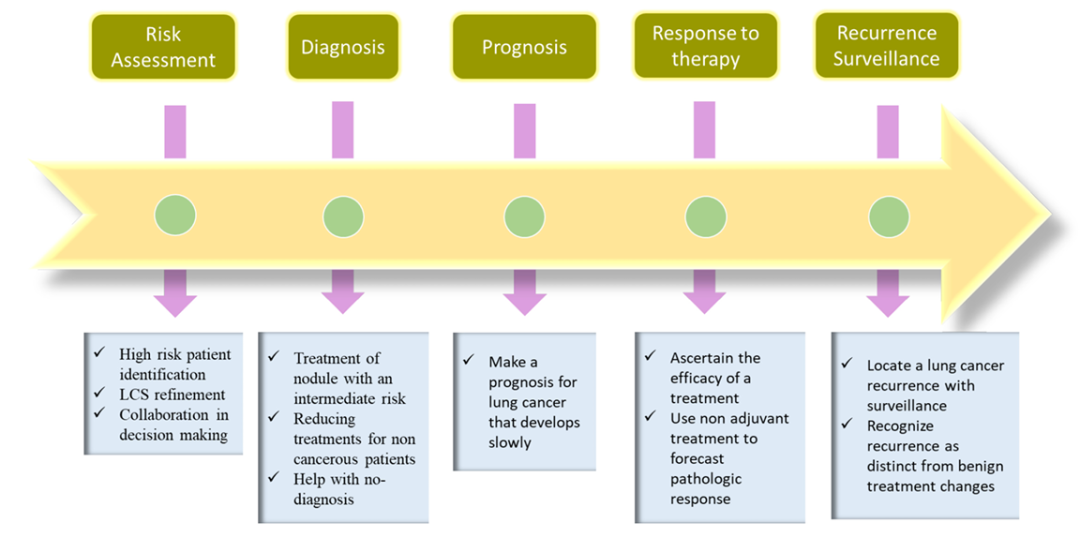
图3. 生物标志物在肺癌不同病程阶段中的应用
技术赋能与应用挑战
传统统计方法认为,NSCLC的生物标志物在治疗决策中呈相互排斥关系,但越来越多证据表明其可在肿瘤中共存,需同时分析线性与非线性效应。机器学习(ML)凭借灵活的模型构建能力,能够精准识别高维数据中的复杂非线性关联,为多标志物协同分析提供技术可能。
在临床应用中,AI/ML辅助医疗设备可自动完成肺CT图像的组织分割与特征提取,深度学习方法则助力数字病理的全切片图像分析,显著优化了NSCLC的诊断流程,同时为新型生物标志物的挖掘提供了高效技术支撑。
此外,Biomarker Base、TCGA、GEO、MetaboAnalyst等丰富的数据库与分析工具,能够实现基因组、转录组、蛋白组等多组学数据的可视化与深度解析,加速了生物标志物的发现、表征与临床转化进程。
当前肺癌生物标志物的临床应用仍面临多重核心挑战。肺癌的高度异质性导致单一标志物难以全面覆盖不同亚型与个体差异,多标志物联合检测虽为必然趋势,但缺乏统一的最优组合方案与标准化检测流程。多数标志物停留在临床前或小样本研究阶段,缺乏大规模、多中心前瞻性试验验证,制约了其向临床常规应用的转化。同时,生物样本库的规范化建设、患者数据隐私保护等伦理与实操问题,也需重点考量。
未来,肺癌生物标志物的发展将通过融合基因组、转录组、蛋白组、微生物组等多维度数据开展多组学整合分析,构建全面的肿瘤分子图谱,突破单一维度检测的局限性,实现更精准的风险分层、疗效预测与治疗指导。同时,相关研究应聚焦肿瘤微环境、代谢组学、单细胞水平等新兴研究领域,研发新型标志物,挖掘更多潜在可行动靶点,丰富肺癌生物标志物的类型与临床价值,为精准诊疗提供新的突破方向。

小结

参考文献:Mangang KN, Rao GSNK. Lung cancer biomarkers. Clin Chim Acta. 2026 Jan 30;580:120707.
撰写:Kenken
审校:Faline
排版:Kenken
执行:Faline
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。