难治性 SLE 相关免疫性血小板减少症(SLE-ITP),最新指南推荐的标准化诊疗流程与治疗方案是什么?
????点击下图,进入MedSeeker,一键获取该类患者结构化诊疗路径与推荐治疗方案

研究设计
本研究为一项研究者发起的单臂、开放标签、剂量递增临床试验(NCT05930314),纳入6例难治性SLE-ITP患者。患者接受自体抗CD19 CAR-T细胞单次输注,前3例为低剂量组(0.5×10⁶ CAR阳性T细胞/kg),后3例为高剂量组(1×10⁶/kg),输注前予以
研究结果
截至末次随访(中位12个月),所有6例患者均获得临床缓解,其中3例达到CR,3例为PR(图1A)。血小板计数在中位2个月(1-5个月)首次达到缓解水平,并在长期随访中保持稳定(图1B)。
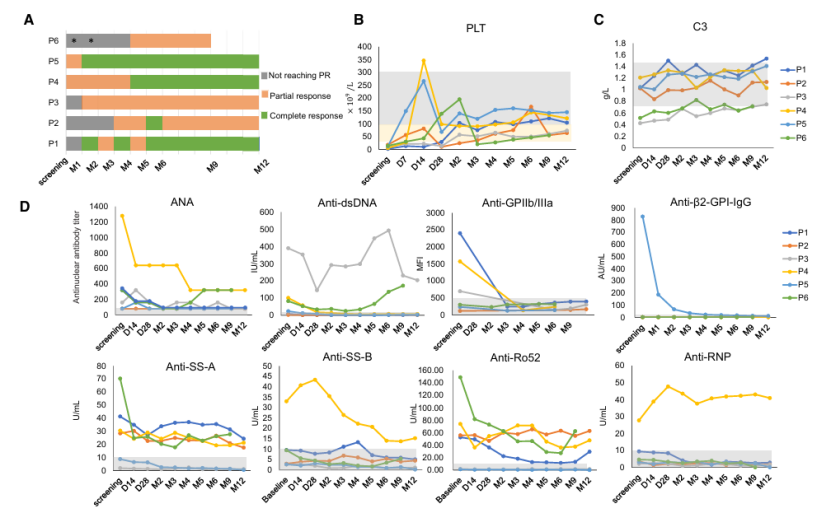
图1:CD19 CAR-T 细胞治疗在系统性红斑狼疮难治性免疫性血小板减少症患者中的临床疗效
所有患者均停用免疫抑制剂,并将
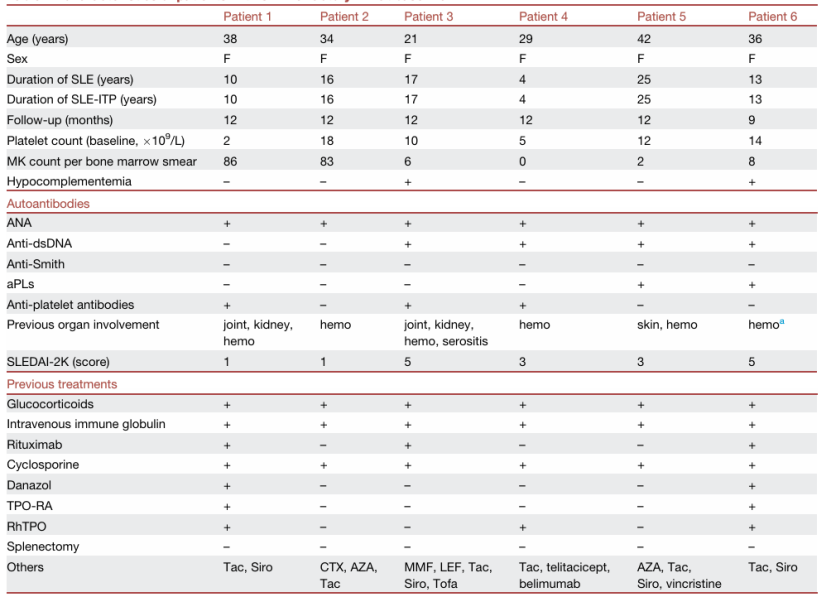
表1:基线时系统性红斑狼疮难治性免疫性血小板减少症患者的特征
所有患者输注后CAR-T细胞数量快速扩增,中位峰值出现在第14天(380/μL),随后逐渐下降,但部分患者可检测至12个月。外周血CD19⁺ B细胞在输注后第7天基本清除,中位B细胞缺乏持续时间为83天(53-263天)。B细胞重建后以幼稚B细胞为主,记忆B细胞比例在早期重建时显著降低,提示免疫系统重置。
为进一步探索CR与PR患者疗效差异的机制,研究对治疗前后骨髓样本进行了单细胞多组学分析。结果显示,CR患者治疗后骨髓呈显著免疫重置特征:祖B细胞(pro-B及pre-B)比例明显上升,
巨核细胞生成方面,PR患者表现出持续的巨核细胞成熟障碍。单细胞ATAC测序显示,PR患者巨核细胞祖细胞中与成熟及多倍体化相关的通路活性明显减弱(图2D),且多个关键调控基因(如GATA2、RUNX1、FLI1)启动子区染色质可及性降低(图2E)。外周血小板来源RNA测序进一步验证,PR患者中巨核细胞功能相关基因(如ATXN2、GP9)表达下调(图2F)。
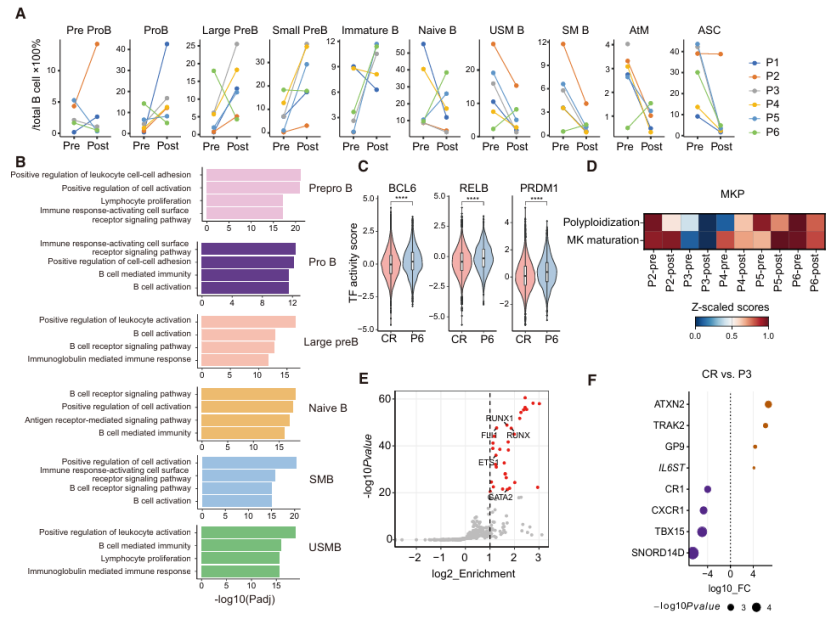
图2:单细胞多组学揭示部分应答者骨髓中不完全免疫重置特征
研究结论
本研究证实,抗CD19 CAR-T细胞疗法在难治性SLE-ITP患者中具有良好的安全性与显著疗效,所有患者均获临床缓解并实现免疫抑制剂减停。部分患者仅达部分缓解,其机制与骨髓中持续存在的浆细胞、B细胞信号通路过度活化及巨核细胞成熟障碍密切相关。上述发现提示,单纯外周B细胞清除不足以实现完全免疫重塑,骨髓微环境的深度重置可能是达到完全缓解的关键。本研究为CAR-T细胞疗法在难治性自身免疫病中的应用提供了重要依据,并提示未来需针对骨髓内残留浆细胞及巨核细胞功能进行更精准的治疗干预。
研究讨论
本研究为抗CD19 CAR-T细胞疗法在难治性SLE-ITP中的应用提供了重要临床证据,并通过单细胞多组学揭示了CR与PR患者间骨髓免疫重塑的差异。尽管所有患者均实现外周B细胞深度清除,但部分患者仅获PR,提示外周血指标无法完全反映治疗的真实深度。PR患者(如P3、P6)治疗后抗dsDNA抗体持续阳性,骨髓中浆细胞持续存在,表明CD19 CAR-T疗法可能因浆细胞表面CD19表达下调而难以彻底清除长寿命浆细胞,这可能是PR的核心机制之一,为未来靶向BCMA或CD19/BCMA双靶点CAR-T疗法提供了理论依据。
值得注意的是,PR患者骨髓中不仅存在B细胞谱系异常重建,还表现出巨核细胞成熟持续障碍。单细胞ATAC-seq数据显示,PR患者巨核细胞祖细胞中与分化及多倍体化相关的转录因子(如GATA2、RUNX1、FLI1)活性显著下降,提示骨髓微环境中可能存在独立于B细胞的病理机制,持续抑制血小板生成。该发现解释了为何外周B细胞清除后仍无法实现完全缓解。
此外,本研究通过多组学数据识别了若干潜在外周血生物标志物,如ATXN2、GP9等,其在PR患者中表达显著下调。ATXN2已被报道在早期巨核细胞生成中调控mRNA翻译,提示其可能作为预测疗效的候选标志物,但尚需更大规模队列验证。
参考文献:Li M, Zhao J, Lu ZJ, Ning C, Jiang N, Zhang Y, Li Y, Feng Y, Wang Q, Xu D, Leng X, Li J, Zhang S, Wang Z, Peng L, Tian X, Lv L, Zhou D, Zeng X. Anti-CD19 CAR-T cell therapy for refractory SLE-ITP. Med. 2026 Mar 18:101039.
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。