导 语
本期要点
mIDH1导致2-HG异常代谢,促进AML的疾病发生发展。前IDH1抑制剂时代,mIDH1 AML患者缓解率低、预后不佳。
艾伏尼布(IVO)作为全球首个、目前国内唯一获批的IDH1抑制剂,单药治疗复发/难治性(R/R)mIDH1 AML可带来持久深度缓解。
临床研究显示,以IVO为基础的联合治疗方案可显著提升新诊断mIDH1 AML的缓解率、延长生存期,对伴共突变的高危患者同样有效。
多项真实世界研究一致证实,以IVO为基础的联合治疗方案缓解率高、生存获益显著、耐受性良好,与临床研究结论一致。目前国内外指南均推荐含IVO方案治疗mIDH1 AML。
▲ 点击观看视频
mIDH1 AML疾病特征:机制明确,
预后不良,需求未满足
异柠檬酸脱氢酶(IDH)是三羧酸循环中的关键代谢酶,哺乳动物体内存在三种IDH酶:IDH1、IDH2和IDH3,其中IDH1和IDH2的突变与多种肿瘤的发生发展密切相关[1-4]。IDH突变驱动AML的核心机制在于:编码IDH的基因突变后,IDH突变体将α-酮戊二酸(α-KG)异常催化生成D-2-羟基戊二酸(D-2HG)。由于2-HG与α-KG结构相似,可竞争性抑制α-KG依赖性酶(包括羟基化酶、组蛋白甲基化酶、DNA甲基化酶等),导致DNA和组蛋白高度甲基化,进而阻断原始细胞分化并促进其无节制增殖,最终导致AML发生[5-7]。
流行病学数据显示,我中国AML患者mIDH1发生率为6%-10%[8-9]。值得注意的是,既往研究表明IDH突变率随年龄增长呈上升趋势:儿童(0-17岁)中为3.4%,年轻人(18-39 岁)中为11.3%,中年人(40-59岁)中为17.7%,≥60岁老年人群中高达21%(图1)[10]。
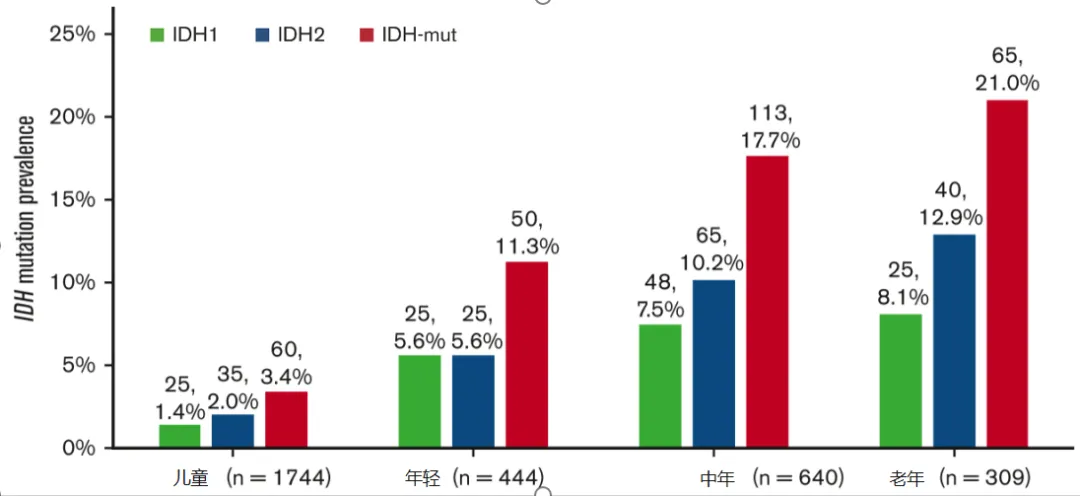
图1. AML患者中IDH突变率随年龄增加
在IDH1抑制剂问世之前,mIDH1 AML患者的治疗结局显著不佳。中国一项多中心回顾性研究分析了IDH突变AML患者在真实世界中的生存情况[11]。结果显示,接受强化疗方案治疗的mIDH1患者中位OS仅9.8个月,低于IDH野生型及mIDH2患者;即便是使用当时主流的维奈克拉联合去甲基化药物(VEN+HMA)方案,mIDH1 AML患者的生存获益仍十分有限——中位OS仅13.3个月(图2),凸显了这类患者在传统治疗下存在的巨大未被满足的临床需求。
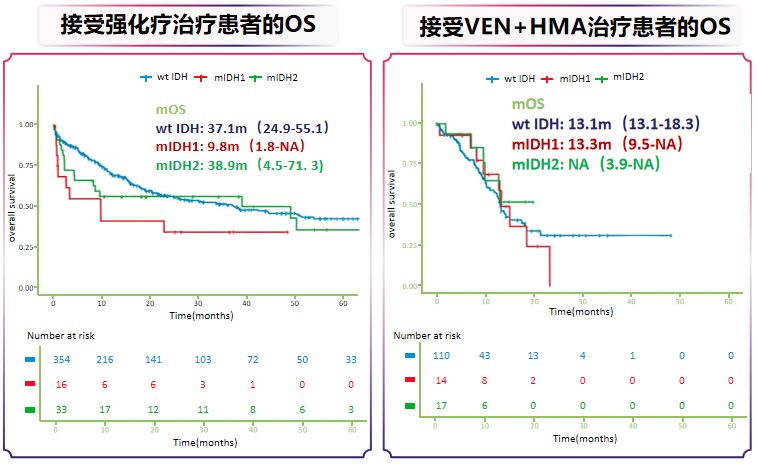
图2. 接受强化疗治疗(左)以及VEN+HMA治疗(右)的患者的OS
IVO临床研究探索:从单药到联合,
从后线到前线,持续拓展治疗边界
随着对IDH1突变机制的深入理解,针对mIDH1的靶向治疗成为突破传统治疗瓶颈的关键方向。基于IVO在临床研究中展现的优异临床获益,2018年美国FDA正式批准其上市,随后于2022年在中国上市,成为全球首款且国内目前唯一获批的IDH1抑制剂[12-13]。IVO作用机制具有双重特性:一方面精准阻断突变IDH1酶活性,抑制2-HG的异常生成和累积;另一方面诱导IDH1突变AML细胞向正常髓系细胞分化,恢复造血功能(图3)[14-15]。
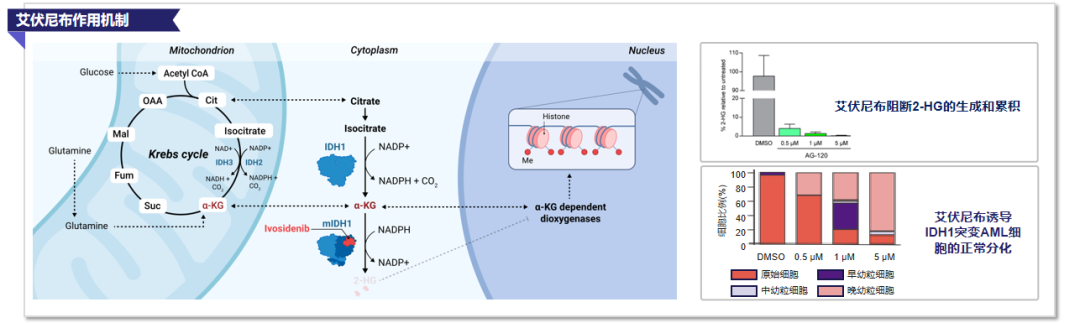
图3. IVO的作用机制
艾伏尼布单药治疗R/R mIDH1 AML,
起效迅速且疗效持久
全球AG120-C-001研究中,IVO单药治疗R/R mIDH1 AML患者的总缓解率(ORR)为41.9%,完全缓解(CR)+部分血液学恢复的完全缓解(CRh)率为31.8%,中位至首次缓解时间为1.9个月(图4);整体人群中位OS为9.0个月,CR+CRh人群中位OS达18.8个月(图5)[16]。
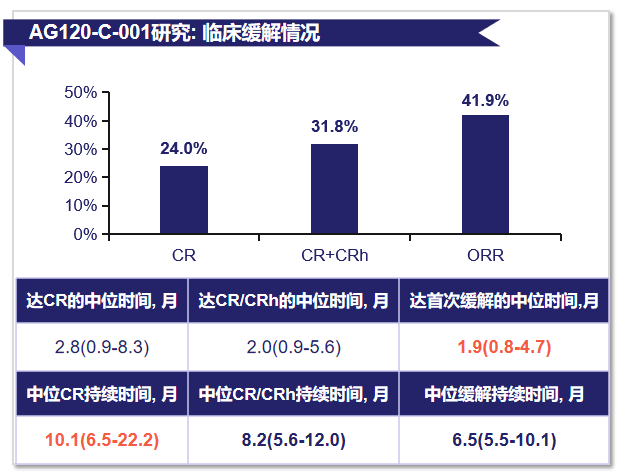
图4. AG120-C-001研究中IVO单药治疗的缓解情况
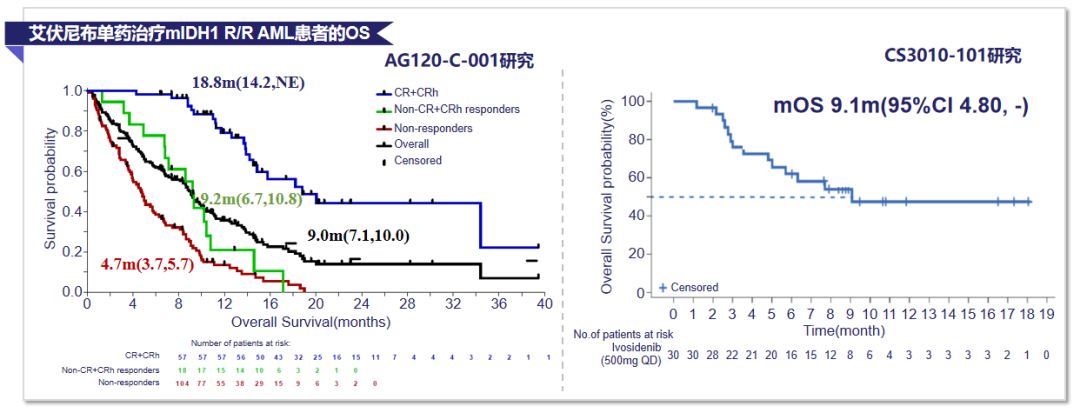
图5. IVO单药治疗mIDH1 R/R AML患者的OS
中国CS3010-101桥接研究显示,中国mIDH1 R/R AML患者接受IVO单药治疗的ORR为43.3%,CR+CRh率36.7%,中位至首次缓解时间仅1.5个月(图6),中位OS 9.1个月,与全球数据一致[17-18]。
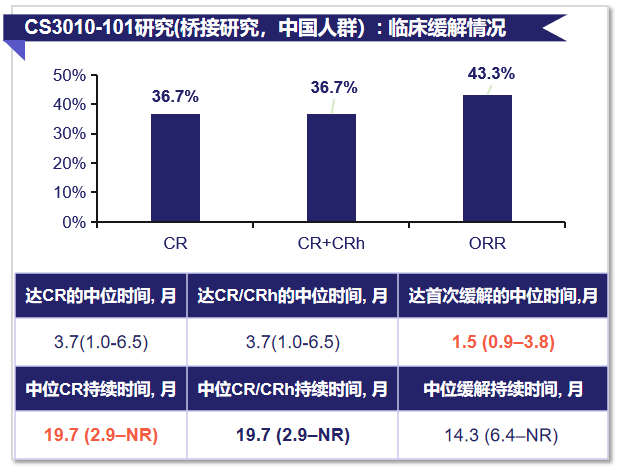
图6. CS3010-101研究中IVO单药治疗的缓解情况
值得一提的是,目前其他多款新型IDH1抑制剂亦展现出一定的临床应用前景。例如,一项开放标签、单臂、多中心的1/2期研究(2102-HEM-101)评估了147例mIDH1 R/R AML成人患者接受Olutasidenib治疗的疗效。结果显示,中位随访10.2个月,ORR为48%,CR/CRh率为35%[19]。另一项中国Ⅰ期研究则探索了HMPL-306治疗mIDH R/R AML的疗效和安全性[20],初步研究数据显示,该药展现出积极的抗肿瘤活性,总体耐受性良好,未出现剂量限制性毒性,为IDH靶向治疗提供了更多潜在选择。
艾伏尼布联合方案一线治疗探索,
显著改善疗效与生存
基于单药活性,研究者进一步探索了IVO联合阿扎胞苷(治疗AZA)方案的前线治疗价值。全球Ⅲ期AGILE研究纳入了146例不适合强化化疗的新诊断mIDH1 AML患者,按1:1随机接受IVO+AZA或安慰剂+ AZA(PBO+AZA)治疗。研究结果显示,IVO+AZA组CR率47.2%、CR+CRh率52.8%、ORR 62.5%,均显著优于对照组(图7)[21-22]。
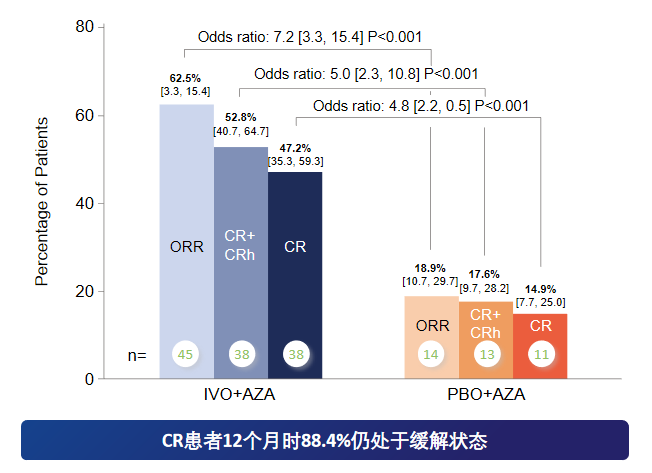
图7.IVO+AZA组对比
中位随访28.6个月时,IVO+AZA组中位OS达29.3 个月,而对照组仅7.9 个月。大中华区亚组分析显示,中位随访22.4个月,IVO+AZA方案中位OS长达30.6个月,CR率50%,疗效与全球人群一致(图8)[23]。此外,AGILE研究还表明对于携带DNMT3A、RUNX1、SRSF2等常见共突变或RTK通路突变的患者,IVO+AZA均能带来显著缓解与生存获益(图9)[24]。
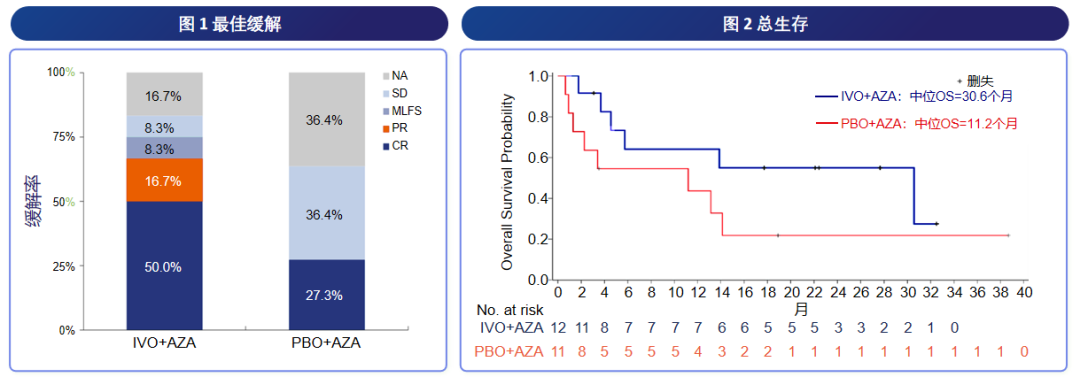
图8. 大中华区人群IVO+AZA对比PBO+AZA的缓解率(左)和中位OS(右)
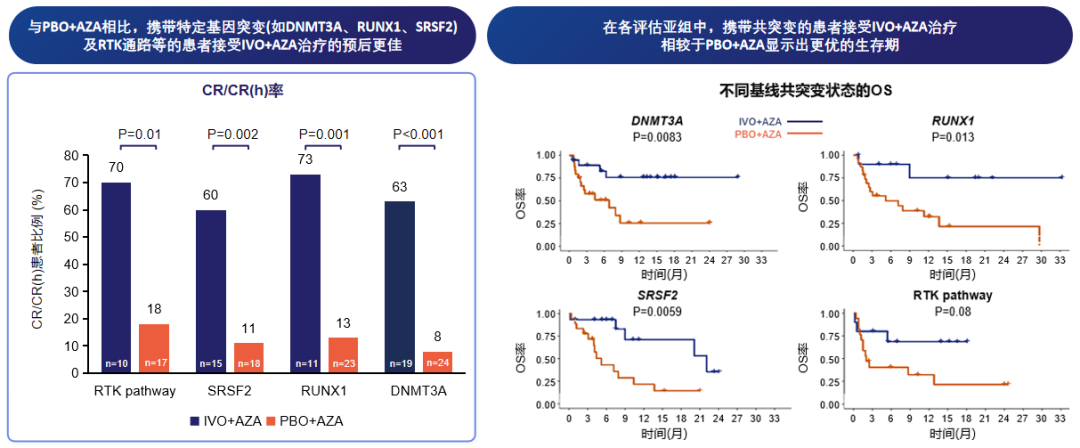
图9. IVO+AZA对比PBO+AZA治疗存在共突变的AML的CR率和OS
以艾伏尼布为基础的三药联合方案进一步提升疗效获益
为进一步提高缓解深度与MRD阴性率,一项Ⅰb/Ⅱ期研究探索了IVO+VEN+AZA方案的有效性及安全性。研究结果表明,相较于IVO+VEN方案,该三药联合方案的复合缓解率更高,更快获得缓解:IVO+VEN(400mg)+AZA方案(推荐Ⅱ期剂量)的ORR为100%,复合完全缓解(CRc)率达85%,中位至缓解时间仅37天,第1周期骨髓原始细胞下降91%(图10)[25]。在生存获益方面,三药联合方案的无事件生存期(EFS)、OS、缓解持续时间(DOR)均更长,且MRD阴性率呈现获益趋势(三药组和双药组MRD阴性率分别为86%和50%,P=0.037)(图11)[26]。上述研究数据充分证实,以IVO为基础的三药联合方案可进一步提升治疗获益,为mIDH1 AML患者提供更高效的治疗选择。
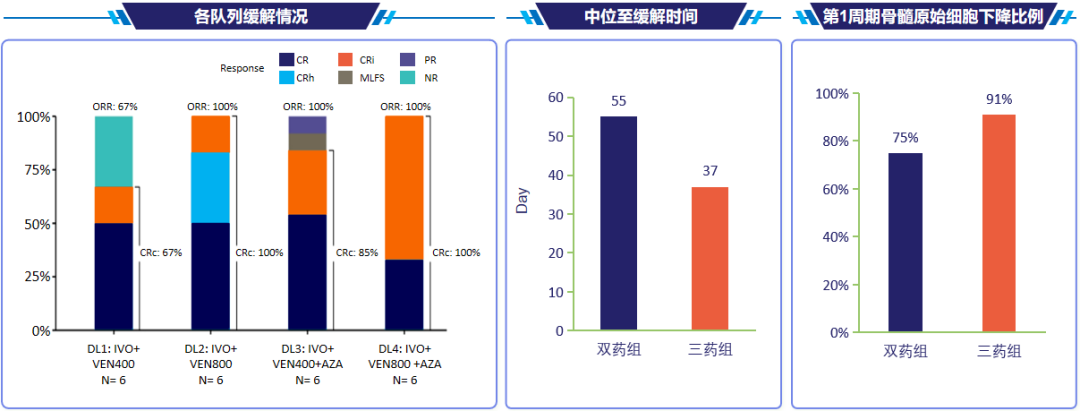
图10.三药组和双药组的缓解情况
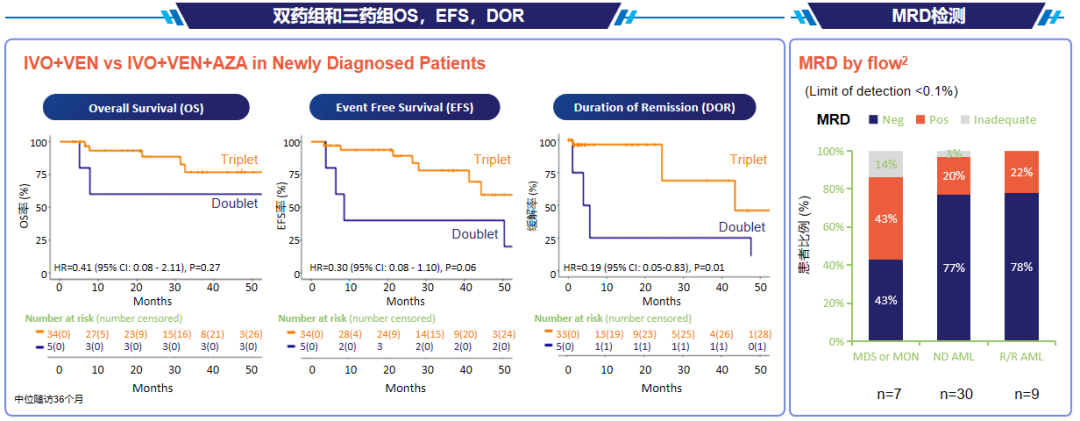
图11. 三药组和双药组的的生存获益和MRD阴性率
真实世界应用:
与临床研究高度一致,疗效安全双重验证
临床试验的严格入排标准与现实临床存在差异,真实世界研究成为验证疗效外推性的关键。目前已有多项大型回顾性真实世界研究进一步验证了IVO的临床价值。
美国一项回顾性真实世界研究对比评估了IVO+HMA与VEN+HMA治疗280例新诊断mIDH1 unfit AML的临床结局[27]。两组的CR率分别为42.5% vs 26.3%(P=0.007),达最佳缓解时间分别为3.3个月 vs 4.1个月(P=0.006);IVO+HMA组治疗后30天内≥3级发热性中性粒细胞减少发生率更低(1.7% vs 8.1%;P=0.008),治疗前12周非计划就医率显著下降(38.6% vs 70.7%;P<0.001)。美国另一项纳入387例患者的多中心回顾性研究显示,IVO+AZA治疗新诊断mIDH1 AML的中位OS达31.9个月,IVO单药为14.9个月[28]。
法国IVOOBS回顾性研究纳入49例患者(中位年龄78岁,93%的患者ECOG PS≥2,83%为ELN中/高危),其中67%接受IVO+AZA治疗。该队列CRc率达73%,中位随访16.6个月时中位OS尚未达到,2年OS率52%(图12),表明IVO+AZA方案在高危人群中仍展现出显著活性[29]。
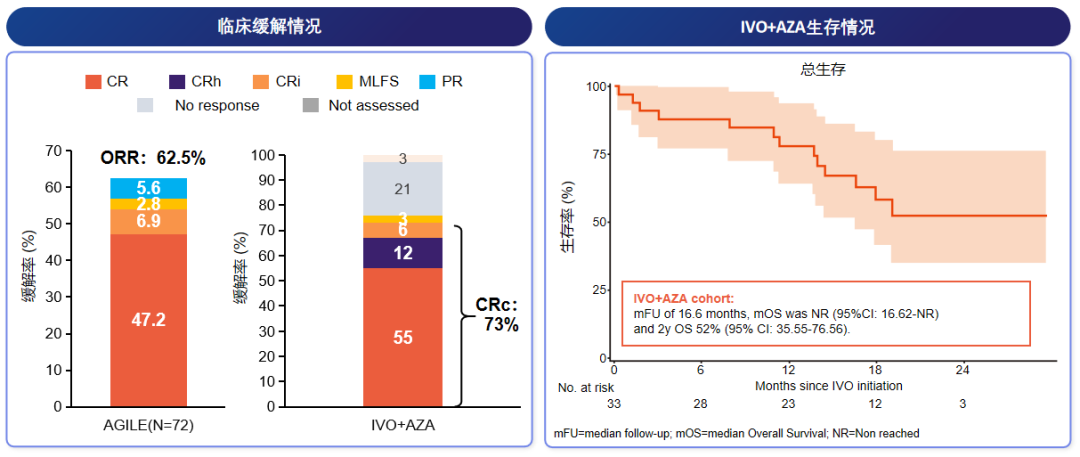
图12. IVO+AZA治疗新诊断mIDH1 AML的缓解和生存情况
指南推荐:
艾伏尼布成为mIDH1 AML核心治疗方案
基于充分的临床研究与真实世界证据,含IVO的治疗方案已获得国内外权威指南的一致推荐(图13)[30-35]。

图13. 国内外AML指南均推荐mIDH1 AML患者选择含IVO方案
孙明媛教授
中国医学科学院血液病医院(中国医学科学院血液学研究所)GCP病房
副主任医师、医学硕士
本科毕业于复旦大学上海医学院临床医学专业、辅修生物医学工程专业,后于中国医学科学院肿瘤医院肿瘤内科获肿瘤学临床型硕士学位
于中国医学科学院血液病医院工作十余年,对血液病尤其白血病、淋巴瘤及骨髓瘤有丰富的临床诊疗经验
天津市抗癌协会药物临床试验专业委员会委员
天津市医疗健康学会血液病防治专业委员会委员
临床试验经验丰富,参与编写《药物临床试验设计与实施中疑难问题处理的专家共识》,现在血液病医院临床试验研究中心负责白血病、淋巴瘤、骨髓瘤等众多新药临床试验
参考文献
免责声明:本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批编号:M-TIBSO-CN-202604-00019