
2026年4月13日,英国糖尿病协会(Diabetes UK)官网发布题为《基因疗法与更安全的胰岛移植:

文章聚焦两项前沿技术的突破——一种即将进入临床试验的首创基因疗法,以及一种能显著提高胰岛细胞移植安全性与成功率的新型抗排异药物,正有望彻底改变1型糖尿病患者的日常生活。
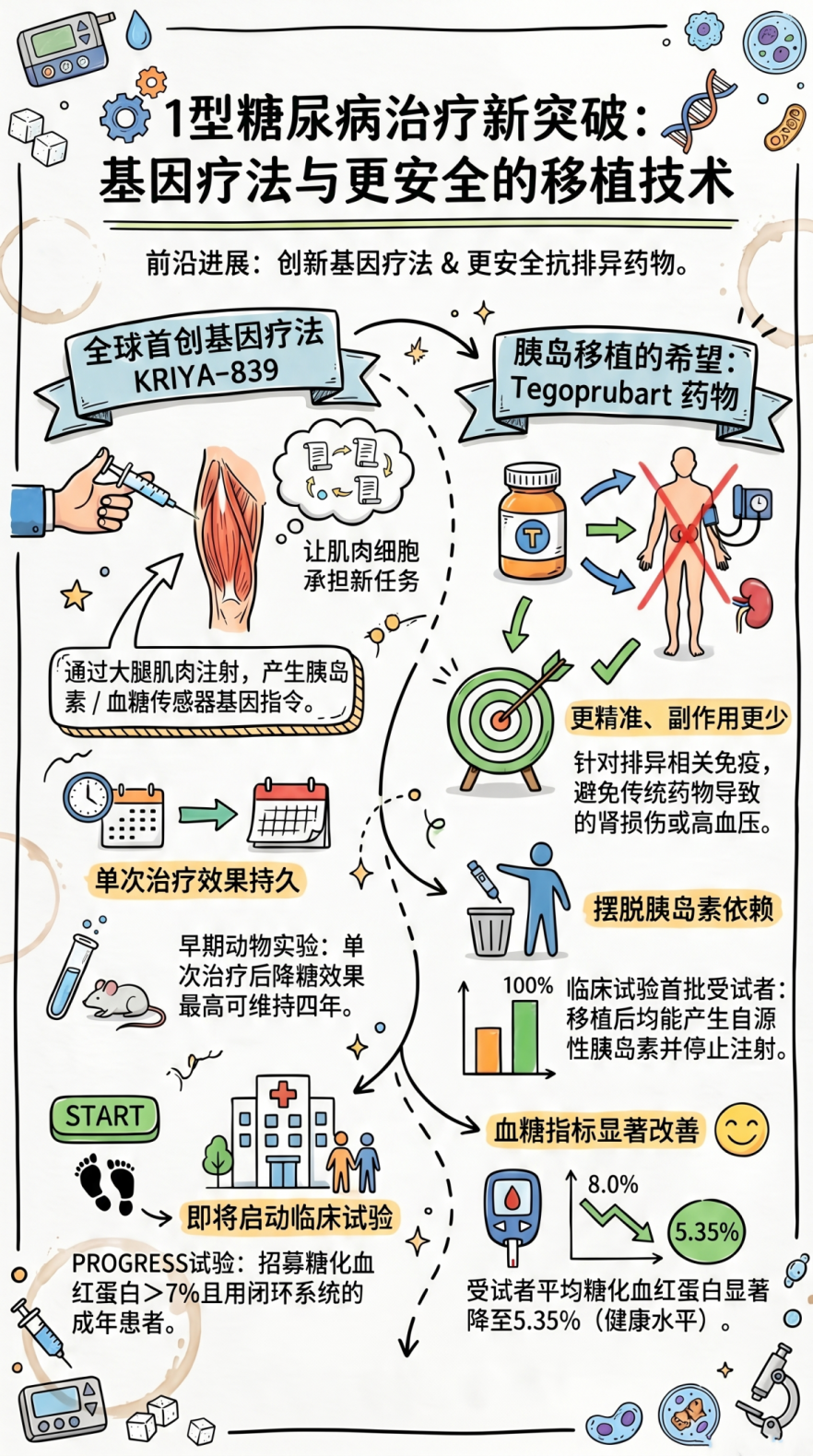


今年,研究人员将在一项全球首创的临床试验中,测试名为KRIYA-839的基因疗法在1型糖尿病患者身上的安全性和有效性。在早期的动物模型研究中,该疗法不仅展现了良好的安全性,而且能有效降低血糖,部分案例中单次治疗的降糖效果甚至长达四年之久。
与传统的基因编辑不同,KRIYA-839疗法不会直接改变患者自身的DNA。它利用一种对人体无害的腺相关病毒(AAV)作为载体,通过大腿肌肉注射的方式,将遗传指令递送至细胞内。值得一提的是,这种类型的基因治疗方法此前已被批准用于治疗某些罕见的遗传疾病,具备较高的安全性基础。
该疗法的核心在于传递两个关键基因:一个负责指导细胞产生
在即将开展的PROGRESS试验中,研究人员计划招募


胰岛细胞移植是通过将供体胰腺中产生胰岛素的细胞移植给患者,从而暂时恢复患者自主合成胰岛素的能力。然而,由于免疫系统会将这些供体细胞视为异物并加以攻击,患者必须长期服用强效的免疫抑制剂。
现有的免疫抑制药物会抑制整个免疫系统,可能导致严重的副作用,包括肾脏损伤和高感染风险。因此,目前胰岛移植通常仅限用于那些频繁发生严重低血糖、具有低血糖感知障碍,或同时需要进行
一项早期的临床试验结果显示,新型药物tegoprubart能够在不产生有害副作用的情况下,有效保护移植的产生胰岛素的细胞。与传统药物不同,tegoprubart仅针对参与移植排斥反应的特定免疫环节发挥作用,这种“精准打击”大大降低了全身性副作用。
在芝加哥大学医学中心(University of Chicago Medicine)开展的试验中,12名平均患病约33年、初始HbA1c高达64 mmol/mol (8.0%) 的成年1型糖尿病患者接受了tegoprubart联合胰岛移植治疗。数据显示:
在首批移植满四周的10名参与者中,所有人均恢复了自主产生胰岛素的能力,并成功停用了胰岛素治疗。
平均HbA1c水平显著降至35 mmol/mol (5.35%)。
首批接受治疗的3名患者,已经超过一年无需注射任何胰岛素。
在安全性方面,tegoprubart耐受性良好,副作用易于治疗,且没有证据表明它会引起血压升高、肾脏损伤或神经系统问题(这些都是传统抗排异药物的常见副作用)。
研究人员下一步计划开展规模更大、周期更长的临床试验,以进一步确认其长期疗效和安全性。未来,tegoprubart甚至可能被用于保护实验室培育的β细胞(beta cells),为新兴的细胞替代疗法提供强有力的支持,从而让这项足以改变命运的治疗手段惠及更广泛的1型糖尿病患者群体。


不论是让肌肉细胞具备智能控糖能力的KRIYA-839基因疗法,还是为新生胰岛细胞保驾护航的tegoprubart,都代表了现代医学在攻克1型糖尿病道路上的巨大飞跃。这些突破性进展不仅展现了科学的严谨与魅力,更切切实实地为患者描绘了一个无需终日依赖胰岛素注射的光明未来。
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学
