[1]Devarbhavi H, Asrani SK, Arab JP, et al. Global burden of liver disease: 2023 update[J]. J Hepatol, 2023, 79(2):516-537.DOI: 10.1016/j.jhep.2023.03.017.
[2]Deng X, Li H, Zhong Y, et al. Burden of liver cancer attributable to hepatitis B and alcohol globally, in China, and for five sociodemographic index regions from 1990 to 2021:a population-based study[J]. J Clin Transl Hepatol, 2025, 13(1):1-14. DOI: 10.14218/jcth.2024.00351.
[3]段钟平 . 防微杜渐,关注肝衰竭前期诊疗[J]. 中华肝脏病杂志, 2020, 28(4):289-291. DOI: 10.3760/cma.j.cn501113-20200‑318-00124.
[4]中华医学会感染病学分会肝衰竭与人工肝学组, 中华医学会肝病学分会重型肝病与人工肝学组 . 肝衰竭诊治指南(2024年版)[J]. 中华肝脏病杂志, 2025, 33(1):18-33. DOI: 10.3760/cma.j.cn501113-20241206-00614.
[5]中华医学会肝病学分会重型肝病与人工肝学组, 中华医学会肝病学分会终末期肝病营养与再生学组 . 慢加急性肝衰竭诊治指南(2025 年版) [J]. 中华肝脏病杂志, 2025, 33(4):329-339. DOI: 10.3760/cma.j.cn501113-20250312-00089.
[6]Mezzano G, Juanola A, Cardenas A, et al. Global burden of disease:acute-on-chronic liver failure, a systematic review and meta-analysis[J]. Gut, 2022, 71(1):148-155. DOI: 10.1136/gutjnl-2020-322161.
[7]Davison BA, Harrison SA, Cotter G, et al. Suboptimal reliability of liver biopsy evaluation has implications for random‑ized clinical trials[J]. J Hepatol, 2020, 73(6):1322-1332. DOI: 10.1016/j.jhep.2020.06.025.
[8]Liver EAftSot. EASL clinical practice guidelines on non-invasive tests for evaluation of liver disease severity and prognosis-2021 update[J]. J Hepatol, 2021, 75(3):659-689. DOI:10.1016/j.jhep.2021.05.025.
[9]Starekova J, Hernando D, Pickhardt PJ, et al. Quantification of liver fat content with CT and MRI:state of the art[J]. Radiology,2021, 301(2):250-262. DOI: 10.1148/radiol.2021204288.
[10]Zhang D, Shi C, Wang Y, et al. Metabolic dysregulation and metabolite imbalances in acute-on-chronic liver failure:impact on immune status[J]. J Clin Transl Hepatol, 2024, 12(10):865-877. DOI: 10.14218/jcth.2024.00203.
[11]De Vincentis A, Vespasiani-Gentilucci U, Sabatini A, et al.Exhaled breath analysis in hepatology: state-of-the-art and perspectives[J]. World J Gastroenterol, 2019, 25(30):4043-4050.DOI: 10.3748/wjg.v25.i30.4043.
[12]Chen T, Liu T, Li T, et al. Exhaled breath analysis in disease detection[J]. Clin Chim Acta, 2021, 515:61-72. DOI: 10.1016/j.cca.2020.12.036.
[13]Moura PC, Raposo M, Vassilenko V. Breath volatile organic compounds (VOCs) as biomarkers for the diagnosis of pathological conditions: a review[J]. Biomed J, 2023, 46(4):100623. DOI: 10.1016/j.bj.2023.100623.
[14]Boon-Yasidhi P, Karnsakul W. Non-invasive biomarkers and breath tests for diagnosis and monitoring of chronic liver diseases[J]. Diagnostics (Basel), 2024, 15(1):68. DOI: 10.3390/diagnosti‑cs15010068.
[15]Haworth JJ, Pitcher CK, Ferrandino G, et al. Breathing new life into clinical testing and diagnostics: perspectives on volatile biomarkers from breath[J]. Crit Rev Clin Lab Sci,2022, 59(5):353-372. DOI: 10.1080/10408363.2022.2038075.
[16] Ferrandino G, De Palo G, Murgia A, et al. Breath biopsy® to identify exhaled volatile organic compounds biomarkers for liver cirrhosis detection[J]. J Clin Transl Hepatol, 2023, 11(3):638-648. DOI: 10.14218/jcth.2022.00309.
[17] Verdam FJ, Dallinga JW, Driessen A, et al. Non-alcoholic steatohepatitis:a non-invasive diagnosis by analysis of exhaled breath[J]. J Hepatol, 2013, 58(3):543-548. DOI: 10.1016/j.jhep.2012.10.030.
[18] Sinha R, Lockman KA, Homer NZM, et al. Volatomic analysis identifies compounds that can stratify non-alcoholic fatty liver disease[J]. JHEP Rep, 2020, 2(5):100137. DOI: 10.1016/j.jhepr.2020.100137.
[19]Sukaram T, Tansawat R, Phathong C, et al. Volatile organic compounds for diagnosis of early hepatocellular carcinoma inat-risk patients[J]. Clin Chim Acta, 2024, 556:117831. DOI: 10.1016/j.cca.2024.117831.
[20]Drabińska N, Flynn C, Ratcliffe N, et al. A literature survey of all volatiles from healthy human breath and bodily fluids: the human volatilome[J]. J Breath Res, 2021, 15(3):034001. DOI:10.1088/1752-7163/abf1d0.
[21] van Vorstenbosch R, van Munster K, Stavropoulos G, et al.The potential of volatile organic compounds to diagnose primary sclerosing cholangitis[J]. JHEP Rep, 2024, 6(8):101103. DOI: 10.1016/j.jhepr.2024.101103.
[22]Li Y, Wei X, Zhou Y, et al. Research progress of electronic nose technology in exhaled breath disease analysis[J]. Microsyst Nanoeng, 2023, 9:129. DOI: 10.1038/s41378-023-00594-0.
[23]Ishida J, Oikawa T, Nakagawa C, et al. Real-time breath ammonia measurement using a novel cuprous bromide sensor device in patients with chronic liver disease: a feasibility and pilot study[J]. J Breath Res, 2021, 15(2):026010. DOI: 10.1088/1752-7163/abb477.
[24] Spacek LA, Mudalel M, Tittel F, et al. Clinical utility of breath ammonia for evaluation of ammonia physiology in healthy and cirrhotic adults[J]. J Breath Res, 2015, 9(4):047109. DOI:10.1088/1752-7155/9/4/047109.
[25] van den Berg EH, Flores-Guerrero JL, Garcia E, et al. High plasma levels of betaine, a trimethylamine N-Oxide-related metabolite, are associated with the severity of cirrhosis[J].Liver Int, 2023, 43(2):424-433. DOI: 10.1111/liv.15310.
[26] Stavropoulos G, van Munste K, Ferrandino G, et al. Liver impairment-the potential application of volatile organic compo‑unds in hepatology[J]. Metabolites, 2021, 11(9):618. DOI: 10.3390/metabo11090618.
[27] Nguyen TTP, Nguyen PL, Park SH, et al. Hydrogen sulfide and liver health: insights into liver diseases[J]. Antioxid Redox Signal, 2024, 40(1-3):122-144. DOI: 10.1089/ars.2023.0404.
[28] Ferrandino G, Ricciardi F, Murgia A, et al. Exogenous volatile organic compound (EVOC(®)) breath testing maximizes classification performance for subjects with cirrhosis and reveals signs of portal hypertension[J]. Biomedicines, 2023,11(11):2957. DOI: 10.3390/biomedicines11112957.
[29] Weber IC, Oosthuizen DN, Mohammad RW, et al. Dynamic breath limonene sensing at high selectivity[J]. ACS Sens,2023, 8(7):2618-2626. DOI: 10.1021/acssensors.3c00439.
[30] Ratcliffe N, Wieczorek T, Drabińska N, et al. A mechanistic study and review of volatile products from peroxidation of unsaturated fatty acids: an aid to understanding the origins of volatile organic compounds from the human body[J]. J Breath Res, 2020, 14(3):034001. DOI: 10.1088/1752-7163/ab7f9d.
[31] Kiejzik R, Wasilewski T, Kamysz W. Exhaled aldehydes and ketones as biomarkers of lung cancer and diabetes: review of sensor technologies for early disease diagnosis[J]. Biosensors(Basel), 2025, 15(10):668. DOI: 10.3390/bios15100668.
[32]P H, Rangarajan M, Pandya HJ. Breath VOC analysis and machine learning approaches for disease screening:a review[J]. J Breath Res, 2023, 17(2):024001. DOI: 10.1088/1752-7163/acb‑283.
[33] Heng W, Yin S, Chen Y, et al. Exhaled breath analysis:from laboratory test to wearable sensing[J]. IEEE Rev Biomed Eng,2025, 18:50-73. DOI: 10.1109/rbme.2024.3481360.
[34] Son A, Kim W, Park J, et al. Mass spectrometry advancements and applications for biomarker discovery, diagnostic innovations,and personalized medicine[J]. Int J Mol Sci, 2024, 25(18):9880.DOI: 10.3390/ijms25189880.
[35] Bajo-Fernández M, Souza-Silva ÉA, Barbas C, et al. GC-MS-based metabolomics of volatile organic compounds in exhaled breath: applications in health and disease. A review [J]. Front Mol Biosci, 2023, 10:1295955. DOI: 10.3389/fmolb.2023.1295955.
[36] Le T, Priefer R. Detection technologies of volatile organic compounds in the breath for cancer diagnoses[J]. Talanta,2023, 265:124767. DOI: 10.1016/j.talanta.2023.124767.
[37] Scheepers M, Al-Difaie Z, Brandts L, et al. Diagnostic performance of electronic noses in cancer diagnoses using exhaled breath: a systematic review and meta-analysis[J].JAMA Netw Open, 2022, 5(6):e2219372. DOI: 10.1001/jamanet‑workopen.2022.19372.
[38] Sinha R, Gillespie SL, Brinkman P, et al. Volatomics for diagnosis and risk stratification of MASLD:a proof-of-concept study[J]. Aliment Pharmacol Ther, 2025, 62(2):180-192. DOI:10.1111/apt.70176.
[39] Zaim O, Diouf A, El Bari N, et al. Comparative analysis of volatile organic compounds of breath and urine for distinguishing patients with liver cirrhosis from healthy controls by using electronic nose and voltammetric electronic tongue[J]. Anal Chim Acta, 2021, 1184:339028. DOI: 10.1016/j.aca.2021.339028.
[40] Lujan-Cabrera IA, Morales-Narváez E. Harnessing surface enhanced raman spectroscopy for breath-based diagnostics[J]. Anal Chem, 2025, 97(19):10099-10109. DOI: 10.1021/acs.ana‑lchem.5c00167.
[41] Liu S, Li Y, Zhang Y, et al. Hydrogen sulfide in precision medicine:connecting basic science, sensing, and clinical appli‑cation[J]. Med Gas Res, 2026, 16(3):277-285. DOI: 10.4103/mgr.MEDGASRES-D-25-00190.
[42] Henderson B, Khodabakhsh A, Metsälä M, et al. Laser spectroscopy for breath analysis:towards clinical implementation[J]. Appl Phys B, 2018, 124(8):161. DOI: 10.1007/s00340-018-7030-x.
[43] K SK, Jothimani D, Manoharan M, et al. Quartz-enhanced photoacoustic spectroscopy-based acetone and ammonia measu‑rements from human breath near 8 μm wavelength band[J]. ACS Sens, 2025, 10(1):254-263. DOI: 10.1021/acssensors.4c02336.
[44] Ferrandino G, Orf I, Smith R, et al. Breath biopsy assessment of liver disease using an exogenous volatile organic compound-tow‑ard improved detection of liver impairment[J]. Clin Transl Gastroenterol, 2020, 11(9):e00239. DOI: 10.14309/ctg.00000000‑00000239.
[45] Wlodzimirow KA, Abu-Hanna A, Schultz MJ, et al. Exhaled breath analysis with electronic nose technology for detection of acute liver failure in rats[J]. Biosens Bioelectron, 2014, 53:129-134. DOI: 10.1016/j.bios.2013.09.047.
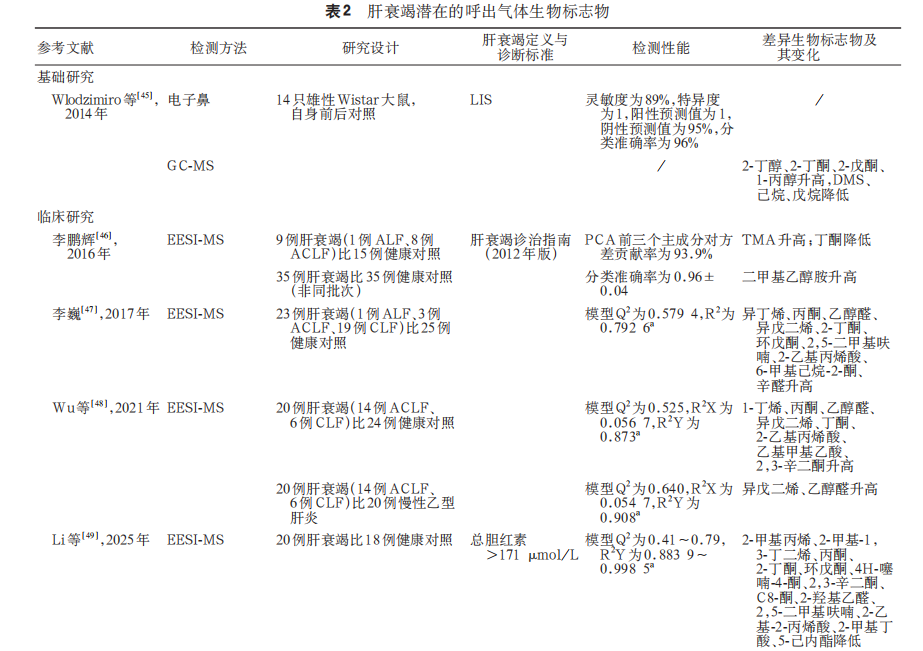
[46] 李鹏辉 . 肝衰竭患者呼出气体的电喷雾萃取电离质谱研究[D]. 东华理工大学, 2016.
[47]李巍 . 肝衰竭患者呼出气体中标志性化合物与血清生化指标的相关研究[D]. 南昌大学, 2017.
[48] Wu X, Zhang J, Yan X, et al. Characterization of liver failure by the analysis of exhaled breath by extractive electrospray ionization mass spectrometry (EESI-MS): a pilot study[J].Analytical Letters, 2021, 54(6):1038-1054. DOI: 10.1080/0003‑2719.2020.1793993.
[49] Li X, Zhang W, Yang T, et al. Discovering the metabolic pathway of liver disease by breath mass spectrometry combined with machine learning[J]. J Pharm Biomed Anal, 2025, 265:116988. DOI: 10.1016/j.jpba.2025.116988.
[50] 王仲霞, 桑秀秀, 余思邈, 等. 乙型肝炎失代偿期肝硬化及慢性肝衰竭患者的呼出气代谢组学差异性分析[J]. 世界科学技术-中医药现代化, 2019, 21(10):2032-2040. DOI: 10.11842/wst.20190726003.
[51]韩涛. 2025年肝衰竭与人工肝领域研究进展[J]. 中华肝脏病杂志, 2026, 34(1):13-17. DOI: 10.3760/cma.j.cn501113-2024‑1204-00611.
[52]李承木 . 呼出气体监测肝衰竭病情变化及预后的相关研究[D]. 南昌大学, 2022.
[53]Jing J, Sang XX, You SL, et al. Metabolomic profiles of breath odor compounds for prognostic prediction in patients with acute-on-chronic liver failure: a pilot study[J]. Hepatol Res, 2021, 51(4):490-502. DOI: 10.1111/hepr.13594.
[54]Fernández Del Río R, O'Hara ME, Holt A, et al. Volatile biomarkers in breath associated with liver cirrhosis-comparisons of pre-and post-liver transplant breath samples[J]. EBioMedicine,2015, 2(9):1243-1250. DOI: 10.1016/j.ebiom.2015.07.027.
[55] Cresci GAM, Liu Q, Sangwan N, et al. The impact of liver graft preservation method on longitudinal gut microbiome changes following liver transplant:a proof-of-concept study[J].J Clin Transl Hepatol, 2025, 13(4): 284-294. DOI: 10.14218/jcth.2024.00352.
[56]朱滢 . 肝衰竭患者经人工肝治疗前后的呼出气体分析[D].南昌大学, 2019.