2026年3月6日,两款基于诱导多能干细胞(iPS细胞)衍生的再生医疗产品在日本正式获得了附条件和期限的上市许可。
在小鼠iPS细胞问世整整20周年之际,这项曾经只存在于实验室中的技术,终于迎来了全球首批实用化产品的获批。
更值得关注的是,此类技术已在脆性

京都大学iPS细胞研究所开放实验室
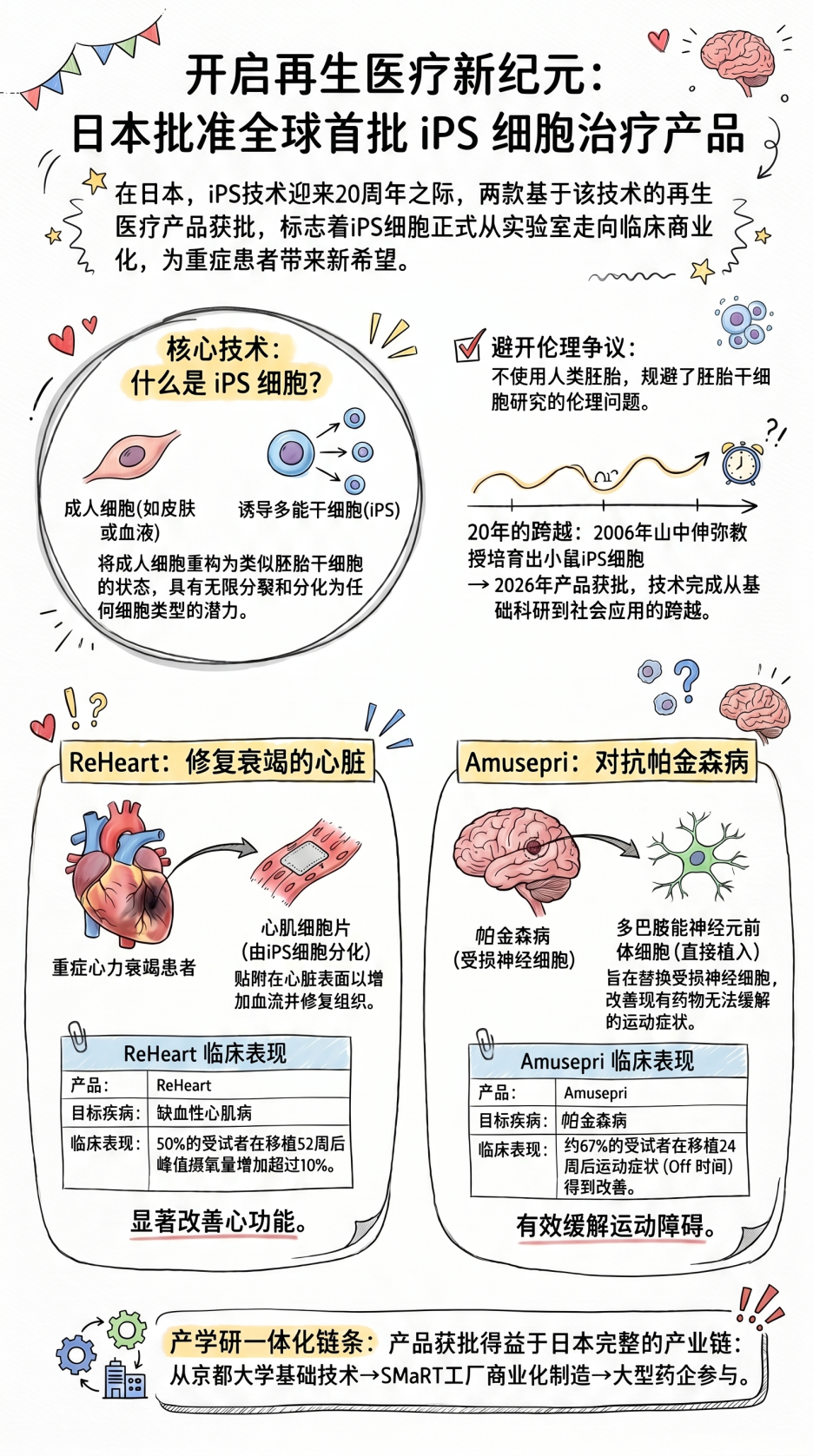
iPS细胞(诱导多能干细胞)是通过对皮肤细胞或血液细胞等成体细胞进行重新编程,使其具备类似于胚胎干细胞功能的细胞。它们能够无限分裂,并可以分化为任何类型的细胞。这项技术的突出之处在于,它不仅为测试新药和再生医学研究提供了强大的工具,更重要的是,它完全避开了使用胚胎干细胞所带来的伦理争议。
京都大学iPS细胞研究所名誉所长山中伸弥表示:“在小鼠iPS细胞发布20周年之际,我们非常高兴能在迈向社会应用的道路上迈出重要一步。”他同时强调,为了将其确立为一种医疗手段,必须在更多病例中确认其安全性和有效性,保持科学的谨慎,稳步向前。
本次获批的首款产品是来自大阪大学初创公司Qualipse的 ReHeart。这是一种由健康供体iPS细胞分化而成的特制心肌细胞片,专门用于治疗因缺血性
重度心衰是一种进行性恶化的严重疾病,传统的终极治疗手段仅有心脏移植或植入人工心脏。然而,心脏移植面临供体短缺和年龄限制的困境,而人工心脏则伴随着感染、颅神经损伤以及患者长期生活质量下降的风险。
ReHeart 精准填补了这一未被满足的医疗需求。在治疗过程中,医生通过左胸切口手术,将三片心肌细胞片直接贴附在患者心脏表面。这些移植的细胞能够分泌信号蛋白,帮助增加血流量并修复受损组织。在一项包含8名重度心衰患者的全国多中心合作研究中,有4名患者在移植52周后显示出改善趋势,其峰值耗氧量(VO2 peak)增加了10%以上。
另一款获批产品是住友制药(Sumitomo Pharma)和Racthera共同研发的 Amusepri(通用名:laguneprocell)。这是一种由供体iPS细胞制成的
帕金森病是一种神经退行性疾病,其根本原因是大脑中产生多巴胺的神经细胞逐渐丢失,从而导致肢体
Amusepri 提供了一种全新的治疗思路:直接将多巴胺能神经元前体细胞移植入大脑。通过微创脑外科手术,医生在患者颅骨两侧钻出小孔,将细胞分散并通过三条输送路径注入目标区域。一项由医生主导的临床试验显示,在接受移植24个月后,6名受试者中有4名的运动症状诊断与治疗评定量表(MDS-UPDRS Part III)的“关期”得分(即药效消退时的得分)得到了改善。此外,研究人员确认细胞在所有6名患者的移植部位均保持存活。
在审批机制方面,这两款产品获得了“附条件和期限的上市许可”。这种机制允许在难以开展大规模临床试验的再生医学领域进行早期审批。
这意味着,即使在初步获批后,这些产品的疗效和安全性仍需通过上市后的临床试验和最终用户研究来持续验证。
尽管产品已经获批,但业内专家依然保持着科学的严谨与克制。主导 Amusepri 试验的京都大学iPS细胞研究所所长高桥淳强调:“虽然获批是一大进步,但这并非终点,而仅仅是这种新疗法的开始。”他指出,从有限的病例开始谨慎推进并积累长期数据至关重要。
目前,这些疗法尚未能普及给所有患者。ReHeart 计划进行一项目标为75名患者的综合使用结果研究,预计于2026年秋季开始销售;AmShepli 也需要继续收集数据以获得正式批准。患者要真正用上这些产品,还需等待其完成纳入公共健康保险的程序,这通常需要获批后数月的时间。
二十年光阴流转,发轫于实验室的iPS技术,终于走到了细胞培养、分化并最终注入患者体内的这一步。由iPS细胞改写的医学未来,才刚刚拉开帷幕。
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学